高中化学必修1化学方程式总结
1.钠及其化合物:
钠在空气中颜色变暗: 4Na + O2 = 2Na2O
钠在空气中点燃: 2Na + O2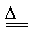 Na2O2 (发出黄色火焰,生成淡黄色固体)
Na2O2 (发出黄色火焰,生成淡黄色固体)
钠与水反应的化学方程式: 2Na + 2H2O = 2NaOH + H2↑ (浮、熔、动、响、红)
钠与水反应的离子方程式: 2Na + 2H2O = 2Na+ + 2OH- + H2 ↑ (钠起火不能用水灭火)
过氧化钠与水的反应: 2Na2O2 + 2H2O = 4NaOH + O2 ↑
过氧化钠与二氧化碳的反应: 2Na2O2 + 2CO2 = 2Na2CO3 + O2 ↑(过氧化钠可以做供氧剂)
碳酸钠与稀盐酸反应:Na2CO3 + 2HCl = 2NaCl + CO2↑ + H2O 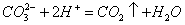
碳酸氢钠与稀盐酸反应:NaHCO3 + HCl = NaCl + CO2↑ + H2O
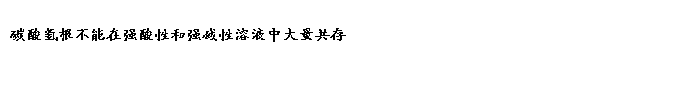
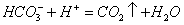 (碳酸氢根不能拆)
(碳酸氢根不能拆)
碳酸氢钠与氢氧化钠溶液反应: NaHCO3 + NaOH = Na2CO3 + H2O

加热碳酸氢钠固体: 2NaHCO3 Na2CO3 + H2O +CO2↑ (碳酸氢钠热稳定性差)
Na2CO3 + H2O +CO2↑ (碳酸氢钠热稳定性差)
2. 铝及其化合物
铝在空气中加热:4Al + 3O2 2Al2O3 (铝熔化,但不滴落)
2Al2O3 (铝熔化,但不滴落)
铝与盐酸反应的方程式: 2Al + 6HCl = 2AlCl3 +3H2↑ 2Al + 6H+ = 2Al3+ + 3H2↑
铝与氢氧化钠溶液溶液的反应:2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑(一定不要忘记水!!!)
氧化铝与强酸强碱的反应:Al2O3 + 6HCl = 2AlCl3 +3H2O Al2O3 + 6H+ = 2Al 3++3H2O
Al2O3 + 2NaOH = 2NaAlO2 + H2O Al2O3 + 2OH- = 2Al + H2O
+ H2O
制取氢氧化铝:AlCl3 + 3NH3·H2O = Al(OH)3 ↓+ 3NH4Cl Al3+ + 3NH3·H2O = Al(OH)3↓+ 3NH4+
氢氧化铝与强酸强碱的反应:Al(OH)3 + 3HCl = AlCl3 + 3H2O Al(OH)3 + 3H+ = Al3++ 3H2O
Al(OH)3 + NaOH =NaAlO2 +2H2O Al(OH)3 +OH- = AlO2- +2H2O
氯化铝中加入少量强碱:AlCl3 + 3NaOH = Al(OH)3 ↓+ 3NaCl Al3+ + 3OH- =Al(OH)3
氯化铝中加入过量强碱:AlCl3 + 4NaOH = NaAlO2 + 3NaCl +2H2O Al3+ + 4OH- =AlO2- + 2H2O
加热氢氧化铝: 2Al(OH)3 Al2O3 + 3H2O
Al2O3 + 3H2O
明矾在水溶液中的电离:KAl(SO4)2 = K+ + Al3+ + 2SO42-
3.铁及其化合物
铁与高温水蒸气反应:3Fe + 4H2O(g)  Fe3O4 + 4H2
Fe3O4 + 4H2
铁在氧气中点燃:3Fe + 2O2 Fe3O4(剧烈燃烧,火星四射,生成黑色物质,放出大量的热)
Fe3O4(剧烈燃烧,火星四射,生成黑色物质,放出大量的热)
铁在氯气中点燃:2Fe + 3Cl2 2FeCl3(发出棕褐色烟,加水生成棕黄色溶液)
2FeCl3(发出棕褐色烟,加水生成棕黄色溶液)
氧化铁溶于稀盐酸: Fe2O3 + 6HCl = 2FeCl3 + 3H2O Fe2O3 + 6H+ = 2Fe3+ + 3H2O
氧化亚铁溶于稀盐酸: FeO + 2HCl = FeCl2 + H2O FeO + 2H+ = Fe2+ + H2O
四氧化三铁溶于稀盐酸:Fe3O4+8HCl=2FeCl3+FeCl2 + 4H2O Fe3O4 + 8H+ = 2Fe3+ + Fe2+ + 4H2O
制备氢氧化铁:FeCl3 + 3NaOH = Fe(OH)3 ↓+ 3NaCl Fe3++ 3OH-= Fe(OH)3 ↓
制备氢氧化亚铁:FeCl2 + 2NaOH = Fe(OH)2 ↓+ 2NaCl Fe2++ 2OH-= Fe(OH)2 ↓
氢氧化亚铁氧化:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(先出现白色沉淀,迅速变成灰绿色,最后变成红褐色)
Fe3+中加入KSCN溶液: Fe3+ + 3SCN- = Fe(SCN)3 (血红色,检验铁离子存在)
Fe3+中加入铁粉: 2Fe3+ + Fe = 3Fe2+
Fe2+中加入氯水: 2Fe2+ + Cl2 = 2Fe3+ + 2Cl-
Fe2+中加入双氧水:H2O2 + 2Fe2+ + 2H+ = 2Fe3+ + 2H2O
氯化铁与铜的反应: 2FeCl3 + Cu = 2FeCl2 + CuCl2 (工业上用氯化铁腐蚀铜电路板)
4.硅及其化合物
二氧化硅与氢氟酸反应:SiO2 + 4HF = SiF4↑ + 2H2O (氢氟酸用来刻蚀玻璃)
二氧化硅与氢氧化钠反应:SiO2 +2NaOH = Na2SiO3 + H2O (碱性试剂瓶不能用磨口玻璃塞)
二氧化硅与生石灰的反应:SiO2 + CaO = CaSiO3
碳单质还原二氧化硅: SiO2 + 2C = Si(粗硅)+ 2CO ↑ (工业上制取粗硅)
粗硅的提纯: Si(粗硅) + 2Cl2 = SiCl4 SiCl4 + 2HCl = Si (纯硅)+ 4HCl
水玻璃在空气中变质: Na2SiO3 + CO2 + H2O = H2SiO3(胶体)+ Na2CO3
硅与氢氧化钠溶液的反应: Si + 2NaOH + H2O = Na2SiO3 + 2H2↑
5. 氯及其化合物
实验室制取氯气: MnO2 + 4HCl (浓)  MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
氯气与氧气反应: H2 + Cl2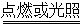 2HCl (发出苍白色火焰,瓶口有白雾)
2HCl (发出苍白色火焰,瓶口有白雾)
氯气与铁反应: 2Fe + 3Cl2 2FeCl3 (生成棕褐色烟,加水生成棕黄色溶液)
2FeCl3 (生成棕褐色烟,加水生成棕黄色溶液)
氯气与铜反应: Cu + Cl2  CuCl2 (生成棕黄色烟,加水生成蓝色溶液)
CuCl2 (生成棕黄色烟,加水生成蓝色溶液)
氯气溶于水: Cl2 + H2O = HCl + HClO (次氯酸有漂白性)
次氯酸在光照下分解: 2HClO 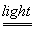 2HCl + O2↑
2HCl + O2↑
制取漂白液: Cl2 + 2NaOH = NaCl + NaClO +H2O Cl2 + 2OH- = Cl- + ClO- +H2O
制取漂白粉: 2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 +2H2O
漂白粉作用原理:Ca(ClO)2 + CO2 + H2O = CaCO3↓ + 2HClO
氯水与淀粉KI试纸作用: Cl2 + 2KI = 2KCl + I2 (碘单质遇到淀粉变蓝色)
氯水与SO2混合通入水中:Cl2 + SO2 + 2H2O = 2HCl + H2SO4 (失去漂白性)
6.硫及其化合物
硫在纯氧中点燃: S + O2 = SO2 (产生蓝紫色火焰)
硫与铁混合加热:Fe + S  FeS (黑色) 硫与铜混合加热:2Cu + S
FeS (黑色) 硫与铜混合加热:2Cu + S  Cu2S (黑色)
Cu2S (黑色)
硫与氢氧化钠溶液反应: 3S + 6NaOH = Na2SO3 + 2Na2S + 3H2O
二氧化硫溶于水: SO2 + H2O = H2SO3 (可逆反应,亚硫酸是弱酸)
二氧化硫与氢氧化钠溶液的反应: SO2 + 2NaOH = Na2SO3 +H2O
二氧化硫与澄清石灰水反应:Ca(OH)2 + SO2(少量) = CaSO3 ↓+ H2O
CaSO3 + SO2(足量)+ H2O = Ca(HSO3)2 (与二氧化碳和澄清石灰水反应现象类似)
二氧化硫催化氧化: 2SO2 + O2 2SO3 (工业制硫酸重要反应)
2SO3 (工业制硫酸重要反应)
二氧化硫与硫化氢反应: SO2 + 2H2S = 3S ↓ + 2H2O
煤脱硫处理: SO2 + CaO = CaSO3 蔗糖脱水碳化:C12H22O11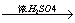 12C + 11H2O
12C + 11H2O
铜与浓硫酸加热反应:Cu + 2H2SO4(浓) CuSO4 + SO2 ↑ +2H2O
CuSO4 + SO2 ↑ +2H2O
碳与浓硫酸加热反应:C + 2H2SO4(浓) CO2 ↑ + 2SO2 ↑ +2H2O
CO2 ↑ + 2SO2 ↑ +2H2O
7. 氮及其化合物
氮气和氧气的反应: N2 + O2 2NO
2NO
一氧化氮与氧气反应: 2NO + O2 = 2NO2 二氧化氮溶于水: 3NO2 + H2O = 2HNO3 + NO
二氧化氮和氧气混合气体溶于水: 4NO2 + O2 + 2H2O = 4HNO3
一氧化氮和氧气混合气体溶于水: 4NO + 3O2 + 2H2O = 4HNO3
工业合成氨:
实验室制取氨气: Ca(OH)2 + 2NH4Cl = CaCl2 + 2NH3 ↑+ 2H2O
氨气与氯化氢气体反应:HCl + NH3 = NH4Cl (冒出白烟)
加热浓氨水: NH3·H2O  NH3 ↑+ H2O 氨水显碱性:NH3·H2O = NH4+ + OH-
NH3 ↑+ H2O 氨水显碱性:NH3·H2O = NH4+ + OH-
加热氯化铵:NH4Cl  NH3 ↑+ HCl ↑ 加热碳酸氢铵:NH4HCO3
NH3 ↑+ HCl ↑ 加热碳酸氢铵:NH4HCO3 NH3 ↑+H2O +CO2 ↑
NH3 ↑+H2O +CO2 ↑
硝酸铵与氢氧化钠的反应: NH4NO3 + NaOH  NaNO3 + H2O + NH3↑
NaNO3 + H2O + NH3↑
氨的催化氧化: 4NH3 + 5O2 = 4NO + 6H2O (工业制取硝酸的重要反应)
硝酸见光分解: 4HNO3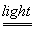 4NO2 ↑+ 2H2O +O2 ↑
4NO2 ↑+ 2H2O +O2 ↑
碳与浓硝酸反应: C + 4HNO3 CO2 ↑ + 4NO2↑ +2H2O
CO2 ↑ + 4NO2↑ +2H2O
铜与浓硝酸反应: Cu + 4HNO3(浓) = Cu(NO3) 2 + 4NO2↑ +2H2O
铜与稀硝酸反应: 3Cu + 8HNO3(稀) = 3Cu(NO3) 2 + 2NO↑ + 4H2O
3Cu + 8H+ + 2NO3-= 3Cu2+ + 2NO↑ + 4H2O
第二篇:人教版高中化学必修1化学方程式总结
高中化学必修1化学方程式总结
1、钠及其化合物的转化关系
2 ② NaCl
2
①Na2O+2HCl=2NaCl+H2O ②2Na+2HCl=2NaCl+H2↑
Na2O+2H+=2Na++H2O 2Na+2H+=2Na++H2↑ ③2Na2O2+4HCl=4NaCl+O2↑+2H2O ④4Na+O2=2Na2O
2Na2O2+4H=4Na+O2↑+2H2O
2Na+2H2O=2NaOH+H2↑ ※⑤2Na+O2
△
+
+
Na2O2 2Na+2H2O=2Na+2OH+H2↑
+
-
⑦Na2O+H2O=2NaOH
※⑧2Na2O2+2H2O=4NaOH+O2↑
Na2O+H2O=2Na++2OH- 2Na2O2+2H2O=4Na++4OH-+O2↑ ⑨Na2O+CO2=Na2CO3 ※⑩2Na2O2+2CO2=2Na2CO3+O2
⑾2NaOH+CO2=Na2CO3+H2O ⑿Na2CO3+Ca(OH)2=CaCO3↓+2NaOH 2OH-+CO2=CO32-+H2O CO32-+Ca2+=CaCO3↓ ⒀NaOH+CO2=NaHCO3 ※⒁Na2CO3+H2O+CO2=2NaHCO3 OH-+CO2=HCO3- CO32-+H2O+CO2=2HCO3- ※⒂2NaHCO3
△
Na2CO3+H2O+CO2↑ 或 ※NaHCO3+NaOH=Na2CO3+H2O
HCO3-+OH-=CO32-+H2O ⒃Na2CO3+2HCl=2NaCl+H2O+CO2↑ ⒄NaHCO3+HCl=NaCl+H2O+CO2↑
2-+-+
CO3+2H=H2O+CO2↑ HCO3+H=H2O+CO2↑
补充:①石灰水中加入少量NaHCO3 : Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O Ca2++OH-+HCO3-=CaCO3↓+H2O
②石灰水中加入过量NaHCO3 : Ca(OH)2+2NaHCO3=CaCO3↓+Na2CO3+2H2O Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O 2、铝及其化合物的转化关系
3
⑥
⑦
⑧ ⑾
2O3OH)3KAl(SO4)2
⑨
⑩
①2Al+6HCl=2AlCl3+3H2↑ ②4Al+3O2 2Al+6H+=2Al3++3H2↑
△
2Al2O3
※③2Al+2NaOH+2H2O=2NaAlO2+3H2↑ ④Al2O3+6HCl=2AlCl3+3H2O 2Al+2OH-+2H2O=2AlO2-+3H2↑ Al2O3+6H+=2Al3++3H2O
※⑤Al2O3+2NaOH=2NaAlO2+H2O ⑥AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl
--3++
Al2O3+2OH=2AlO2+H2O Al+3NH3·H2O = Al(OH)3↓+3NH4 ⑦Al(OH)3+3HCl=AlCl3+3H2O ⑧2Al(OH)3 Al(OH)3+3H=Al+3H2O
☆⑨NaAlO2+HCl+H2O =Al(OH)3↓+NaCl或NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO3 AlO2-+H++H2O=Al(OH)3↓ AlO2-+2H2O+CO2=Al(OH)3↓+HCO3- ※⑩Al(OH)3+NaOH = NaAlO2+2H2O ☆⑾Al+3H2O Al(OH)3+OH-= AlO2-+2H2O 明矾净水
3+
+
△
Al2O3+3H2O
3+
Al(OH)3胶体+3H
+
⑿AlCl3+4NaOH = NaAlO2+3NaCl+2H2O Al3++4OH-= AlO2-+2H2O 3、铁及其化合物的转化关系 ⑦ ③ ①
Fe(OH)2 Fe3O4 FeCl2 ⑧ ②
⑤ ⑥ ⑨
Fe(SCN)3 O3
①Fe3O4+4CO
△
+4CO2
3Fe+4H2O(g)
高温
Fe3O4+4H2 Fe3O4
Fe+2HCl=FeCl2+H2↑ 或3Fe+2O2 Fe+2H+=Fe2++H2↑ ④2Fe+3Cl2
点燃
点燃
2FeCl3
※⑤2FeCl2+Cl2 = 2FeCl3 ※⑥Fe+2FeCl3 = 3FeCl2 2Fe2++Cl2 = 2Fe3++2Cl- Fe+2Fe3+= 3Fe2+
⑦FeCl2+2NaOH = Fe(OH)2↓+2NaCl ⑧Fe(OH)2+2HCl = FeCl2+2H2O Fe2++2OH-= Fe(OH)2↓ Fe(OH)2+2H+= Fe2++2H2O
※⑨4Fe(OH)2+O2+2H2O = 4Fe(OH)3 ⑩FeCl3+3NaOH = Fe(OH)3↓+3NaCl 白色沉淀迅速变成灰绿色,最后变成红褐色 Fe3++3OH-= Fe(OH)3↓ ⑾Fe(OH)3+3HCl = FeCl3+3H2O Fe+3H2O Fe(OH)3+3H+= Fe3++3H2O ⑿2Fe(OH)3
3+
Fe(OH)3胶体+3H(净水)
△
+
Fe2O3+3H2O
⒀Fe2O3+6HCl = 2FeCl3+3H2O ※⒁FeCl3+3KSCN = Fe(SCN)3+3KCl Fe2O3+6H+= 2Fe3++3H2O Fe3++3SCN-= Fe(SCN)3
4 ①Si+O2
△
SiO2
④
高温
②SiO2+2CSi+2CO↑(工业制粗硅)
Si 2CaSiO 3 ※③SiO2+4HF = SiF4↑+2H2O(刻蚀玻璃)
②
④Si+4HF = SiF4↑+2H2↑ ⑦ Na H 2 SiO 233 SiO2+CaO
⑧
高温
CaSiO3
CaSiO3+CO2↑
SiO2+2NaOH = Na2SiO3+H2O SiO2+CaCO3高温
SiO2+2OH-= SiO32-+H2O ※⑦Na2SiO3+2HCl = H2SiO3↓+2NaCl SiO2+Na2CO3高温
Na2SiO3+CO2↑ SiO32-+2H+= H2SiO3↓
※⑦Na2SiO3+H2O+CO2=H2SiO3↓+Na2CO3或Na2SiO3+2H2O+2CO2=H2SiO3↓+2NaHCO3 SiO32-+H2O+CO2=H2SiO3↓+CO32-或SiO32-+2H2O+2CO2=H2SiO3↓+2HCO3- ⑧H2SiO3+2NaOH = Na2SiO3+2H2O ⑨H2SiO3 H2SiO3+2OH-= SiO32-+2H2O 5、氯及其化合物的转化关系
点燃
⑩ ①2Fe+3Cl2 2FeCl3 2
点燃
②Cu+Cl2 CuCl2
△
H2O+SiO2
※⑥Cl2+H2O = HCl+HClO ※⑦2HClO 光照 2HCl+O2↑
⑤ ⑧ ③2FeCl3+Cu = 2FeCl2+CuCl2
ClNaClO 2 2Fe3++Cu = 2Fe2++Cu2+
④
点燃
④H2+Cl2 2HCl
或光照 △
③ ※⑤MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
CuCl2 FeCl3
+- △ 2+
MnO2+4H+2ClMn+Cl2↑+2H2O Cl2+H2O = H++Cl-+HClO 光照 2H++2Cl-+O2↑
※⑧Cl2+2NaOH = NaCl+NaClO+H2O ※⑨2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O Cl2+2OH-= Cl-+ClO-+H2O 工业制漂白粉
※⑩Ca(ClO)2+H2O+CO2 = CaCO3↓+2HClO或Ca(ClO)2+2HCl = CaCl2+2HClO Ca+2ClO+H2O+CO2= CaCO3↓+2HClO或ClO+H= HClO 漂白粉的漂白原理
向漂白粉溶液中通入过量的CO2:Ca(ClO)2+2H2O+2CO2 = Ca(HCO3)2+2HClO
--
ClO+H2O+CO2 = HCO3+HClO
2+
-
-
+
⑨Cu ⑩C
点燃
①S+O2 SO2
① S 4 ②2H2S+SO2
=3S+2H2O
② 催化剂
※③SO2+O22SO3
加热
④SO3+H2O = H2SO4 ⑤SO2+CaO
△
CaSO3 或 SO2+Ca(OH)2 = CaSO3↓+H2O
△
SO3+CaO = CaSO4 SO2+Ca2++2OH-=CaSO3↓+H2O SO3+Ca(OH)2 = CaSO4+H2O ⑦2CaSO3+O2CaSO4
※⑧SO2+Cl2+2H2O = H2SO4+2HCl ※⑨Cu+2H2SO4(浓 SO2+Cl2+2H2O = 4H++SO42-+2Cl- Cu+2H2SO4(浓※⑩C+2H2SO4(浓)
△
△
CuSO4+SO2↑+2H2O
△
2++SO42-+SO2↑+2H2O
2↑+2SO2↑+2H2O
7、氮及其化合物的转化关系 ⑥ ⑦ ※①N2+O2高温或放电 2NO
4Cl N2 3 ⑧ NH ※②2NO+O2 = 2NO2
⑨ ※③3NO2+H2O = 2HNO3+NO ①
3NO2+H2O =2H++2NO3-+NO
② ③
以上三个反应为“雷雨发庄稼”原理
3
扩展反应有:4NO2+O2+2H2O = 4HNO3 4NO+3O2+2H2O = 4HNO3 ※④Cu+4HNO3(浓) = Cu(NO3)2+2NO2↑+2H2O 上面两个反应主要用于气体溶于水时的计算
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O 4HNO3 光照4NO2↑+ O2↑+ 2H2O
C+4HNO3(浓)
△
2↑+2NO2↑+2H2O 浓硝酸见光易变黄的原因
催化剂 高温高压
※⑤3Cu+8HNO3(稀) = 3Cu(NO3)2+2NO↑+4H2O ⑥N2+3H2⑦NH3+HCl = NH4Cl ⑧NH4Cl
△
2NH3
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 合成氨反应是人工固氮的主要途径
NH3↑+HCl↑
△
NH3+H+ = NH4+(水溶液中) 补充:NH4HCO3 NH3↑+H2O+CO2↑
※⑧NH4Cl+NaOH +NH3↑+H2O NH4+OH
所有的铵盐都能与碱作用放出氨气,可利用此反应鉴别铵离子。
△
氨气与酸均能反应生成铵盐,且与挥发性酸 铵盐受热都易分解,但并不是所有的铵盐 (如浓HCl、浓HNO3)相遇时空气中有白烟 都分解出氨气,如NH4NO3、(NH4)2SO4
△ △ +-
NH3↑+H2O
※⑧⑶2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
实验室制氨气,此反应为固体反应,不能写成离子方程式。
催化剂
☆⑨4NH3+5O2△ 4NO+6H2O 氨的催化氧化反应,工业制硝酸的第一步。 注:带“※”的反应为重要反应,必须熟记。
