一、化学方程式 总结
(1) 硫酸根离子的检验: BaCl2 + Na2SO4 = BaSO4↓+ 2NaCl
(2) 碳酸根离子的检验: CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
(3)  碳酸钠与盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
碳酸钠与盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(4) 木炭还原氧化铜: 2CuO + C 2Cu + CO2↑
(5) 氯化钙与碳酸钠溶液反应:CaCl2 + Na2CO3高温 CaCO3↓+ 2NaCl
(6) 氧化物的反应
a) 氧化铁与盐酸反应:Fe2O3 + 6HCl = 2FeCl3 + 3H2O
b) 氧化钙与水反应:CaO + H2O = Ca(OH)2
c) 氧化铝与盐酸反应:Al2O3 + 6HCl = 2AlCl3 + 3H2O
d) 氧化铝与氢氧化钠溶液反应:Al2O3 + 2NaOH = 2NaAlO2 + H2O
(7) Na的化学反应方程式
a)
 钠在空气中:4Na + O
2 = 2Na
2O
钠在空气中:4Na + O
2 = 2Na
2O
b)  钠与空气中燃烧反应: 2Na + O2 Na2O2
钠与空气中燃烧反应: 2Na + O2 Na2O2
c) 钠与水反应:2Na + 2H2O = 2NaOH + H2↑
d) 过氧化钠与水反应:2Na2O2 +2H2O = 4NaOH + O2↑
e) 过氧化钠与二氧化碳反应:2Na2O2 + 2CO2 = 2Na2CO3 + O2
f) 碳酸钠与二氧化碳:Na2CO3+H2O+CO2=2NaHCO3
g) 氢氧化钠与少量二氧化碳:2NaOH+CO2=Na2CO3+H2O
h) 氢氧化钠与过量二氧化碳:NaOH+CO2=NaHCO3
i) 侯氏制碱法:①NaCl(饱和)+NH3+H2O+CO2=NH4Cl+NaHCO3↓
 ②2NaHCO3 Na2CO3+H2O+CO2↑
②2NaHCO3 Na2CO3+H2O+CO2↑
j) 足量的CO2通入饱和碳酸钠溶液中: CO2+2Na++CO32-+H2O=2NaHCO3↓
(8) Fe及化合物的化学反应方程式
a) 铁与水蒸气反应:3Fe + 4H2O(g) 高温Fe3O4 + 4H2
b) 铁片与硫酸铜溶液反应: Fe + CuSO4 = FeSO4 + Cu
c) 氧化铁与盐酸反应:Fe2O3 + 6HCl = 2FeCl3 + 3H2O
d) 氯化铁与氢氧化钠溶液反应:FeCl3 + 3NaOH = Fe(OH)3↓+ 3NaCl
e) 硫酸亚铁与氢氧化钠溶液反应,后被氧化成氢氧化铁:
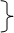 FeSO4 + 2NaOH = Fe(OH)2↓+ Na2SO4
FeSO4 + 2NaOH = Fe(OH)2↓+ Na2SO4
4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3 先生成白色沉淀,后迅速变成灰绿色最后变成红褐色
f)  氢氧化铁加热分解:2Fe(OH)3 Fe2O3 + 3H2O
氢氧化铁加热分解:2Fe(OH)3 Fe2O3 + 3H2O
g) 三氯化铁溶液与铁粉反应:2FeCl3 + Fe = 3FeCl2
h) 氯化亚铁中通入氯气:2FeCl2 + Cl2 = 2FeCl3
i) 氯化亚铁与过氧化氢:2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O
(9) Al及其化合物的化学反应方程式
a) 铝与氢氧化钠溶液反应:2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
b) 实验室制取氢氧化铝: Al2(SO4)3 + 6NH3·H2O = 2Al(OH)3↓ + 3(NH4)2SO4
c) 氢氧化铝与盐酸反应:Al(OH)3 + 3HCl = AlCl3 + 3H2O
d)  氢氧化铝与氢氧化钠溶液反应:Al(OH)3 + NaOH = NaAlO2 + 2H2O
氢氧化铝与氢氧化钠溶液反应:Al(OH)3 + NaOH = NaAlO2 + 2H2O
e) 氢氧化铝加热分解:2Al(OH)3 Al2O3 + 3H2O
f) 氧化铝与盐酸:Al2O3+6HCl=2AlCl3+3H2O
g) 氧化铝与氢氧化钠:Al2O3+2NaOH=2NaAlO2+H2O
h) 偏铝酸钠与盐酸:NaAlO2+HCl+H2O =Al(OH)3↓+NaCl
i) 偏铝酸钠与过量二氧化碳:NaAlO2+2H2O+CO2(过)=Al(OH)3↓+NaHCO3
j) 氯化铝与过量氢氧化钠: AlCl3+4NaOH(过)= NaAlO2+3NaCl+2H2O
(10) 硅及硅化合物、冶炼纯硅
a) 硅与氟气反应:Si + 2F2 = SiF4
b) 硅与氢氟酸反应:Si+4HF = SiF4↑+2H2↑
c) 硅与氢氧化钠溶液:Si + 2NaOH + H2O = Na2SiO3 +2H2↑
d) 二氧化硅与氢氟酸反应:SiO2 + 4HF = SiF4 + 2H2O
e) 二氧化硅与氢氧化钠溶液反应:SiO2 + 2NaOH = Na2SiO3 + H2O
f) 二氧化硅与氧化钙高温反应:SiO2 + CaO高温 CaSiO3
g) 硅酸钠与盐酸反应:Na2SiO3 + 2HCl = 2NaCl + H2SiO3↓
h) 往硅酸钠溶液中通入少量二氧化碳: Na2SiO3 + CO2 + H2O = Na2CO3 + H2SiO3↓
i) 往硅酸钠溶液中通入过量二氧化碳: Na2SiO3 + 2CO2 + 2H2O = 2NaHCO3 + H2SiO3↓
j) 二氧化硅与碳酸钠固体:SiO2+Na2CO3 Na2SiO3+CO2↑
Na2SiO3+CO2↑
k) 硅单质的实验室制法:
粗硅的制取:SiO2 + 2C 高温电炉 Si + 2CO
(石英砂)(焦碳) (粗硅)
l) 粗硅转变为纯硅:Si(粗) + 2Cl2△ SiCl4 SiCl4 + 2H2高温Si(纯)+ 4HCl
(11) 氯及其化合物的反应方程式
a) 氯气与金属铁反应:2Fe + 3Cl2点燃 2FeCl3
b) 氯气与金属铜反应:Cu + Cl2点燃 CuCl2
c) 氯气与金属钠反应:2Na + Cl2点燃2NaCl
d) 氯气与水反应:Cl2 + H2O ? HCl + HClO
e) 次氯酸光照分解:2HClO 光照 2HCl + O2↑
f) 氯气与氢氧化钠溶液反应:Cl2 + 2NaOH = NaCl + NaClO + H2O
g) 氯气与消石灰反应:2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
h) 盐酸与硝酸银溶液反应:HCl + AgNO3 = AgCl↓ + HNO3
i) 漂白粉长期露置在空气中:Ca(ClO)2 + H2O + CO2 = CaCO3↓ + 2HClO
(12)氮及其化合物的反应方程式
a) 氮气与氧气在放电下反应:N2 + O2放电 2NO
b) 氮气与氢气:N2+3H2 2NH3
2NH3
c) 一氧化氮与氧气反应:2NO + O2 = 2NO2
d) 二氧化氮与水反应:3NO2 + H2O = 2HNO3 + NO
e) 氨气与氯化氢反应:NH3 + HCl = NH4Cl (遇挥发性酸(如浓HCl、浓HNO3)时空气中有白烟)
f) 氨水受热分解:NH3·H2O △ NH3↑ + H2O
g) 氯化铵受热分解:NH4Cl △NH3↑ + HCl↑(不可用于制备氨气)
h) 碳酸氢氨受热分解:NH4HCO3△ NH3↑ + H2O↑ + CO2↑
(铵盐受热都易分解,但并不是所有的铵盐都分解出氨气,如NH4NO3、(NH4)2SO4)
i) 硫酸铵与氢氧化钠反应: (NH4)2SO4 + 2NaOH= 2 NH3·H2O+ Na2SO4 + 2H2O
j) 硝酸铵与氢氧化钠反应:NH4NO3 + NaOH △ NH3↑ + NaNO3 + H2O
k) 氨气的实验室制取:2NH4Cl + Ca(OH)2△ CaCl2 + 2H2O + 2NH3↑
l) 氨的催化氧化:4NH3+5O2 4NO+6H2O
4NO+6H2O
m) NO、NO2的回收:NO2 + NO + 2NaOH = 2NaNO2 + H2O
n) 浓硝酸见光分解:4HNO3 光照4NO2↑+ O2↑+ 2H2O
o) 浓硝酸与铜反应:Cu + 4HNO3(浓) = Cu(NO3)2 + 2H2O + 2NO2↑
p) 稀硝酸与铜反应:3Cu + 8HNO3(稀)=3Cu(NO3)2 + 4H2O + 2NO↑
q) 碳和浓硝酸反应:C+4HNO3(浓) △CO2↑+2NO2↑+2H2O
r) 少量铁和稀硝酸反应: Fe + 4HNO3(稀)=Fe(NO3)3 + NO↑+ 2H2O
s) 过量铁和稀硝酸反应: 3Fe(过) + 8HNO3(稀) = 3Fe(NO3)2 + 2NO↑+ 4H2O
(13) 硫及其化合物的化学反应方程式
a) 硫化氢和二氧化硫: 2H2S+SO2=3S+2H2O
b) 二氧化硫与氧气:SO2+O2 2SO3
2SO3
c) 二氧化硫与水反应:SO2 + H2O ? H2SO3
d) 二氧化硫与氯水:SO2 + Cl2 + 2H2O = 2HCl + H2SO4
e) 二氧化硫与碘水:SO2 + I2 + 2H2O = 2HI + H2SO4
f) 二氧化硫与氧化钙:SO2+CaO △CaSO3 (脱硫剂)
g) 亚硫酸钙与氧气:2CaSO3+O2= 2CaSO4
h) 浓硫酸与铜反应:Cu + 2H2SO4(浓) △ CuSO4 + 2H2O + SO2↑
i) 浓硫酸与木炭反应:C + 2H2SO4(浓) △CO2 ↑+ 2SO2↑ + 2H2O
j) 硫酸铵与氢氧化钠反应: (NH4)2SO4 + 2NaOH △ 2NH3↑ + Na2SO4 + 2H2O
(14)铜的化学反应方程式
1)Cu
2Cu+O2加热 1373K 2CuO
2Cu+O2+H2O+CO2=Cu2(OH)2CO3
(碱式碳酸铜)
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
Cu+Cl2点燃CuCl2
2Cu+4HCl+O2=2CuCl2+2H2O
Cu+2FeCl3=2FeCl2+CuCl2

 2H2SO4(浓)+Cu CuSO4+2H2O+SO2↑
2H2SO4(浓)+Cu CuSO4+2H2O+SO2↑
2Cu+2H2SO4(稀)+O2 2CuSO4+2H2O
2)氢氧化铜和氧化铜
4CuO==Cu2O+O2↑(>1273K)
Cu(OH)2=CuO+H2O (353K)
Cu(OH)2+H2SO4=CuSO4+2H2O
Cu2+ + 2OH- =Cu(OH)2↓
3)硫酸铜
(a)无水硫酸铜为白色粉末;其晶体俗名为胆矾或蓝矾;其水溶液呈蓝色
 (b)硫酸铜的制备: Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
(b)硫酸铜的制备: Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
 2Cu+2H2SO4(稀)+O2 2CuSO4+2H2O
2Cu+2H2SO4(稀)+O2 2CuSO4+2H2O
(c) 硫酸铜的加热:CuSO4==CuO+SO3↑(无水硫酸铜>923K时,分解成CuO)
 或者:2CuSO4 2CuO+2SO2↑+O2↑(加热)
或者:2CuSO4 2CuO+2SO2↑+O2↑(加热)
(15)
 铁的化学方程式
铁的化学方程式
1) 铁在氯气中燃烧 2Fe +3Cl2 ===2FeCl3
2)  铁与硫反应 Fe + S FeS
铁与硫反应 Fe + S FeS
3) 铁与水反应 3Fe + 4H2O(g) 高温 Fe3O4 +4H2
4) 铁与非氧化性酸反应 Fe +2HCl = FeCl2 + H2↑
5) 铁和稀硝酸反应: Fe + 4HNO3(稀,过量)=Fe(NO3)3 + NO↑+ 2H2O
6) 铁和稀硝酸反应: 3Fe(过量) + 8HNO3(稀) = 3Fe(NO3)2 + 2NO↑+ 4H2O
7) 铁与硫酸铜反应 Fe + CuSO4 = FeSO4 + Cu
8) 氧化亚铁与酸反应 FeO +2HCl = FeCl2 + H2O
3FeO + 10HNO3(稀) = 3Fe(NO3)3 + NO↑+ 5H2O
9) 氧化铁与酸反应 Fe2O3 + 6HNO3 = 2Fe(NO3)3 + 3H2O
Fe2O3+6HCl(稀)=2FeCl3+3H2O (除锈,还要用水冲洗)
Fe2O3+6HI=2FeI2+I2+3H2O
Fe2O3+3H2SO4(稀) =Fe2(SO4)3+3H2O
10)  氯化铁与氢氧化钠反应 FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
氯化铁与氢氧化钠反应 FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
11) 氢氧化铁受热反应 2Fe(OH)3 ==== Fe2O3 + 3H2O
12) 氢氧化亚铁转化成氢氧化铁 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
13) 氢氧化亚铁与酸反应 3Fe(OH)2+ 10HNO3 (稀)= 3Fe(NO3)3 + NO↑+ 8H2O
Fe(OH)2+H2SO4 = FeSO4+2H2O
Fe(OH)2+2HCl = FeCl2 +2H2O
14) 氢氧化铁与酸反应 Fe(OH)3 + 3HNO3 = Fe(NO3)3 + 3H2O
2 Fe(OH)3 + 6HI =2 FeI2 +I2+ 6H2O
15) 硫酸亚铁与氢氧化钠反应 FeSO4 + 2NaOH = Fe(OH)2↓+ Na2SO4
16) 氯化铁与硫氰化钾溶液反应 FeCl3 + 3KSCN = Fe(SCN)3 + 3KCl
(用硫氰化钾检测三价铁离子的存在)
17) 亚铁离子转化成铁单质 Fe2+ + Zn = Fe + Zn2+
18) 铁转化成亚铁离子 Fe + 2H+ = Fe2+ + H2↑
19) 铁离子转化成铁 Fe2O3 + 3CO 高温2Fe + 3CO2
20) 亚铁离子转化成铁离子 2Fe2+ + Cl2 = 2Fe3+ +2Cl-
21) 铁离子转化成亚铁离子 2Fe3+ + Fe =3 Fe2+
22) 氯化铁与碳酸钠溶液 2FeCl3 + Na2CO3 + 3H2O = 2Fe(OH)3↓ +3CO2↑+6NaCl
23) 亚铁离子与铁氰化钾溶液:3Fe2+ +2[Fe(CN)6]3- = Fe3[Fe(CN)6]2↓ (蓝色)
二、 高中常用的离子方程式
1) 氢氧化钡溶液与稀 H2SO4 反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
Ba(OH)2 + H2SO4 == BaSO4 + 2H2O
2) 硫酸氢钠溶液中加入氢氧化钡溶液至中性:
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O H2SO4+Ba(OH)2=BaSO4+2H2O
3) 硫酸氢钠溶液中加入氢氧化钡溶液至硫酸根沉淀完全:
H++SO42-+Ba2++2OH-=BaSO4↓+2H2O NaHSO4+ Ba(OH)2=BaSO4↓+NaOH+H2O
4) 碳酸氢钠溶液和氢氧化钠溶液混合: HCO3-+OH-=CO32-+H2O
NaHCO3+ NaOH=Na2CO3+H2O
5) 氢氧化钠溶液中加入过量碳酸氢钙溶液: Ca2++HCO3-+OH-=CaCO3↓+H2O
NaOH+CaHCO3=CaCO3↓+ Na2CO3+H2O
6) 氢氧化钠溶液中加入少量碳酸氢钙溶液:Ca2++2HCO3-+2OH-=CaCO3↓+H2O+ CO32-
NaOH+CaHCO3=CaCO3+Na2CO3+H2O
7) 澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-= CaCO3↓+H2O
Ca(OH)2+NaHCO3= CaCO3↓+NaOH+H2O
8) 澄清石灰水与过量小苏打溶液混合:Ca2++2OH-+2HCO3-= CaCO3↓+2H2O+ CO32-
Ca(OH)2+2NaHCO3= CaCO3↓+2H2O+ Na2CO3
9) 向AlCl3溶液中加入少量的NaOH溶液:
Al3+ + 3OH- = Al(OH)3↓ AlCl3+3NaOH=Al(OH)3+3NaCl
10) 向AlCl3溶液中加入过量的NaOH溶液:
Al3+ +4OH- =AlO2-+2H2O AlCl3+4NaOH= NaAlO2+3NaCl+2H2O
11) 氯化铁溶液中加过量氨水:
Fe 3++3NH3?H2O= Fe (OH)3↓+3NH4+ FeCl3+3NH3?H2O= Fe (OH)3↓+3NH4Cl
12) 氯化铝溶液中加入过量的氨水 A13++3NH3?H2O= Al(OH)3↓+3NH4+
A1Cl3+3NH3?H2O= Al(OH)3↓+3NH4Cl
13) 氯化铝溶液中加入少量的氨水(同上) A13++3NH3?H2O= Al(OH)3↓+3NH4+
A1Cl3+3NH3?H2O= Al(OH)3↓+3NH4Cl
14) 铝片溶于苛性钠溶液:2Al+2OH-+2H2O =2AlO2-+3H2↑
2Al+2NaOH+2H2O =2NaAlO2+3H2↑
(15) 金属铜与稀硝酸反应:3Cu + 8H+ + 2NO3- = 3Cu2+ +4H2O+ 2NO↑
3Cu+8HNO3(稀)=3Cu(NO3)2 + 4H2O + 2NO↑
(16) 金属铜与浓硝酸反应:
Cu + 4H+ + 2NO3- = Cu2+ + 2NO2↑ +2H2 O Cu + 4HNO3 (浓)= Cu(NO3)2 + 2NO2↑ +2H2 O
(17) 稀硝酸与过量的铁屑反应
Fe+4H++2NO3-= Fe2++2NO↑+2 H2O Fe+4HNO3(稀)= Fe(NO3)2+2NO↑+2 H2O
(18) 稀硝酸与少量的铁屑反应
Fe+4H++NO3-= Fe3++NO↑+2H2O Fe+4HNO3(稀)= Fe(NO3)3+NO↑+2H2O
(19) 氢氧化亚铁溶于稀盐酸 Fe (OH)2+2H+ = Fe2++2H2O
(20) 氢氧化亚铁溶于稀硝酸 3Fe (OH)2+10H+ + NO3- = 3Fe3++8H2O+ NO↑
(21) 向次氯酸钙溶液中通人少量的二氧化碳:Ca2++2CIO-+CO2+H2O=CaCO3↓+2HClO
(22) 向次氯酸钙溶液中通人过量的二氧化碳 CIO一+CO2+H2O= HCO3-+HClO
(23) 氯化铁溶液中加过量氨水 :A13++3NH3?H2O= Al(OH)3↓+3NH4+
(24) Na2CO3溶液与少量硝酸溶液:H+ + CO32- =HCO3-
(25) CaCO3溶液与硝酸溶液:2H+ + CaCO3 = CO2↑+ H2O+ Ca2+
(26) CaCO3溶液与醋酸溶液: 2CH3COOH+ CaCO3 =Ca2++2CH3COO-+CO2↑+ H2O
(27) 硫酸铜溶液和氢氧化钡溶液混合:Cu2+ + SO42-+Ba2+ + 2OH-= Cu(OH)2↓+ BaSO4↓
(28) 硫酸镁溶液和氢氧化钡溶液混合 Mg2++SO42-+Ba2+ +2OH-= Mg (OH)2↓+ BaSO4↓
(29) 等体积等物质的量浓度的氢氧化钡稀溶液与碳酸氢铵稀溶液混合
Ba2++2OH一+ NH4++HCO3一=BaCO3↓+H2O+ NH3?H2O
(30) 在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合 HSO3-+OH-=SO32-+H2O
(31) 在稀溶液中亚硫酸氢铵与过量氢氧化钠混合:NH4++HSO3-+2OH-=SO32-+H2O+ NH3?H2O
(32) 铜片插入硝酸银溶液中 : Cu + 2Ag+ = Cu2+ + 2Ag
(33) Cl2通入NaOH溶液: Cl2 + 2OH- Cl- + ClO- + H2O
 Cl2通入NaOH溶液,加热:3Cl2 + 6OH- 5Cl- + ClO3- +3 H2O
Cl2通入NaOH溶液,加热:3Cl2 + 6OH- 5Cl- + ClO3- +3 H2O
(34)氯化铁和铜反应: 2Fe3++Cu=2Fe2++Cu2+
(35) FeCl2溶液中通入Cl2: 2Fe2++Cl2 = 2Fe3++2 Cl-
(36) 溴化亚铁溶液中通入少量氯气:2Fe2++Cl2 = 2Fe3++2 Cl-
(37) 溴化亚铁溶液中通入过量氯气: 2Fe2++4Br-+3Cl2=2Fe3++2Br2+6 Cl-
(38) 在碘化亚铁溶液中通入少量氯气 2 I-+Cl2 = I2+2 Cl-
 (39) 在碘化亚铁溶液中通入足量氯气 :2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-
(39) 在碘化亚铁溶液中通入足量氯气 :2Fe2++4I-+3Cl2=2Fe3++2I2+6Cl-
(40) 实验室用MnO2和浓盐酸制取Cl2: MnO2+4 H++2 Cl- Mn2++Cl2↑+2H2O
(41) 足量的CO2通入饱和碳酸钠溶液中: CO2+2Na++CO32-+H2O=2NaHCO3↓
(42) 少量的CO2通入澄清石灰水中::CO2+ Ca2++2OH-=CaCO3↓+H2O
(43) 足量的CO2通入澄清石灰水中: CO2+ OH-=2HCO3-
(44) 少量的SO2通入澄清石灰水中: SO2+ Ca2++2OH-=CaSO3↓+H2O
(45) 足量的SO2通入澄清石灰水中: SO2+ OH-=2HSO3-
(46) AgNO3溶液中滴入过量氨水:Ag+ + 2 NH3?H2O = ﹝Ag(NH3)2﹞+ + 2H2O
(47) 向氯化铁溶液中加入铁粉 :2Fe3++ Fe =3Fe2+
(48) 钠和冷水反应:2Na+2H2O=2Na++2OH-+H2↑
(49) 铁粉和稀硫酸:Fe + 2H+ = Fe2+ + H2↑
(50) FeSO4酸性溶液中加过量双氧水:2Fe2++H2O2+2H+=2Fe3++2H2O
(51) 二氧化硅与氢氧化钠溶液反应: SiO2+2OH-=SiO32-+ H2O
(52) Na2O与H2O反应:Na2O+2H2O=2Na++2OH-
(53) Na2O2与H2O反应:2Na2O2+2H2O=4Na++4OH-+O2↑
(54) Al2O3与盐酸反应:Al2O3 + 6H+ =2 Al3++ 3H2O
(55) Al2O3与NaOH溶液反应:Al2O3+ 2OH-=2 AlO2-+H2O
(56) Al(OH)3与HCl反应:Al(OH)3 + 3H+= Al3++ 3H2O
(57) Al(OH)3与NaOH溶液反应:Al(OH)3 +OH- =AlO2-+2H2O
(58) Na2SiO3溶液与稀盐酸反应:SiO32-+ 2H+= H2SiO3↓
(59) Na2SiO3溶液中通入少量CO2气体:SiO32-+ CO2+ H2O = H2SiO3↓+ CO32-
Na2SiO3溶液中通入过量CO2气体:SiO32-+ 2CO2+ 2H2O = H2SiO3↓+2HCO3-
(60) Si与NaOH溶液反应:Si + 2 OH- + 2H2O= SiO32- + 2H2↑
(61) SO2通入氯水中,氯水褪色:SO2 + Cl2 + 2H2O=4H++SO42-+2 Cl-
(62) SO2通入溴水中,溴水褪色:SO2 + Br2 + 2H2O=4H++SO42-+2 Br-
(63) 氨水中滴加稀盐酸:NH3?H2O +H+=NH4++H2O
(64) 向Na2CO3溶液中滴入几滴稀盐酸(少量):H+ + CO32- =HCO3一
(65) 向Na2CO3溶液中滴入过量稀盐酸:2H+ + CO32- =CO2↑+ H2O
(66) 向Na2SO3溶液中滴入几滴稀盐酸(少量):H+ + SO32- =HSO3一
(67) 向Na2SO3溶液中滴入过量稀盐酸:2H+ + SO32- =SO2↑+ H2O
(68)向Na AlO2溶液中滴入几滴稀盐酸(少量):AlO2-+H2O +H+ = Al(OH)3↓
(69) 向Na AlO2溶液中滴入过量稀盐酸:4H+ + AlO2- =Al3++2H2O
(70) Ca(HCO3)2与硝酸反应:H+ + HCO3- =CO2↑+ H2O
(71) 铝与盐酸反应 :2Al + 6H+ = 2Al3++ 3H2↑
(72) 银与稀硝酸反应:3Ag+4H++NO3-=3Ag++NO↑+2 H2O
(73) 银与浓硝酸反应:Ag+2H++NO3-=Ag++NO2↑+ H2O
(74) AlCl3水解显酸性 :Al3++3H2O ? Al(OH)3+3H+
(75) Na2CO3水解显碱性 :CO32-+H2O ?HCO3-+OH-
(76) (NH4)2SO4水解显酸性:NH4++H2O ? NH3?H2O+H+
(77) AlCl3 与 NaAlO2溶液反应:Al3+ + 3AlO2-+6H2O=4Al(OH)3↓
(78) Al2(SO4)3与NaHCO3溶液反应 : Al3+ + 3HCO3-=Al(OH)3↓+ 3CO2↑
(79) Fe(NO3)3与NaHCO3溶液反应 :Fe3++ 3HCO3-=Fe(OH)3↓+ 3CO2↑
(80) 氯气与水反应 : Cl2 + H2O ? Cl- + H+ + HClO(次氯酸)
(81) NaHCO3与盐酸反应 :H+ + HCO3- =CO2↑+ H2O
(82) 氨水与醋酸反应:NH3?H2O+CH3COOH=NH4++CH3COO-+H2O
(83) Fe2O3 与 HI(碘化氢,碘酸)溶液反应 :Fe2O3+6H++2I-=2Fe2++I2+3H2O
(84) Fe(OH)3与 HI溶液反应 2Fe(OH)3+6H++2I-= 2Fe2++I2+6H2O
(85) 电解饱和食盐水 2Cl-+2H2O电解 Cl2↑+H2↑+2OH-
(86) 电解CuSO4溶液 2Cu2++2H2O电解2Cu+O2↑+4H+
(87) 明矾溶液加氢氧化钡至SO42-完全反应
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
(88) 明矾溶液加氢氧化钡至Al3+完全沉淀
Al3++ 2SO42-+2Ba2++3OH-=2BaSO4↓+ Al(OH)3↓
(89)硫酸氢铵与氢氧化钠等量反应 H++OH- = H2O
硫酸氢铵与氢氧化钠过量反应:H++ NH4++2OH- = H2O+NH3?H2O
(90)Cl2 + H2SO3 + H2O = 2Cl- + SO42- + 4H+
(91) Cl2 + H2S = 2Cl- + 2H+ + S↓
(92) 2Cl2 + 2Fe2+ + 2Br- = 2Fe3+ + Br2 + 4Cl- (当n(FeBr2)/n(Cl2)= 1 :1时)
(93) 8Cl2 +6Fe2+ +10Br- = 6Fe3+ + 5Br2 + 16Cl- (当n(FeBr2)/n(Cl2)= 3 :4时)
(94) 4Cl2 + 2Fe2+ + 6I- = 2Fe3+ + 3I2 + 8Cl- (当n(FeI2)/n(Cl2)= 3 :4时)
(95) ClO- + SO2 +H2O = 2H+ + Cl- + SO42-
