必修1 化学方程式汇总
一、钠及其重要化合物
1、钠与非金属的反应
4Na +O2=2Na2O (白色) 2Na + O2 Na2O2 (淡黄色) 2Na +Cl2 2NaCl 2、钠与水反应:2Na + 2H2O = 2NaOH + H2↑ (浮、熔、游、响、红)
3、 氧化钠 过氧化钠
Na2O+H2O=2NaOH 2Na2O2+2H2O=4NaOH+O2↑ Na2O+CO2=Na2CO3 2Na2O2+2CO2=2Na2CO3+O2↑ Na2O+2HCl=2NaCl+H2O 2Na2O2+4HCl=4NaCl+2H2O+O2↑
6、Na2CO3和NaHCO3
①、与酸的反应
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H 2O+CO2↑(反应速率更快)
②、与碱的反应
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O
NaHCO3+NaOH = Na2CO3+H2O
③、与盐的反应
Na2CO3+CaCl2=2NaCl+CaCO3↓
Na2CO3+BaCl2=2NaCl+BaCO3↓
④、相互转化
2NaHCO2CO3+H2O+CO2↑ (加热分解)
Na2CO3+H2O+CO2=2NaHCO3 (向Na2CO3溶液中通入足量的CO2)
二、铝及其重要化合物 (结合Al2O3 和Al(OH)3的两性进行记忆!)
1、铝与非金属: 4Al + 3O2 错误!未找到引用源。2Al2O3 2、铝与弱氧化性酸:2Al + 6HCl == 2AlCl3 + 3H2↑ 2Al+6H+ == 2Al3++3H2 ↑ 铝与强氧化性酸:钝化(浓H2SO4、浓HNO3)
--3、铝与碱:2Al+2NaOH +2H2O==2NaAlO2 + 3H2↑ ; 2Al+2H2O+2OH==2AlO2+3H2↑
4 ①、氧化铝与酸反应:Al2O3 + 6HCl == 2AlCl3 + 3H2O ②、氧化铝与碱反应:Al2O3 +2NaOH == 2NaAlO2 + 2H2O
5、氢氧化铝制备:可溶性铝盐和NH3·H2O
++AlCl3+3NH3·H2O==Al(OH)3↓+3NH4Cl Al3+3NH3·H2O==Al(OH)3↓+3NH4
6、氢氧化铝的不稳定性: 2Al(OH)3 Al2O3+2H2O
7、氢氧化铝与酸反应:Al(OH)3 + 3HCl == AlCl3 + 3H2O
8、氢氧化铝与碱反应:Al(OH)3 +NaOH == NaAlO2 + 2H2O
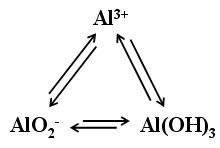
9、“铝三角”(氢氧化铝的反应在上面已经提到,略):
++AlCl3+3NaOH(少量)=Al(OH)3↓+3NaCl Al3+3OH-=Al(OH)3↓
AlCl3+4NaOH(过量)=2NaAlO2 + 2H2O +3NaCl Al3++4OH- = AlO2- +2H2O NaAlO2+HCl(少量)+H2O=Al(OH)3↓+NaCl AlO2- +H+ +H2O =Al(OH)3 ↓ NaAlO2+4HCl(过量)=AlCl3+3NaCl+2H2O AlO2- +4H+ =Al 3+ + 2H2O
10、明矾净水原理
明矾溶于水后发生电离:KAl(SO4)2==K+
+Al3++2SO42-
铝离子与水反应生成:Al(OH)3胶体:Al3+3H2O==Al(OH)3(胶体)+3H+
三、铁及其重要化合物
1、工业炼铁原理:Fe2O3+3CO2Fe+3CO2 2、铁与非金属反应:2Fe+3Cl2 2FeCl3 3Fe+2O2 Fe3O4 3、与水反应:3Fe+4H2O(g)Fe3O4+4H2 4、铁与酸反应:Fe+2HCl== FeCl2+H2↑ Fe+2H+== Fe2++H2↑
5、铁与盐溶液反应:Fe+CuSO4==Cu+FeSO4 Fe+Cu2+==Cu+Fe2+
Fe+2FeCl3 == 3FeCl2 Fe+2Fe3+ == 3Fe2+
6、铁的氧化物
Fe2O3 + 6H+ == 2Fe3+ + 3H2O FeO + 2H+ == Fe2+ + H2O
7、Fe2+与Fe3+的检验
①、Fe2+的检验:
(1) 颜色:浅绿色 (2)加NaOH溶液:先产生白色沉淀,后变成灰绿色,最后成红褐色 Fe2++2OH-== Fe(OH)2↓ (白色) 4Fe(OH)2+O2+2H2O== 4Fe(OH)3(红褐色)
(3) 先加KSCN溶液,不变色,再加新制氯水,溶液变成血红色 2Fe2++Cl2==2Fe3++2Cl- ②、Fe3+的检验
(1)颜色:棕黄色
(2)加KSCN溶液:溶液变成血红色
(3)加NaOH溶液:红褐色沉淀 Fe3++3OH-== Fe(OH)3↓
8、氢氧化铁受热分解:2Fe(OH)3 Fe2O3 + 3H2O +
9、 Fe2+与Fe3+的转化
(1)Fe2+→Fe3+ 2Fe2++Cl2==2 Fe3++2Cl-
(2) Fe3+→Fe2+ Fe+2Fe3+ == 3Fe2+
四、硅及其重要化合物
1、 二氧化硅
① 酸性氧化物:SiO2+2NaOH==Na2SiO3+H2O SiO2+CaOCaSiO3 ② 弱氧化性: SiO2 +4HF==SiF4↑+2H2O
2、硅酸盐 Na2SiO3+2HCl==H2SiO3↓+2NaCl
Na2SiO3+ CO2+H2O==H2SiO3 ↓ +Na2CO3 (酸性:H2CO3 > H2SiO3)
五、氯的重要化合物
1、氯气与金属的反应 2Fe+3Cl3 Cu+Cl2 2Na+Cl2、氯气与非金属的反应
H2+Cl2HCl 3、氯气与水的反应
Cl2+H2O错误!未找到引用源。 HCl + HClO( 次氯酸) 4、次氯酸光照分解:2HClO 2 ↑
5、Cl2与碱溶液的反应
Cl2+2NaOH=NaCl+NaO+H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O(制漂白粉)
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO(漂白原理) (酸性:H2CO3 > HClO)
六、硫及其重要化合物
1、 硫的可燃性 S+O2SO2
2、 2SO2 + O2 催化剂
加热 2SO3
3、与水反应: SO2+H2OH2SO3 SO3+H2O== H2SO4
4、与碱反应: SO2 + Ca(OH)2 = CaSO3 + H2O SO3 + Ca(OH)2 = CaSO4 + H2O
5、与碱性氧化物反应:SO2+CaO == CaSO3 SO3+CaO == CaSO4
6、浓硫酸强氧化性
C + 2H2SO4(浓) CO2↑+ 2SO2↑+ 2H2O Cu+2H2SO4(浓) CuSO4+SO2↑十2H2O
七、氮及其重要化合物
1、 合成氨: N2 + 3H2 催化剂
高温高压 2NH3
2、NH3 ①氨气与水:NH3 + H2O
②氨气与酸:NH3+HCl=NH4Cl NH3+HNO3=NH4NO3
3、铵盐与碱反应: NH3·H2O NH4 + + OH -
NH4NO3+NaOH NaNO3+NH3↑+H2O
2NH4Cl + Ca(OH)2 CaCl2 + 2NH3 ↑+ 2H2O(实验室制氨气) 4、铵盐不稳定性:NH4ClNH3↑+HCl ↑ NH4HCO3NH3+H2O+CO2 ↑ 5、HNO3强氧化性:4HNO3(浓)+Cu==Cu(NO3)3+3NO2↑+2H2O
8HNO3+3Cu==3Cu(NO3)3+2NO↑+4H2O
6、雷雨发庄稼
N2 + O2 2NO 2NO + O2 == 2NO2 3NO2 + H2O == 2HNO3 + NO
第二篇:高一化学必修1_化学方程式汇总(练习)
《化学必修1》方程式总结(练习)
第一、二章: H+、OH-、Cl-、SO42- 、HCO3-、CO32-、银离子的检验
第三章:
一. 钠
1. 钠在空气中燃烧(黄色的火焰): Na+O2 2. 钠块在空气中变暗: Na+O2=
3. 钠与水反应(浮、熔、游、响、红): Na+H2O= Na+H2O=
Na2O 、Na2O2的相关反应:
4. 碱性氧化物Na2O与水的反应 :Na2O+H2O=
5. 过氧化钠与水的反应(放热反应、Na2O2是强氧化剂,可用于漂白)
Na2O2 + H2O = Na2O2 + H2O =
6. 碱性氧化物Na2O与CO2的反应:Na2O + CO2 =
7. 过氧化钠在潜水艇中作为供氧剂原因是: Na2O2 + CO2 =
9. Na2O+HCl= Na2O2 +HCl=
10. 小苏打受热分解:NaHCO3

-- 11. 氢氧化钠和碳酸氢钠溶液:NaHCO3+NaOH= HCO3+OH=
12. 向NaOH溶液中通入少量CO2 :NaOH + CO2 =
14. 继续通入过量CO2 :Na2CO3 + CO2 + H2O = (总反应式:NaOH+CO2=NaHCO3)
15. 苏打(纯碱)与盐酸反应:
①盐酸中滴加纯碱溶液:Na2CO3+HCl = ↑ CO32 +2H+ = -
②小苏打与盐酸反应:NaHCO3+HCl= HCO3+H+= -
16. Na2CO3溶液、NaHCO3溶液与CaCl2反应:(用CaCl2或BaCl2鉴别Na2CO3溶液、NaHCO3)
Na2CO3 +CaCl2= (NaHCO3溶液与CaCl2 不反应)
二. 经典Al三角:
17. 铝与氢氧化钠:Al+NaOH+H2O=
Al+OH-+H2O=
18. 不稳定性:2Al(OH)3 △
19. 硫酸铝溶液中滴过量氨水(实验室制备Al(OH)3)
化学《必修Ⅰ》方程式总结
第1页 共4页
Al2(SO4)3 +6NH3·H2O= Al3++3NH3·H2O=
20. 氧化铝溶于氢氧化钠溶液:Al2O3+NaOH= Al2O3+OH-=
21. 氧化铝溶于盐酸:Al2O3 + HCl= Al2O3 + H+=
22、Al(OH)3溶液中加盐酸: Al(OH)3+HCl= Al(OH)3+H+=
23. Al(OH)3与NaOH溶液:Al(OH)3+NaOH= Al(OH)3+OH-=
三. 铁及其重要化合物:
㈠.铁单质:
24. 铁与硫加热反应:

Fe + S
26. 铁与氧气加热反应:Fe+O2

25. 铁在氯气中加热反应:Fe+Cl2
高温
27. 高温下铁与水蒸气反应:Fe + H2O(g)
㈡.铁的氧化物FeO 、Fe2O3 、Fe3O4溶于盐酸中:
28. FeO + HCl = FeO + H+ =
29. 铁锈用盐酸浸泡(除)铁锈:Fe2O3+HCl= Fe2O3+H+=
30. 磁铁矿与盐酸:Fe3O4+HCl= Fe3O4+H+= ㈢.Fe(OH)2、Fe(OH)3 的制备:
31. 氯化铁中滴氢氧化钠溶液(红褐色沉淀)
FeCl3 + NaOH = Fe3+ + OH= -
32. 氢氧化亚铁在空气中被氧化:Fe(OH)2 + O2 + 2H2O =
33. 不稳定性:

Fe(OH)3
㈣.Fe2+ 、Fe3+ 之间的转化:
34. 氯化亚铁溶液中通入氯气(或氯水):FeCl2 + Cl2 = Fe2++Cl2=
35. 氯化铁溶液中加入铁粉:FeCl3 + Fe = Fe3+ + Fe =
36. 用KSCN检验Fe3+的存在:离子方程式:Fe3++3SCN-= Fe (SCN)3 (血红色)
37. 印刷电路板:FeCl3 + Cu =
化学《必修Ⅰ》方程式总结
第2页 共4页
第四章:
一. 无机非金属材料的主角——硅
38. 工业制单质硅(碳在高温下还原二氧化硅):SiO2+C 2. Si及其化合物:
(一)二氧化硅
39. 二氧化硅与氢氧化钠反应:SiO2+2NaOH= SiO2+2OH=
40. 二氧化硅与氧化钙高温反应:SiO2 + CaO 41. 二氧化硅与氢氟酸反应:SiO2 + HF =
(二)硅酸(H2SiO3)
42. 往硅酸钠溶液中通入二氧化碳:Na2SiO3 + CO2 + H2O =
43. 硅酸钠与盐酸反应:Na2SiO3 + HCl =
44. 硅酸受热分解:H2SiO3 △
高温 (硅单质的实验室制法) -高温 SiO2 + H2O
高温
45. 工业制玻璃原理:SiO2+Na2CO3 二. 富集在海水中的元素——氯
(一)氯气 SiO2+CaCO3 高温
46. 氯气实验室制法:(仪器:分液漏斗,圆底烧瓶)MnO2 +HCl(浓

) ⑴氯气性质:
A.金属和氯气的反应:
47. 铜丝在氯气中燃烧(棕色烟):Cu+Cl2
48. 铁在氯气中燃烧:Fe + Cl2
B.氯气与水反应 点燃 点燃
49. 氯气溶于水(新制氯水中含H+ 、Cl 、ClO 、OH、Cl2、HClO、H2O) --- Cl2 + H2O = Cl2 + H2O =
化学《必修Ⅰ》方程式总结
第3页 共4页
新制氯水注入盛溴化钠溶液的试管中
50. Cl2 + NaBr = Cl2 + 2Br =
51. Cl2 + NaI = Cl2 +I =
52. 次氯酸见光分解(强氧化剂、杀菌消毒,漂白剂):2HClO
C.氯气和碱和的反应:
53. 工业制漂白粉的原理:Ca(OH)2 + Cl2 =
Ca(OH)2 +Cl2 =
54. 漂白粉长期置露在空气中失效的原理:
Ca(ClO)2+CO2+H2O= Ca2+ClO + CO2 + H2O = +---
55. 制漂白液(或氯气尾气处理): Cl2 +NaOH =
三. 硫和氮的化合物:
56. 硫与非金属:S + O2 点燃
(还原性)
△
57. 硫与金属(氧化性): Fe + S 2Cu + S △
58. 二氧化硫与水反应:SO2 + H2O
59. 二氧化硫与碱性氧化物反应:SO2 + CaO =
60. 二氧化硫与碱反应:SO2 + NaOH = SO2 + Ca(OH)2 =
61. 二氧化硫通入氯水中:SO2 + Cl2 + H2O = (Cl2可换作Br2、I2)
62. 二氧化硫被O2氧化:SO2 + O2
63. 三氧化硫与水:SO3 + H2O =
84. 三氧化硫与碱:SO3+Ca(OH)2 =
64. 工业合成氨:N2 + H2 催化剂
高温高压
第4页 共4页 65. 氨的催化氧化 :NH3 +O2 化学《必修Ⅰ》方程式总结
66. NH3在水中的反应:NH3 + H2NH3? H2O NH4+ + OH -
67. 氨水受热分解:NH3?H2O △
68. 实验室制取氨气:NH4Cl + Ca(OH)2
69. 碳酸氢铵受热分解 :NH4HCO3 △ △
70. 用浓盐酸检验氨气(白烟生成): HCl + NH3 =
71.氯化铵受热分解:NH4Cl △
72. 硝酸铵溶液与氢氧化钠溶液混合(不加热)(检验NH4+的方法)
NH4NO3 + NaOH = NH4+ + OH-=
73. 氮气和氧气放电下反应(雷雨发庄稼)N2 + O2 2NO + O2
74. 二氧化氮溶于水:NO2 + H2O NO2 + H2O
75. NO2 、O2 的混合气通入水中无剩余气体 : NO2 + O2 + H2O =
76. NO 、O2 的混合气通入水中无剩余气体 : NO + O2 + 2H2O =
四.浓硫酸、HNO3与Cu反应:
Al、Fe遇浓HNO3、浓硫酸钝化(常温)
77. Cu与浓HNO3加热:Cu+HNO3 (浓)
78. Cu与稀HNO3反应:Cu+HNO3 (稀)=
79. 铜与浓硫酸反应:Cu+H2SO4 (浓)
80. 浓硫酸与木炭反应:C+H2SO4(浓)
81. 浓硝酸与木炭反应:C+HNO3(浓)
化学《必修Ⅰ》方程式总结
第5页 共4页

