实验 氢氧化钠标准溶液的配制与标定
一、实验目的
1、掌握氢氧化钠滴定液的配制和标定方法。
2、巩固用递减法称量固体物质。
3、熟悉滴定操作并掌握滴定终点的判断。
4、本实验需4学时。
二、仪器与试剂
仪器:分析天平、台秤、滴定管(50mL)、玻棒、量筒、试剂瓶(1000mL)、电炉、表面皿、称量瓶、锥形瓶
试剂:固体NaOH、基准邻苯二甲酸氢钾、纯化水、酚酞指示剂
三、原理与方法
NaOH易吸收空气中CO2而生成Na2CO3,反应式为:
2NaOH + CO2 = Na2CO3 + H2O
由于Na2CO3在饱和NaOH溶液中不溶解,因此将NaOH制成饱和溶液,其含量约52%(w/w),相对密度为1.56。待Na2CO3沉待淀后,量取一定量的上清液,稀释至一定体积,即可。用来配制NaOH的纯化水,应加热煮沸放冷,除去水中CO2。
标定NaOH的基准物质有草酸(H2C2O4·2H2O)、苯甲酸(C7H6O2)、邻苯二甲酸氢钾(KH C8H4O4)等。通常用邻苯二甲酸氢钾标定NaOH滴定液,标定反应如下:

计量点时,生成的弱酸强碱盐水解,溶液为碱性,采用酚酞作指示剂。按下式计算NaOH滴定液的浓度:
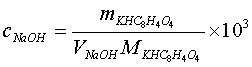
四、实验内容
1、NaOH溶液的配制
(1)NaOH饱和溶液的配制:用台称称取120g NaOH固体,倒入装有100mL纯水的烧杯中,搅拌使之溶解成饱和溶液。贮于塑料瓶中,静置数日,澄清后备用。
(2)NaOH滴定溶液的配制(0.1mol/L):取澄清的饱和NaOH溶液2.8mL,置于1000 mL试剂瓶中,加新煮沸的冷纯化水500 mL,摇匀密塞,贴上标签,备用。
2、NaOH溶液的标定
用递减法精密称取在105~110℃干燥至恒重的基准物邻苯二甲酸氢钾3份,每份约0.5g,分别置于250 mL锥形瓶中,各加纯化水50 mL,使之完全溶解。加酚酞指示剂2滴,用待标定的NaOH溶液滴定至溶液呈淡红色,且30秒不褪色,即可。平行测定三次,根据消耗NaOH溶液的体积,计算滴定液NaOH的浓度和相对平均偏差。
五、数据记录与处理
1. 记录递减法称取基准物邻苯二甲酸氢钾的质量。
2. 记录消耗NaOH滴定液的体积。
3. 计算的NaOH浓度及所标定浓度的相对平均偏差。
六、思考题

七、【注意事项】
1、固体氢氧化钠应放在表面皿上或小烧杯中称量,不能在称量纸上称量,因为氢氧化钠极易吸潮。 因而称量速度尽量快
2、滴定前,应检查橡皮管内和滴定管尖处是否有气泡,如有气泡应排除。 否则影响其读数,会给测定带来误差。
3、盛放基准物的3个锥形瓶应编号,以免混淆。 防止过失误差。
误差分析等
第二篇:实验4 NaOH标准溶液的标定
实验二 NaOH标准溶液的标定
一、实验目的
1.掌握用邻苯二甲酸氢钾标定氢氧化钠溶液的原理和方法。
2.熟练减量法称取基准物质的方法。
3.熟练滴定操作和用酚酞指示剂判断滴定终点。
二、实验原理
固体NaOH具有很强的吸湿性,且易吸收空气中的水分CO2,因而常含有Na2CO3,且含少量的硅酸盐、硫酸盐和氯化物,因此不能直接配制成准确浓度的溶液,而只能配制成近似浓度的溶液,要用基准物质进行标定,才能获得准确的浓度。 由于NaOH溶液中碳酸钠的存在,会影响酸碱滴定的准确度,在精确的测定中应配制不含Na2CO3的NaOH溶液并妥善保存。
用邻苯二甲酸氢钾基准物质标定NaOH准确浓度。邻苯二甲酸氢钾易制得纯品,在空气中不吸收水,容易保存,摩尔质量大,是一种较好的基准物质。 用邻苯二甲酸氢钾标定NaOH溶液的反应式为:
KHC8H4O4 + NaOH ==KNaC8H4O4 + H2O
由反应可知,1mol KHC8H4O4与1mol NaOH完全反应。到化学计量点时,溶液呈碱性,pH值约为9,可选用酚酞作指示剂,滴定至溶液由无色变为浅粉色,30s不褪即为滴定终点。
三、实验试剂及仪器
1.待标定的NaOH溶液
2.邻苯二甲酸氢钾基准试剂
3.酚酞指示剂
4.碱式滴定管
5.锥形瓶
6.量筒
四、实验步骤
用差减法称取KHC8H4O4基准物质约0.6g于250 mL锥形瓶中,加入50mL蒸馏水,加入2滴酚酞指示剂,用待标定的NaOH溶液滴定至呈微红色并保持30 s不褪色,平行标定3份。
五.实验要点
1.滴定之前,一定要检查滴定管下端是否有气泡。
2.由于氢氧化钠容易吸收空气中的二氧化碳,所以采用酚酞做指示剂,这样可以消除二氧化碳的影响。
3.计算NaOH溶液的浓度公式是:CNaOH=1000*mKHC8H4O4/(VNaOH* MKHC8H4O4)
六、实验数据
表1 KHC8H4O4标定NaOH溶液
编号 mKHC8H4O4/g VNaOH/mL CNaOH/(mol.L-1) CNaOH平均值/(mol.L-1)
相对标准偏差 相对标准偏差/%
1 0.6008 31.49 0.09343
2 0.5998 30.90 0.09505 0.09441
3 0.5999 31.00 0.09476
七、结果讨论
NaOH易吸收CO2和水分,所以只需要用台秤称取NaOH即可;由于NaOH固体易吸收空气中的CO2和水分,固配制NaOH标准溶液时不能用直接法;标定时,为了避免装入后的NaOH标准溶液被稀释,应用NaOH标准溶液润洗滴管2~3次;而锥形瓶中有水不会影响被测物质量的变化,所以锥形瓶不需先用标准溶液润洗或烘干;盛氢氧化钠溶液的试剂瓶应用橡皮塞,因NaOH与玻璃的成分之一SiO2作用会使塞子与瓶口粘结而打不开。橡皮塞耐碱腐蚀,但易被酸侵蚀,它与有机液体、有机蒸气接触容易发生溶胀,引起有机溶剂污染;滴定开始时,可快。由于离终点远,滴落点颜色无明显变化,但不能成“水线”,以免溶液溅出。滴落点颜色有变化或消失慢时,滴定放慢。随着终点的接近,改为
滴1滴搅几下(一滴多搅),或控制滴加速度为加1滴,经搅拌后溶液颜色稳定,下1滴正好滴下。
