氢氧化钠标准溶液的配制和标定
一、实验目的
1、掌握NaOH标准溶液的配制和标定。
2、掌握碱式滴定管的使用,掌握酚酞指示剂的滴定终点的判断。
二、实验原理
NaOH有很强的吸水性和吸收空气中的CO2,因而市售NaOH中常含有Na2CO3。
反应方程式:2NaOH+CO2→Na2CO3+H2O
由于碳酸钠的存在,对指示剂的使用影响较大,应设法除去。
除去Na2CO3最通常的方法是将NaOH先配成饱和溶液(约52%,W/W),由于Na2CO3在饱和NaOH溶液中几乎不溶解,会慢慢沉淀出来,因此,可用饱和氢氧化钠溶液,配制不含Na2CO3的NaOH溶液。待Na2CO3沉淀后,可吸取一定量的上清液,稀释至所需浓度即可。此外,用来配制NaOH溶液的蒸馏水,也应加热煮沸放冷,除去其中的CO2。
标定碱溶液的基准物质很多,常用的有草酸(H2C2O4?2H2O)、苯甲酸(C6H5COOH)和邻苯二甲酸氢钾(C6H4COOHCOOK)等。最常用的是邻苯二甲酸氢钾,滴定反应如下:
C6H4COOHCOOK+NaOH→C6H4COONaCOOK+H2O
计量点时由于弱酸盐的水解,溶液呈弱碱性,应采用酚酞作为指示剂。
三、仪器和试剂
仪器:碱式滴定管(50ml)、容量瓶、锥形瓶、分析天平、台秤。
试剂:邻苯二甲酸氢钾(基准试剂)、氢氧化钠固体(A.R)、10g/L酚酞指示剂:1g酚酞溶于适量乙醇中,再稀释至100mL。
四、 操作步骤
1、0.1mol/L NaOH标准溶液的配制
用小烧杯在台秤上称取120g固体NaOH,加100mL水,振摇使之溶解成饱和溶液,冷却后注入聚乙烯塑料瓶中,密闭,放置数日,澄清后备用。
准确吸取上述溶液的上层清液5.6mL到1000毫升无二氧化碳的蒸馏水中,摇匀,贴上标签。
2、 0.1mol/L NaOH标准溶液的标定
将基准邻苯二甲酸氢钾加入干燥的称量瓶内,于105-110℃烘至恒重,用减量法准确称取邻苯二甲酸氢钾约0.6000克,置于250 mL锥形瓶中,加50 mL无CO2蒸馏水,温热使之溶解,冷却,加酚酞指示剂2-3滴,用欲标定的0.1mol/L NaOH溶液滴定,直到溶液呈粉红色,半分钟不褪色。同时做空白试验。
五、结果结算
NaOH标准溶液浓度计算公式:
m 0.2042(V1?V2)
式中:m---邻苯二甲酸氢钾的质量(g); V1---氢氧化钠标准滴定溶液用量(mL); CNaOH?
V2---空白试验中氢氧化钠标准滴定溶液用量(mL);
0.2042---与1mmol氢氧化钠标准滴定溶液相当的基准邻苯二甲酸氢钾的质量(g)。
第二篇:氢氧化钠标准溶液
氢氧化钠标准溶液浓度测量不确定度评定报告
编制:付学飞
审核:王淑芳
批准:许百红
京博农化科技股份有限公司分析检测中心
20##-8-2
氢氧化钠标准溶液浓度测量不确定度评定报告
1目的
评定0.5mol/L氢氧化钠标准溶液浓度测量的不确定度
2依据标准
《化学试剂标准滴定溶液的制备》GB /T 601-2002
3试验条件
1) 设备名称:分析天平 设备型号:AE-240 设备编号:CARC0007
测量范围:0-200g 准确度等级或示值误差:±0.0001g 分辨率或最小分度值:0.0001g
2) 玻璃仪器名称: 50ml碱式滴定管 准确度等级:A级 最大允许误差±0.05ml
最小分度值:0.01ml
3) 工作基准试剂名称名称:基准邻苯二甲酸氢钾
3.2 检测环境条件:温度——25℃ 湿度—— 50%
3.3标准溶液编号:20110712
4过程描述与数学模型
4.1配制过程
称取110g氢氧化钠溶于100ml无二氧化碳的水中,注入聚乙烯容器中,密闭放置至溶液清亮,用塑料管量取上层清液,用无二氧化碳的水稀释至1000ml。
4.2标定过程
称取于105-110℃下用电烘箱箱至干燥的工作基准试剂邻苯二甲酸氢钾3.6g,加无二氧化碳的水溶解,加入两滴酚酞指示液(10g/L),用配制好的氢氧化钠滴定溶液滴定至浅粉色。并保持30s,同时做空白试验。
氢氧化钠标准滴定溶液的浓度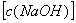 ,数值以mol/L表示,按照下式计算
,数值以mol/L表示,按照下式计算

式中:m——邻苯二甲酸氢钾的质量分数的准确值,g;
V1——滴定消耗氢氧化钠滴定溶液的体积,ml;
V2——空白试验耗用的氢氧化钠滴定溶液的体积,ml;
M——邻苯二甲酸氢钾的摩尔质量的数值,g/mol, =204.22
=204.22
5不确定度来源的分析
关于不确定度的来源可依据中国合格评定国家认可委员会制定的《化学分析中不确定度的评估指南》进行分析。氢氧化钠标准滴定溶液的浓度的测量不确定来源主要有:测定的重复性,称取邻苯二甲酸氢钾的质量(m)邻苯二甲酸氢钾的摩尔质量(M),滴定邻苯二甲酸氢钾耗用氢氧化钠标准滴定溶液的体积(V1),空白耗用的氢氧化钠标准滴定溶液的体积(V2)。
6不确定度分量的评定
6.1 氢氧化钠标准滴定溶液浓度的平均值A类标准不确定度的计算
表1是两个标准员双人八平行的测定结果
表1 0.5mol/L氢氧化钠标准滴定溶液标定结果
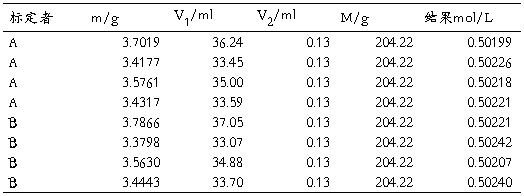
根据上述表格中的数据,氢氧化钠结果的平均值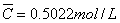 ,其标准偏差
,其标准偏差 ,其A类相对标准不确定度分量
,其A类相对标准不确定度分量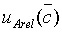 按照下式
按照下式
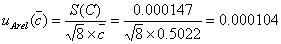
6.2标准滴定溶液浓度平均值的B类相对合成不确定度分量的计算
根据氢氧化钠标准滴定溶液的计算公式,氢氧化钠标准滴定溶液的浓度的平均值的B类相对标准不确定度分量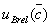 按照下式合成
按照下式合成
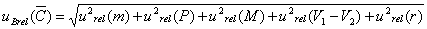
式中: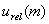 ——邻苯二甲酸氢钾质量的数值的相对标准不确定度分量;
——邻苯二甲酸氢钾质量的数值的相对标准不确定度分量;
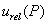 ——邻苯二甲酸氢钾的质量分数的数值的相对标准不确定度分量;
——邻苯二甲酸氢钾的质量分数的数值的相对标准不确定度分量;
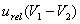 ——被标定溶液体积的数值的相对标准不确定度分量;
——被标定溶液体积的数值的相对标准不确定度分量;
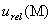 ——工作基准试剂摩尔质量数值的相对标准不确定度分量;
——工作基准试剂摩尔质量数值的相对标准不确定度分量;
 ——氢氧化钠溶液浓度的数值修约的相对标准不确定度分量。
——氢氧化钠溶液浓度的数值修约的相对标准不确定度分量。
6.2.1邻苯二甲酸氢钾质量的数值的相对标准不确定度分量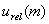
称量使用电子天平的检定证书,其最大允许误差为±0.1mg。按均匀分布,K=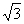 ,则标准不确定度为
,则标准不确定度为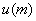 =
=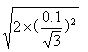 =0.082215mg
=0.082215mg
相对标准不确定度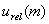 =
=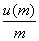 =
=
6.2.2邻苯二甲酸氢钾纯度引起的不确定度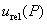
供应商(科密欧)证书上给出的邻苯二甲酸氢钾的纯度值为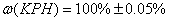 ,其引起的不确定度可考虑矩形分布,标准不确定度为:
,其引起的不确定度可考虑矩形分布,标准不确定度为:
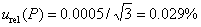
6.2.3邻苯二甲酸氢钾的摩尔质量引起的不确定度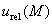
邻苯二甲酸氢钾(KPH)各组成元素的原子量及其不确定度见表2
表2 KPH各组成元素的原子量及其不确定度

对于每个元素来说,其标准不确定度可按IUPAC给出的数值以矩形分布求得,将所给出的数值除以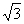 可的其标准不确定度。
可的其标准不确定度。
KPH摩尔质量及其不确定分别为:
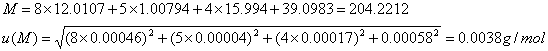
相对标准不确定度分量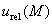 =
=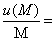
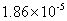
6.2.4滴定耗用的氢氧化钠标准溶液的体积引起的不确定度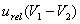
6.2.4.1 滴定耗用的氢氧化钠标准溶液的体积V1引起的不确定度
(1)滴定管体积 JJG196-2006《常用玻璃量器检定规程》中给出的50mlA级滴定管的允许差为±0.05ml,近似于三角形分布,换算成标准不确定度为: =0.05/
=0.05/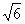 =0.020ml
=0.020ml
(2)温度引起的不确定度分量
实验室室温变化的范围为±2℃,水的膨胀系数为 ℃,近似于矩形分布,滴定0滴定大约消耗氢氧化钠标准溶液的体积的平均值为34.62ml,换算成标准不确定度为:
℃,近似于矩形分布,滴定0滴定大约消耗氢氧化钠标准溶液的体积的平均值为34.62ml,换算成标准不确定度为:
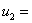

(3)终点判定偏差
多次测定的重复性表明,此步引入终点误差不大于0.010ml,该误差是由人的视觉所带来的测定误差,在滴定终点,也存在这种观测误差,前后两次引入的滴定误差为
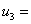
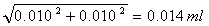
将上述将三个分量合成为体积V1的不确定度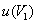 为
为
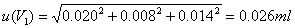
6.2.4.2 空白耗用的氢氧化钠标准溶液的体积引起的不确定度
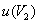 的计算和
的计算和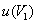 类似,由于空白耗用的氢氧化钠标准溶液的体积很小V2=0.13ml,第二项和第三项可以忽略,因此
类似,由于空白耗用的氢氧化钠标准溶液的体积很小V2=0.13ml,第二项和第三项可以忽略,因此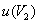 =0.020ml
=0.020ml
根据上述计算
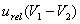 =
=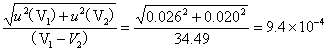
6.2.5氢氧化钠标准溶液浓度数值修约的相对标准不确定度
双人八平行测定时数值修约引入的相对标准不确定度按照下式计算
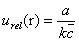
式中:a表示两人八平行实验测定的氢氧化钠标准溶液浓度平均值修约误差区间的半宽度,mol/L,结果至少保留小数点后5位,按照0.00005mol/L计算,按照均匀分布k=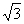 ,代入上式计算得
,代入上式计算得 =5.7
=5.7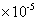
标准溶液浓度的平均值的B类相对标准不确定度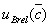 得到
得到
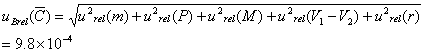
7合成不确定度
氢氧化钠标准溶液的合成不确定度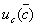 按照下式计算
按照下式计算

8扩展不确定度
当置信概率p=95%时,包含因子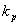 =2,计算扩展不确定度:
=2,计算扩展不确定度:
U=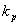 ×
×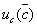 =2×
=2×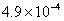 =
=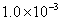
9结果报告
氢氧化钠标准滴定溶液的浓度C=0.5022±0.0010mol/L,其中扩展不确定度U=0.0010是由合成不确定度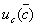 =4.9
=4.9 乘以包含因子
乘以包含因子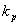 =2而得到。
=2而得到。
——以下空白——
