��ͨ��ѧʵ��Ҫ��
ʵ��ǰ�������Ԥϰ��
�� �����Ķ�ʵ��̲ġ��ο��̲ġ������е��й����ݡ�
�� ��ȷ��ʵ���Ŀ�ĺ�������Ҫ��
�� ���ձ�ʵ���Ԥ��֪ʶ��ʵ��ؼ���
�� �˽Ȿʵ������ݡ����衢������ע�����
�� д�ü�����Ҫ��Ԥϰ������ܽ���ʵ�飬������Ԥϰ������֣�Ӧֹͣʵ�飬Ҫ����Ϥʵ�����ݺ��ٽ���ʵ�顣
�� Ԥϰ���������д��ר�õĵ�ʵ���¼���ϣ����ݰ�����
һ��ʵ��Ŀ��
����ʵ��ԭ��
����ʵ��ؼ�
�ġ�ʵ�鲽�裨��������ʾ��ͼ�����˵ر�ʾ��
�塢ʵ�����ݼ�¼�����ݴ��������ñ�����ʽ��ʾ���ڱ�������¶�ע�����㹫ʽ�Լ� ���õ��������ݣ���
����˼���⣨�����������
2. ��ʵ���Ҫ��
�� ���������ϸ�Ĺ۲죬��ʵ��¼�����ó�Ϯ�������ݡ�ʵ���в�����ԭʼ���ݱ����¼��ʵ���¼���ϣ�����Ԥϰ������棩�����ý����ݼ�¼��ֽƬ�ϻ������ط�������α���Ϳ��ԭʼ���ݡ�
�� �����Ķ���ʵ���ҹ��͡�ʵ����ѧ����֪����Ҫ����ʵ���ƶȣ��������õĿ�ѧʵ��ϰ�ߣ�ʵ���б����ྲ�����ع���ע�ⰲȫ�������Լ��
�� ʵ�������Ӧ����˼������ϸ�����������Լ�������⣬�������Խ����������ʱ�������ʦָ�㡣
�� �����ʵ������涨�����ʵ��ʱ��Ӧ�Ⱦ�ָ����ʦ������
�� ʵ�����ҩƷ�����Ҫ��ʱ�Ż�ԭ����
�� ����Я������Ʒ����������÷�����ʵ��̨���ϣ�Ӧ����ʵ��̨����ij���� �� ʵ�����ڲ��Զ�����ˮ�����������ա�
�� ʵ����Ϻ����������Ż�ԭ����λ�ã��������棬���ʵ���¼����������ָ����ʦ�������ֵ���������ɨ������װȥ����ˮ������ˮ�ط����������
�� ʵ�鲻�óٵ���ȱ�Ρ��ٵ�5����ȡ���˴�ʵ���ʸ����ش����鲻����ʵ��
�εģ�����������������ʽ����ʦ��٣������Կ�ͷ��ʽ�ñ���֪ͨ��ʦ���Ժ���ָ����ʦ��ϵ�ٲ�����ȱʵ�顣��ʲ��ܰ�ʱ�ϿΡ��������˴���ʵ���ߣ�һ�������ȡ�������ʵ���ʸ�
�� ʵ����ɺ�����ʵ����ʦͬ�ⷽ���뿪ʵ���ң�����˽���뿪������ʵ���
����������
3. ��ʵ�鱨���Ҫ��
ʵ�������Ӧ�ϸ�ظ���ʵ���¼���ݽ��д����ͼ��㣬������Ӧ�Ľ��ۣ�����ʵ���е�����������ۣ��������ʵ�鱨�棬��ʱ����ָ����ʦ���ġ�
��д����Ӧ�ּ���������Ҫ��������ࡣʵ�鱨��д���ʲ��ߣ�Ӧ��д��ʵ�鱨���������dz�Ϯ���˵Ļ���α��ģ�ʵ��ɼ���Ϊ��0���֡�
ʵ�鱨��������������ݣ�
һ��ʵ��Ŀ��
����ʵ��ԭ��
����ʵ���������Լ�����Ҫ��
�ġ�ʵ�鲽���ʵ������
����ʵ������еIJ���������ʵ��ϸ�ؼ�¼��
�塢ʵ�����ݴ����ͽ������
ʵ�����ݴ������ñ�����ʽ��ʾ�������е������������������������ڱ�������¶�ע�����㹫ʽ�Լ����õ��������ݡ�
�������Ҫ���ʵ�����Ŀɿ���������Խ������ۣ����������۲쵽��ʵ������
����ʵ�����ͽ���
��Ա�ʵ�����������������⣬����Լ��ļ�����ջ�Ҳ�ɶ�ʵ�鷽����ʵ����������Լ��ļ��⣬��ѵ������˼ά�ʹ��������кΰ�����
�Ȼ��Ƶ��ᴿ
ʵ��Ŀ��
1�������ᴿNaCl��ԭ���ͷ�����
2��ѧϰ�ܽ⡢��������ѹ���ˡ�����Ũ�����ᾧ�Ȼ���������
ʵ��ԭ��
��ѧ�Լ���ҽҩ�õ�NaCl�����Դ�ʳ��Ϊԭ���ᴿ�ģ���ʳ���к���Ca2+��Mg2+��K+��SO42-�ȿ��������ʺ���ɳ�Ȳ��������ʡ�ѡ���ʵ����Լ���ʹCa2+��Mg2+��
SO42-���������������γ�������ȥ��һ������ʳ����Һ�м�BaCl2��Һ����ȥSO42-���ӣ�
Ba2+ + SO42- = BaSO4��
Ȼ��������Һ�м�Na2CO3��Һ����Ca2+��Mg2+������Ba2+��
Ca2+ + CO32- = CaCO3��
Ba2+ + CO32- = BaCO3��
2Mg + 2OH + CO3 = Mg2(OH)2CO3��
������Na2CO3��Һ��HCl�кͣ���ʳ���е�K+��������Һ�С�����KCl�ܽ�ȱ�NaCl���Ҵ�ʳ���к����٣�������������Ũ��ʳ����Һʱ��NaCl�Ƚᾧ��������KCl��������Һ�С�
��ѹ���˲������ܽ�Ϊ��һ�ǡ��������͡��͡�����������һ�ǡ�����ֽ���۵��������©���ĽǶ������ʹ������©���ڣ�����ˮʪ�����͡�����ֽ�ı�Ե�����©����5�������ң�©����Һ����Ҫ�Ե�����ֽ��Ե���Է����������Һ�����������ǹ���ʱ��ʢ������Һ���ձ���Ͳ��������Һ���ز���������������������ĩ�˺���ֽ���㲿�����©���¶˵Ĺܿ�������װʢ��Һ���ձ��ڱ����ʹ���˺����Һ��ϸ����©�������ձ��ڱ������ձ��С�
����ʱ����©����©�����ϣ�©��������������������ò���������������ֽһ�ߣ�a.�����ز�����������ϲ���Һ��һ���������Һһ�����ֻ������ֽ��2/3����������������ëϸ����Խ����ֽ���ض���ʧ��������ɺ����ձ��ڽ�����������ϴ��Һ����ϴ�ӣ����ó����������Ϸ��������Һ�����3-4�Ρ����������������������·���ȫ��ת�Ƹɾ������ֳ��ձ���б������©���Ϸ����ձ�������©������ʳָ��������������ձ����ϣ����������¶�������ֽ�����㴦����ϴƿ����ϴҺ����ϴ�ձ��ڱڣ�������ͬ��Һ�ز���������©���С�B.����ȫ��ת�Ƶ���ֽ���Ժ���������ֽ��ϴ�ӳ������Գ�ȥ�����������������ʺͲ�����ĸҺ���䷽���Ǵ���ֽ�������²�λ��ʼ����ϴƿ������ˮ�����������������ƶ���2+-2-
����˽��������е���ֽ����²���ϴ��ʱӦע�⣬����ʹϴ��ҺͻȻ���ڳ�����
ע�⣺1.Ϊ�����ϴ��Ч�ʣ�ÿ��ʹ������ϴ��Һ��ϴ�������ɣ���ϴ���Σ�ͨ����Ϊ��������Ρ���ԭ��
2.����ϴ��������øɾ����Թܽ�ȡ������Һ��ѡ�������Ķ��Է�Ӧ�����鹲�����ӣ��ж�ϴ���Ƿ���ɣ���������ʧ�� ���ĺ�ҩƷ
1������
��ż��Ƚ�������ѭ��ˮ�ã�����ƿ������©������ͨ©�����ձ���������̨�ӣ���ֽ��pH��ֽ��
2��ҩƷ
NaCl(��)��
ʵ�鷽��
һ��NaCl���ᴿ
1�������ܽ�
��ȡ5g��ʳ����50mL�ձ��У�����20mLˮ���õ�ż��Ƚ�����(��ƾ���)���Ƚ���ʹ���ܽ⡣
2����SO42-
������Һ���У��߽���ߵμ�1mol��L-1 BaCl2��ҺԼ3��4mL����������5min��
ʹ���������������ڳ�����
3�����SO42-�Ƿ����
����Ž�����(��ƾ���)�ƿ�����������ȡ��������Һ�Ӽ���6mol��L-1 HCl���ټӼ���1mol��L-1 BaCl2��Һ�����л��ǣ���ʾSO42-��δ���������ټ�BaCl2��Һֱ����ȫ����SO42-��
4����Ca2+��Mg2+������Ba2+
��������Һ�������У��߽���ߵμӱ���Na2CO3��Һ��������Na2CO3��Һ�����ɳ���Ϊֹ���ٶ��0.5mL Na2CO3��Һ�����á�
5�����Ba2+�Ƿ����
�õι�ȡ����Һ�����Թ��У��ټӼ���3mol��L-1 H2SO4�����л���������
��ʾBa2+δ������������Na2CO3��Һ��ֱ������Ϊֹ����ѹ���ˣ���ȥ������
6����HCl������ȳ�ȥCO32-
����Һ�еμ�6mol��L-1HCl�����Ƚ��裬�к͵���Һ������(pH=3��4����)��
7��Ũ����ᾧ
���������а���ҺŨ����ԭ�����1/3����ȴ�ᾧ���������ˣ���������2��1�ƾ�ˮ��Һϴ�Ӿ��壬����������©���¶���ˮ�Ρ�
Ȼ��ת�Ƶ���������С����(��ȥ���)����ȴ��Ʒ�����顣
������Ʒ���ȵļ���
ȡ��ʳ�κ��ᴿ��IJ�ƷNaCl��0.5g���ֱ�����Լ5mL����ˮ�У�Ȼ�������з��������ӽ��ж��Լ��鲢�Ƚ϶��ߵĴ��ȡ�
1����������ӵļ���
����֧�Թ��зֱ���������֡���NaCl��ҺԼ1mL���ֱ����2��
6mol��L-1HCl��3��4��0.2mol��L-1 BaCl2��Һ���۲�������
2�������ӵļ���
����֧�Թ��зֱ����֡���NaCl��ҺԼ1mL����2mol��L-1HAcʹ�����ԣ��ٷֱ����3��4�α��Ͳ������Һ���۲�����
3��þ���ӵļ���
����֧�Թ��зֱ����֡���NaCl��ҺԼ1mL���ȸ�����Լ4��5��
6mol��L-1NaOH��ҡ�ȣ��ٷֱ��3��4��þ�Լ���Һ����Һ����ɫ��״����ʱ����ʾ��þ���Ӵ��ڡ���֮������Һ��Ϊ��ɫ����ʾ��þ���Ӵ��ڡ�
����ʵ����
1. ��Ʒ��ۣ�(1)���Σ�________(2)���Σ�_________��
2. ��Ʒ������________g, ����________��
�ڶ�ƪ���Ȼ��Ƶ��ᴿ
�Ȼ��Ƶ��ᴿ
һ.ʵ��Ŀ��
1. �˽��йس��������������Ļ���֪ʶ���˽�SO42-��Ca2+��Mg2+��K+�����ӵļ��������ͼ���������
2. ѧϰ�������Թܵ�ϴ�ӡ����Ļ���ʹ�á��������������ķ��롢��Һ��ȵĵ��� �����γ�����ϴ�ӡ�����ĺ��������
��.ʵ��ԭ����
1����ʳ���к��в���������(����ɳ)�Ϳ���������(��Ҫ��Ca2+��Mg2+��K+��SO42-)�����������ʣ������ܽ���˵ķ�����ȥ��
2.���������ʿ������з�����ȥ��
�� �ڴ�ʳ����Һ�м�����������BaCl2��Һʱ�����ɽ�SO42-ת��Ϊ���ܽ��BaSO4��������ȥ��
Ba2++SO42- = BaSO4��
�� ����Һ���ˣ���ȥBaSO4�������ټ���Na2CO3��Һ�����ڷ������з�Ӧ��Mg2++2OH- = Mg(OH)2�� Ca2++CO32- = CaCO3�� Ba2++ CO32- = BaCO3��
ʳ����Һ�е�����Mg2+��Ca2+�Լ�����SO42-ʱ����Ĺ���Ba2+ת��Ϊ���ܵ�Mg(OH)2,CaCO3,BaCO3��������ͨ�����˵ķ�����ȥ��
�ǹ�����NaOH��Na2CO3�����ô������кͳ�ȥ
OH- + H + = H2O 2H+ +CO32+ = H2O + CO2��
�����������Ե�����(��KCl)���ں������٣�������Ũ���ͽᾧ��������������Һ�У������NaClͬʱ�ᾧ������
��.��Ҫ�������Լ�
��Ҫ�������ձ����Թܣ���������©��������ƿ�����Ļ�
��Ҫ�Լ������Σ�BaCl2��Һ��Na2CO3��Һ��H2SO4 ϡ��Һ��6������Һ,����������������Һ��þ�Լ���2mol/L NaOH, ( NH4)2C2O4��Һ��
��.�������裺
1. �Ȼ��Ƶ��ᴿ�� 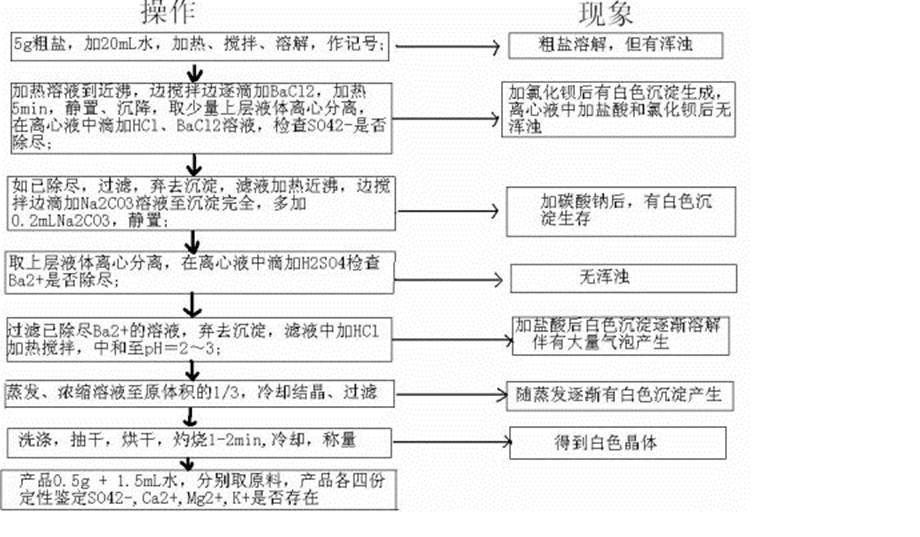
2�����Լ�����
�� K+�ļ�����
.ȡ2��K+��Һ����3����������������(Na3[Co(NO2)6])��Һ������Ƭ�̣���ɫ��K2Na[Co(NO2)6]����������ʾ��K+ ��
2K++Na++[Co(NO2)6]3��=K2Na[Co(NO2)6]��
�� Mg2+�ļ�����ȡ2��Mg2+��Һ����2��2mol·L-1NaOH��Һ��1��
þ�Լ���������������ɫ��ʾ.��Mg2+ ��

��������ż�������ӣ��׳�þ�Լ�����,�ڼ��Ի����³ʺ�ɫ�����ɫ����Mg(OH)2�������������ɫ��
��Ca2+�ļ�����
ȡ2��Ca2+��Һ���μӱ��ͣ�NH4��2C2O4��Һ���а�ɫ��CaC2O4�����γɣ� ʾ��Ca2+
��SO42+�ļ�����
��Һ��6mol·L-1HCl�ữ����2��0.5mol·L-1BaCl2��Һ����ɫ����������ʾ��SO42-
��.ʵ����������
�����1.�ᴿ���Ȼ���Ϊ1.79g
�ᴿ���ʣ�1.79 / 5.0 *100% = 35.8%
2.���Լ��������

3.����������ʵ��õ��ᴿ����Ȼ��Ʋ�Ʒ��ƫ�٣���Ҫ��Ϊ��������Ũ���̶Ȳ���������������ӵĶ��Լ������ϸ�˵������ʵ��Ҫ���ȥ���������Ӵﵽ�˱���
�������⼰˼����
��˼����
1.�����в����ԣ�������������γ�ȥ��
�𣺴����в��������ʿ�ͨ�����˳�ȥ�����������ʿ��Ը������������������ٹ��˳�ȥ��
2���ܷ���CaCl2���涾�Ժܴ��BaCl2����ȥSO42-��
�𣺲��ܡ������Է�����Ҫ����Һ������Ũ�ȡ�10-5mol·L-1��������������Ҫ������Ũ�ȡ�10-6mol·L-1������Ϊ�������ѳ�ȥ��
���� ��10-6mol·L-1Ϊ����ѡ�����������ɷ������� ��
��֪Ksp(BaSO4)=1.08×10-10����[SO42-]=10-6mol·L-1����
[Ba2+]��1.68×10-4mol·L-1�����ɳ���SO42-����ѡ��CaCl2������CaSO4��
���Σ�Ksp(CaSO4)=9.6×10-6����[SO42-]=10-6mol·L-1����[Ca2+]��9.6mol·L-1�����ѳ�����CaCl2���ܽ�ȡ�
3.�ܷ���������������ȥ�����CO32-?
�𣺲��ܣ��������µ����ʡ�
4����ȥ�������������ӵ��Ⱥ�����Ƿ�������ɷ�����任����
�𣺺�������������ı䡣
5.�ӳ����������ʣ�Ϊ�˵õ��ϴ����ij�����������������ʲô��
������Һ��Ũ�Ȳ��ߣ���ȴ���������ó»���
6.�ڳ����ʹ����У����������¶ȸ���ʱ�䳤��Һ���ϻ��о�����֣�����ʲô���ʣ���ʱ�ܷ���˳�ȥ���ʣ��粻�ܣ���ô�죿
�𣺾�����NaCl�������Dz�Ʒ����ʱ���ܹ��ˣ�Ӧ��ˮ�����ȣ�ʹ���ܽ⣬�������ˡ�
������
1���ܷ�һ�ι��˳�ȥ���ᱵ��̼���Σ����������������
�𣺲��ܡ����������ᱵ�ij����еμ�̼������Һ����ʱ��ϵ�д�������ƽ�⣺
BaSO4(s)+CO32- BaCO3(s)+SO42-
��Ksp(BaSO4)=1.1×10-10��֪�������������������ı�
[SO42-]��10-6mol·L-1������[Ba2+]��1.1×10-4mol·L-1����Na2CO3��Ba2+ʱ������CO32-�ļ��룬ƽ�����ƣ�����SO42-��ʹ[SO42-]���ӡ���˲���һ�ι��ˡ�
2.����˵���������ȥʣ���CO32-����Һ��PHӦ�ÿ����ں�ֵ��
�𣺿���pH=2��3
��֪��Һ�ܽ������̼�ﵽ����ʱ[H2CO3]=0.04mol·L-1��CO32-�����ı���[HCO3-]=1.0×10-6mol·L-1�������Һ��pHֵΪ1.8������[HCO3-]=1.0×10-5mol·L-1�Ķ��Ա��������Һ��pHֵΪ2.7���ɲ�Ʒ����������֪��pH=3ʱ��NaCl����������Ϊ99.8%�Ѵﵽ�Ȼ��ƻ�ѧ�Լ��Ĺ��ұ���������ȿ�����pH=2��3��
3.�Ȼ�����Һ��Ũ���̶ȶԲ�Ʒ�������к�Ӱ�죿
��Ũ��̫�٣���Һ�����е��Ȼ��ƶ࣬ʹ���ʵ�;
��Һ�л���K+��Ũ��̫����ʹ��Ʒ�к��н϶��K+��û�дﵽ�ᴿ��Ŀ�ġ�
��.ע������
1����ʳ����Ҫ��ϸ��
2��ʳ����ҺŨ��ʱ�в������ɣ�
3����ͨ�������ѹ���˵���ȷʹ��������
4.Ϊ��ֹ��ɡ����պ�NaCl��ɿ�״��Ҫ��ʱ���Խ��裬���һ���̫��
