实验一 蛋白质的沉淀及变性
发布时间:2010-12-23 浏览次数:850
一、实验目的
1.熟悉蛋白质的沉淀反应。
2.进一步掌握蛋白质的有关性质。
二、实验原理
蛋白质因受某些物理或化学因素的影响,分子的空间构象被破坏,从而导致其理化性质发生改变并失去原有的生物学活性的现象称为蛋白质的变性作用。变性作用并不引起蛋白质一级结构的破坏,而是二级结构以上的高级结构的破坏,变性后的蛋白质称为变性蛋白。
引起蛋白质变性的因素很多,物理因素有高温、紫外线、X-射线、超声波、高压、剧烈的搅拌、震荡等。化学因素有强酸、强碱、尿素、胍盐、去污剂、重金属盐(如Hg、Ag、Pb等)三氯乙酸,浓乙醇等。不同蛋白质对各种因素的敏感程度不同。
用大量中性盐使蛋白质从溶液中析出的过程称为蛋白质的盐析作用。蛋白质是亲水胶体,在高浓度的中性盐影响下脱去水化层,同时,蛋白质分子所带的电荷被中和,结果蛋白质的胶体稳定性遭到破坏而沉淀析出。经透析或用水稀释时又可溶解,故蛋白质的盐析作用是可逆过程。盐析不同的蛋白质所需中性盐浓度与蛋白质种类及pH有关。分子量大的蛋白质(如球蛋白)比分子量小的(如白蛋白)易于析出。改变盐浓度,使不同分子量的蛋白质分别析出。
三、实验材料
1.新鲜蛋清或血清,蛋白质溶液。
2.固体硫酸铵及饱和硫酸铵溶液。
3.95%乙醇,1%CuSO4,饱和苦味酸,0.1mol/LHAC,NaCl,
4.试管,三角漏斗、玻棒,滤纸,试管架酒精灯,移液管。
四、操作方法
1.卵清蛋白的分离 2++2+
(1)、取卵清约2 ml于试管中,加等体积的饱和硫酸铵溶液,搅拌均匀,蛋白质析出,静置,用滤纸过滤致滤液澄清,沉淀为卵球蛋白,将此沉淀用2 ml半饱和硫酸铵洗涤一次。
(2)、将析出卵清球蛋白后的滤液放人试管中,再加人固体硫酸铵使之达饱和,观察有无沉淀产生,若有沉淀,则过滤之,滤出的沉淀却为卵清白蛋白。
2.乙醇沉淀蛋白质(乙醇为脱水剂,能破坏蛋白质胶体质的水化层而使其沉淀析出)。
取蛋白质滤液1ml,加晶体NaCl少许(加速沉淀并使沉淀完全)。带溶解后再加入95%乙醇2ml混匀,观察有无沉淀析出。
3.重金属盐沉淀蛋白质。蛋白质与重金属离子结合成不容性盐类而沉淀。取试管1支加蛋白质溶液2ml,滴加1%CuSO4溶液,至有沉淀生成。
4.生物碱试剂沉淀蛋白质。植物体内具有显著生理作用的含氮碱性化合物称为生物碱。能沉淀生物碱或与其产生颜色反应的物质称为生物碱试剂,如苦味酸。生物碱试剂能和蛋白质结合生成沉淀,可能因蛋白质和生物碱含有相似的含氮基团。2ml蛋白质溶液及1%醋酸溶液4-5滴,加5%苦味酸数滴。
第二篇:蛋白质的沉淀和变性实验
蛋白质的沉淀与变性反应
目的
(1)了解蛋白质的沉淀反应、变性作用和凝固作用的原理及它们的相互关系。
(2)学习盐析和透析等生物化学的操作技术。
原理
在水溶液中,蛋白质分子的表面,由于形成水化层和双电层而成为稳定
的胶体颗粒,所以蛋白质溶液和其他亲水胶体溶液相类似。但是,蛋白质胶
体颗粒的稳定性是有条件的,相对的。在一定的物理化学因素影响下,蛋白
质颗粒失去电荷,脱水,甚至变性,则以固态形式从溶液中析出,这个过程
称为蛋白质的沉淀反应。这种反应可分为以下两种类型:
一、可逆淀汲反应
在发生沉淀反应时,蛋白质虽已沉淀析出,但它的分子内部结构并未发
生显著变化,基本上保持原有的性质,沉淀因素除去后,能再溶于原来的溶
剂中。这种作用称为可逆沉淀反应,又叫作不变性沉淀反应。属于这一类的
反应有盐析作用; 在低温下,乙醇、丙酮对蛋白质的短时间作用以及利用等
电点的沉淀等。
二、不可逆沉淀反应
在发生沉淀反应时,蛋白质分子内部结构、空间构象遭到破坏,失去原
来的天然性质,这时蛋白质已发生变性。这种变性蛋白质的沉淀不能再溶解
于原来溶剂中的作用叫作不可逆沉淀反应。重金属盐、植物碱试剂、过酸、
过碱、加热、震荡、超声波,有机溶剂等都能使蛋白质发生不可逆沉淀反应。
试剂和器材
一、试剂
1.蛋白质溶液
取5m1鸡蛋蛋白蛋清,用蒸馏水稀释至100ml,搅拌均匀后用4-8层纱
布过滤,新鲜配制。
2.蛋白质氯化钠溶液
取20ml蛋清,加蒸馏水200ml和饱和氯化钠溶液100ml,充分搅匀
后,以纱布滤去不溶物(加入氯化钠的目的是溶解球蛋白)。
硫酸铵粉末,饱和硫酸铵溶液,3%硝酸银,0.5% 醋酸铅,10% 三氯醋
酸,浓盐酸,浓硫酸,浓硝酸,5% 磺基水杨酸(sulfosalicyclic acid),0.1%
硫酸铜,饱和硫酸铜溶液,0.1% 醋酸,10% 醋酸,饱和氯化钠溶液,10%
氢氧化钠溶液。
二、器材
试管,试管架,小玻璃漏斗,滤纸,玻璃纸,玻璃棒,500ml
烧杯,10 ml量筒。
操作方法
一、蛋白质的可逆沉淀反应 蛋白质的盐析作用
用大量中性盐使蛋白质从溶液中沉淀析出的过程称为蛋白质的盐析作用。蛋白质是亲水胶体,在高浓度的中性盐影响下,蛋白质分子被盐脱去水化层,同时蛋白质分子所带的电荷被中和,结果蛋白质的胶体稳定性遭受破坏而沉淀析出。析出的蛋白质仍保持其天然蛋白质的性质。减低盐的浓度时,还能溶解。
沉淀不同的蛋白质所需中性盐的浓度不同,而盐类不同也有差异。例如:向含有白蛋白和球蛋白的鸡蛋清溶液中加硫酸镁或氯化钠至饱和,则球蛋白沉淀析出。加硫酸钱至饱和,则白蛋白沉淀析出。另外,在等电点时,白蛋白可被饱和硫酸镁或氯化钠或半饱和的硫酸铵溶液沉淀析出。所以在不同条件下,用不同浓度的盐类可将各种蛋白质从混合溶液中分别沉淀析出,该法称为蛋白质的分级盐析。目前在腌的生产和制备、科学研究工作和临床化验等工作中广泛应用。
取一支试管加入3m1蛋白质氯化钠溶液和3m1饱和硫酸铵溶液,混匀,静置约10 min,球蛋白则沉淀析出,过滤后向滤液中加入硫酸铵粉末,边加边用玻璃棒搅拌,直至粉末不再溶解,达到饱和为止。析出的沉淀为白蛋白。静置,倒去上部清液,白蛋白沉淀,取出部分加水稀释,观察它是否溶解,留存部分作透析用。
二、蛋白质的不可逆沉激反应
1.重金属沉淀蛋白质
重金属盐类易与蛋白质结合成稳定的沉淀而析出。蛋白质在水溶液中是酸碱两性电解质,在碱性溶液中(对蛋白质的等电点而言),蛋白质分子带负电荷,能与带正电荷的金属离子结合成蛋白质盐。在有机体内,蛋白质常以其可溶性的钠盐或钾盐的形式存在,当加入汞,铅、铜、银等重金属盐时,则蛋白质形成不溶性的盐类而沉淀。经过这种处理后的蛋白质沉淀不再溶解于水中,说明它已发生了变性。重金属盐类沉淀蛋白质的反应通常很完全,特别是在碱金属盐类存在时。因此,生化分析中,常用重金属盐除去体液中的蛋白质;临床上用蛋白质解除重金属盐的食物性中毒。但应注意,使用醋酸铅或硫酸铜沉淀蛋白质时,试剂不可加过量,否则可使沉淀出的蛋白质重新溶解。
取2支试管,各加入约1m1蛋白质溶液,分别加入3 % 硝酸银3-4滴,0.5% 醋酸铅1-3滴和0.1%硫酸铜3-4滴,观察沉淀的生成。第一、二支试管再分别加入过量的醋酸铅和饱和硫酸铜溶液,观察沉淀的再溶解。
2.有机酸沉淀蛋白质
有机酸能使蛋白质沉淀。三氯醋酸和磺基水杨酸最有效,能将血清等生物体液中的蛋白质完全除去,因此得到广泛使用。
取两支试管,各加入蛋白质溶液约0.5 m1,然后分别滴加10% 三氯醋酸和5%磺基水杨酸溶液各数滴,观察蛋白质的沉淀。
3.无机酸沉淀蛋白质
浓无机酸(除磷酸外)都能使蛋白质发生不可逆的沉淀反应。这种沉淀作用可能是蛋白质颗粒脱水的结果。过量的无机酸(硝酸除外)可使沉淀出的蛋白质重新溶解。临床诊断上,常利用硝酸沉淀蛋白质的反应,检查尿中蛋白质的存在。
取3支试管,分别加入浓盐酸15滴,浓硫酸、浓硝酸10滴。小心地向3支试管中,沿管壁加入蛋白质溶液6滴,不要摇动,观察各管内两液界面处有白色环状蛋白质沉淀出现。然后,摇动每个试管。蛋白质沉淀应在过量的盐酸及硫酸中溶解。在含硝酸的试管中,虽经振荡,蛋白质沉淀也不溶解。
4.加热沉淀蛋白质
几乎所有的蛋白质都因加热变性而凝固,变成不可逆的不溶状态。盐类和氢离子浓度对蛋白质加热凝固有重要影响。少量盐类促进蛋白质的加热凝固。当蛋白质处于等电点时,加热凝固最完全、最迅速。在酸性或碱性溶液中,蛋白质分子带有正电荷或负电荷,虽加热蛋白质也不会凝固。若同时有足量的中性盐存在,则蛋白质可因加热而凝固。
取5支试管。编号,按下表加入有关试剂(单位:滴):
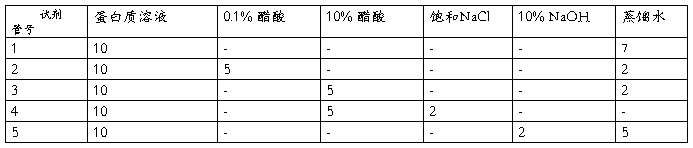
将各管混匀,观察记录各管现象后,放人沸水浴中加热10 min,注意观察比较各管的沉淀情况。然后将第3,4,5号管分别用10% NaOH或10% 醋酸中和,观察并解释实验结果。
将3,4,5号管继续分别加入过量的酸或碱,观察它们发生的现象。然后,用过量的酸或碱中和第3,5号管,沸水浴加热10 min,观察沉淀变化,检查这种沉淀是否溶于过量的酸或碱中,并解释实验结果。
问题:
1.为什么蛋清可用作铅中毒或汞中毒的解毒剂?
2.蛋白质分子中的哪些基团可以与
(1)重金属离子作用而使蛋白质沉淀?
(2)有机酸、无机酸作用而使蛋白质沉淀?
3.高浓度的硫酸铵对蛋白质溶解度有何影响,为什么?
4.在蛋白质可逆沉淀反应的实验中,为何要用蛋白质氯化钠溶液?
