实验四 蛋白质的等电点测定和沉淀反应
一、实验目的
1、了解蛋白质的两性解离性质。
2、学习测定蛋白质等电点的一种方法。
3、加深对蛋白质胶体溶液稳定因素的认识。
4、了解沉淀蛋白质的几种方法及其实用意义。
二、实验原理
蛋白质是两性电解质。在蛋白质溶液中存在下列平衡:
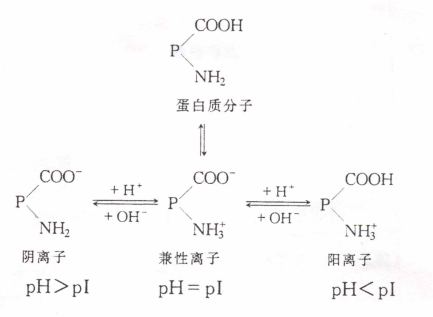
蛋白质分子的解离状态和解离程度受溶液的酸碱度影响。当溶液的PH达到一定数值时,蛋白质颗粒上正负电荷的数目相等,在电场中,蛋白质既不向阴极移动,也不向阳极移动,此时溶液的pH值称为此种蛋白质的等电点。不同蛋白质各有特异的等电点。在等电点时,蛋白质的理化性质都有变化,可利用此种性质的变化测定各种蛋白质的等电点。最常用的方法是测其溶解度最低时的溶液pH值。
本实验通过观察不同pH溶液中的溶解度以测定酪蛋白的等电点。用醋酸与醋酸钠(醋酸钠混合在酪蛋白溶液中)配制各种不同pH值的缓冲液。向诸缓冲溶液中加入酪蛋白后,沉淀出现最多的缓冲液的pH值即为酪蛋白的等电点。
在水溶液中的蛋白质分子由于表面生成水化层和双电层而成为稳定的亲水胶体颗粒,在一定的理化因素影响下,蛋白质颗粒可因失去电荷和脱水而沉淀。
蛋白质的沉淀反应可分为两类:
(1)可逆的沉淀反应 此时蛋白质分子的结构尚未发生显著变化,除去引起沉淀的因素后,蛋白质的沉淀仍能溶解于原来溶剂中,并保持其天然性质而不变性。如大多数蛋白质的盐析作用或在低温下用乙醇(或丙酮)短时间作用于蛋白质。提纯蛋白质时,常利用此类反应。
(2)不可逆沉淀反应 此时蛋白质分子内部结构发生重大改变,蛋白质常变性而沉淀,不再溶于原来溶剂中。加热引起的蛋白质沉淀与凝固。蛋白质与重金属离子或某些有机酸的反应都属于此类。
蛋白质变性后,有时由于维持溶液稳定的条件仍然存在(如电荷),并不析出。因此变性蛋白质并不一定都表现为沉淀,而沉淀的蛋白质也未必都已变性。
三、实验器材
1、实验仪器
1) 水浴锅
2) 温度计
3) 200mL锥形瓶
4) 100mL容量瓶
5) 吸管
6) 试管及试管架
7) 乳钵
2、实验材料
1) 新鲜鸡蛋
2) 0.4%酪蛋白醋酸钠溶液
取0.4g酪蛋白,加少量水在乳钵中仔细地研磨,将所得的蛋白质悬胶液移入200mL锥形瓶内,用少量40—50℃的温水洗涤乳钵,将洗涤液也移入锥形瓶内。加入10mL 1mol/L醋酸钠溶液。把锥形瓶放到50℃水浴中,并小心地旋转锥形瓶,直到酪蛋白完全溶解为止。将锥形瓶内的溶液全部移到100mL容量瓶内,加水至刻度,塞紧玻塞,混匀。
3) 1.00mol/L 醋酸溶液
4) 0.10 mol/L醋酸溶液
5) 0.01 mol/L醋酸溶液
6) 蛋白质溶液
10%卵清蛋白溶液或鸡蛋清的水溶液(新鲜鸡蛋清 :水=1:9)
7) pH4.7醋酸—醋酸钠的缓冲溶液
8) 3%硝酸银溶液
9) 5%三氯乙酸溶液
10) 95%乙醇
11) 饱和硫酸铵溶液
12) 硫酸铵结晶粉末
13) 0.1mol/L盐酸溶液
14) 0.1mol/L氢氧化钠溶液
15) 0.05mol/L碳酸钠溶液
16) 甲基红溶液
四、实验步骤
(一)酪蛋白等电点的测定
(1)取同样规格的试管4支,按下表顺序分别精确地加入各试剂,然后混匀。

(2)向以上试管中各加酪蛋白的醋酸钠溶液1mL, 加一管,摇匀一管。此时1、2、3、4管的pH依次为5.9、5.5、4.7、3.5。观察其混浊度。静置10分钟后,再观察其混浊度。最混浊的一管pH即为酪蛋白的等电点。
(二)蛋白质的沉淀及变性
1、蛋白质的盐析
加蛋白质溶液5mL于试管中,再加等量的饱和硫酸铵溶液,混匀后静置数分钟则析出球蛋白的沉淀。倒出少量混浊沉淀,加少量水,观察是否溶解,为什么?向清液中添加硫酸铵粉末到不再溶解为止。此时析出沉淀为清蛋白。取出部分清蛋白,加少量蒸馏水,观察沉淀的再溶解。
2、重金属离子沉淀蛋白质
取1支试管,加入蛋白质溶液2mL,再加3%硝酸银溶液1—2滴,振荡试管,有沉淀产生。放置片刻,向沉淀中加入少量的水,沉淀是否溶解?为什么?
3、某些有机酸沉淀蛋白质
取1支试管,加入蛋白质溶液2mL,再加入1ml5%三氯乙酸溶液,振荡试管,观察沉淀的生成。放置片刻,向沉淀中加入少量水,观察沉淀是否溶解?为什么?
4、有机溶剂沉淀蛋白质
取1支试管,加入2mL蛋白质溶液,再加入2mL95%乙醇。观察沉淀的生成(如果沉淀不明显,加点NaCl,混匀)。
5、乙醇引起的变性与沉淀 取3支试管,编号。依下表顺序加入试剂:

振摇混匀后,观察各管有何变化。放置片刻向各管内加入水8毫升,然后在第2,3号管中各加一滴甲基红,再分别用0.1mol/L 醋酸溶液及0.05mol/L碳酸钠溶液中和之。观察各管颜色的变化和沉淀的生成。每管再加0.1mol/L盐酸溶液数滴,观察沉淀的再溶解。解释各管发生的全部现象。
五、实验结果
以表格形式总结实验结果,包括观察到的现象,分析各实验现象的原因。
六、注意事项
等电点测定的实验要求各种试剂的浓度和加入量必须相当准确。
七、思考题
1、什么是蛋白质的等电点?
2、在等电点时,蛋白质溶液为什么容易发生沉淀?
