第二篇:H2SO4和H3PO4混合酸的电位滴定
H2SO4和H3PO4混合酸的电位滴定
姓名:杨力生 班级:化学生物学2012级1班 学号:20122994 摘 要:本实验采用电位滴定法测定H2SO4和H3PO4混合酸的pH,然后运用pH-V曲线和(△pH/△V)-V曲线与二级微商法确定其滴定终点的pH,通过pH可求得H2SO4和混合酸中两种酸的各自含量。
关键词:磷酸混合;酸硫酸;电位滴定;pH
Abstract:Determination of H2SO4 pH and H3PO4 mixed acid by potentiometric titration of the experiment , and then use pH-V curves and (△ pH / △ V)-V curve and its second derivative to determine the titration endpoint pH, pH can be obtained by H2SO4 and mixed acid content of each of the two acids .
Keywords:Sulfuric acid ; phosphoric acid mixture ; potentiometric titration ; pH
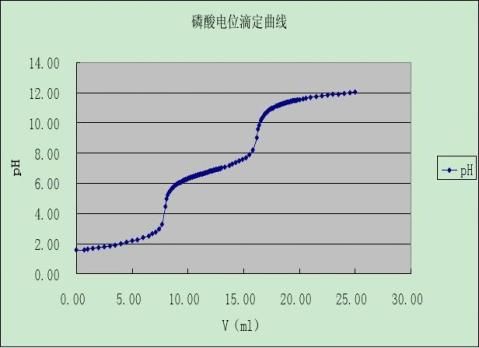
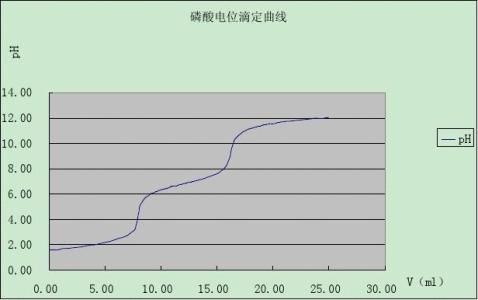
电位分析包括电位测定法和电位滴定法两种分析方法。其中电位滴定法是利用滴定分析化学中化学计量点附近的突跃(如酸碱滴定中pH 的突跃、配位滴定与沉淀滴定中pM的突跃、氧化还原中电位的突跃),以一对适当的电极监测滴定过程中的电位变化,从而确定滴定终点,并由此求得待测组分的浓度或含量。电位滴定法优于通常的化学滴定分析,它不仅可用于一般化学滴定分析的场合,而且还可用于有色或浑浊试液的滴定,以及找不到合适指示剂的各种滴定,此外用电位法也比一般用化学指示剂确定终点更为准确。 H2SO4和H3PO4都为强酸,H2SO4的pKa2=1.99,H3PO4的pKa1=2.12,pKa2=7.20,pKa3=12.36,由pKa值可知,当用标准碱溶液滴定时,H2SO4可全部被中和,且产生pH的突跃,而在H3PO4的第二化学计量点时,仍有pH值的突跃出现,因此根据滴定过程中pH值的变化情况,可以确定滴定终点,进而求得各组分的含量。确定混合酸的滴定终点可用指示剂法(最好是采用混合指示剂),也可以用玻璃电极作指示电极,饱和甘汞电极作参比电极,同试液组成工作电池: Ag,AgCl|HCl(0.1mol/L)|玻璃膜| H2SO4,H3PO4(试液)‖KCl(饱和)|Hg2Cl2,Hg 在滴定过程中,通过测量工作电池的电动势,了解溶液pH值随加入标准碱溶液体积V的变化情况,然后由pH-V曲线或(ΔpH/ΔV)-V曲线求得终点时耗去NaOH标准溶液的体积,也可用二级微商法求出Δ2pH/ΔV2 =0时,相应的NaOH标准溶液体积,即得出滴定终点。根据标准碱溶液的浓度、用去的体积和试液的用量,即可求出试液中各组分的含量。
用电位滴定法测量硫磷混合酸,随着NaOH滴定剂的加入,H2SO4可全部被中和,在化学计量点附近,产生pH的突跃,而在H3PO4的第二化学计量点时,仍有pH的突跃产
生,因此根据滴定过程中pH的变化情况,可以确定滴定终点,从而求出硫酸与磷酸的浓度。
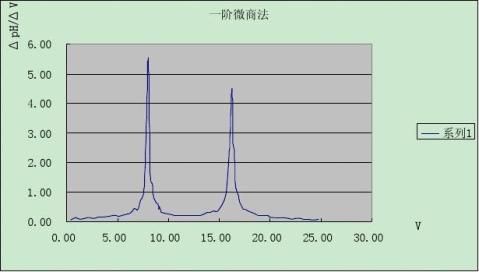
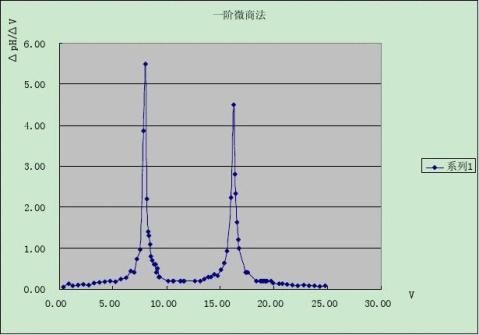
滴定终点可通过绘制电位滴定曲线来确定,即
(或
(或

)一次微商曲线和
)二次微商曲线;但用作图法手续较烦且不准确,因此常用二次微商
计算法计算滴定终点(内插法)。 1.实验部分 1.1.仪器和试剂
酸度计,复合电极,100mL容量瓶,吸量管,10mL微量滴定管 1.000mol/L草酸标准液,0.1mol/LNaOH标准溶液,硫磷混酸溶液 1.2实验方法
1.2.1NaOH溶液浓度的标定
准确移取草酸标准溶液10.0mL于100mL烧杯中,加水定容,取5mL于烧杯中,加水至30mL,将待标定的NaOH标准溶液装入滴定管中,调整液面于零点;开动搅拌器,滴加NaOH标准溶液、读pH(电位)值,每次1mL,初步判断突跃点的体积范围;重复上述操作,加液至近突跃体积处,再以每次0.1mL的间隔读取pH(电位)-体积关系。以插值法求终点,计算NaOH标准溶液浓度。 1.2.2混合酸的测定
准确移取混酸10.0mL于100mL烧杯中,加水定容,取5mL于烧杯中,加水至30mL; 仿照标定NaOH溶液时的粗测和细测步骤,但要获取两个突跃点的体积范围;在超过第一终点后,再加液至近第二突跃体积处,再测出第二突跃点附近的pH(电位)-体积关系;
以插值法求终点,计算混酸中各组分的浓度。
2.结果与讨论
2.1.NaOH溶液浓度的标定 2.1.1.实验数据及计算
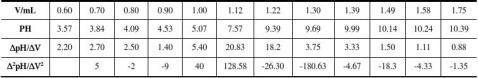
2.1.2.作图
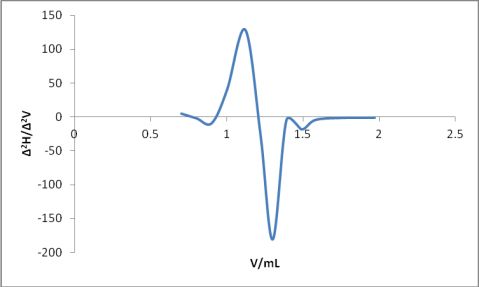
2.1.3.计算NaOH溶液的浓度
根据内插法计算NaOH标准溶液用量=1.12+[128.58/(128.58+26.30)]×(1.22-1.12)=1.20mL,则NaOH标准溶液浓度C=0.4464mol/L。 2.2.混酸测定 2.2.1.实验数据及计算
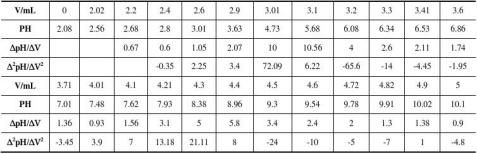
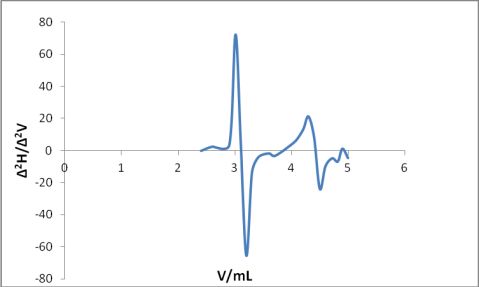
2.2.2.作图
2.2.3.计算混酸中SO3和P2O5的含量
根据内插法计算两突跃点NaOH标准溶液用量V1=3.1+[6.22/(6.22+65.6)]×(3.2-3.1)=3.11mL ,V2=4.4+[8/(8+24)]×(4.5-4.4)=4.43mL ;所以P2O5的含量为:{[(0.00443-0.00311)×0.4464 ×10×141.95] /2}/0.010=41.82 g/L,SO3含量为:{[(0.00311-0.00132)×0.4464×10×80.06] /2}/0.010=31.97 g/L
参考文献
[1] 苏克曼, 张济新. 仪器分析实验[M]. 高等教育出版社, 2005, 75-78
[2] 王冬梅.分析化学实验[M].武汉:华中科技大学出版社,2007. 致谢:衷心感谢吴明君老师的指导!
