结构化学实验报告
——溶液法测定极性分子的偶极矩
一、实验目的
1.用溶液法测定正丁醇的偶极矩
2.了解偶极矩与分子电性质的关系
3.掌握溶液法测定偶极矩的实验技术
二、实验原理
1.偶极矩与极化度
(1)两个大小相等方向相反的电荷体系的偶极矩定义为:
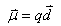
(2)极化程度可用摩尔定向极化度P定向来衡量:
P定向=4/3πNA*μ02/(3kT)=4/9πNA*μ02/(kT)
(3)极性分子所产生的摩尔极化度P是摩尔定向极化度、摩尔电子诱导极化度和摩尔原子诱导极化度的总和:
P=P定向+P诱导=P定向+P电子+P原子
2.偶极矩的测定方法(溶液法测定偶极矩)
(1)无限稀释时溶质的摩尔极化度的公式:
P=P2∞=3αε1/(ε1+2)2 * Μ1/ρ1 + (ε1-1)/(ε1+2) * (Μ2-βΜ1)/ρ1
(2)习惯上用溶质的摩尔折射度R2表示高频区测得的摩尔极化度,因为此时P定向=0,P原子=0,推导出无限稀释时溶质的摩尔折射度的公式:
P电子=R2∞=n2-1/(n12+2) * (Μ2-βΜ1)/ρ1+6n12Μ1γ/[(n12+2)2*ρ1]
(3) 近似公式:
ε溶=ε1(1+α* x2)
ρ溶=ρ1(1+β*x2)
n溶=n1(1-γ*x2)
(4) 永久偶极矩的获得
考虑到摩尔原子诱导极化度通常只有摩尔电子极化度的5%-15%,而且P定向又比P原子大得多,故常常忽略P原子,可得P定向=P2∞-R2∞=4/9πNA*μ02/(kT)
μ0=0.0128*[(P2∞-R2∞)*T]1/2
(5)介电常数的测定:用空气与一已知介电常数ε溶的标准物质分别测得电容C/空 ,C/标
C/空=C空+Cd= C0+Cd C/标=C标+Cd
则通过上两式可求得C0=(C/标-C/空)/(ε标-1) Cd=C/空-C0=C/空-(C/标-C/空)/(ε标-1)
ε溶= C溶/ C0=(C/溶- Cd)/ C0
三、仪器和试剂
仪器:阿贝折光仪1台;比重管1只;电容测量仪一台;电容池一台;电子天平一台;电吹风一只;25ml容量瓶4支;25ml、5ml、1ml移液管各一支;滴管5只;5ml针筒一支;针头一支;吸耳球一个;
试剂:正丁醇(分析纯);环己烷(分析纯);蒸馏水;丙酮
四、实验步骤
1.溶液的配制
配制4种正丁醇的摩尔分数分别是0.05、0.10、0.15、0.20的正丁醇-环己烷溶液。操作时应注意防止溶质和溶剂的挥发以及吸收极性较大的水气,为此溶液配好后应迅速盖好瓶盖,并置于干燥箱中。
2.折光率的测定
在恒温(25±0.10C)条件下用阿贝折光仪测定环己烷和各配制溶液的折光率。测定时注意各样品需加样三次,每次读取一个数据,取平均值。
3.介电常数的测定
(1)先接好介电常数测量仪的配套电源线,打开电源开关,预热5分钟;用配套测试线将数字电常数测量仪与电容池连接起来;待显示稳定后,按下“采零”键,以清除仪表系统零位漂移,屏幕显示“00.00”。
(2)电容C0 和Cd 的测定:本实验采用环己烷为标准物质,其介电常数的温度公式为: ε标=2.203-0.0016(t-20)
式中t为实验室温度(0C)。用电吹风将电容池加样孔吹干,旋紧盖子,将电容池与介电常数测量仪接通。读取介电常数测量仪上的数据。重复三次,取平均值。用移液管取1ml纯环己烷加入电容池的加样孔中,盖紧盖子,同上方法测量。倒去液体,吹干,重新装样,用以上方法再测量两次,取三次测量平均值。
(3)溶液电容的测量:测定方法与环己烷的测量方法相同。每个溶液均应重复测定三次,三次数据差值应小于0.05pF,所测电容读数与平均值,减去Cd,即为溶液的电容C溶。由于溶液易挥发而造成浓度改变,故加样时动作要迅速,加样后迅速盖紧盖子。
4.溶液密度的测定
取干净的比重管称重m0。然后用针筒注入已恒温的蒸馏水,定容,称重,记为m1。用丙酮清洗并吹干。同上,测量各溶液,记为m2 。则环己烷和各溶液的密度为:
ρ溶=(m2-m0)/(m1-m0) *ρ水 ,ρ25℃水=0.99707g/mL
5.清洗、整理仪器
上述实验步骤完成后,确认实验数据的合理性。确认完毕,将剩余溶液回收,容量瓶、比重管、针筒洗净、吹干。整理实验台,仪器恢复实验前的摆放。
五、数据记录和处理
1. 溶液的配制

2.折光率的测定
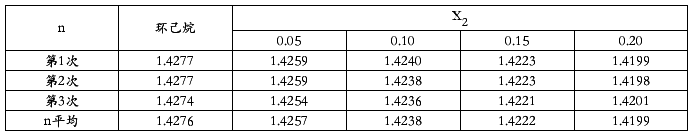

由上图可知:n1=1.4276
γ=0.0378/1.4276=0.0265
3.介电常数的测定

t=17.8℃ ε标=2.203-0.0016(t-20)=2.207
C0=(C/标-C/空)/(ε标-1)=(5.48-5.24)/(2.207-1)=0.199
Cd=C/空-C0=5.24-0.199=5.04
由ε溶=(C/溶- Cd)/ C0 ,可算出:
ε(环己烷)=2.207
ε(0.05)=2.66
ε(0.10)=2.56
ε(0.15)=3.16
ε(0.20)=2.86

由上图可知:ε1=2.3282
α=3.612/2.3282=1.551
4.溶液密度的测定
m0=25.0273
m1=28.4069
m2(环己烷)=27.6384
m2(0.05)=27.6410
m2(0.10)=27.6457
m2(0.15)=27.6470
m2(0.20)=27.6491
由ρ溶=(m2-m0)/(m1-m0) *ρ水,可算出:
ρ(环己烷)=0.7726
ρ(0.05)=0.7734
ρ(0.10)=0.7748
ρ(0.15)=0.7752
ρ(0.20)=0.7758

由上图可知:ρ1=0.7727
β=0.0164/0.7727=0.0212
5.求P2∞、R2∞
P2∞=3αε1/(ε1+2)2 * Μ1/ρ1 + (ε1-1)/(ε1+2) * (Μ2-βΜ1)/ρ1
=91.71
R2∞=(n12-1)/(n12+2) * (Μ2-βΜ1)/ρ1 + 6n12Μ1γ/[(n12+2)2*ρ1]
=26.23
6.求偶极矩μ0(当时温度为17.80C)
μ0=0.0128*[(P2∞-R2∞)*T]1/2=0.0128*[(91.71-26.23)*290.8]1/2
=1.77
六、分析讨论
1.分析本实验误差的主要来源,如何改进?
答:(1)溶液的配制:移液管使用过程中量取溶液并不十分精确,会导致溶液配置的时候X2的值与要求值有一定的偏差。所以,在移液的过程中要保证移液管使用操作迅速准确。
(2)折光率的测定:折光率的线性还比较好,测量中除了取样,试剂瓶盖子应随时盖好.以免样品挥发影响溶液浓度。而且样品滴加要均匀,用量不能太少,以免测量不准确。
(3)介电常数的测定:仪器不是很稳定,而且并未用移液管移取1mL,而是用每种溶液的专用滴管吸取50滴,滴管的构造不一样,也导致了移取的样品量不一致,这是造成介电常数与浓度关系的线性很差的两个原因。应该用同一个移液管准确移取,且每次都要用丙酮洗净用待测液润洗,而且在重新装样前,为了证实电容池电极间的残余液确已除净,须先测量空气的电容值,待空气的电容值恢复到测量之前,或者在±0.05pF的误差范围内,方可进行下一次测量。
(4)溶液密度的测定:因为电子天平非常灵敏,当有电吹风在吹或稍有动静时,读数就变得很厉害,两次测量的数据都会很不一样,所以每个样品测了两次,取了比较合理的数据。减小误差的方法是确保每次装样品前比重管都要洗净吹干(内外管壁都是),溶液要装满比重管,且外壁不能沾溶液,测量的环境要尽可能安静。
2.本实验中,为什么要将被测的极性物质溶于非极性的溶剂中配成稀溶液?
答:因为溶液法的基本想法是,在无限稀释的非极性溶剂的溶液中,溶质分子所处的状态和气态时相近,于是无限稀释的溶液中就可以使用如下稀溶液的近似公式:
ε溶=ε1(1+α* x2)
ρ溶=ρ1(1+β*x2)
n溶=n1(1-γ*x2)
从而可以推导出无限稀释时溶质的摩尔极化度及摩尔折射度的公式,最终得到永久偶极矩。
3.根据实验结果,判断正丁醇的对称性(所属点群)。
答:由于正丁醇具有永久偶极矩,且只有属于Cn、Cnv(包括Cs)点群的分子才具有永久偶极矩,所以正丁醇所属点群为C1 。
第二篇:偶极矩的测定
偶极矩的测定
一、实验目的:
1、会用溶液法测定乙酸乙酯的偶极矩;
2、了解偶极矩与分子电性质的关系;
3、掌握溶液法测定偶极矩的原理、方法和计算。
二、实验原理:
1、偶极矩与极化度
分子的结构可以近似地看成是由电子云和分子骨架(原子核和内层电子)所构成。由于其空间构型的不同,其正负电荷中心可以是重合的(此时为非极性分子),也可以是不重合的(此时为极性分子)。

图1 偶极矩示意图
1912年Debye提出“偶极矩”μ的概念来度量分子极性的大小,如图1所示,其定义是:
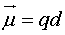 (1)
(1)
式中 q为正、负电荷中心所带的电荷量;d为正、负电荷中心间的距离;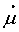 为向量,其方向规定为从正到负,单位为Debye或C·m(10-30)。
为向量,其方向规定为从正到负,单位为Debye或C·m(10-30)。
通过偶极矩的测定,可以了解分子结构中有关电子云的分布,分子的对称性,还可以用来判别几何异构体和分子的立体结构等。
极性分子具有永久偶极矩,在没有外电场存在时,由于分子热运动,偶极矩在各个方向上的取向机会均等,故其偶极矩的统计值为零。
若将极性分子置于均匀的外电场中,分子会沿电场方向作定向转动,同时分子中的电子云对分子骨架发生相对移动,分子骨架也会变形,这叫分子极化,极化的程度可由摩尔极化度(Pm)来衡量。因转向而极化称为摩尔极化度(P转向)。由变形所致的为摩尔变形极化度(P变形)。而P变形又是电子极化度(P电子)和原子极化度(P原子)之和。显然:
Pm=P转向+P变形=P转向+(P电子+P原子) (2)
已知P转向与永久偶极矩μ的平方成正比,与绝对温度成反比。即
 (3)
(3)
式中 K为Boltzmann常数;N为Avogadro常数。
对于非极性分子,因其永久偶极矩μ=0,分子不能沿电场方向作定向转动,其P转向=0,所以Pm=P电子+P变形
若外电场是交变电场,则极性分子的极化与交变电场的频率有关。当在电场的频率小于1010Hz的低频电场作用下,极性分子产生摩尔极化度为转向极化度与变形极化度之和。若在电场频率为1012Hz~1014Hz的中频电场下(红外光区),因为电场交变周期小于偶极矩的松弛时间,极性分子的转向运动跟不上电场变化,即极性分子无法沿电场方向定向,即P转向=0,此时分子的摩尔极化度Pm=P变形=P电子+P原子。当交变电场的频率大于1015Hz(即可见光和紫外光区)的高频电场下,极性分子的转向运动和分子骨架变形都跟不上电场的变化,此时极性分子的摩尔极化度Pm等于电子极化度P电子。
因此,原则上只要在低频的电场下测得极性分子的摩尔极化度Pm,在红外频率下测得极性分子的摩尔变形极化度P变形,两者之差得到极性分子的摩尔转向极化度P转向,然后代入(2)式就可算出极性分子的永久偶极矩μ来。
2、极化度和偶极矩的测定
Clausius、Mosotti和Debye从电磁理论得到摩尔极化度与介电常数ε之间的关系式:
 (4)
(4)
式中 M为被测物质的分子量; ρ为该物质在ToK时的密度;但(4)式是假定分子间无相互作用而推导得到的,所以只能适用于温度不太低的气相体系,然而测定气相的介电常数和密度在实验上困难较大,对某些物质甚至无法获得其气相状态,因此后来提出了一种溶液法来解决这一困难,溶液法的基本思想是,在无限稀释的非极性溶液中,溶质分子所处的状态和气相时相近,于是无限稀释溶液中溶质的摩尔极化度Pm,就可以看作(4)式中的摩尔极化度P。
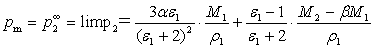 (5)
(5)
式中 ε1、M1、ρ1为溶剂的介电常数,摩尔质量和密度,M2为溶质的摩尔质量。α、β为两常数,它可由下面两个稀溶液的近似公式求出。
ε12=ε1(1+αX2) (6)
ρ12=ρ1(1+βX2) (7)
式中ε12、ρ12和X2为溶液的介电常数,密度和溶质的摩尔分数。因此,从测定纯溶剂的ε1、ρ1以及不同浓度(X2)溶液的ε12、ρ12,代入(5)式就可求出溶质分子的总极化度。
上面提到在红外频率的电场下可以测得极性分子的摩尔变形极化度,但在实验上由于条件的限制,很难做到这一点,所以一般是在高频电场下测定极性分子的电子极化度。
根据光的电磁理论,在同一频率的高频电场作用下,透明物质的介电常数ε与折光率n的关系为:
ε=n2 (8)
习惯上用摩尔折射度R2来表示高频区测得的极化度,而此时P转向=0,P电子=0,则

 (9)
(9)
同样测定不同浓度溶液的摩尔折射度,外推至无限稀释,就可求出该溶质的摩尔折光度的公式。
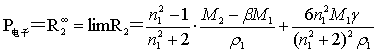 (10)
(10)
式中 n1为溶剂的摩尔折光率,γ为常数,它可由下式求出
n12=n1(1+γX2) (11)
式中 n12为溶液的摩尔折光率。综上所述,可得
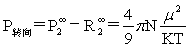 (12)
(12)
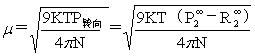
= (Debye)
(Debye)
= (C·m) (13)
(C·m) (13)
在某种情况下,若要考虑P原子的影响时,只需要对R2作部分修改就行了,上述测定极性分子偶极矩的方法称为溶液法。
此外,测定偶极矩的实验方法还有很多,如湿度法、分子束法、分子光谱法以及微波谱的斯塔克法等。
3、介电常数的测定:
介电常数是通过测定电容,计算而得到。
如果我们在电容器的两个极板间充以某种电介质,电容器的电容量就会增大,如果维持极板上的电荷量不变,那么充以电介质的两极板间电势差就会减小。若Co为极板间处于真空时的电容量,C为充以电介质时的电容量,则C和Co之比值ε称为该电介质的介电常数。
ε=C/C0 (14)
测定电容的方法一般有电桥法、拍频法和谐振法。本实验用的是电桥法。选用的仪器为PGM-II数字小电容测试议。其桥路为变压器比例臂电桥,图2为其示意图,电桥平衡条件是:
Cx/Cs=Ux/Us (15)
式中 Cx为电容池二极板间的电容,Cs为标准的差动电容,调节Cs,当Cx=Cs时,Ux=Us,此时指示器的输出趋近于零,Cs值可直接读出, Cx值便可求得。
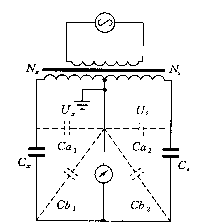

图2 电容电桥原理图 图3 电容池的结构
1、外电极 2、内电极 3、恒温室 4、样品室 5、绝缘板
6、池盖 7、外电极接线 8、内电极接线
电容池的结构如图3所示,由于在电桥法测量电路中被测电容Cx二端都不能接地,因此恒温介质不能用水,本实验用介电常数很小的变压器油为介质或不加介质,电容池外壳兼作屏蔽之用,这样就可以避免人体对测量的影响。
由于在小电容测量仪测定电容时,除电容池两极板间的电容Cc外,整个测试系统中还有分布电容Cd的存在,所以实际测得的电容应为Cc和Cd之和,即
Cx=Cc+Cd (16)
Cc随测物质而异,而Cd对一台仪器(包括所配的导线和电容池)来说是一定值,因此在以后各次测量中必须扣除分布电容值Cd,才能得到待测物的电容Cc。其测定方法为先测定一已知介电常数ε标的标准物质的电容C`标,则
C`标=C标+Cd (17)
而不放样品时所测C`空为
C`空=C空+Cd (18)
两式相减得
C`标-C`空=C标-C空 (19)
已知物质介电常数ε等于电介质的电容与真空时的电容之比,如果把空气的电容近似看作真空时的电容,则可得
ε标=C标/ C空 (20)
所以式(19)变为:
C`标-C`空=ε标·C空-C空=(ε标-1)C空 (21)
C空=(C`标-C`空)/(ε标-1) (22)
从而求出
Cd=(ε标C`空-C`标)/(ε标-1) (23)
三、仪器与试剂:
PGM—Ⅱ型数字小电容测试仪(1台); 电容池(1个); 阿贝折射仪(1台);密度管(1支); 电吹风(1个); 容量瓶(4个); 烧杯(6个);注射器(1支)。 CCl4(分析纯); CH3COOC2H5(分析纯)。
四、实验步骤:
1、配制溶液
配制摩尔分数X2为0.050、0.100、0.150、0.200的溶液各25mL。为了配制方便,先计算出所需乙酸乙酯的毫升数,移液,然后称量配制。算出溶液的正确浓度,操作时注意防止溶液的挥发和吸收极性较大的水汽。
2、折光率测定
在25oC±0.1oC条件下,用阿贝折光仪测定CCl4,以及配制的四个溶液的折光率。注意测定时各样品需加样三次,读取三个数据,取平均值。
3、介电常数测定
① 电容Co和Cd的测定:本实验采用四氯化碳作为标准物质,其介电常数的温度公式为:
ε(CCl4)=2.238-0.002(t-20) (24)
式中 t为摄氏温度。
用洗耳球将电容池样品室吹干,旋上金属盖,并将电容池和电容测定仪连接线接好,将电容测定仪的电源开关置于“通”位,预热5~10min。按下“采零”键,使显示器显示“00.00”。然后将电容池测试线的一端与电容测试议接好,另一端置于电容池近处,电容池座测试线接入电容池座,使测试线尽量不要晃动,以取得较为稳定的分布电容。将仪器“采零”。接着将测试头插入电容池,待数值稳定后记下,此即是C`空。
拔下电容池测试线,用移液管量取1mL标准液CCl4注入样品室,然后用滴管逐滴加入样品,直至液面高于中间柱面,(注意样品不可多加,样品过多会腐蚀密封材料渗入恒温室,实验无法正常进行。)迅速旋紧金属盖,待读数稳定后,按“采零”键,再插上电容池测试线,测出电容池的电容值C`标( 测量三次取平均值。)然后用注射器抽去样品室内样品,再用洗耳球吹扫,复测一次C`空,其值与上面所测C`空的值偏差小于0.05PF,否则需再吹。
②溶液电容的测定:测定方法与测四氯化碳相同,重复测定时,不但要抽去样品室内的溶液,还要用洗耳球将样品室吹干,然后复测C`空值,再加入该溶液,测出电容值C`溶。各溶液电容测定两次,取平均值,减去Cd,即为该溶液的电容值C溶。
4、溶液密度测定:
将密度管(见图4)洗净,干燥后挂在天平上称量得m0,然后取下磨口小帽,将a支管插入蒸馏水中,用洗耳球在b支管慢慢吸气,将蒸馏水吸入密度管内,使充满b端小球,然后将密度管的b端略向上仰,用滤纸从a支管管口吸取多余的蒸馏水,以调节b支管的液面到刻度线,调好后放水平,盖上a、b管口。(应先套a端,后套b端),并且用滤纸吸干管外沾的蒸馏水,在天平上称量得到m水。倒去蒸馏水,吹干后盛以液体四氯化碳,用上法一样可称量得含有四氯化碳的密度管质量为mi,则在某温度时被测液体的密度为:
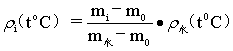 (25)
(25)
五、数据处理:
1、计算各溶液的物质的量的浓度X2。
2、计算CCl4及4种溶液的密度ρ,作ρ12~X2图,由直线斜率求算β值。
3、作n12~X2图,由直线斜率求算γ值。
4、计算C0、Cd和4个溶液的Cx值,求出各溶液的介电常数ε12,作ε12~X2图,由直线斜率求算α值。
5、将ρ1、ε1、α、β值代入(5)式,计算 。
。
6、将ρ1、n1、β、γ值代入(10)式,计算 。
。
7、将 、
、 值代入(13)式,计算乙酸乙酯的偶极矩μ值。
值代入(13)式,计算乙酸乙酯的偶极矩μ值。
六、思考题:
1、测定介电常数时,如何最大限度保证分布电容Cd为定值?
2、准确测定溶质摩尔极化度与摩尔折射度时,为什么要外推至无限稀释?
3、溶液法测得溶质偶极矩与气相测得的真实值间存在偏差,其原因是什么/
4、试分析影响结果的因素,如何改进?
七、实验注意事项:
1、在操作时应注意防止溶液的挥发及吸收极性较大的水蒸汽,影响测定值,故操作要迅速,试剂和溶液应随时盖紧;且配制溶液的器具应干燥,溶液应透明不发生浑浊。
2、在电桥法测量中,被测电容Cx二端不能接地,因此,恒温介质不能是水,而用介电常数较小的矿物油或变压器油。
