华南师范大学实验报告
学生姓名 学 号
专 业化学(师范) 年级、班级
课程名称结构化学实验 实验项目 稀溶液法测定偶极矩
实验类型 1验证2 设计1 综合实验时间 年 月 日
实验指导老师 实验评分
一、实验目的
1. 掌握溶液法测定偶极矩的主要实验技术
2. 了解偶极矩与分子电性质的关系
3. 测定正丁醇的偶极矩
二、实验原理
1.偶极矩与极化度
分子结构可以近似地看成是由电子云和分子骨架(原子核及内层电子)所构成。由于空间构型的不同,其正负电荷中心可能重合,也可能不重合。前者称为非极性分子,后者称为极性分子。
1912年,德拜提出“偶极矩”的概念来度量分子极性的大小,其定义是

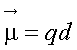 ①
①
式中,q是正负电荷中心所带的电量;d为正负电荷中心之间的距离; 是一个矢量,其方向规定为从正到负。因分子中原子间的距离的数量级为10-10m,电荷的数量级为10-20C,所以偶极矩的数量级是10-30C·m。
是一个矢量,其方向规定为从正到负。因分子中原子间的距离的数量级为10-10m,电荷的数量级为10-20C,所以偶极矩的数量级是10-30C·m。
通过偶极矩的测定,可以了解分子结构中有关电子云的分布和分子的对称性,可以用来鉴别几何异构体和分子的立体结构等。
极性分子具有永久偶极矩,但由于分子的热运动,偶极矩指向某个方向的机会均等。所以偶极矩的统计值等于零。若将极性分子置于均匀的电场E中,则偶极矩在电场的作用下,趋向电场方向排列。这时称这些分子被极化了。极化的程度可以用摩尔转向极化度Pμ来衡量。Pμ与永久偶极矩μ的平方成正比,与绝对温度T成反比。
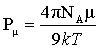 ②
②
式中,k为波兹曼常数;NA为阿弗加德罗常数;T为热力学温度;μ为分子的永久偶极矩。
在外电场作用下,不论极性分子或非极性分子,都会发生电子云对分子骨架的相对移动,分子骨架也会发生形变。这称为诱导极化或变形极化。用摩尔诱导极化度P诱导来衡量。显然,P诱导可分为两项,即电子极化度Pe和原子极化度Pa,因此
P诱导 = Pe + Pa ③
如果外电场是交变场,极性分子的极化情况则与交变场的频率有关。当处于频率小于1010HZ的低频电场或静电场中,极性分子所产生的摩尔极化度P是转向极化、电子极化和原子极化的总和。
P = Pμ+ Pe +Pa ④
如何从测得的摩尔极化度P中分别出Pμ的贡献呢?介电常数实际上是在107HZ以下的频率测定的,测得的极化度为 Pμ+ Pe +Pa。若把频率提高到红外范围,分子已经来不及转向,此时测得的极化度只有Pe和Pa的贡献了。所以从按介电常数计算的P中减去红外线频率范围测得的极化,就等于Pμ,在实验上,若把频率提高到可见光范围,则原子极化也可以忽略,则在可见光范围:
Pμ =P -( Pe +Pa) ≈ P - Pe ⑤
2. 摩尔极化度的计算
克劳休斯、莫索和德拜从电磁场理论得到了摩尔极化度P与介电常数 ε 之间的关系式。
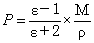 ⑥
⑥
式中,M为被测物质的摩尔质量;ρ 为该物质的密度;ε 是介电常数。
但式⑥是假定分子与分子间没有相互作用而推导得到的。所以它只适用于温度不大低的气相体系,对某种物质甚至根本无法获得气相状态。因此后来就提出了用一种溶液来解决这一困难。溶液法的基本想法是,在无限稀释的非极性溶剂中,溶质分子所处的状态和气相时相近,于是无限稀释溶液中的溶质的摩尔极化度可以看作是式⑥中的P。
在稀溶液中,若不考虑极性分子间相互作用和溶剂化现象,溶剂和溶质的摩尔极化度等物理量可以被认为是具有可加性。因此,式⑥可以写成:
 ⑦
⑦
式中,下标1表示溶剂;下标2表示溶质;x1表示溶剂的摩尔分数;x2表示溶质的摩尔分数;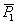 表示溶剂的摩尔极化度;
表示溶剂的摩尔极化度;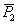 表示溶质的摩尔极化度。
表示溶质的摩尔极化度。
对于稀溶液,可以假设溶液中溶剂的性质与纯溶剂相同,则
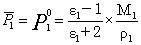 ⑧
⑧
 ⑨
⑨
Hedestrand 首先推导出经验公式,指出在稀溶液中溶液的介电常数和密度可以表示为
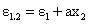 ⑩
⑩
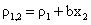 ?
?
因此
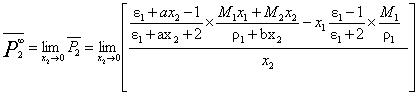
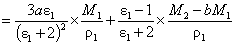 ?
?
做ε1,2-x2图,根据式⑦由直线测得斜率a,截距ε1;作ρ1,2 -x2图,并根据式 ?由直线测得斜率b,截距ρ1,代入式?得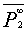
3. 由折光度计算电子极化度Pe
电子极化度可以使用摩尔折光度R代替,即
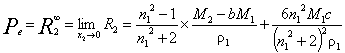 ?
?
根据测量的溶液折射率n1,2作图n1.2-x2,由斜率求出c,就可以按照式?计算出Pe 。
4. 介电常数的测定
介电常数是通过测定电容计算而得的。如果在电容器的两个板间充以某种电解质,电容器的电容量就会增大。如果维持极板上的电荷量不变,那么充电解质的电容器两板间电势差就会减少。设C0为极板间处于真空时的电容量,C为充以电解质时的电容量,则C与C0的比值ε称为该电解质的介电常数:
ε = ?
法拉第在1837年就解释了这一现象,认为这是由于电解质在电场中极化而引起的。极化作用形成一个反向电场,因而抵消了一部分外加电场。
测定电容的方法一般有电桥法、拍频法和谐振法,后两者为测定介电常数所常用,抗干扰性能好,精度高,但仪器价格昂贵。本实验中采用电桥法。实际所测得的电容C'样品包括了样品的电容C样品和电容池的分布电容Cx两部分,即
C'样品 = C样品 + Cx ?
对于给定的电容池,必须先测出其分布电容 Cx。可以先测出以空气为介质的电容,记为C'空 ,再用一种已知介电常数的标准物质,测得其电容C'标 。
C'空 = C空 + Cx
C'标 = C标 + Cx
又因为
ε标 = ≈
可得
Cx = C'空 -
C0 =
计算出 Cx 、C0 之后,根据式⑥和式?可得样品的介电常数:
ε溶 =
5. 偶极矩的计算
通过上述步骤分别计算出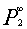 、
、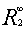 之后,根据式②可得:
之后,根据式②可得:
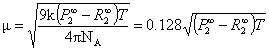
三、仪器与试剂
(1)仪器
电容测量仪、25mL容量瓶,移液管、电子天平、阿贝折射仪、滴管、烧杯、洗耳球、干燥器等。
(2)试剂
乙酸乙酯 分析纯
环己烷 分析纯
丙酮 分析纯
四、实验步骤
1. 溶液配制
将四个干燥的容量瓶编号,称量并记录空瓶重量。在空瓶内分别加入0.5mL、1.0mL、1.5mL和2.0mL的乙酸乙酯再称重。然后加环己烷至刻度线,称重。操作时应注意防止溶质、溶剂的挥发以及吸收极性较大的水汽。为此,溶液配好以后应迅速盖上瓶塞,并置于干燥器中。
2. 折射率的测定
用阿贝折射仪测定环己烷及配制溶液的折射率,注意测定时各样品需加样两次,读取数据,计算时取平均值。
3. 介电常数的测定
本实验采用环己烷作为标准物质,其介电常数的温度公式为:
ε环 = 2.023-0.0016(t-20)
式中,t为温度,℃。
打开电容测量仪,待读数稳定后,记录空气的电容值。分别测量纯环己烷和配制的4个样品溶液的电容,记录测量的数据。每个样品测量两次,计算时取平均值。测量一个样品后,需用滤纸把残留样品吸干,才能继续性测量。
五、数据处理
1. 数据处理
(1)溶液摩尔分数x的计算
(2)绘制折射率n1,2和溶液摩尔分数x2的工作曲线,并求出斜率c。
(3)计算环己烷的介电常数ε,求出电容池的分布电容Cx。
(4)计算溶液的介电常数ε。
(5)绘制ε-x2 工作曲线,由直线测得斜率a,截距ε1。
(6)绘制作ρ1,2 -x2 工作曲线,由直线测得斜率b,截距ρ1 。
(7)计算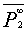 ,计算Pe 。
,计算Pe 。
(8)计算Pμ,计算偶极矩。
2.数据结果:
(1)溶液摩尔分数x的计算
表一 溶液配制及相关计算
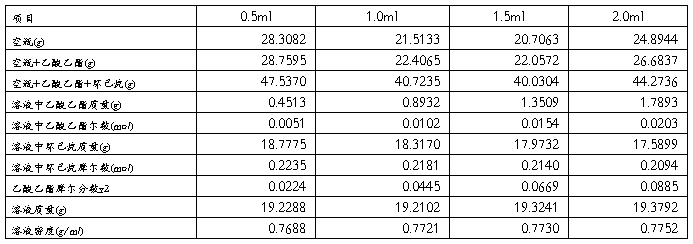
注:乙酸乙酯C4H9OH,分子量: 88
环己烷C6H12,分子量: 84
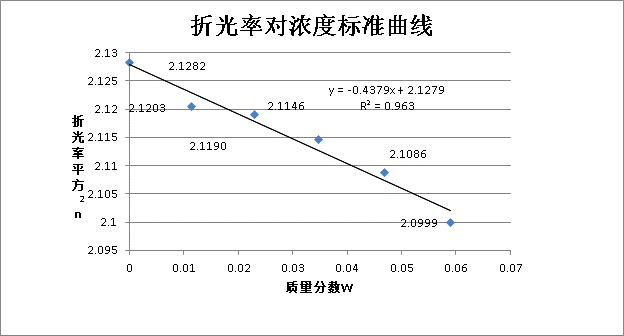
(2)绘制折射率n1,2和溶液摩尔分数x2的工作曲线,并求出斜率c
表二 折射率测定


绘制折射率n1,2和溶液摩尔分数x2的工作曲线得下图:
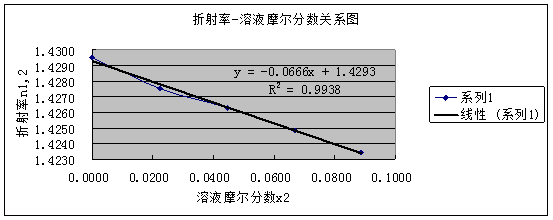
由上图可得斜率为:-0.0666 ,截距为:1.4293 ,相关系数R2为:0.9938
(3)计算环己烷的介电常数ε,求出电容池的分布电容Cx。
表三 电容测定
温度(℃):27 空气的电容(PF): 0.01
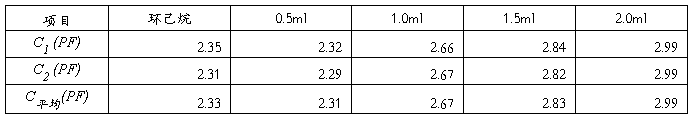
根据式ε环 = 2.023-0.0016(t-20)计算环己烷介电常数得:ε环 =2.0118
根据 Cx = C'空 - 计算电容池的分布电容为Cx =-2.28
(4)计算溶液的介电常数ε。
根据C0 = 得:C0 =2.29
根据ε溶 = 得各溶液的介电常数如下表所示:

(5)绘制ε-x2 工作曲线,由直线测得斜率a,截距ε1。
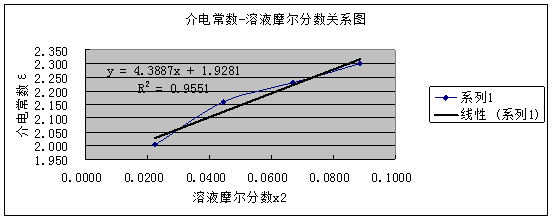
由上图可得:斜率为4.3887,截距为1.9281 ,相关系数R2为:0.9551
(6)绘制作ρ1,2 -x2 工作曲线,由直线测得斜率b,截距ρ1

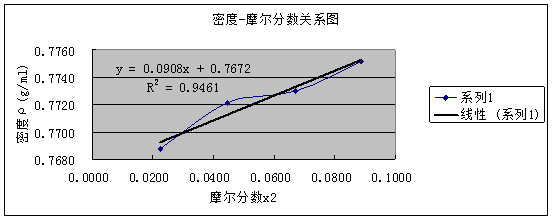
由图可得斜率为:0.0908 ,截距为0.7672 ,相关系数R2为:0.9461
(7)计算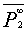 ,计算Pe 。
,计算Pe 。
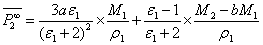 根据
根据
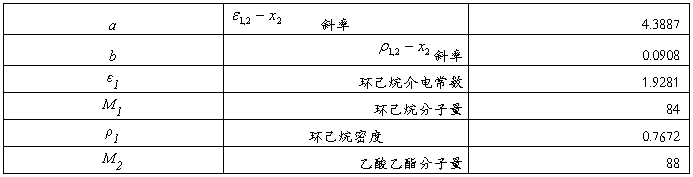
解得:204.8832
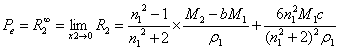 由
由
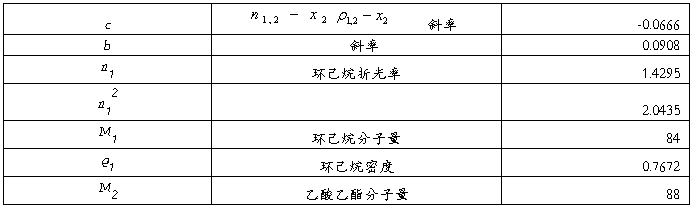
解得结果为:21.5669
(8)计算Pμ,计算偶极矩。
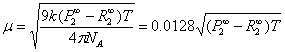 根据上述结果解得:
根据上述结果解得:
=3.0017D
六、实验评注与拓展
本实验测量项目比较多,处理数据也比较复杂。使用Guggenheim-Smith提出的简化和改进方法,用质量分数对折射率和介电常数作图,可以省去测量溶液密度的步骤。
七、实验结果分析与讨论
1、移取乙酸乙酯到容量瓶中,该过程对精确度的要求不高,因为接下来我们会称量乙酸乙酯的质量,数据处理也只用到其质量;而用环己烷定容时却应准确,因为计算溶液密度时需用到其体积。
2、误差的来源主要有:
(1) 溶液的配制:使用的容量瓶没完全干燥。配制过程中未及时称量,导致部分溶液挥发。
(2) 由于溶质和溶剂分子之间存在相互作用即溶剂化作用,导致溶液法测得的溶质偶极矩与气相所测得的真实值之间存在偏差。
(3) 实验仪器的稳定性不好,导致部分操作过程的相关系数偏低,影响实验结果的准确性。
3、实验改进:
(1) 溶液的配制:配制过程中定容需准确,先称量后再摇匀,操作是要注意防止溶质、溶剂的挥发以及吸收极性较大的水汽。为此,溶液配好后应迅速盖上瓶塞,并置于干燥器中。若溶液浑浊需重配。
(2) 折光率的测定:测定时各样品需加样两次以求平均值。取样后试剂瓶要及时盖紧,以免溶液挥发,样品滴加要均匀,以覆盖棱镜为宜,不能太少也不能有气泡,以免影响测量结果的准确性。
(3) 介电常数的测定:测空气电容时,将电容池两极间空隙吹干;每次测定前要用冷风将电容池吹干,并重测C′空,与原来的C′空值相差应小于0.02PF。测C′溶时,操作应迅速,池盖要盖紧,防止样品挥发和吸收空气中极性较大的水汽,影响测定值,溶液应透明不发生浑浊;同种样品、不同样品换样时,必须把电容池两极间空隙处的溶液抽干,然后彻底吹干。每次装入量严格相同,不能超过刻度线,样品过多会腐蚀密封材料渗入恒温腔,实验无法正常进行。
4、准确测定溶质摩尔极化度和摩尔折射度时,为什么要外推至无限稀释?
测定气相介电常数和密度在实验上困难较大,所以提出溶液法来解决这一问题,但在溶液中存在有溶质分子与溶剂分子以及溶剂分子与溶剂分子间作用的溶剂效应。溶液法的基本思想是:在无限稀释的非极性溶剂的溶液中,溶质分子所处的状态和气相时相近,于是无限稀释溶液中溶质的摩尔极化度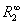 就可看作P。
就可看作P。
八、参考文献
[1]何广平,南俊民,孙艳辉等.物理化学实验[M].北京:化学工业出版社,2009.131-134.
[2]吴子生,严忠主.物理化学实验指导书[M].长春:东北师范大学出版社,1995.
[3]孙尔康,徐维清,丘金恒.物理化学实验[M].南京:南京大学出版社,2005.
第二篇:溶液法测定偶极矩
溶液法测定极性分子偶极矩实验报告
一、实验目的
1. 测定乙酸乙酯在四氯化碳中的介电常数和偶极矩,了解偶极矩与分子电性质的关系。
2. 测定某些化合物的折光率和密度,求算化合物、基团和原子的摩尔折光度,判断化合物的分子结构。
二、实验原理
分子是由带正电荷的原子核和带负电荷的电子组成的。分子呈电中性,但因空间构型的不同,正负电荷中心可能重合,也可能不重合,前者为非极性分子,后者称为极性分子,分子极性大小用偶极矩μ来度量,其定义为
μ=qd(1)
式中:q为正、负电荷中心所带的电荷量,单位是C;d是正、负电荷中心的距离,单位是m。μ是偶极矩,单位是(SI制)库[仑]米(C·m)。而过去习惯使用的单位是德拜(D):
1D =1×10-18静电单位·厘米=3.338×10-30C·m
在不存在外电场时,非极性分子虽因振动,正负电荷中心可能发生相对位移而产生瞬时偶极矩,但宏观统计平均的结果,实验测得的偶极矩为零。极性分子具有永久偶极矩,由于分子热的运动,偶极矩在空间各个方向的取向几率均等,统计值等于零。若将极性分子置于均匀的外电场中,分子将沿电场方向转动,同时还会发生电子云对分子骨架的相对移动和分子骨架的变形,称为极化。极化的程度用摩尔极化度P来度量。分子因转向而极化的程度用摩尔转向极化度P转向来表示,因变形而极化的程度用摩尔变形极化度P变形来表示。而P变形又由P电子 (电子极化度)和P原子 (原子极化度)两部分组成,于是有
P =P转向+P变形=P转向+(P电子+P原子)(2)
P转向与永久偶极矩的平方μ2的值成正比,与热力学温度T成反比: (3)
(3)
式中:NA为阿佛加德罗(Avogadro)常数;k为玻耳兹曼(Boltzmann)常数。
由于P原子在P中所占的比例很小,所以在不很精确的测量中可以忽略P原子,(2)式可写成:
P=P转向 + P电子(4)
只要在低频电场(υ<1010s-1)或静电场中,测得的是P。在中频电场(υ=1012~1014s-1) (红外频率)时,极性分子的转向运动跟不上电场的变化,故P转向=0,P =P变形=P电子+P原子。在高频电场(υ≈1015s-1)(紫外可见光)中,由于极性分子的转向和分子骨架变形跟不上电场的变化,故P转向=0,P原子=0,所以测得的是P电子。此时电子极化度可以用摩尔折射度R代替。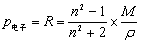 (5)
(5)
因此,分别在低频和中频电场下测出分子的摩尔极化度,两者相减即可得到P转向,再由(3)式计算μ。
通过测定偶极矩,可以了解分子中电子云的分布和分子对称性,判断几何异构体和分子的立体结构。
所谓溶液法就是将极性待测物溶于非极性溶剂中进行测定,然后外推到无限稀释。因为在无限稀的溶液中,极性溶质分子所处的状态与它在气相时十分相近,此时分子的摩尔极化度就可视为(5)的P。
在稀溶液当中,溶液的摩尔极化度P可用下式求出:
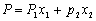 (1-溶剂,2-溶质,x-摩尔分数)(6)
(1-溶剂,2-溶质,x-摩尔分数)(6)
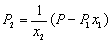
将(5)式代入(6)得
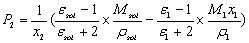
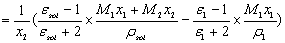
式中:sol代表溶液,ε1,M1,ρ1分别是溶剂的相对介电常数、摩尔质量和密度。M2为溶质摩尔质量。
为了省去溶液密度的测量,经Guggenheim和Smith的简化与改进,得到如下公式:
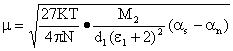
d1为溶剂的密度。
分子的偶极矩可按下式计算:
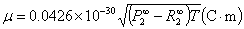
式中,P∞2和R∞2分别表示无限稀时极性分子的摩尔极化度和摩尔折射度(习惯上用摩尔折射度表示折射法测定的P电子);T是热力学温度。
三、仪器与试剂
1、仪器
阿贝折光仪,电容测试仪,电容池,电吹风,吸量管。
2、试剂
氯化碳,乙酸乙酯
四、实验步骤
1、标准溶液的配制
准确6组配制含乙酸乙酯的四氯化碳溶液,其质量分数为0.01~0.05
2、介电常数的测定
介电常数ε可通过测量电容来求算
ε = C/C0
式中,C0为电容器在真空时的电容;C为充满待测液时的电容,由于空气的电容非常接近于C0,故(11)式改写成
ε=C/C空
由于整个测试系统存在分布电容,所以实测的电容C′是样品电容C和分布电容Cd之和,即
C′=C +Cd
显然,为了求C首先就要确定Cd值,方法是:先测定无样品时空气的电空C′空,则有
C′空 =C空 + Cd
再测定一已知介电常数(ε标)的标准物质的电容C′标,则有
C′标 = C标+Cd=ε标C空 + Cd
可得: 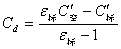
将Cd代入即可求得C溶和C空。这样就可计算待测液的介电常数。
3、测定折光率
在室温条件下用阿贝折光仪测定环己烷及各配制溶液的折光率.测定时注意各样品需加样三次,每次读取四个数据,然后取平均值.
4、测定样品的电容和折光率
电容值读取3组,折光率与之前测量方法相同。
五、数据记录与处理

(2)计算电容C0和C分
室温为19.5℃,则环己烷介电常数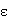 =2.0238
=2.0238

带入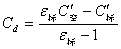 ,计算的Cd=2.12PF,C0=2.52pF
,计算的Cd=2.12PF,C0=2.52pF
(3)由样品折光率计算样品质量组成
将测得的折光率求平均后平方,带入之前做出的标准曲线,即可得到样品的质量分数

(4)计算样品介电常数,做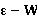 图
图
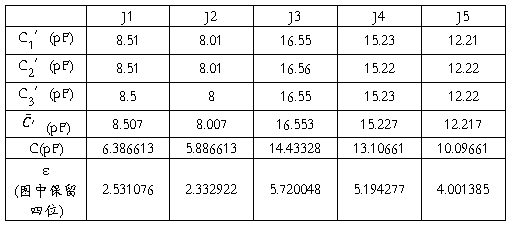
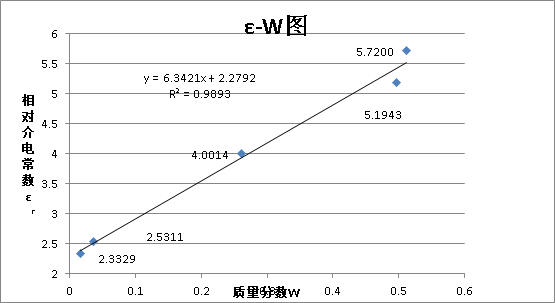
(5)计算偶极矩
利用公式
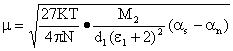 其中
其中 =6.3421,
=6.3421,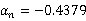 ,
,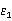 =2.2792
=2.2792
求的
六、注意事项
1、测C’溶时,操作应迅速,池盖要盖紧,防止样品挥发和吸收空气中极性较大的水汽。装样品的滴瓶也要随时盖严。
2、注意不要用力扭曲电容仪连接电容池的电缆线,以免损坏。
3、使用密度管进水口是无小球的一端,不能颠倒。
4、重复测定时,要倾去原溶液,电容池干燥后再测定。
七、思考题
1、偶极矩是如何定义的?
分子可近似看成由电子云与分子骨架(包括原子核与内层电子)组成。非极性分子的正负电荷中心是重合的,而极性分子的正负电荷中心是分离的,其分离程度的大小于分子的极性大小有关,可用“偶极矩”这一物理量来描述。以q代表正负电荷中心所带的电荷量,d代表正负电荷之间的距离,则分子的偶极矩:μ=q·d μ为矢量,其方向规定为从正电荷中心到负电荷中心。
2、试分析本实验中误差的主要来源,如何改进?
1在测定溶液的折光率时发现,不同浓度的溶液的折光率几乎不发生变化,这导致了读数上的偏差。由于过于接近,数据稍有偏差就会造成大的影响。所以最后n1-x2图拟合程度并不是很好。建议采用多次读数,或采用更精确的仪器来测定折光率。
2上学期使用过的密度管再次成为实验误差的罪魁祸首,由于1滴水造成的影响就有0.05g,而密度管就在这个数量级上操作。由于难于把握密度管中的水的流动,造成密度管称量的不精确。这是实验误差的主要来源,建议弃用密度管。换其他测密度的仪器。
3本实验没有采用25度恒温操作,读数是在室温下读数,而测电容确实是恒温箱中的温度。所以这里面的温度差导致了实验误差,建议将两者温度统一。
4使用电容池时,由于不方便拔下电容池的两极,故无法容易的将电容池两级间空隙处的溶液抽干,也无法用电吹风吹干,只能用纸巾去擦干,这过程会实验结果造成偏差。
八、结果与讨论
本次测得氯仿分子的偶极矩为1.13D,与文献值1.11~1.22D相对照,发现本次实验应该是取得了圆满的成功。但介于上述讨论的误差分析,可能实验结果也是由于错进错出才比较精确。若能消除一些误差来源,相信实验将会更加精确。
另外由于三氯甲烷有毒性,具有麻醉作用,对心、肝、肾有损害。所以实验时一定要格外小心,避免碰触液体,吸入蒸汽。最好在通风橱进行操作,同时要佩戴防护眼镜和面具。
