实验十二 偶极矩的测定
摘要:本实验利用溶液法,通过测定不同浓度的正丁醇的环己烷溶液在同一条件(20℃、1atm)下的折射率、电容、密度等各种性质计算出分子的偶极矩,并对比实验结果分析了解电介质在外电场中的极化现象。
关键词 : 极化现象偶极矩 溶液法
前言:分子结构可以被看成是由电子和分子骨架所构成。由于其空间构型不同其正负电荷中心可以重合,也可以不重合,前者称为非极性分子,后者称为极性分子,分子的极性可用偶极矩来表示。
电介质分子处于电场中,电场会使非极性分子的正负电荷中心发生相对位移而变得不重合,电场也会使极性分子的正负电荷中心间距增大这样会使分子产生附加的偶极矩(诱导偶极矩)。这种现象称为分子的变形极化。可以用平均诱导偶极矩m来表示变形极化的程度。在中等电场下设
m = α DE内 (1)
式中E内为作用于个别分子上的强场。α D为变形极化率,因为变形极化产生于两种因素:分子中电子相对于核的移动和原子核间的微小移动,所以有
α D = α E +α A (2)
式中α E、α A分别称为电子极化率和原子极化率。
有Clausius-Mosotti方程,
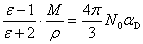 (3)
(3)
定义摩尔变形极化度PD为
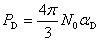 (4)
(4)
电场中的分子除了变形极化外,还会产生取向极化,即具有永久偶极矩的分子在电场的作用下,会或多或少地转向电场方向。它对极化率的贡献为PO,总的摩尔极化度为
P = PD + PO = PE + PA + PO (5)
式中PE、PA、PO分别为摩尔电子极化度,摩尔原子极化度和摩尔取向极化度。
如将电介质置于交变电场中,则其极化和电场变化的频率有关。交变电场的频率小于1010秒-1时,极性分子的摩尔极化度P中包含了电子原子和取向的贡献。当频率增加到1012-1014秒-1时(即红外场),电场的交变周期小于分子偶极矩的松弛时间,极性分子的取向运动跟不上电场的变化,这时极性分子来不及沿电场取向,故PO = 0。当交变电场的 频率进一步增加到大于1015秒-1高频场(可见光和紫外)时,分子的取向和分子骨架的变形都跟不上电场的变化,这时PO = 0、PA = 0、P = PE。这时ε = n2,n为介质的折射率,这时的摩尔极化度称为摩尔折射度R
频率进一步增加到大于1015秒-1高频场(可见光和紫外)时,分子的取向和分子骨架的变形都跟不上电场的变化,这时PO = 0、PA = 0、P = PE。这时ε = n2,n为介质的折射率,这时的摩尔极化度称为摩尔折射度R
 (6)
(6)
因为PA只有PE的10%左右,一般可以略去,或按PE10%修正。
计算μ,有
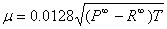 (7)
(7)
在实验中要测不同浓度下的P、R,即可用外推法求P∞和R∞。
对于由溶剂1和溶剂2组成的溶液体系,根据Hedestrand(Z. Phys. Cnem.,2438(1929))的理论,其介电常数、折射率、摩尔极化度以及密度均和浓度成线性关系。
这样我们用交变频率为1000HZ的交流电桥测出电容池中各浓度下溶液的电容,用此电容除以真空下电容池的电容即得介电常数。用阿贝折射仪测出可见光下各溶液的折射率,再用分析天平测出各溶液的密度,经过相关计算即可算出分子的永久偶极矩μ。
实验部分
(一) 仪器与试剂
试剂:正丁醇(分析纯)
环已烷(分析纯)
仪器:容量瓶(50毫升)5只
5毫升移液管5支
胶头滴管5只
阿贝折射仪一台
分析天平一台
超级恒温槽一台
电吹风一只
CCJ-1型精密电容测量仪一台
电容池1只
(二) 实验过程
1.溶液配制
用称量法配制0%、1%、5%、10%和15%(摩尔分数)的环已烷溶液各20毫升(除0%外,其余溶液的浓度只要求精确标出浓度值,其值控制在1%、5%、10%、15%左右)。操作时应注意防止溶质、溶剂的挥发以及吸收水汽。为此溶液配好后应迅速盖上瓶盖并置于干燥器中。
2.折射率的测定
用阿贝折射仪测出溶液的折射率。测定时各样品需加样三次,每次取三个数据,最后取平均值。
3.介质常数的测定
(1)电容池分布电容Cd和真空电容Co的测定
因为电容池总是存在着和真空电容Co并联的分布电容Cd,为了从实测溶液的电容中扣除此分布电容的影响,我们必须测出此分布电容。
用电吹风将电容池二极间的空隙吹干,旋上金属盖,将恒温槽电源打开,使温度固定在某一实验工作温度,测定其电容Co。测量中要反复交替调节相位平衡旋钮,使表头指针趋于最小,电桥平衡后,读出电容值,重复调节三次,以三次读数的平均值。
再用针筒吸取纯环已烷加入电容池,使液面超过二电极表面。恒温数分钟后如上述步骤测定电容值。然后打开金属盖,用针筒吸取二极间的环已烷,重新装入样品,再次测定电容值,取二次平均值为C环。
由于Cd总是并联于电容池,所以有
ε环 = C环 / Co = 2.023-0.0016 ( t-20 ) (8)
C ′环 = C环 + Cd (9)
C ′o = Co + Cd (10)
式中t为(℃),(8)式为环已烷的介电常数随温度变化的公式,解上述方程组,可得Co、Cd。
(2)加溶液电容的测定
测定方法同于纯环已烷。重复测定时,要去掉电极间的溶液,还要用电吹风将二极间的空隙吹干,然后再加入该浓度溶液,恒温数分钟,测出电容值。两次测定数的差值应小于0.05PF,否则要重新测量。测得的电容减去Cd后才是该溶液对应的电容值。
4.溶液密度的测定
用比重瓶在分析天平上分别称得瓶重W0,加液后的质量W1,和加水后的W2,按
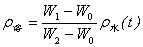 (11)
(11)
计算溶液的密度ρ溶。式中ρ水 ( t )为在工作温度下的密度,可由表中查出。
测量中要避免比重瓶中气泡的产生,等测完所有溶液的密度后,才加水测量W2。
结果与讨论
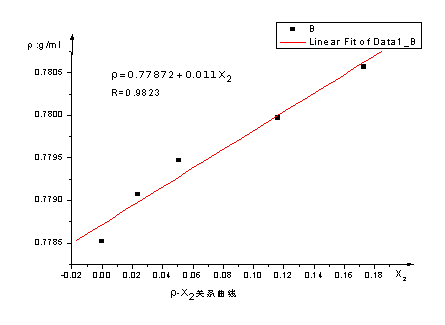
1、计算各溶液的摩尔分数浓度X2及各溶液的密度ρ,作ρ溶-X2图,用β = 斜率 / ρ环 算出β。
作ρ溶-X2图,线性拟合得到:
斜率=0.011
所以β = 斜率 / ρ环 =0.011/0.77852=0.01413
2.作n溶-X2图,用γ = 斜率 / n环 算出γ。
作n溶-X2图,线性拟合得到:
斜率=-0.03184
γ = 斜率 / n环=-0.03184/1.4256= -0.022315
3、算出Co、Cd和ε溶,由ε溶 = C溶 / Co算出ε溶,作ε溶-X2图,由α = 斜率 /ε环 算出α。
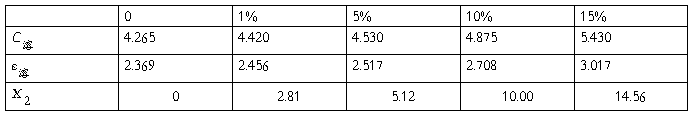
T=20℃
ε环 = C环 / Co=2.203 (8) C ′环 = C环 + Cd (9) C ′o = Co+ Cd (10)
联立(8)(9)(10)建立方程,得到:
Co=1.800PF Cd=2.515PF
由C溶=C ′溶-Cd,ε溶 = C溶/ Co计算可得C溶与ε溶,
并做ε溶-X 2图,线性拟合,可得
斜率为:4.360
α = 斜率 /ε环=4.360/2.369=1.84
4、算出P∞,R∞,以及正丁醇的偶数矩μ
由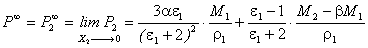

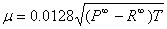
以及1~3中算出来的相关值,可以计算得到:
P∞=103.42
R∞= 21.43
μ=1.98 Debye
5.实验误差
查阅《兰氏化学手册》知正丁醇的固有偶极矩为1.66Debye故误差为:
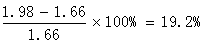
通过上面的计算可以看出,所有的曲线并不严格成线性,而实验中的很多原因也会导致最终的实验误差,比如:(1)尽管实验要求尽快地进行实验,并且在实验过程中要将瓶塞塞好,但是溶液中两种物质挥发度不同,实验过程中溶液的浓度的改变对于测量结果仍有影响;(2)电容测量仪老化,读数跳跃大、不稳定,实验中通过多次测量取平均的方法来减小这一误差,但是仍对结果有一定的影响;(3)实验测密度并没有用比重法,而是直接计算正丁醇和环己烷的总质量后除以20ml得到,20ml只是正丁醇和环己烷各自体积的代数和,并没有严格测量;(4)实验推导中忽略了分子间相互作用,故需要用稀溶液进行实验,但事实上稀溶液中分子也存在一定的作用,会导致系统误差;(5)实验忽略了分子间作用,存在系统误差。
结论:
电介质分子处于电场中,电场会使非极性分子的正负电荷中心发生相对位移而变得不重合,电场也会使极性分子的正负电荷中心间距增大这样会使分子产生附加的偶极矩(诱导偶极矩)。具有永久偶极矩的分子在电场的作用下,会稍微
地转向电场方向,而对于溶液来说,其浓度、密度、电容和折射率等性质与其极化率有关。本实验利用溶液法,通过测定不同浓度的正丁醇溶液在同一条件下的折射率、电容、密度等各种性质计算出分子的永久偶极矩,计算得到正丁醇的永久偶极矩为1.98 Debye。
参考文献
《物理化学实验》崔献英,柯燕雄,单绍纯 中国科学技术大学出版社
《物理化学》傅献彩等 高等教育出版社
《普通化学原理》华彤文等 北京大学出版社
《兰氏化学手册》
Determination of dipole moment matter
Abstract:The determination of the different concentrations of n-butanol solution of the refractive index in the same condition, capacitance, density and other properties, familiar with the dipole moment of the solution method for the determination of the principles of material and methods, and compare the experimental results to understand the dielectric in uniform electric field Polarization.
Keywords:polarization, dipole moment, the solution method
附件:
1、计算各溶液的摩尔分数浓度X2及各溶液的密度ρ,作ρ溶-X2图,用β = 斜率 / ρ环 算出β。
Table1正丁醇摩尔分数
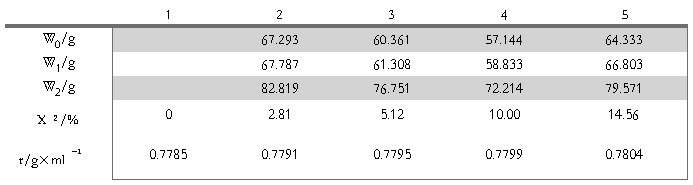
作ρ溶-X2图,线性拟合可以得到:
斜率=0.011
所以β = 斜率 / ρ环 =0.011/0.77852=0.01413
2.作n溶-X2图,用γ = 斜率 / n环 算出γ。
Table2 折射率
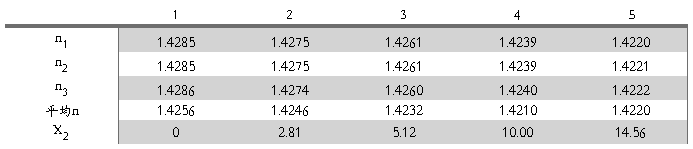
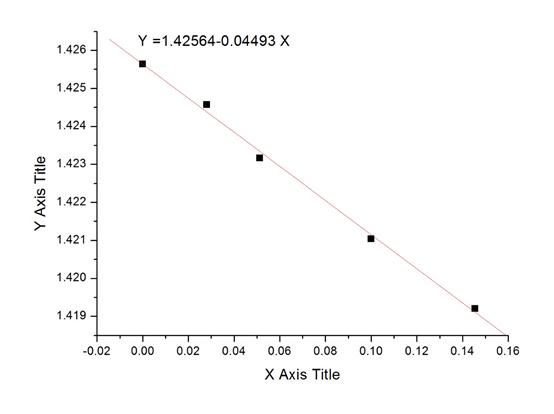
作n溶-X2图,线性拟合得到:
斜率=-0.04493
γ = 斜率 / n环=-0.04493/1.4256= -0.03149
3、算出Co、Cd和ε溶,由ε溶 = C溶 / Co算出ε溶,作ε溶-X2图,由α = 斜率 /ε环 算出α。
T=20℃
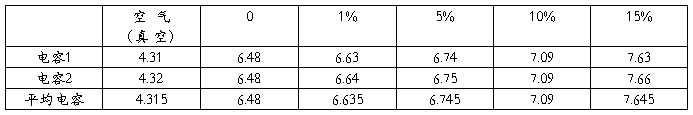
则ε环 = C环 / Co = 2.023-0.0016*( T-20 )=2.023
ε环 = C环 / Co (8) C ′环 = C环 + Cd (9) C ′o = Co+ Cd (10)
联立(8)(9)(10)建立方程,
则Co=1.800PF Cd=2.515PF
由C溶=C ′溶-Cd,ε溶 = C溶/ Co计算可得C溶与ε溶,结果如下:
以ε溶对X 2作图,可得
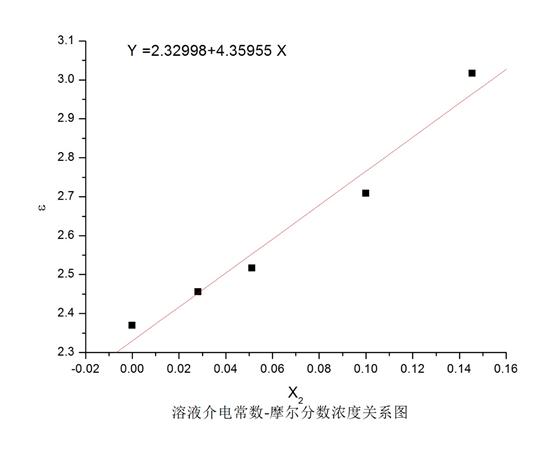
斜率为:4.360
α = 斜率 /ε环=4.360/2.369=1.84
4、将α、β、ρ1、ε1代入公式算出P∞。
有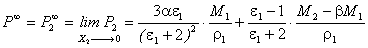
相关数据如下:
β =0.01413 α =1.84
ε环=2.369 ρ环=0.77852g/mL M环=84.16g/mol M正=74.12g/mol
代入可得,
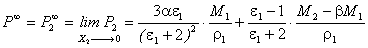
=
=103.42
5、将β、γ、n1、ρ1代入公式算出R∞。
有
相关数据如下:
β=0.01413 γ=-0.03149
ρ环=0.77852g/mL n环=1.4256 M环=84.16g/mol M正=74.12g/mol
代入可得,

=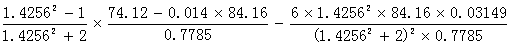
= 21.4343
6、将P∞和R∞代入公式计算出正丁醇的偶数矩μ。
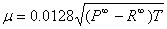
=0.0128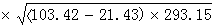
=1.98 Debye
第二篇:物理化学实验报告_偶极矩
华南师范大学实验报告
课程名称:结构实验 实验项目:稀溶液法测定偶极矩
实验类型:□验证□设计□综合 实验时间:20##年11月20日
一、实验名称:稀溶液法测定偶极矩
二、实验目的
(1) 掌握溶液法测定偶极矩的主要实验技术。
(2) 了解偶极矩与分子电性质的关系。
(3) 用溶液法测定乙酸乙酯的偶极矩。
三、实验原理
(1) 偶极矩与极化度:分子结构可以近似地看成是由电子云和分子骨架(原子核及内层电子)所构成。由于其空间构型的不同,其正负电荷中心可以是重合的,也可以不重合。前者称为非极性分子,后者称为极性分子。

图1电偶极矩示意图 图2极性分子在电场作用下的定向
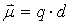 1912年德拜提出“偶极矩”
1912年德拜提出“偶极矩” 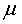 的概念来度量分子极性的大小,如图1所示,其定义是 (1)
的概念来度量分子极性的大小,如图1所示,其定义是 (1)
式中,q是正负电荷中心所带的电量; d为正负电荷中心之间的距离;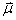 是一个向量,其方向规定为从正到负。因分子中原子间的距离的数量级为10-10m,电荷的数量级为10-20C,所以偶极矩的数量级是10-30C·m。
是一个向量,其方向规定为从正到负。因分子中原子间的距离的数量级为10-10m,电荷的数量级为10-20C,所以偶极矩的数量级是10-30C·m。
通过偶极矩的测定,可以了解分子结构中有关电子云的分布和分子的对称性,可以用来鉴别几何异构体和分子的立体结构等。
极性分子具有永久偶极矩,但由于分子的热运动,偶极矩指向某个方向的机会均等。所以偶极矩的统计值等于零。若将极性分子置于均匀的电场E中,则偶极矩在电场的作用下,如图2所示趋向电场方向排列。这时我们称这些分子被极化了。极化的程度可用摩尔转向极化度P转向来衡量。
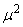
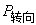 与永久偶极矩 的值成正比,与绝对温度T成反比。
与永久偶极矩 的值成正比,与绝对温度T成反比。
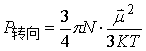
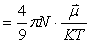 (2)
(2)
式中: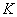 为玻兹曼常数,
为玻兹曼常数,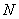 为阿伏加德罗常数。
为阿伏加德罗常数。
在外电场作用下,不论极性分子或非极性分子,都会发生电子云对分子骨架的相对移动,分子骨架也会发生形变。这称为诱导极化或变形极化。用摩尔诱导极化度P诱导来衡量。显然P诱导可分为二项,即电子极化度P电子和原子极化度P原子,因此P诱导=P电子+P原子。P诱导与外电场强度成正比,与温度无关。
如果外电场是交变场,极性分子的极化情况则与交变场的频率有关。当处于频率小于1010s-1的低频电场或静电场中,极性分子所产生的摩尔极化度P是转向极化、电子极化和原子极化的总和。
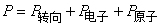 (3)
(3)
当频率增加到1012~1014的中频(红外频率)时,电子的交变周期小于分子偶极矩的松弛时间,极性分子的转向运动跟不上电场的变化,即极性分子来不及沿电场方向定向,故 =0,此时极性分子的摩尔极化度等于摩尔诱导极化度 。当交变电场的频率进一步增加到>1015秒-1的高频(可见光和紫外频率)时,极向分子的转向运动和分子骨架变形都跟不上电场的变化。此时极性分子的摩尔极化度等于电子极化度 。
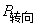
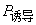
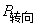
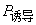
 因此,原则上只要在低频电场下测得极性分子的摩尔极化度
因此,原则上只要在低频电场下测得极性分子的摩尔极化度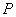 ,在红外频率下测得极性分子的摩尔诱导极化度 ,两者相减得到极性分子摩尔转向极化度 ,然后代入(2)式就可算出极性分子的永久偶极矩
,在红外频率下测得极性分子的摩尔诱导极化度 ,两者相减得到极性分子摩尔转向极化度 ,然后代入(2)式就可算出极性分子的永久偶极矩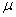 来。
来。
(2) 极化度的测定:克劳修斯、莫索和德拜从电磁场理论得到了摩尔极化度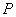 与介电常数ε之间的关系式:
与介电常数ε之间的关系式:
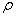
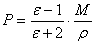 (4)式中,
(4)式中,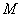 为被测物质的分子量; 为该物质在
为被测物质的分子量; 为该物质在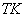 下的密度;ε可以通过实验测定。
下的密度;ε可以通过实验测定。
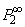 但(1)式是假定分子与分子间无相互作用而推导得到的。所以它只适用于温度不太低的气相体系,对某些物质甚至根本无法获得气相状态。因此后来提出了用一种溶液来解决这一困难。溶液法的基本想法是,在无限稀释的非极性溶剂的溶液中,溶质分子所处的状态和气相时相近,于是无限稀释溶液中溶质的摩尔极化度 , 就可以看作为(4)式中的
但(1)式是假定分子与分子间无相互作用而推导得到的。所以它只适用于温度不太低的气相体系,对某些物质甚至根本无法获得气相状态。因此后来提出了用一种溶液来解决这一困难。溶液法的基本想法是,在无限稀释的非极性溶剂的溶液中,溶质分子所处的状态和气相时相近,于是无限稀释溶液中溶质的摩尔极化度 , 就可以看作为(4)式中的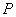 。海台斯纳特首先利用稀释溶液的近似公式。
。海台斯纳特首先利用稀释溶液的近似公式。
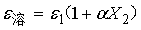 (5)
(5) 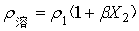 (6)
(6)
再根据溶液的加和性,推导出无限稀释时溶质摩尔极化度的公式:
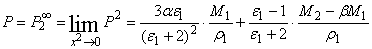 (7)
(7)

 上述(5)、(6)、(7)式中,
上述(5)、(6)、(7)式中,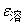 、
、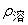 是溶液的介电电常数和密度;M2、 X2 是溶质的分子量和摩尔分子数;ε1、p1、M1分别是溶剂的介电常数、密度和分子量;α、β是分别与 直线斜率有关的常数。
是溶液的介电电常数和密度;M2、 X2 是溶质的分子量和摩尔分子数;ε1、p1、M1分别是溶剂的介电常数、密度和分子量;α、β是分别与 直线斜率有关的常数。
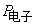 上面已经提到,在红外频率的电场下,可以测得极性分子摩尔诱导极化度 。但是在实验上由于条件的限制,很难做到这一点。所以一般总是在高频电场下测定极性分子的电子极化度 。
上面已经提到,在红外频率的电场下,可以测得极性分子摩尔诱导极化度 。但是在实验上由于条件的限制,很难做到这一点。所以一般总是在高频电场下测定极性分子的电子极化度 。
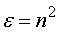 根据光的电磁理论,在同一频率的高频电场作用下,透明物质的介电常数
根据光的电磁理论,在同一频率的高频电场作用下,透明物质的介电常数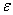 与折光率
与折光率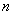 的关系为: (8)
的关系为: (8)
习惯上用摩尔折射度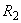 来表示高频区测得的极化度,而此时,
来表示高频区测得的极化度,而此时, ,
,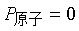 .
.
则 (9)
(9)
在稀溶液情况下,还存在近似公式:

同样,从(9)式可以推导得无限稀释时,溶质的摩尔折射度的公式:
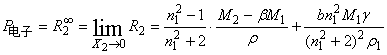 (11)
(11)
上述(10)、(11)式中,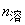 是溶液的折射率,
是溶液的折射率, 是溶剂的折射率,γ是与
是溶剂的折射率,γ是与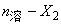 直线斜率有关的常数。
直线斜率有关的常数。

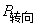 (3) 偶极矩的测定:考虑到原子极化度通常只有电子极化度的5%~15%,而且 又比 大得多,故常常忽视原子极化度。
(3) 偶极矩的测定:考虑到原子极化度通常只有电子极化度的5%~15%,而且 又比 大得多,故常常忽视原子极化度。
从(2)、(3)、(7)和(11)式可得
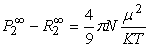 (12)
(12)
上式把物质分子的微观性质偶极矩和它的宏观性质介电常数、密度、折射率联系起来,分子的永久偶极矩就可用下面简化式计算:

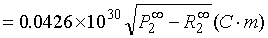 (13)
(13)
在某种情况下,若需要考虑  影响时,只需对
影响时,只需对 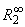 作部分修正就行了。
作部分修正就行了。
上述测求极性分子偶极矩的方法称为溶液法。溶液法测溶质偶极矩与气相测得的真实值间存在偏差。造成这种现象的原因是由于非极性溶剂与极性溶质分子相互间的作用—“溶剂化”作用。这种偏差现象称为溶剂法测量偶极矩的“溶剂效应”。
此外测定偶极矩的方法还有多种,如温度法、分子束法、分子光谱法及利用微波谱的斯诺克法等。
(4) 介电常数的测定:介电常数是通过测定电容计算而得的。
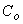 我们知道,如果在电容器的两个极板间充以某种电解质,电容器的电容量就会增大。如果维持极板上的电荷量不变,那么充电解质的电容器二板间电势差就会减少。设 为极板间处于真空时的电容量,
我们知道,如果在电容器的两个极板间充以某种电解质,电容器的电容量就会增大。如果维持极板上的电荷量不变,那么充电解质的电容器二板间电势差就会减少。设 为极板间处于真空时的电容量, 为充以电解质时的电容量,则
为充以电解质时的电容量,则 与 之比值ε称为该电解质的介电常数:
与 之比值ε称为该电解质的介电常数:
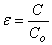 (14)
(14)
法拉第在1837年就解释了这一现象,认为这是由于电解质在电场中极化而引起的。极化作用形成一反向电场,因而抵消了一部分外加电场。
测定电容的方法一般有电桥法、拍频法和谐振法,后二者为测定介电常数所常用,抗干扰性能好,精度高,但仪器价格较贵。本实验中采用电桥法,选用的仪器为CC—6型小电容测定仪。其桥路为变压器比例臂电桥。电桥平衡条件是:
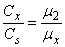
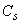
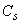
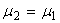

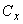

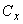 为电容池二极之间的电容, 为标准的差动电容器,调节 ,只有当 时, 。此时指示放大器的输出趋近于零(用表头指示)。 值可以从度盘上直接读出, 值也即得到。
为电容池二极之间的电容, 为标准的差动电容器,调节 ,只有当 时, 。此时指示放大器的输出趋近于零(用表头指示)。 值可以从度盘上直接读出, 值也即得到。
由于在电桥法测量电路中被测电容 二端都不能接地,因此恒温介质不能用水。本实验中采用介电常数很小的变压器油。变压器油从超级温槽中用循环泵压出,经电容池再回入。温度由超级恒温槽控制在25±0.1℃,电容池外壳兼作屏蔽之用,并直接插入仪器插孔上,这样就可以避免人体对测量的影响。
二端都不能接地,因此恒温介质不能用水。本实验中采用介电常数很小的变压器油。变压器油从超级温槽中用循环泵压出,经电容池再回入。温度由超级恒温槽控制在25±0.1℃,电容池外壳兼作屏蔽之用,并直接插入仪器插孔上,这样就可以避免人体对测量的影响。
但电容池插在小电容测量仪的插孔上呈现的电容Cx可看作电容池两电极间的电容Cc和整个测试系统中的分布电容并联所构成。即Cx=Co +Cd,显然,Cc值随介质而异,而Cd 是一个恒定值。如果直接将Cx 值当作Cc值来计算,就会引进误差。因此,必须先求出 Cd 值(又称底值)并在以后的各次测量中给予扣除。
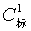 测求Cd的方法如下:用一个已知介电常数的标准物质测得电容
测求Cd的方法如下:用一个已知介电常数的标准物质测得电容
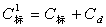 (Ⅱ-29-16)
(Ⅱ-29-16)


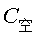 上述(Ⅱ-29-15)、(Ⅱ-29-16)式中 、 分别为标准物质和空气的电容。近似地可将 ,则:
上述(Ⅱ-29-15)、(Ⅱ-29-16)式中 、 分别为标准物质和空气的电容。近似地可将 ,则:

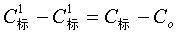 (Ⅱ-29-17)
(Ⅱ-29-17)
因:
(Ⅱ-29-18)
代入(Ⅱ-29-16)即能算出Cd。
四、注意事项
1、本实验测量项目比较多,数据处理也较复杂,所以,一定要做好实验的记录。
2.本实验溶液中防止含有水分,所配制溶液的器具需干燥,溶液应透明不发生浑浊.
3.测定电容时,应防止溶液的挥发及吸收空气中极性较大的水汽,影响测定值.
4.电容池个部件的连接应注意绝缘。
五、仪器 试剂
(1)仪器
阿贝折光仪 1台 容量瓶(25mL) 5个
CC—6型小电容测定仪 1台 干燥器 1只
电子天平 移液管
滴管、洗耳球、烧杯
(2)试剂
乙酸乙酯(分析纯) 环己烷(分析纯)
丙酮(分析纯)
五、 实验步骤
(1) 溶液配制:将4个干燥的容量瓶编号,分别称量空瓶重。在空瓶内分别加入0.5mL、1.0mL、1.5mL和2.0mL的乙酸乙酯再称重。然后加环己烷至刻度,再称重。操作时应注意防止溶质、溶剂的挥发以及吸收极性较大的水汽。为此,溶液配好后应迅速盖上瓶塞,并置于干燥器中。
(2) 折光率的测定:用阿贝折光仪测定环己烷及各配制溶液的折光率,注意测定时各样品需加样2次,计算时取平均值。
(3) 介电常数的测定
①电容C0和Cd的测定。本实验采用环己烷作为标准物质。其介电常数的温度公式为:
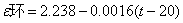
式中的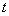 为恒温温度(摄氏温标)。
为恒温温度(摄氏温标)。
打开电容测试仪,待读书稳定后,记录客气的电容值。分别测量纯环己烷和配制的4个样品溶液的电容,记录测量数据。每个样品测量2次,计算时取平均值。
六、 数据处理(部分数据记录与处理在末页)
1、溶液摩尔分数X2的计算。
2、绘制折光率n1,2和溶液摩尔分数X2的工作曲线,求出直线斜率求α:
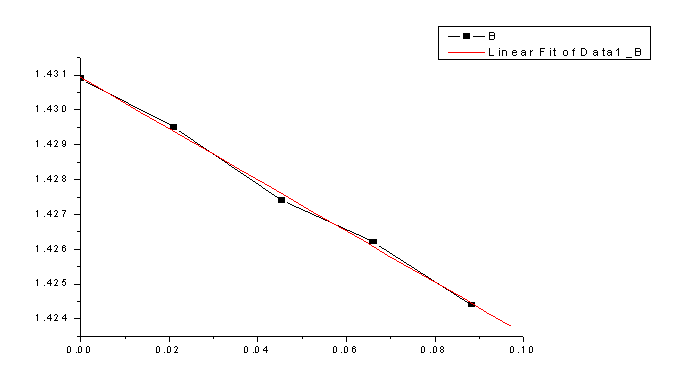 [20##-12-2 23:16 "/Graph1" (2455167)]
[20##-12-2 23:16 "/Graph1" (2455167)]
Linear Regression for Data1_B:
Y = A + B * X
Parameter Value Error
------------------------------------------------------------
A 1.43093 1.18269E-4
B -0.07357 0.00218
------------------------------------------------------------
R SD N P
------------------------------------------------------------
-0.99868 1.53078E-4 5 <0.0001
3、计算环己烷的介电常数ε,电容池的分布电容Cx,并求出溶液的介电常数ε:
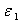 4、作ε—X2图,由直线斜率求得β,截距 ;
4、作ε—X2图,由直线斜率求得β,截距 ;
 作 —X2图,由直线斜率求得γ,截距 。
作 —X2图,由直线斜率求得γ,截距 。

Y = A + B * X
Parameter Value Error
------------------------------------------------------------
A 2.00123 0.01919
B 1.08704 0.27846
------------------------------------------------------------
R SD N P
------------------------------------------------------------
0.96872 0.00847 3 0.15965
------------------------------------------------------------
[20##-12-2 23:12 "/Graph1" (2455167)]
Linear Regression for Data1_B:
Y = A + B * X
Parameter Value Error
------------------------------------------------------------
A 2.02917 0.00572
B 0.99692 0.09431
------------------------------------------------------------
R SD N P
------------------------------------------------------------
0.99117 0.0047 4 0.00883
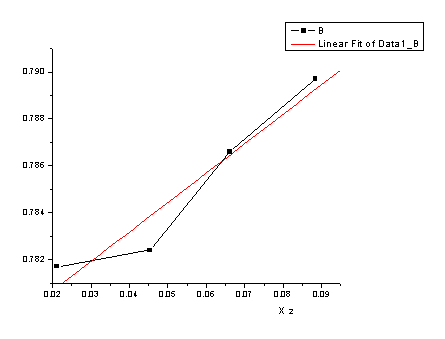
[20##-12-2 23:06 "/Graph1" (2455167)]
Linear Regression for Data1_B:
Y = A + B * X
Parameter Value Error
------------------------------------------------------------
A 0.77816 0.00152
B 0.1256 0.02516
------------------------------------------------------------
R SD N P
------------------------------------------------------------
0.96213 0.00125 4 0.03787
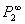
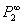 5、根据(Ⅱ-29-7)式,求得 。
5、根据(Ⅱ-29-7)式,求得 。
6、 将 、 (即P电子)值代入(Ⅱ-29-13)式计算偶极矩μ。(见末页)
七 思考题
1.准确测定溶质摩尔极化度和摩尔折射度时,为什么要外推至无限稀释 ?
答:测定气相介电常数和密度在实验上困难较大,所以提出溶液法来解决这一问题,但在溶液中存在有溶质分子与溶剂分子以及溶剂分子与溶剂分子间作用的溶剂效应.溶液法的基本思想是:在无限稀释的非极性溶剂的溶液中,溶质分子所处的状态和气相时相近,于是无限稀释溶液中溶质的摩尔极化度就可看作P.
2、电容池的使用应注意哪些问题?
答:(1)测空气电容时,将电容池两极间空隙吹干;
(2)溶液注入电容池时,所加溶液的量必须淹没电容池的两电极;
(3)同种样品、不同样品换样时,必须把电容池两极间空隙处的溶液抽干,然后彻底吹干。
八、讨论
1.从偶极矩的数据可以了解分子的对称性,判别其几何异构体和分子的主体结构等问题.偶极矩一般是通过测定介电常数,密度,折射率和浓度来求算的.对介电常数的测定除电桥法外,其他还有拍频法和谐振法等.对气体和电导很小的液体以拍频法为好,有相当电导的液体用谐振法较为合适;对于有一定电导但不大的液体用电桥法较为理想.
2.溶液法测得的溶质偶极矩和气相测得的真空值之间存在着偏差,造成这种偏差现象主要是由于在溶液中存在有溶质分子与溶剂分子以及溶剂分子与溶剂分子间作用的溶剂效应.
九、参考文献
【1】何广平,男俊民 等. 物理化学实验 。北京:化学工业出版社,2007。12
【2】韩喜江,张云天。物理化学实验。哈尔滨:哈尔滨工业出版社,2004,4
【3】傅献彩,沈云霞,姚天杨。物理化学,第四版。北京:高等教育出版社,1990
