六、实验数据处理
1、计算各溶液的摩尔分数浓度x2.
表1、实验数据处理表一
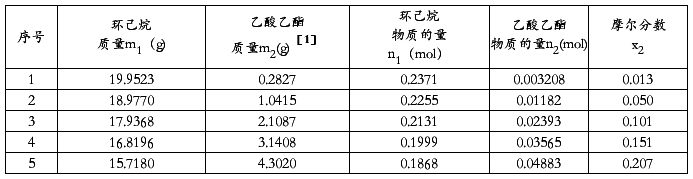
计算过程举例:(以序号1为例)
已知:环己烷相对分子质量M1=84.16g/mol、乙酸乙酯相对分子质量M2=88.11g/mol。
环己烷物质的量n1=m1/M1=19.9523/84.16=0.2371mol
乙酸乙酯物质的量n2=m2/M2=0.2827/88.11=0.003208mol
溶液的摩尔分数浓度x2=n2/n1=0.003208/0.2371=0.013
2、计算环己烷及各溶液的密度ρ溶,作ρ溶—x2图,由直线斜率求算β值。
表2、实验数据处理表二
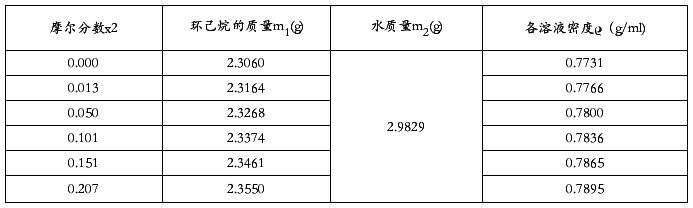
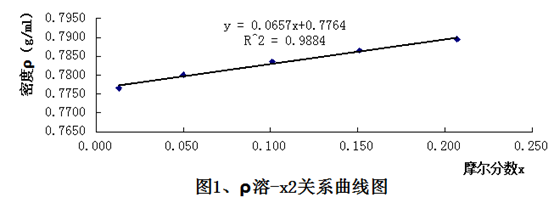
由表2实验数据作ρ溶—x2图如下:
 计算过程举例:(纯环己烷为例)
计算过程举例:(纯环己烷为例)
ρ环己烷=m环己烷/m水=2.3060/2.9829=0.7731(g/ml)
由图1的直线斜率为k=0.0657;根据公式ρ溶=ρ环己烷(1+βx2):
k=βρ环己烷 ∴β=k/ρ环己烷=0.0657/0.7731=0.08498
3、作n溶-x2图,由直线斜率求算γ值。
表3、实验数据处理表三
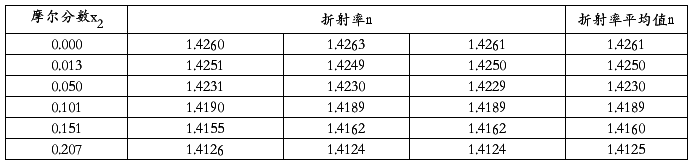
计算过程举例:(以x2=0.000为例)
折射率平均值n=(1.4260+1.4263+1.4261)/3=1.4261
由表3实验数据作n溶-x2图,如图3:
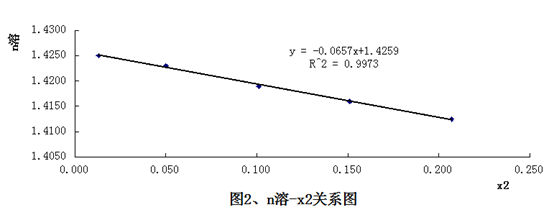
由图2得直线斜率为k=-0.0657;根据公式:n溶=n环己烷(1+γx2)得
k=γn环己烷 γ=k/n环己烷 =-0.0657/1.4261=-0.04607
4、计算C0、Cd和各溶液的C溶值,求出各溶液的介电常数,作ε溶-x2图,由直线斜率求算α值。
已知环己烷的介电常数温度公式为:ε环己烷=2.052-0.00155t
实验室温度为t=21.9℃,则:ε标=ε环己烷=2.052-0.00155×21.9=2.018
对于环己烷:C’空=5.66PF,C’标=8.19PF
Cd=(ε标C’空-C’标)/(ε标-1)=(2.018×5.66-8.19)/(2.018-1)=3.17PF
因为近似地认为空气与真空电容C0相等,即C空=C0,则:
C0=C空=C’空-Cd=5.66-3.17=2.49PF
各溶液的介电常数列表如下:
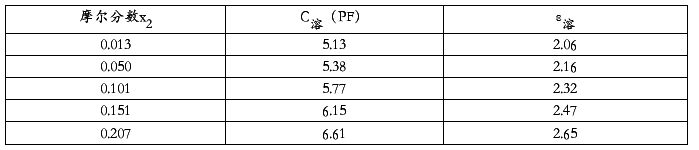
表4、 数据处理表四
计算过程举例:(以x2=0.013为例)
实验中测得的C’溶=8.30PF
∴C溶=C’溶-Cd=8.30-3.17=5.13PF
∴ε溶=C溶/C0=5.13/2.49=2.06
由表4实验数据作ε溶-x2图如下:

由上图可得直线斜率:k=3.07
根据公式:ε溶=ε环己烷(1+αx2)
∴k=αε环己烷 ∴α=k/ε环己烷=3.07/2.018=1.52
第二篇:实验二 介电常数与偶极矩的测定
实验二 介电常数与偶极矩的测定
一、实验目的
1、 用溶液法测定三氯甲烷的偶极矩
2、 了解介电常数法测定偶极矩的原理
3、 掌握测定液体介电常数的实验技术
二、实验原理
(一) 介电常数ε的测定
两带电极板间为真空时的电场强度为E0,当充以某种绝缘物质时,电场强度被削弱到E,ε=E0/E。介电常数是通过测定电容得到的,ε=C/C0,式中C0是以真空为介质时的电容,C是充以电介质时的电容。因为空气与真空的电容很接近,所以实验中通常将C0取为空气时的电容。
实验室测定介电常数常用的方法有电桥法、谐振法、频拍法。因为分布电容的存在,通常需要对测得的电容进行校正, 校正方法如下:
第一步,电 容 池盛空气,测定C`空气, C`空气=C空+Cd ⑴;
第二步,电容池盛标准物质 (如:苯),测定C`标,C`标=C标+Cd ⑵ ;
第三步,计算。ε标≈C标/C空 ⑶,
⑴⑵⑶三式联立求解,可得Cd=(ε标C`空气—C`标)/(ε标-1)。
ε苯=2.283-0.00190(t-20)
(二) 偶极矩的测定
对于稀薄气体、极稀溶液:
偶极距 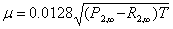 (单位为德拜) (4), 其中
(单位为德拜) (4), 其中
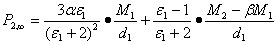 (5)
(5)
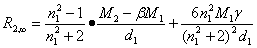 (6)
(6)
此外,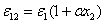 ,
, ,
,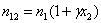 ,α、β、γ分别根据ε12~ x2 、d12~ x2和n12~ x2图求出。脚标1、2、12分别指溶剂、溶质、溶液。
,α、β、γ分别根据ε12~ x2 、d12~ x2和n12~ x2图求出。脚标1、2、12分别指溶剂、溶质、溶液。
三、仪器与试剂
阿贝折射计 1台; 比重瓶 1个; PCM-1A型精密电容测量仪 1台;电吹风 1个;超级恒温槽 1套;苯(A.R.);三氯甲烷(A.R.)
四、实验步骤
1、 溶液配制:用称量法配制四种浓度的三氯甲烷—苯溶液,分别盛于容量瓶中,其浓度(三氯甲烷摩尔分数)分别为0.010、0.050、0.100、0.150左右。操作时注意防止溶质、溶剂的挥发和吸收水气。溶液配制好后,迅速盖上瓶塞,并置于干燥器中。
2、 折射率测定:用阿贝折射计测定纯苯和配制的四种浓度溶液的折射率。
3、 液体密度测定:先将比重瓶洗净,烘干冷却至室温,在分析天平上(连瓶塞一起)称量为g1,然后用蒸馏水充满比重瓶,盖上磨口塞,恒温10分钟,擦干比重瓶,再称其质量为g2。倒出瓶中液体,将瓶吹干,放入待测液体(纯苯和配置的四种浓度溶液),再恒温10分钟,同法称其质量为g3。待测液体的密度按下式计算:d=dtH2O ×(g3-g1)/(g2-g1)
4、 介电常数的测定:
用小电容测量仪测定,测定步骤如下:1)打开电源开关,预热10分钟。2)每台仪器配有两根接有莲花插头的屏蔽线,将这两根线分别插到仪器上标有“电容池”和“电容池座”字样的莲花插座内,屏蔽线的另一端暂时不插入电容池和电容池座的插座。3)保持两根屏蔽线不要短路和接触其它导电体。4)按下校调按钮,使表头指示为零。5)将两根屏蔽线的另一端分别插在“电容池”和“电容池座”,这时表头指示的便是空气的电容值。电容池内加入待测样品,便可以从表头上读出有介质时的电容值。请用移液管加样品,每次加入的量必须严格相同,且每次测C/溶液后均需复测C空/,以检验样品室是否还残留样品。
。6)用吸管吸出电容池内液体样品,用电吹风吹干剩余的液体样品。
五、数据记录与处理
将测定结果列于下表:
温度:___________
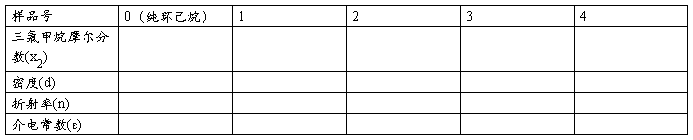
1. 作d12—x2图,由直线斜率求β值。
2. 作n12—x2图,由直线斜率求γ值。
3. 作ε12—x2图,由直线斜率求α值。
4. 将d1、ε1、α、β值代入(5)式计算P2,∞。
5. 将d1、n1、β、γ值代入(6)式计算R2,∞。
6. 将P2,∞、R2,∞值代入(4)式计算三氯甲烷的永久偶极矩μ。
六、思考题
准确测定溶质摩尔极化度和摩尔折射度时,为什么要外推至无限稀释?
