重要化学方程式小结
一、按要求书写化学方程式。
1.铁/铜在氯气中燃烧(方程式及现象)
2Fe+3Cl2 2FeCl3(产生棕黄色的烟,加水振荡,溶液呈黄色)
2FeCl3(产生棕黄色的烟,加水振荡,溶液呈黄色)
Cu+Cl2 CuCl2(产生棕色的烟,加水振荡,溶液呈蓝绿色)
CuCl2(产生棕色的烟,加水振荡,溶液呈蓝绿色)
2. 漂白粉在空气中变质 / 在工业上应用
Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO (在空气中变质)
Ca(ClO)2+2HCl==CaCl2+2HClO (工业上应用)
3.实验室制氢氟酸 / 氢氟酸腐蚀玻璃
NaF+H2SO4==Na2SO4+2HF↑ (反应须在铅皿或塑料制品中进行)
4HF+SiO2==SiF4↑+2H2O
4. 铜粉/铁粉与硫粉共热
2Cu+S Cu2S(黑色)(S的氧化性不强,只能将变价金属氧化成低价态)
Cu2S(黑色)(S的氧化性不强,只能将变价金属氧化成低价态)
Fe+S FeS(黑色)
FeS(黑色)
5.将硫粉/碳粉/铜粉与浓硫酸/硝酸共热
S+2H2SO4(浓)==3SO2↑+2H2O (浓H2SO4、浓HNO3与非金属反应
C+2H2SO4(浓)==CO2↑+2SO2↑+2H2O 只作氧化剂;与金属反应既作Cu+2H2SO4(浓)==CuSO4+SO2↑+2H2O 氧化剂又作酸。)
S+6HNO3(浓)==H2SO4+6NO2↑+2H2O
C+4HNO3(浓)==CO2↑+4NO2↑+2H2O
Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
6. H2S/HI通入浓硫酸中
H2S+H2SO4(浓)==SO2↑+S↓+2H2O
2H2S+H2SO4(浓)==3S↓+4H2O
2HI+H2SO4(浓)==SO2↑+I2+H2O
7.工业上用接触法制硫酸
4FeS2+11O2 2Fe2O3+8SO2 (沸腾炉)
2Fe2O3+8SO2 (沸腾炉)
2SO2+O2 2SO3 (接触室)
2SO3 (接触室)
SO3+H2O==H2SO4 (98.3%的浓硫酸 吸收塔)
8. 电解熔融的Al2O3
2Al2O3 4Al+3O2↑
4Al+3O2↑
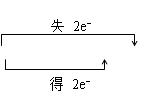
 9.Na2O2与CO2/H2O反应(标出电子转移)
9.Na2O2与CO2/H2O反应(标出电子转移)
2Na2O2+2CO2=2Na2CO3+O2 2Na2O2+2H2O+4NaOH+O2
10.侯氏制碱法制取纯碱
第一步:CO2+NH3+NaCl+H2O==NaHCO3↓+NH4Cl (NH3必须先通入到溶液中,然后再通入CO2。NaHCO3的溶解度较小,呈固体析出。)
第二步:2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
11.工业上生产HNO3/H3PO4
(1)HNO3: 4NH3+5O2 4NO+6H2O(氧化炉)
4NO+6H2O(氧化炉)
2NO+O2==2NO2
3NO2+H2O==2HNO3+NO(吸收塔)
(2)Ca3(PO4)2+H2SO4(浓)==CaSO4+H3PO4
12.工业上生产晶体硅/玻璃
(1)晶体硅: SiO2+2C==2CO+Si(粗硅,后两步用于提纯)
Si+2Cl2==SiCl4(气体) SiCl4+2H2==Si+4HCl
(2)玻璃:Na2CO3+SiO2 Na2SiO3+CO2↑
Na2SiO3+CO2↑
CaCO3+SiO2 CaSiO3+CO2↑(CaSiO3的热稳定性比CaCO3强)
CaSiO3+CO2↑(CaSiO3的热稳定性比CaCO3强)
13.Mg在空气/CO2气体中燃烧
(1)在CO2中燃烧:2Mg+CO2  2MgO+C
2MgO+C
(2)在空气中燃烧:2Mg+O2 2MgO 3Mg+N2
2MgO 3Mg+N2 Mg3N2
Mg3N2
2Mg+CO2  2MgO+C
2MgO+C
14.Al与Fe2O3/CO3O4/V2O5发生铝热反应
2Al+Fe2O3 Al2O3+2Fe
Al2O3+2Fe
8Al+3Co3O4 9Co+4Al2O3
9Co+4Al2O3
10Al+3V2O5 6V+5Al2O3
6V+5Al2O3
15.Fe粉在O2/水蒸汽中加热
3Fe2+O2 Fe3O4(剧烈反应,火星四射)
Fe3O4(剧烈反应,火星四射)
3Fe+4H2O(g) Fe3O4+4H2
Fe3O4+4H2
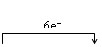 16.将Al粉/硅单质投入NaOH溶液中共热(标电子转移)
16.将Al粉/硅单质投入NaOH溶液中共热(标电子转移)
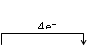 2Al+2NaOH+6H2O==2NaAlO2+3H2↑+4H2O
2Al+2NaOH+6H2O==2NaAlO2+3H2↑+4H2O
Si+2NaOH+2H2O==Na2SiO3+2H2↑+H2O
17.实验室制NH3/CH4
(1)2NH4Cl(固)+Ca(OH)2(固) CaCl2+2NH3↑+2H2O (此方程式
CaCl2+2NH3↑+2H2O (此方程式
不能写离子反应方程式。虽然是离子反应,但离子不能自由移动。)
(2)CH3COONa+NaOH CH4↑+Na2CO3(脱羧反应)
CH4↑+Na2CO3(脱羧反应)
18.实验室制HCl/SO2/C2H2/HBr
(1)NaCl(固)+H2SO4(浓)=NaHSO4+HCl↑ NaHSO4+NaCl HCl↑+Na2SO4
HCl↑+Na2SO4
2NaCl(固)+H2SO4(浓) Na2SO4+2HCl↑(总反应)
Na2SO4+2HCl↑(总反应)
(2)Na2SO3+H2SO4(中等浓度)==Na2SO4+SO2↑+H2O
(不能使用启普发生器原理制取)
(3)CaC2+2H2O Ca(OH)2+C2H2↑(不能使用启普发生器原理制取)
Ca(OH)2+C2H2↑(不能使用启普发生器原理制取)
(4)NaBr(固)+H3PO4(浓) NaH2PO4+HBr↑(不能用浓硫酸代替浓磷酸)
NaH2PO4+HBr↑(不能用浓硫酸代替浓磷酸)
19.实验室制C2H4及主要副反应
CH3CH2OH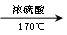 CH2=CH2↑+H2O
CH2=CH2↑+H2O
2CH3CH2OH CH3CH2-O-CH2CH3+H2O
CH3CH2-O-CH2CH3+H2O
CH3CH2OH+2H2SO4(浓) 2C+2SO2↑+5H2O
2C+2SO2↑+5H2O
C+2H2SO4 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
20.苯的取代反应(溴代/硝化)
 (1) + Br2
(1) + Br2 +HBr (不用加热)
+HBr (不用加热)
 (2) +HNO3
(2) +HNO3 +H2O (水浴加热)
+H2O (水浴加热)
21.卤代烃的主要反应(水解/消去)
 R-CH
2CH
2X + H
2O
R-CH
2CH
2X + H
2O
 R-CH
2CH
2OH + HBr (取代反应)
R-CH
2CH
2OH + HBr (取代反应)
 R-CH
2CH
2X
R-CH
2CH
2X
 RCH
2=CH
2 + HX (消去反应)
RCH
2=CH
2 + HX (消去反应)
22.乙醇的催化氧化
 2CH
3CH
2OH+O
2
2CH
3CH
2OH+O
2
 2CH
3COOH+2H
2O
2CH
3COOH+2H
2O
23.乙醇与活泼金属(Na/Mg等)反应
2CH3CH2OH+2Na==2CH3CH2ONa+H2↑(置换反应)
2CH3CH2OH+Mg==Mg(CH3CH2O)2+H2↑(置换反应)
24.苯酚的酸性(与Na/NaOH/Na2CO3等)
 2 +2Na
2 +2Na  2 +H2↑
2 +H2↑
 +NaOH
+NaOH +H2O
+H2O

+Na2CO3 +NaHCO3
+NaHCO3
25.酚醛缩聚反应

 n + n HCHO
n + n HCHO  [ CH2 ] n + nH2O
[ CH2 ] n + nH2O
26.乙醛的催化氧化
2CH3CHO+O2  2CH3COOH
2CH3COOH
27.乙醛的铜淀反应
CH3CHO+2Cu(OH)2 CH3COOH+Cu2O+2H2O
CH3COOH+Cu2O+2H2O
28.实验室制乙酸乙酯(反应条件)
CH3COOH+CH3CH2OH  CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
29.硫粉与NaOH溶液共热
3S+6NaOH==2Na2S+Na2SO3+3H2O
30.金属钠长期暴露在空气中的变化过程
(1)Na+O2==Na2O (2)Na2O+H2O==2NaOH
(3)2NaOH+CO2==Na2CO3+H2O (4)Na2CO3+CO2+H2O==2NaHCO3
(5)2NaHCO3==Na2CO3+CO2+H2O(风化) (6)Na2CO3+xH2O==Na2CO3·xH2O
31. 用硫粉除去洒落的Hg珠
S+2Hg==HgS 2Ag+S==Ag2S(两个反应均不须加热)
32.Mg2N3/Al2S3的水解
Mg2N3+6H2O==2Mg(OH)2↓+3NH3↑
Al2S3+6H2O==2Al(OH)3↓+3H2S↑
33. NO+O2/NO2+O2与水充分反应的总反应方程式
4NO+3O2+2H2O==4HNO3
4NO2+O2+2H2O==4HNO3
第二篇:高三化学化学方程式复习