山东大学实验报告 20##年3月30日
姓名 张行润 系年级 2009级生科4班 学号 200900140177 同组者 张少华
科目 细胞生物学实验 题目 小鼠脾细胞培养实验 仪器编号 105
一、 实验目的
了解原代细胞培养的基本方法及操作过程。学习细胞计数、营养液的配制等,初步掌握无菌操作方法。
二、 实验原理
(一) 细胞原代培养
原代细胞培养是指直接从动物体内获取的细胞、组织和器官,经体外培养后,直到第一次传代为止。这种培养,首先用无菌操作的方法,从动物体内取出所需的组织(或器官),经消化,分解成单个游离细胞,在人工培养下,使其不断的生长及繁殖。
细胞培养是一种操作繁琐而又要求十分严谨的实验技术。要使细胞能在体外长期生长,必须满足两个基本要求:一是供给细胞存活所必须的条件,如适量的水、无机盐、氨基酸、维生素、葡萄糖及其有关的生长因子、氧气、适宜的温度,注意外环境酸碱度与渗透压的调节。二是严格控制无菌条件。
(二) 细胞死活鉴定
死活细胞的鉴定方法有很多种,常用的有染色法和仪器分析法。染色法是常用的细胞死活鉴定方法,简便,易于操作。不同的死活细胞鉴定方法有各自不同具体的反应机理,但无论采用何种办法,都是利用了死活细胞在生理机能和性质上的差异。
染色法分化学染色法和荧光染色法,根据染色机理的不同,染料或使死细胞着色,或使活细胞着色。死活细胞在生理机能和性质上的差异主要包括:
死活细胞细胞膜通透性的差异:活细胞的细胞膜是一种选择性膜,对细胞起保护和屏障作用,只允许物质选择性的通过;而细胞死亡之后,细胞膜受损,通透性增加。常用的以台盼蓝鉴别细胞死活的方法就是利用了这一性质。台盼蓝,又称锥蓝,是一种阴离子型染料,不能透过完整的细胞膜。所以经台盼蓝染色后只能使死细胞着色,而活细胞不被着色。甲基蓝有类似的染色机理。植物细胞的质壁分离也可鉴定死活。
死活细胞在代谢上的差异:是采用美蓝染料鉴定酵母细胞死活的依据。美蓝是一种无毒染料,氧化型为蓝色,还原型为无色。由于活细胞中新陈代谢的作用,使细胞内具有较强的还原能力,能使美蓝从蓝色的氧化性变为无色的还原型,因此美蓝染色后活的酵母细胞无色;而死细胞或代谢缓慢的老细胞,则因它们的无还原能力或还原能力极弱,使美蓝处于氧化态,从而被染成蓝色或淡蓝色。
除此之外,还有一些细胞器的专有染料。如液泡系的专有染料中性红。中性红是一种低毒性染料,可以使活细胞液泡着红色,而细胞质和细胞核不被着色;死细胞的液泡不被着色或浅染,染料弥散于整个细胞中,细胞核和细胞质被染成红色。有时侯为了增加染色效果可以将两种染料结合使用,如甲基蓝-中性红混合染色法。
三、 实验器材
剪子,棉球,75%酒精,移液枪,无菌操作台,正置光学显微镜,倒置光学显微镜, 解剖盘,滴管,离心管,离心机,注射器,Eppendorf管,培养皿,酒精灯,塑料培养皿,载玻片,盖玻片,血细胞计数板等。
四、 实验材料
小鼠1只,细胞培养液(含生长因子),Trypen Blue染液,PBS缓冲液,
五、 实验步骤
(一) 细胞的原代培养
1. 取材:
取小鼠一只,采用断头法处死。清水洗小鼠浸入75%酒精中消毒3min,取出转入超净工作台内的解剖盘中,无菌操作打开腹腔,取出其脾脏,除去其周围的脂肪组织,并用PBS液自上而下淋洗1-2次,转入无菌培养皿中待用。
2. 分离脾细胞:
用滴管向培养皿中注入30滴PBS缓冲液,再用’L’型针头注射器在皿中吸取0.2毫升PBS液注入脾脏,注射时沿长轴注射。然后再用针头在脾脏上扎眼,并用’L’型针头轻轻刮出脾细胞。在均匀吹匀脾脏细胞。
吸取上述分离的单个脾细胞悬液,放入Eppendorf管中,使量至1mL,以1000r/min离心5min。
3. 培养脾细胞:
取塑料培养皿一套,用移液枪吸取培养液2mL加入塑料皿中,并将皿标记待用。取离心后的Eppendorf管,弃去上清液,用移液枪(200ul)吸取塑料皿中的培养液400ul加入弃去上清的Eppendorf管中,用枪头吹匀管底的脾细胞,吸取200ul脾细胞悬液接种于上述塑料皿中,混匀后放入37°C,5%CO2的培养箱中培养。
(二) 细胞死活鉴定及计数
1. 试剂配制:用生理盐水配成5%Tyrpen Blue染液,备用。
2. 染色计数:
 取0.5mL细胞悬浊液放入试管中,加入1-2滴染液。混合。2-5min后将细胞放在血细胞计数板上观察死活情况,注意不要有气泡产生,放大倍数为10x10。染色后活细胞不着色,死细胞显示蓝色。注意染色时间不能超过15min,否则染液将细胞毒杀。
取0.5mL细胞悬浊液放入试管中,加入1-2滴染液。混合。2-5min后将细胞放在血细胞计数板上观察死活情况,注意不要有气泡产生,放大倍数为10x10。染色后活细胞不着色,死细胞显示蓝色。注意染色时间不能超过15min,否则染液将细胞毒杀。
3. 计数:
在10x10倍的显微镜下观察,计算血细胞计数板的4个4小方格的细胞数量。包括细胞总数与死细胞数量。压线者计上不计下,计左不计右。
4. 计算细胞活力:
根据公式:
图1.血细胞计数板示例图
六、 注意事项
1、严格进行动物消毒,需用75%酒精消毒。
2、严格进行无菌操作,防止细菌、霉菌、支原体污染,避免化学物质污染。
3、吸取液体前,瓶口和吸管硬行火焰消毒;吸取液体时,避免碰撞。
4、离心管入台前,管口、管壁应消毒。
5、实验者离开超净台时,要随时用肘部关闭工作窗。
6、器材使用时既要注意用火焰消毒,又要防止烫伤、烫死细胞。
七、 实验结果
本次试验中计数所用材料为培养1-2周后的小鼠脾细胞,培养液呈粉红色,且未被染菌,说明原代细胞培养过程中小鼠脾细胞得到增殖,部分营养物质和其生存所必须的物质被消耗掉。
本次试验采取的是Tyrpen Blue染液,活细胞不会被染色而呈无色,死细胞会被其染色而呈蓝色,在光学显微镜下以10×10的倍数来观察得细胞总数和活细胞数,可由公式计算出细胞活力。
图2:细胞Trypen Blue染色后图片(10x10)
下面是我们小组的实验结果:
表1:总细胞数和活细胞数统计表(10×10)

计算得其细胞活力为20.7%
八、 分析总结
本次实验中我们小组所测细胞活力为20.7%,并不算高,分析得应有以下原因可能影响实验结果(包括误差):
a) 若在无菌操作的过程中操作不规范,导致染菌,会极大的影响观察,导致实验失败;
b) 若在离心分离呈单细胞的过程中离心机转速过快或时间过长很可能会导致细胞破裂,导致小鼠脾细胞大量死亡;
c) 染色时间过长,或观察时间过长都会导致染色试剂将细胞杀死,使细胞活力骤降,这是导致细胞活力比较低的重要原因;
d) 实验中的一些操作不正确或不规范的情况、计算带来的误差等也会直接导致实验误差。
第二篇:小鼠脾脏原代细胞
小鼠脾脏原代细胞培养与细胞死活鉴定和计数
一、实验目的
1.学习掌握细胞培养的基本原理及具体操作方法,并对小鼠脾细胞进行原代培养
2.掌握并熟悉无菌操作的要点,并养成无菌操作的习惯
3.学习用染色法鉴别细胞死活并进行细胞计数
4.学会利用血球计数板对细胞总数和活细胞进行计数
二、实验原理
①细胞培养:
多细胞生物的细胞可以被分离出来,然后在体外特殊培养环境中继续存活,并保持其生理、生化特性直接从生物体分离出来,在体外培养过程中尚未分裂、增殖的细胞,称为原代培养细胞。原代培养细胞在一定条件下可以继续增殖,在数量上大量扩增,这时就成为继代培养细胞。
细胞培养基要满足细胞的生长需要,培养细胞的条件有水的质量、无菌环境,最适温度、渗透压、气体条件、最适PH、营养条件和培养基质等。细胞培养皿是特殊制造的使细胞可以贴壁。
细胞培养箱常指二氧化碳培养箱。它可以提供合适的温度和二氧化碳浓度。二氧化碳和培养基中的缓冲系统共同作用,保持细胞培养液的酸碱度。超净台通过将空气进行过滤,为细胞培养的各种操作提供了一个干净的环境,使细胞培养免于细菌和真菌的污染。
②细胞生死状态的鉴别方法主要是化学染色法和荧光染色法:
活细胞和死亡细胞在生理技能和性质上主要存在一下差异:
I.细胞膜通透性的差异:活细胞的细胞膜是一种选择性膜,对细胞起保护和屏障作用,只允许物质选择性地通过;而细胞死后,细胞膜受损,其通透性增加。基于此,发展出了以台盼蓝、伊红、苯胺黑、赤藓红、甲基蓝以及荧光染料碘化丙啶或溴化乙啶等为染料鉴别细胞生死状态的方法,上述染料能使死亡细胞着色,而活细胞不被着色。
II.代谢上的差异:活细胞中新陈代谢作用强,细胞内的酶具有较强的活性和还原能力。基于此,发展处了以荧光素二乙酸酯(FDA)、荧光素二丙酸酯、荧光素二丁酸酯或荧光素二苯甲酰酯等酯化的荧光素鉴别细胞生死状态的方法,上述酯化的荧光素亲脂性提高,容易被细胞吸收进入,活细胞内的酯酶具有较强的活性,可将酯化的荧光素分解而释放出能发荧光的荧光素,该物质不能自由透过活的细胞膜,积累在细胞内,荧光显微镜下显示有明亮的绿色或黄绿色荧光;而死亡细胞内的酯酶因失去活性,不能分解酯化的荧光素,荧光显微镜下显示不发光。另外,可用亚甲基蓝为染料鉴定酵母细胞的生死状态。亚甲基蓝是一无毒染料,氧化型为蓝色,还原型为无色。活细胞因具有较强的还原能力,能使亚甲蓝从蓝色的氧化型变成无色的还原型,故活的酵母细胞在用亚甲基蓝染色后显示无色;死亡酵母细胞或代谢缓慢的衰老酵母细胞,因无还原能力或还原能力极弱,使亚甲蓝仍处于氧化态,故呈现蓝色或淡蓝色。
活细胞必需通过控制物质进出细胞膜来保持内部生理环境的稳定性。细胞死后细胞膜通透性发生改变,原先不能进入细胞的物质也能够进入细胞。台盼蓝染料正常情况下被活细胞阻拦在细胞膜外,只有细胞膜受损或者细胞死亡后,才能进入细胞。因此,活细胞一般不能被台盘蓝染色,而死细胞会被染成蓝色。
伊红和苏木精是最常用的细胞染色剂。本次实验就是用这两个染色剂进行的。
③血球计数板的使用:
血球计数板是一块特制的厚载玻片,载玻片上有4条槽而构成3个平台。中间的平台较宽,其中间又被一短横槽分隔成两半,每个半边上面各有一个方格网。每个方格网共分9大格,其中间的一大格(又称为计数室)常被用作微生物的计数。计数室的刻度有两种:一种是大方格分为16个中方格,而每个中方格又分成25个小方格;另一种是一个大方格分成25个中方格,而每个中方格又分成16个小方格。但是不管计数室是哪一种构造,它们都有一个共同特点,即每个大方格都由400个小方格组成。
 每个大方格边长为1mm,则每一大方格的面积为1mm2,每个小方格的面积为1/400mm2,盖上盖玻片后,盖玻片与计数室底部之间的高度为0.1mm,所以每个计数室(大方格)的体积为0.1mm3,每个小方格的体积为l/4000mm3。使用血球计数板直接计数时,先要测定每个小方格(或中方格)中微生物的数量,再换算成每毫升菌液(或每克样品)中微生物细胞的数量。
每个大方格边长为1mm,则每一大方格的面积为1mm2,每个小方格的面积为1/400mm2,盖上盖玻片后,盖玻片与计数室底部之间的高度为0.1mm,所以每个计数室(大方格)的体积为0.1mm3,每个小方格的体积为l/4000mm3。使用血球计数板直接计数时,先要测定每个小方格(或中方格)中微生物的数量,再换算成每毫升菌液(或每克样品)中微生物细胞的数量。
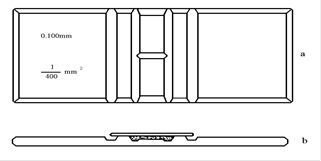
图1 血球计数板的构造(a、平面图;b、侧面图)
三、实验材料
1.材料
小鼠脾脏;PBS缓冲溶液、培养液、台盼蓝、伊红;
2.器材
解剖剪、解剖镊、眼科剪、眼科镊、培养皿、纱布块、吸管、橡皮头、烧杯、移液枪、注射器、针头、Eppendorf管(上述器具彻底清洗、消毒、烤干、包装好);
倒置相差显微镜、酒精灯、酒精棉球、试管架、解剖板等。
四、实验步骤
①原代细胞培养步骤:
1) 取材:取小白鼠一只,采用断头法处死,清水洗净小白鼠并浸于75%酒精中灭菌3min,取出转入超净工作台内的解剖盘内,无菌操作打开腹腔,取出脾脏,去除周围的脂肪组织,镊起脾脏用PBS液自上而下冲洗1-2次,转入无菌玻璃培养皿中,待用。
2) 分离脾细胞:用滴管先向上述无菌玻璃培养皿中滴入PBS液30滴,再用L形针头注射器在皿内吸取PBS液0.2ml,然后将其沿脾脏长轴方向注射入脾内,用针尖在脾脏上扎眼,并用L形针头轻刮脾脏表面挤出脾细胞,用滴管吸皿中的PBS液冲洗脾脏并吹散挂出的脾细胞,稍微倾斜并静置1-2min,吸取上述静置后的脾细胞悬液上清部分放入Eppendorf管,以3000转/分离心1-2min。
3) 培养脾细胞:从超净工作台中区塑料培养皿一个,用“枪(1ml)”加入细胞培养液2ml,并在皿上做记号,待用。取上述离心后的Eppendorf管,在超净工作台内打开弃去上清液,用“枪(200μl)”吸取塑料皿中的培养液400ul,加入弃去上清液的Eppendorf管中,用枪头吹匀管底的脾细胞,然后吸取200ul脾细胞悬液接种于上述塑料培养皿中,混匀,然后放入37℃二氧化碳培养箱中培养。
②细胞死活鉴别步骤
台盼蓝法染色:
1) 细胞悬液制备:将生长有贴壁型细胞的培养瓶(皿)中的培养液倒入干净试管中,向培养瓶(皿)中加入0.25%胰蛋白酶/0.02%EDTA混合消化液1-2ml,静置3-5min,待见到细胞变圆,彼此不连接为止,弃去混合消化液并将上述试管中的培养液倒回培养瓶中,用滴管轻轻吹打细胞,制成细胞悬液。
2) 染色制片:取0.5ml细胞悬液放于干净的试管中,加1-2滴(约0.1ml)染液,混合,2min后制成临时装片,镜检。
3) 染色结果:死细胞染成蓝色,活细胞不着色。
用血球计数板进行细胞计数:
1) 染色计数:取上述步骤二所制备0.5ml细胞悬液放于干净的试管中,加等体积滴染液,混合2-5min,滴加少许染色后的细胞悬液于放有盖片的血球计数板的斜面上,使悬液自然充满计数板小室(注意:不要使小室内有气泡产生,否则要重新滴加;在普通光镜10´物镜下计数四个大格内的细胞数,压线者数上不数下,数左不数右)。
2) 根据染色结果计算活细胞率:依据死细胞染成蓝色、活细胞不着色的原则计数死细胞数和细胞总数,以如下公式计算细胞存活率:

五、实验结果
原代细胞培养结果


倒置显微镜下10×40倍数观察的原代细胞



台盼蓝染色后死活细胞所呈状态10×40

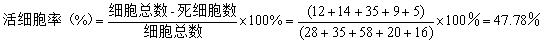
每毫升细胞总数=(28+35+58+20+16)×5×10000=7.85×106/ml
六、注意事项
1.培养液PH为7.0~7.4,其中加有酚酞,正常状况细胞生长过程代谢物使PH下降,培养液的颜色改变呈黄色,因此可通过培养液颜色变化初步判断细胞生长状况。
2.生长状况良好的细胞膜和核完整,细胞质透明,而细胞质出现较多颗粒状或空泡证明细胞衰老。除游离期和衰退期外细胞一般贴壁生长。游离期细胞一般圆形,折光率高,而衰退期细胞皱缩,透明度下降,立体感很差,较易区分。
3.为近一步保证无菌操作台的无菌环境,可在玻璃挡板口点一酒精灯,一般操作都在酒精灯火焰旁操作。
七、思考题
细胞的冻存、复苏、运输
在不加任何条件下直接冻存细胞时,细胞内和外环境中的水都会形成冰晶,能导致细胞内发生机械损伤、电解质升高、渗透压改变、脱水、PH改变、蛋白变性等,能引起细胞死亡。如向培养液加入保护剂,可使冰点降低。在缓慢的冻结条件下,能使细胞内水份在冻结前透出细胞。贮存在-130℃以下的低温中能减少冰晶的形成。
细胞复苏时速度要快,使之迅速通过细胞最易受损的-5~0℃,细胞仍能生长,活力受损不大。
目前常用的保护剂为二甲亚砜(DMSO)和甘油,它们对细胞无毒性,分子量小,溶解度大,易穿透细胞。
实验步骤
(一)冻存
1、消化细胞,将细胞悬液收集至离心管中。
2、1000rpm离心10分钟,弃上清液。
3、沉淀加含保护液的培养,计数,调整至5×106/ml左右。
4、将悬液分至冻存管中,每管1 ml。
5、将冻存管口封严。如用安瓿瓶则火焰封口,封口一定要严,否则复苏时易出现爆裂。
6、贴上标签,写明细胞种类,冻存日期。冻存管外拴一金属重物和一细绳。
7、按下列顺序降温:室温→4℃(20分钟〕→冰箱冷冻室(30分钟)→低温冰箱(-30℃ 1小时)→气态氮(30分钟)→液氮。
注意:操作时应小心,以免液氮冻伤。液氮定期检查,随时补充,绝对不能挥发干净,一般30立升的液氮能用1~1.5月。
(二)复苏
1、准备一个茶缸或1000ml的烧坏,内装2/3杯37℃的温水。
2、从液氮中取出冻存管、迅速置于温水中并不断搅动。使冻存管中的冻存物在1分钟之内融化。
3、打开冻存管,将细胞悬液吸到离心管中。
4、1000rpm离心10分钟,弃去上清液。
5、沉淀加10ml培养液,吹打均匀,再离心10分钟,弃上清液。
6、加适当培养基后将细胞转移至培养瓶中,37℃培养,第二天观察生长情况。
抑制肿瘤细胞增殖药物的筛选方法
若要抑制细胞增殖,就需要筛选一些作用于细胞分裂期的药物。比如抑制DNA合成或直接破坏DNA的药物,抑制微小管有丝分裂的药物。
1.抑制DNA合成药物的筛选 通过阻碍脱氧嘌呤核苷或脱氧嘧啶核苷的合成、互换、还原而干扰DNA的合成,大部分的抗代谢类药物如MTX、6桵P、6-TG、5-FU,HU、Ara-C等居于此类。
2.直接破坏DNA结构 此类药物大多为烷化剂和抗癌抗生素。如HN2、CTX、TSPA、CLB、BUS等烷化剂,通过烷化作用与DNA交叉联结,从而破坏DNA的结构和功能、BLM、MMC、ADM、DNR、ACD等抗癌抗生素和PDD、亚硝脲类药物亦有类似烷化剂的作用,可使DNA链断裂,直接破坏DNA。PCB可使DNA链解聚。
3.抑制有丝分裂 如VCR、VLB、VDS、NVB、VPl6、VM26等植物类抗癌药与细胞的微管蛋白结合,促进微管解聚使其不能形成纺锤体,抑制细胞分裂。紫杉醇为新型的有丝分裂抑制剂,促进微管装配抑制微管解聚,是目前唯一促进微管聚合新型的抗癌药。
诱导肿瘤细胞发生凋亡的药物筛选方法
肿瘤细胞可能失去细胞凋亡的功能,恢复这一功能可用于肿瘤治疗。现认为大多数临床使用的抗癌药物可引起特定癌症细胞的细胞调亡。另外,与正常细胞相比,肿瘤细胞对细胞凋亡的诱导更为敏感。现发现某些癌基因的激活及肿瘤抑制基因的丢失可抑制细胞凋亡,因此,如能抑制癌基因或修复肿瘤抑制基因功能或许可以解决某些癌症对现有化疗药物不敏感的问题。
用米托蒽醌、顺铂、羟基喜树碱、 高三尖杉酯碱诱导Jurkat细胞凋亡,并通过Annexin V /PI法检测细胞凋亡及细胞死亡比例,分析不同作用时间以及不同药物浓度对Jurkat细胞凋亡的影响。
诱导Jurkat细胞凋亡
Jurkat细胞在5% CO2孵箱培养至对数生长期,镜下计数为1×106/ml,加入24孔板,每孔1 ml细胞悬液。用无血清细胞悬液将顺铂、 羟基喜树碱、高三尖杉酯碱和米托蒽醌药物配制成1 mg/ml溶液;每组药物分别设4个浓度:12.5、25、50、100 μg/ml;分别加入24孔培养板,作3个复孔。置于5% CO2孵箱培养。
Annexin V/PI流式双参数分析[1-3]
分别于加入药物作用2、4和8小时,吸取培养细胞悬液,用4℃预冷的PBS洗细胞2次,用250 μl结合缓冲液重悬细胞,使其浓度为1×106/ml;取100 μl细胞悬液,加5 μlAnnexin V/FITC和10 μl 的碘化丙锭;混匀后室温避光孵育15分钟;用PBS洗涤2次,进行流式细胞仪(FACS)分析。Annexin V-FITC/PI双参数进行调试,以此条件进行细胞凋亡和细胞坏死率检测。图1-5横坐标表示荧光强度,纵坐标表示细胞数,图中两个峰中的左边峰表示阴性峰,右峰表示凋亡峰,右峰曲线下面积越大凋亡就越多。根据所测数据计算细胞凋亡率和继发性坏死率。
