
西南大学《细胞生物学自主实验》
课程论文
论文题目:人体外周血淋巴细胞培养与染色体核型分析
学院:生命科学学学院
专业:生物科学(师范)
班级:20##级3班
姓名:张 萌
学号:222012317011060
人体外周血淋巴细胞培养与染色体核型分析
【摘要】本文主要介绍通过对人体外周血淋巴细胞培养与染色体核型分析,初步了解到对人体外周淋巴细胞培养方法与人类体细胞染色体核型分析的方法。采用人工离体培养的方法,采集人体外周血淋巴细胞,在加有植物血球凝集素(PHA ,刺激小淋巴细胞转化为淋巴母细胞而进行有丝分裂)的培养基中培养,经过恒温培养,秋水仙素处理、低渗和固定,获得大量有丝分裂中期细胞,最后经空气干燥法制片,对人体外周淋巴细胞进行染色体核型分析。
【关键词】人体外周血淋巴细胞 染色体核型分析 细胞培养
1 综述
细胞培养是在体外模拟体内的生理环境培养从机体中取出的细胞并使之生存和生长的技术为细胞培养技术。要使细胞能在体外长期生长必须满足两个基本要求:一是供给细胞存活所必需的条件,如适量的水、无机盐、氨基酸、维生素、葡萄糖及其有关的生长因子、氧气、适宜的温度、注意外环境酸碱度和渗透压的调节;二是严格控制无菌条件。
染色体是组成细胞核的基本物质,是基因的载体。人类细胞遗传学研究的主要对象是染色体。本实验采用了微量全血培养技术,既方便又节省人力物力。在正常情况下,人外周血中是没有分裂相的,只有在异常情况下才能发现。 植物血细胞凝集素(PHA)是人类淋巴细胞有丝分裂的刺激剂,在PHA作用下,原处于G0期的淋巴细胞转化为淋巴母细胞,进而进行有丝分裂。利用PHA这一特性, 淋巴细胞经过含有PHA培养液培养,在体外便可获得丰富的含有丝分裂的生长活跃的细胞群体,终止分裂中期的淋巴细胞,经过短期培养,秋水仙素的处理,低渗和固定就可获得大量的中期有丝分裂细胞。最后经空气干燥法制片,便可得到质量较好的染色体标本,即可得到所需的人体染色体图形。
染色体组型又称核型,是指将动物、植物、真菌等的某一个体或某一分类群亚种、种、属等的体细胞内的整套染色体按它们相对恒定的特征排列起来的图像。核型模式图是指将一个染色体组的全部染色体逐个按其特征绘制下来,再按长短、形态等特征排列起来的图像。染色体组型分析就是通过对染色体标本和其照片进行测量、对比分析、配对、分组、排列对各染色体的形态进行分析。在细胞遗传学、现代分类学、生物进化和遗传育种学等研究中是重要的研究手段。对于任何一个染色体的基本形态特征来说重要的参数有以下3个:
(1)相对长度=单条染色体的长度/(单倍体常染色体+X或Y染色体)的总长度×100%
(2)臂指数=长臂/短臂 反映着丝粒位置的指数
(3)着丝粒指数=短臂/整个染色体长度×100%反映着丝粒位置的指数。
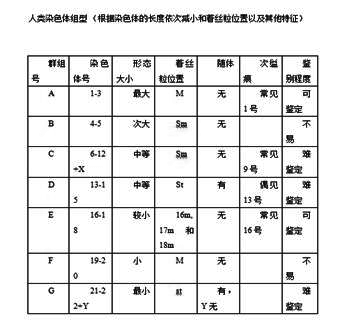
1.0-1.7(50.0%-37.5%):中部着丝粒染色体;
1.7-3.0(37.5%-25.0%):亚中部着丝粒染色体;
3.0-7.0(25.0%-12.5%):亚端部着丝粒;
>7.0(12.5%-0.0%):端部着丝粒染色体
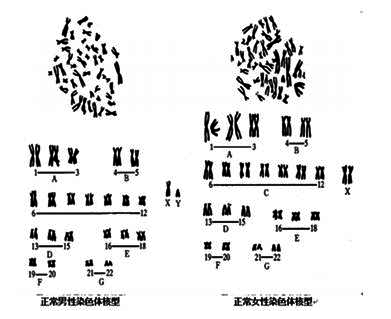
人类体细胞的正常核型是含有23对染色体,共46条。其中22对是男女共有的染色体,一对为男女所不同的性染色体,男XY,女XX。
2 实验仪器试剂及材料
2.1材料:人的静脉外周血。组内选取男女各一名取血样。
2.2试剂:RPMIl640培养基(完全培养基)、浓度为10mg/ml的PHA(植物血球凝集素)、0.1mg/ml秋水仙素溶液、Giemsa染液、低渗溶液(用KCl配制)、NaHCO3(配细胞培养完全培养基时用于调PH)、Carnoy固定液(9ml纯酒精+3ml冰乙酸)等。
2.3器材:恒温培养箱、恒温水浴箱、离心机、分析天平、显微镜、超净工作台、移液管、离心管、培养瓶、试管架及试管、镊子、量桶、烧杯、酒精灯、染缸、染色架、胶头滴管等。
3 实验方法与步骤
3.1 RPMI-1640基础培养基的配制
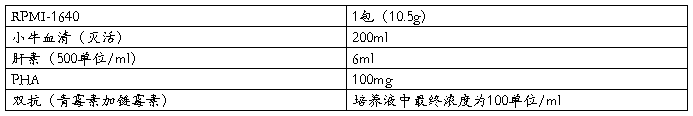
RPMI-1640粉末先用约800ml三蒸水溶解,再加入其他成分混匀,定容到1000ml,用5%NaHCO3调pH至7.2,然后用过滤方式灭菌,最后分装至离心管中。
3.2实验所用药品及器皿的无菌处理
(1)实验用的所有器皿,器具都必须按规定洗净,高压灭菌处理备用。器具清洗方法:
清洗→烘干→浸酸→流水冲洗(不少于8-10次)→蒸馏水冲洗(2—3次→烘干→包装→灭菌
(2)实验用全部药品都要经高压灭菌或过滤除菌处理,具有生物活性的药品要经G6型号细菌过滤漏斗抽滤除菌,其它药品可经过高压灭菌。
3.3采取血样
选一名女组员与一名男组员去校医院各采3ml肘静脉血,采集后加入肝素后立即拿回实验室进行实验(采血时加入肝素应适中,不宜太多,医院提供)。
3.4细胞培养
向培养瓶中加入0.3ml血液,再加入培养液5ml以及PHA 47微升。置于37℃培养箱中培养66到72小时,其间每隔24小时摇一次瓶。
3.5加入秋水仙素
在结束培养前4小时向培养瓶内加入10微升秋水仙素。
3.6收集细胞
将培养瓶从温箱取出,用吸管将贴壁细胞冲散均匀,轻轻吹打使细胞混匀,移到离心管中以1000rpm/min离心8min,弃上清液,每瓶培养细胞各一管。
3.7低渗处理
向四管中均先加入1mlmol/LKCl溶液,轻轻吹打,使细胞重悬,然后补加6mlKCl溶液,37℃低渗20min。
3.8预固定
沿管壁慢慢加入1ml新配carnoy氏固定液,轻轻吹打混匀,1000rpm/min离心8min,去上清液。
3.9固定
沿管壁慢慢加入6ml固定液,用吸管轻轻地吹打,使细胞分散,固定20min,离心去上清液。取上清液,再重复进行此过程。
3.10滴片
沉淀物中加入6ml固定液,用吸管吹打使其成为细胞悬液。用镊子取预先冰冻的干净载玻片,甩干上面剩余酒精,迅速滴上2-3滴细胞悬液(滴片高度至少在2m以上),然后置酒精灯上微微加热干燥或空气干燥(滴片张数尽量多,保证每人至少四张装片——不同培养条件下的装片各一张)。
3.11染色
滴有细胞悬液的载片扣在染色板上,使片、板之间有一缝隙,将稀释后的Giemsa染液滴在片隙中,染色20min(或放于染缸中),自来水冲洗,吹干。(应特别注意染色过程与染色方法,保证染色不出错)
3.12镜检
在低倍镜找到处于中期分裂相的细胞,然后在转至高倍镜下观察。观察时要使用推进器座标尺记录分散良好的细胞位置,便于重新查找,选择染色体分散好、长度适中、姐妹染色单体清楚的中期分裂相进行显微观察。
3.13染色体组型分析
① 在显微镜下找出染色体分散良好、长度适中、姐妹染色单体清楚的中期分裂相进行显微拍摄。
② 将显微拍摄放大的照片上的一个细胞的全部染色体分别一条一条剪下。
③ 根据染色体的长短和形态特征进行同源染色体的目测配对。
④ 测量出每条染色体短壁和长臂长度,计算出各条染色体的相对长度、着丝粒指数、臂指数,记录原始数据。
⑤ 根据测量数据校正目测配对排列结果进行调整排列。
⑥ 把染色体按一定顺序一对一对的排列,排列时注意短臂向上,长臂向下,性染色体单独排列,最后把染色体贴成一完整的染色体核型图。
⑦ 翻拍。
4 实验结果
4.1实验原图
在显微镜下找出的染色体分散良好、长度适中、姐妹染色单体清楚的中期分裂图:
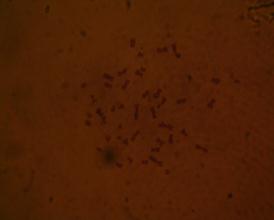
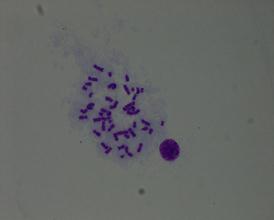
男性染色体图 女性染色体图(第二组原图)
4.2数据处理
根据各染色体形态特征进行同源目测配对后,计算出各条染色体的相对长度、着丝粒指数、臂指数等数据进行分析,结果如下:
表1 男性染色体数据分析表
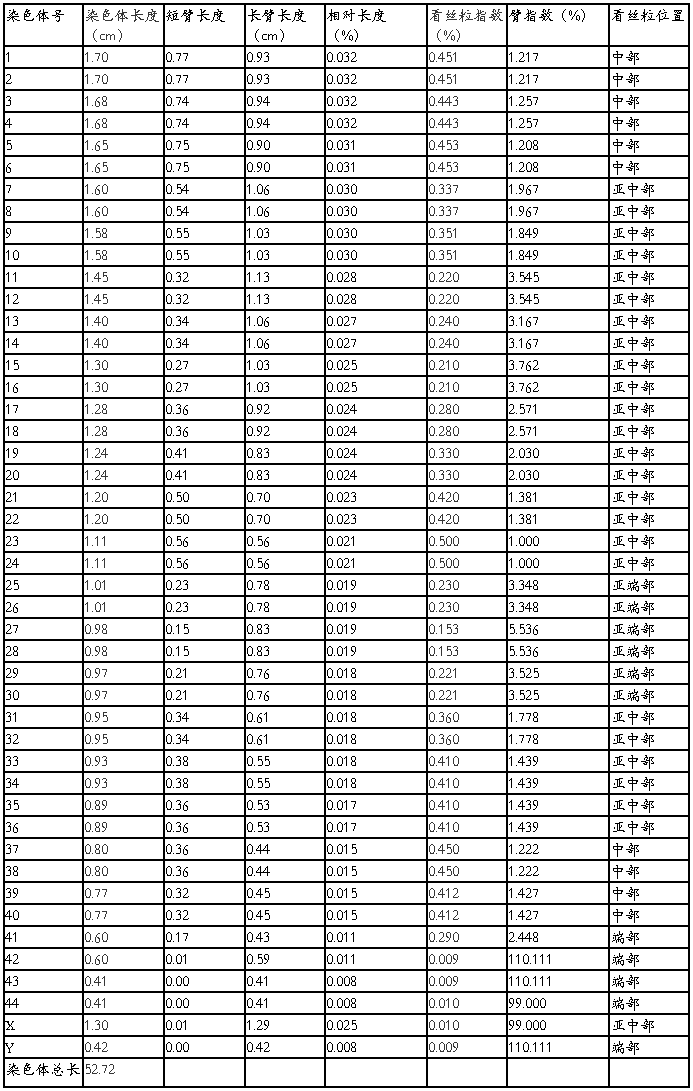
表2 女性染色体数据分析表
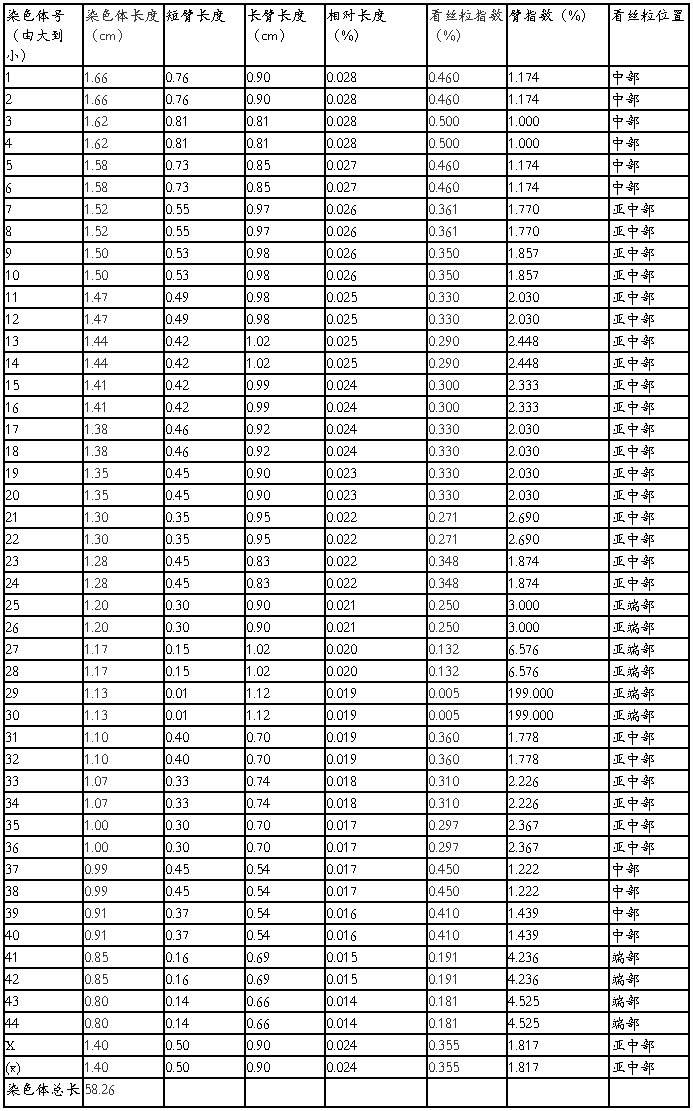
4.3染色体核型图
根据以上测量数据校正目测配对,并把各染色体贴成完整的染色体核型图,结果如下:

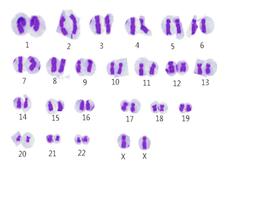
男性染色体核型图 女性染色体核型图
5 实验结论与分析
5.1实验结论
根据以上实验数据可知:人体正常细胞核型含46条染色体,相互配对成23对。其中22对为男女共有的常染色体,另一对XY染色体为男性特有,XX染色体为女性特有,两者是决定性别的性染色体。
5.2实验分析
本组实验得到了较好的实验结果,男性与女性染色体装片上均能够观察到有丝分裂中期染色体,男性染色体装片染色体分散效果较女性染色体装片好,根据实际经验,分析以下几个影响装片效果的重要因素。
(1)pH值:配制成的含20%小牛血清的RPMll640培养液的pH值应调节到7.2左右为宜,pH值低于6.8或高于7.4都不利于细胞的生长。
(2)温度:适宜的温度对细胞的生长和分裂非常重要。如果温度低于37℃,细胞的生长速度减慢;如果温度高于40C,细胞受损,超过43℃,则导致细胞死亡。本实验培养温度为37℃,细胞生长良好。
(3)培养中加入秋水仙素的作用机理是:干扰细胞中微管组装,抑制纺锤丝的形成,使细胞停留在有丝分裂的中期。加秋水仙素的时间是收集细胞制备染色体前2~3h,加入秋水仙素后,使秋水仙素的终浓度为0.04~0.08 ug/mI。培养液。秋水仙素的加入时间、剂量、浓度与有丝分裂中期分裂相的多少和染色体的长短有密切关系。加入量过多,染色体太短;加入量不够,染色体瘦长,都会影响对核型的分析。本实验在结束培养前4小时向培养瓶内加入10微升秋水仙素,加入时间、剂量都较为合适,实验效果理想。
(4)低渗处理是染色体制备中很重要的环节,其目的是使细胞吸收水分膨胀,细胞膜破裂。染色体散开。同时,低渗还可使红细胞膜破裂,经离心后,血影浮于上清液中被去除。观察本组制得装片可知,男性染色体形态清晰,分散度好,女性染色体形态模糊,分散度较差,原因可能是女性血细胞低渗不充分。
(5)滴片是本实验的一个重要环节,本组实验男性细胞悬液滴片较为成功,细胞数量适中,染色体分散度好。女性细胞悬液滴片稍差,细胞数量较少,染色体没有完全分散开。滴片时导致失败的原因很多,例如由于细胞悬液太稀,导致滴片时细胞稀少;载玻片上水太多,导致细胞悬液顺着水流失;载玻片不洁净,染色体分散不佳等。
第二篇:细胞实验报告
《细胞工程》综合实验
——水稻愈伤组织的诱导和分化

摘 要
本实验以水稻成熟种子为实验材料,通过NB诱导、分化培养基培养,诱导出愈伤组织并使其分化形成新的水稻幼苗。在植物组织培养过程中,外植体生长所必需的营养成分和生长因子,主要由培养基提供 不同材料对培养基的要求不尽相同,适当地设计和选用培养基,对组织培养取得成功是至关重要的。以植物器官、组织、细胞等作外植体进行离体培养都能形成愈伤组织。愈伤再经分化培养,通过器官发生途径或体细胞胚胎发生途径可再生成植株。外植体如果是带菌的,在接种前都必须消毒。对于难消毒的材料,有时要几种消毒剂配合使用;对于多茸毛表面粗糙不平的材料,要加展著剂(吐温20)以增强消毒效果。消毒效果的好坏,直接决定后期培养的成功率。如果染菌率太高,后期培养可能无法继续下去。本次实验就是通过组织培养的整个过程,来了解各个步骤的相关知识。
关键词:水稻 愈伤组织 诱导 再分化
目录
1 前言........................................................................................................................................... 4
2 材料与方法................................................................................................................................ 4
2.1 仪器.................................................................................................................................... 4
2.2 设备.................................................................................................................................... 4
2.3 试剂.................................................................................................................................... 5
2.4 实验材料............................................................................................................................ 5
3 实验方法................................................................................................................................ 5
3.1 配母液................................................................................................................................ 5
3.2 配NB诱导、分化培养基................................................................................................... 6
3.3 高温高压灭菌...................................................................................................................... 6
3.4 接种室、培养基及用具表面消毒....................................................................................... 6
3.5 消毒剂的配制..................................................................................................................... 7
3.6 种子去壳............................................................................................................................ 7
3.7 外植体消毒........................................................................................................................ 7
3.8 接种与观察(愈伤组织的诱导)....................................................................................... 7
3.9 愈伤组织的再分化观察...................................................................................................... 8
4 实验结果.................................................................................................................................... 8
4.1愈伤组织的诱导与分化....................................................................................................... 8
4.2 实验结果分析..................................................................................................................... 9
5 讨论分析.................................................................................................................................. 12
5.1愈伤组织的诱导问题分析................................................................................................. 12
5.2愈伤组织再分化问题分析................................................................................................. 12
5.3 操作分析.......................................................................................................................... 13
参 考 文 献................................................................................................................................. 15
1 前言
在我国,愈伤组织的培养和应用已经越来越多以及成熟,如:优良植株的无性繁殖、无病毒植株的获得、优良植株的选育等等。同时,随着消费者对产品安全性要求的日益提高,植物细胞培养的应用已愈来愈广泛,如:药用代谢产物的制造、作为天然食品或者食品添加剂、杀虫剂和杀菌剂、饲料等,不仅更安全,而且能很好地解决现今产品出现的各种问题。因此,愈伤组织的培养变得更加重要,而本实验则针对由水稻胚培养出愈伤组织的诱导形成幼苗的成功率进行了研究。
愈伤组织是指一个离体的细胞、一块组织或一个器官的细胞,通过脱分化不断分裂、增生子细胞,这些细胞胞分裂快,结构疏松,颜色浅而透明,逐渐形成了无序结构的一团细胞。
水稻成熟胚愈伤组织的诱导和再生是组织培养中的两个关键问题,它们涉及到外植体的脱分化过程和愈伤组织的再分化过程。影响水稻胚性愈伤组织形成和植株再生能力的因素包括基因型、外源激素、渗透压、外植体来源、固化剂、培养基其它成份以及温度、光周期和继代时间等多个方面,其中材料和外源激素的种类、浓度和配比是最主要的因素。
植物生长调节物质在分化过程中的作用是极为明显的,合适的植物生长物质配比在器官分化中起着重要的作用。
2 材料与方法
2.1 仪器
万分之一电子天平、百分之一电子天平、超净工作台、高压锅、酸度计、磁力搅拌器及搅拌子、不锈钢过滤器、玻璃蒸馏水器、家用冰箱、超净工作台、培养室
2.2 设备
烧杯:100ml×1, 500ml×1 ;量筒:100ml×3, 250ml×1 ;磨口试剂瓶:100ml×1, 500ml×1;带盖试剂瓶:500ml×2;三角瓶: 100 ml×1,250 ml×1,50ml×2(无菌),1000ml×1;培养皿:¢9cm×1;药匙;称量纸;牛皮纸;棉花塞;橡筋:若干、枪形镊:×4;无菌滤纸:(10cm×10cm)×5;
2.3 试剂
1N HCL;02N KOH;蔗糖(分析纯);琼脂粉;N6大量:KNO3、CaCl2·2H2O 、MgSO4·7H2O、KH2P O4 、(NH4)2SO4;B5微量:KI 、H3BO3、MnO4·H2O、ZnSO4·7H2O、 Na2MoO4·2H2O、CuSO4·5H2O、CoCL2·6H2O、Na2EDTA、FeSO4·7H2O;B5有机:盐酸硫胺素、盐酸吡哆醇、烟酸、肌醇、谷氨酰胺、水解酪蛋白、脯氨酸、2、4-D、6-BA、NAA;75%酒精,2% NaCLO,无菌水(400ml)
2.4 实验材料
水稻种子
3 实验方法
3.1 配母液
3.1.1 B5微量元素母液(1000×/100ml)
按配方的1000倍用万分之一天平依次称量,搅拌溶解(溶解一种后再加另一种)后定容。用量极少的成分(如CuSO4·5H2O、CoCL2·6H2O、Na2MoO4·2H2O)即使按1000倍称量仍很困难。
3.1.2 N6大量元素母液(10×)、B5有机成分母液(100×)
配法同3.1.1。
3.1.3 2,4-D母液(0.5mg/ml)
用万分之一天平称取2,4-D 50mg→用少量95%乙醇溶解→加水定溶为100ml。
3.1.4 6-BA母液(1mg/ml)
用万分之一天平称取6-BA 100mg→用少量1N盐酸溶解→加水定溶为100ml。
3.1.5 NAA母液(1mg/m l)
用万分之一天平称取NAA 100mg→用少量95%乙醇溶解→加水定溶为100ml。
3.1.6 铁盐母液(1000×/1000ml)
用百分之一天平称取FeSO4·7H2O 27.8g, Na2EDTA 37.3g→分别置于1000ml和500ml烧怀,各加水500ml→加热搅拌,充分溶解→趁热混合,冷却装瓶。
以上各母液配好后分别装入磨口试剂瓶,贴上标签,写明名称、浓度和配制日期,置于4℃冰箱保存。
3.2 配NB诱导、分化培养基
3.2.1 诱导培养基
N6大量+B5微量+B5有机+30g/L蔗糖+500mg/L谷氨酰胺+500mg/L脯氨酸+300mg/L水解酪蛋白+2mg/L 2,4-D+8.0g/L 琼脂粉pH5.8
3.2.2 分化培养基
N6大量+B5微量+B5有机+30g/L蔗糖+500mg/L谷氨酰胺+500mg/L脯氨酸+1.25mg/LCuSO4·5H2O+300mg/L水解酪蛋白+2mg/L 6-BA+1mg/L NAA +8.0g/L 琼脂粉pH5.8
3.3 高温高压灭菌
高压锅内加水→将待灭菌物品放入锅内,盖好,打开排气阀和安全阀→通电→水沸后排气10分钟→关上两阀,压力升至108KPa(1.1kg/cm2) 开始计时,维持此压力20分钟→断电→压力表降至0后,打开气阀放气,开盖,取出灭菌好的物品,放入培养室,倒平板。
3.4 接种室、培养基及用具表面消毒
用75%酒精棉球试擦超净工作、镊子,将培养基及用具放工作台,打开紫外灯,照射20分钟以表面消毒。之后关紫外灯,打开工作台风机,通风30分钟后可进行无菌操作。
3.5 消毒剂的配制
3.5.1 75%酒精
每组配95ml。量取95%酒精75ml,加蒸馏水至95ml即可。
3.5.2 2%NaClO
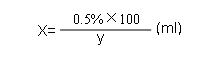
x:应吸取的NaCLO原液的毫升数;
y:NaCLO原液的有效氯浓度。
配100mL。
3.6 种子去壳
用自制的脱壳砂纸脱去谷壳,注意保持胚完整。每人准备30粒去壳种子。
3.7 外植体消毒
在超净工作台内将米粒放入50ml无菌三角瓶→无菌水洗一次→弃水,倒入75%酒精,搅拌,30秒→弃酒精,倒入2% NaClO,不时搅拌,30分钟→弃NaClO,用无菌水洗3次,每次停留1分钟→倒去无菌水,种子放在带无菌滤纸的培养皿中吸干。
3.8 接种与观察(愈伤组织的诱导)
在超净工作台内将吸干的种子接入培养基,注意使胚朝上。每瓶接10粒,每人2皿。写上日期、接种人、放入培养室25℃暗培养。1周后调查计算污染率,2周后调查计算愈伤组织诱导率。
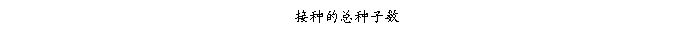


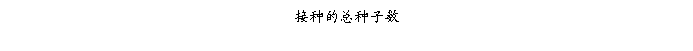


3.9 愈伤组织的再分化观察
在无菌条件下将诱导获得的愈伤组织(从约3周后安排此实验),从原材料中用镊子剥离后,接种到分化培养基中,每瓶接种3粒,每个同学接种2瓶,后置于光照条件下控制培养(25℃,2000lux每天光照10小时下培养),观察分化出苗的状况(一般需要2-3个星期的培养时间)。1个月后调查计算分化率。
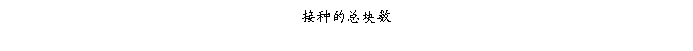

4 实验结果
4.1愈伤组织的诱导与分化
表一 愈伤组织诱导实验结果
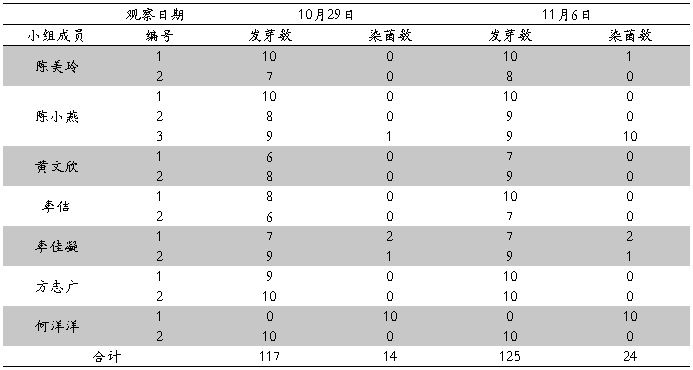
发芽率=125/150=83.3%
表二 愈伤组织的再分化结果

注:
1、表中对照为接种了对照愈伤组织的三角瓶。
2、实验要求为每人接种三个三角瓶,其一为对照。然而我组成员接种的对照组过多是由于愈伤组织的诱导培养结果不明显,因此全部或部分改为接种对照用愈伤组织。
4.2 实验结果分析
4.2.1愈伤组织诱导
染菌与愈伤组织

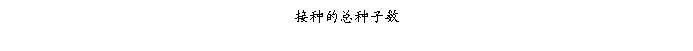

=14/150
=9.33%
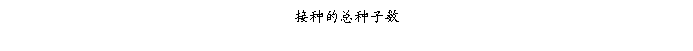

= 32/150×100%
= 9.95%
分析说明:
1. 污染率的计算中,仅把一周后观察的染菌种子列入计算,并未考虑染菌的扩散;由于实验操作不当导致的皿壁染菌也未计入。
2. 形成愈伤组织的种子数并不确切,这是由于小组成员们第一次诱导愈伤组织形成,尚不能明辨愈伤组织,以致我们本以为没有愈伤组织形成的种子,在清洗培养基的时候进一步分开种子的组织时发现其实是有愈伤组织形成的。因此,诱导率的计算并不能作为准确的实验结果。
3. 表中所列的是一周后的染菌情况。事实上,培养皿中只要有一个种子染菌,就极有可能整个培养皿的种子都被污染。例如皿壁染了霉菌的培养皿,在后期观察中,就看到了霉菌逐渐扩大生长,最终污染到许多种子。
4. 不发芽的种子,可能因接种的种子本身营养不良或者在清洗的时候收到损伤。
4.2.2愈伤组织的再分化观察
表三

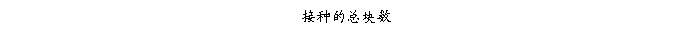

=10/54×l00%
=18.52%
若不把对照愈伤组织计入,如表四:
表四


=10/28×l00%
=35.71%
5 讨论分析
5.1愈伤组织的诱导问题分析
愈伤组织的诱导和再分化,受外植体本身、培养基和培养环境等三大类因素的调控。
来源于不同植物或同一种植物不同部位的愈伤组织,在颜色、结构和生长习性上都可能存在差异,生理功能上可能具有胚性,或是不具有胚性,在不同的实验中由于目的的不同,对愈伤组织状态的要求也不完全相同,本实验为了提高诱导率,选用水稻种子作为外植体。
一般的合成培养基都含有能满足离体组织生长所必需的元素,但各种类型的植物、器官所需要的每种元素的量,特别是大量元素是有区别的,对离子的形式也有不同要求。培养基的物理性质对器官分化对形态发生有明显的影响;培养基的pH值对芽的分化也有一定的影响 ,通常把pH调整到5.6~6.0范围。培养基中的渗透压过低不利于发育,过高则导致细胞易破裂。培养基中激素种类和浓度水平直接影响到外植体能否有效地产生愈伤组织以及愈伤组织能否再分化出完整植株。
本组组员在愈伤组织诱导阶段,出现了不同程度的染菌现象。最严重的达到整个平皿被杂菌覆盖,愈伤组织的生成受到严重影响,种子在脱分化过程中因杂菌影响而全部死亡。
原因:经过观察,污染最严重的平皿上的杂菌分布是由一个种子扩散出来,最终占据整个平皿。所以,染菌原因可能是种子消毒不彻底。具体可能是NaClO消毒时间不够,或者搅拌不到位,导致种子消毒不彻底,进而在后期培养中,杂菌繁殖覆盖平皿。另外,平皿的密封不彻底,后期密封遭破坏等,也有可能导致平皿染菌。
5.2愈伤组织再分化问题分析
光对器官的作用是一种诱导反应,各种植物的器官发生对光的要求是不同的。光照是离体培养中比较复杂的调节因子,光照时间、强度以及光质对器官分化均有影响。光照长度对有正常光周期反应的植物的器官发生有明显影响。本实验中要求对愈伤组织的诱导进行暗培养,对愈伤组织的再分化进行光照培养。
在组织培养中,一般都采用24~28℃的恒温条件进行外植体的培养。对一般植物来讲,可较好地形成芽和根。培养室的温度最好能保持有一定的日夜温差,这对器官的发生和生长都是有利的。
愈伤组织再分化阶段,培养瓶中出现了红酵母污染愈伤组织的情况,长出了红色的菌斑。导致愈伤组织无法出苗。原因:
1.由于本组诱导率不高,接种到分化培养基中时数量不足,所以需要借用提供的愈伤组织。由于多人共用一份,传递过程中的灭菌不彻底,密封不好,都有可能导致材料染菌,随着接种进入分化培养基。
2.操作失误。接种过程中,培养瓶瓶口敞开,很有可能会因操作失误而进入杂菌。手臂酒精消毒不彻底,手臂停留瓶口上方过于频繁等,都有可能导致瓶中进入杂菌。
本组诱导率不高,经分析,可能有以下原因。
1.培养基过薄,一些种子没有足够的营养诱导出愈伤组织。
2.激素加入量过少,导致一些种子没能成功诱导出愈伤组织。
3.种子本身问题。一些种子可能因为本身受到损害,无法成功诱导出愈伤组织
5.3 操作分析
1. 对照愈伤组织均来自同一培养皿,实验过程中发现,所有接种了对照愈伤组织的三角瓶都染红酵母菌,说明染菌原因来自对照愈伤组织。
2. 对照组的愈伤组织因为是与多人共用,所以有可能是因为前面使用的人染了红酵母。但是考虑到红酵母本身在空气中很少,所以很有可能是从操作台的通风系统中,或者是装着对照组的平皿内壁上。
3. 若不把对照愈伤组织计入,分化率达35.71%,这说明经过严格的无菌接种,在适宜的培养条件中,愈伤组织的分化率是很高的。但是我组接种了较多的对照愈伤组织,以致过半数的三角瓶内都有红酵母染菌现象。这说明,植物细胞工程实验环环相扣,若是一开始的实验材料有问题,那么接下来的操作都化作流水。因此,在今后的试验中,我们需得吸取经验,严格遵守操作规范。
4. 前文提及,我组因未能准确识别愈伤组织,以致多日诱导的愈伤组织在最后清洗时才发现,这也是令人惋惜的一点。若不然,分化率的计算会得到很多的可参考数据。
5. 实验结果表明,大部分的愈伤组织都出现了褐化现象。褐化原因可能你不单在于个人操作,愈伤组织的培养条件可能也出了问题。培养基和外界条件均会影响其是否褐化。因此褐化原因可能是:培养基中没有加入抗氧化剂或光照时间过长、光强过大。
6. 诱导期因植物种类和外植体的生理状况和外部因素而异。本实验的诱导时间在3~4周。
7. 培养的环境也是降低污染率的重要因素之一,培养的环境应在细菌含量少的地方培养,这样可以减低污染率。
8. 愈伤组织的诱导与再分化受到各方面的影响,在本实验中,愈伤组织的诱导率、污染率、再分化率都比较低。在再分化接种时,无菌操作不当,使得部分培养基和接种的愈伤组织被污染,而未能再分化形成幼苗,分化率偏低。
参 考 文 献
【1】刘香玲,王玉珍,罗景兰等,水稻成熟胚愈伤组织的诱导和分化因素的研究[J],山东农业科学,2005(5):5-7
【2】刘清波,刘选明,周朴华等,水稻幼穗胚轴愈伤组织培养力的比较观察[J],湖南农业大学学报,第23卷第6期,Vol.23 No.6,504~507
【3】郑贵朝,胡事君,杨跃生等,提高水稻愈伤组织植株再生能力几种方法的评价[J],杂交水稻,2005,20(2):54-57
【4】杨跃生,简玉瑜. 影响水稻愈伤组织再生植株数量和质量的因素[J].农业生物技术学报,1996,4(2):124 - 128.
【5】陈兴春,牛蓓等,水稻愈伤组织分化与不同激素配比关系的研究[J],四川大学学报(自然科学版),20##年2月,第43卷,第1期,222-227
