华 南 师 范 大 学 实 验 报 告
学 号 20130010011 专 业 课程名称实验项目 铅电极在硫酸溶液中的充放电行为
√综合 实验时间月日 实验类型 □验证 □设计 □
实验指导老师 吕 东 生 实验评分
一、实验目的
1.应用线性电位扫描和循环伏安法研究电极性能;
2.掌握恒电流法的基本原理和基本操作;
3.应用恒电流法研究电极的充放电行为。
二、实验原理
恒电流充放电法,又称计时电势法或电流阶跃法。一种研究材料电化学性能中非常重要的方法之一。在恒流条件下对被测电极进行充放电操作,记录其电位随时间的变化规律,研究电位随时间的函数变化的规律。
图1 恒电流法中所施加的电流信号 图2 恒电流法中的电位-时间响应曲线
金属Pb是铅酸蓄电池的负极材料,它在充放电过程中的电极反应是:
Pb+SO42--2e==PbSO4
三、实验器材
CHI电化学工作站;铂片电极;玻碳电极;Hg/Hg2SO4参比电极;氢氧化钠;Hg/HgO
参比电极;电解槽;醋酸铅
四、实验步骤
1. 在玻碳电极上电沉积


Pb
以铂片电极为对电极和Hg/HgO电极为参比电极,用配制好的电沉积Pb的溶液 (其中含7.5 g/L Pb(CH3COO)2 + 20 g/L NaOH)做电解质。预处理电极。打开
仪器和电脑,连接好相应的电极。记录开路电位,使用“阴极电位扫描法”沉积Pb。起始电位为开路电位,设-2V为终止电位,当电极析氢时停止扫描,扫速为5mV/s,温度为85℃;
2. 取出沉积有Pb的玻碳电极,用去离子水清洗后,以铂片电极为对电极和Hg/Hg2SO4电极为参比电极,在38% (质量比) 的硫酸溶液中测量Pb电极的循环
伏安法曲线;扫描范围为- 0.8V— -1.2V,扫速为2mV/s;
4. 以0.1mA的电流对Pb电极进行充电,充电时间为5min,分别以0.1mA、0.05mA和0.02mA的电流进行放电,截止电压为-0.3V。
5. 清洗电极和电解槽,放好,关闭仪器和电脑。
五、实验数据处理及分析
1. 作出在玻碳电极上沉积Pb的阴极极化曲线。指出Pb(AC)2的还原电位和析氢
电位。
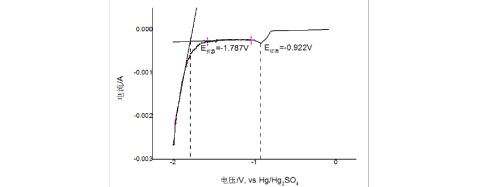
图3 沉积Pb时,玻碳电极以Hg/HgO电极为参比电极的阴极极化曲线
由图可知:Pb(AC)2的还原电位为-0.922V;
析氢电位为-1.787V.
2. 作出Pb电极在38% (质量比) 的硫酸溶液中的循环伏安曲线,指出Pb的电化学氧化和还原峰电位;
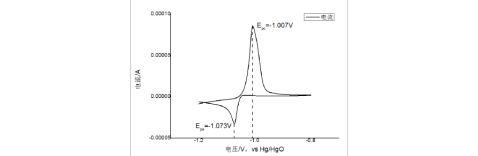
图4 Pb电极在38%硫酸溶液中相对于Hg/Hg2SO4电极的循环伏安曲线
由图可知:Pb的电化学氧化和还原峰电位分别为-1.007V和-1.073V。
3. 在同一张图中作出Pb电极的充放电曲线,纵坐标为电位/V,横坐标为容量/mA?h。比较不同电流放电下的放电容量和充电效率。
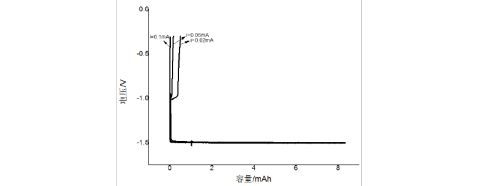
图5 Pb电极的充放电曲线
当放电电流为0.1mA时,放电容量为1.111×10-5mAh,充放电效率
为
1.111×10?5
8.333×10×100%=0.13%;
当放电电流为0.02mA时,放电容量为5.0556×10-4mAh,充放电效率为5.0556×10?4
8.333×10×100%=6.07%;
当放电电流为0.05mA时,放电容量为1.7083×10-4mAh,充放电效率为
1.7083×10?4
8.333×10×100%=2.05%。
第二篇:电化学基础实验报告 4.23
华 南 师 范 大 学 实 验 报 告
学 号 20130010011
专 业 课程名称实验项目循环伏安法测定电极反应参数
√综合 实验时间月日 实验类型 □验证 □设计 □
实验指导老师 吕 东 生 实验评分
一、实验目的
1.了解循环伏安法的基本原理及应用
2. 掌握循环伏安法的实验技术和有关参数的测定方法。 二、实验原理 循环伏安法(CV)是最重要的电化学分析研究方法之一。在电化学、无机化学、有机化学、生物化学的研究领域广泛应用。 CV方法是循环变化的电压施加于工作电极和参比电极之间,记录工作电极上得到的电流与施加电压的关系曲线。如图1.
当工作电极被施加的扫描电压激发时,其上将产生响应电流。以该电流(纵坐标)对电位(横坐标)作图,称为循环伏安图。如图2:0.1mol/LKNO3电解质溶液中,0.006mol/LK3Fe(CN)6在Pt电极上的反应所得到的结果。
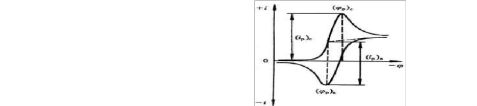
图1.循环伏安法加电压的方式 图2.循环伏安法测得的氧化还原曲线 其电极反应为:选择施加在a点的起始电位Ei为0.8V,然后沿负的电位即正向扫描,当电位负到能够将VO2+还原时,在工作电极上发生还原反应:VO2++2H++e= VO2++H2O,阴极电流迅速增加(b-d),电流在d点达到最高峰,此后由于电极附
+2+
近溶液中的VO2转变为VO而耗尽,电流迅速衰减(d-e);在f点电压沿正的方
2+
向扫描,当电位正到能够将VO氧化时,在工作电极表面聚集的将发生氧化反应:VO2++H2O = VO2++e+2H+阳极电流迅速增加(i-j),电流在j点达到最高峰,此后由于电极附近溶液中的VO2+转变为VO2+而耗尽,电流迅速衰减(j-k);当电压达到a点的起始电位Ei时便完成了一个循环。
循环伏安图的几个重要参数为:阳极峰电流(ipa)、阴极峰电流(ipc)、阳极峰电位(Epa)、阴极峰电位(Epc)。对可逆氧化还原反应E= (Epa+Epc)/2。对于可逆
反应,阴阳极峰电位的值,△E=Epa-Epc≈0.056/n (1)峰电位与扫描速度无关。而峰电流ip=2.69×105n3/2AD1/2V1/2C,ip为峰电流(A),n为电子转移数,A为电极面积(cm2),D为扩散系数(cm2/s),V为扫描速度(V/s),C为浓度(mol/L)。由此可见,ip与V1/2和C都是直线关系。对于可逆的电极反应: ipa/ ipc ≈

1 .
(2) 对一个简单的电极反应过程,式(1)、(2)是判断电极反应是否可逆体系依据。
三、实验器材
CHI电化学工作站;玻碳电极;铂电极;Hg/Hg2SO4电极;0.1 mol/L VO2+ + 0.1 mol/L VO2+ +3 mol/L H2SO4溶液
四、实验步骤
1. 预处理电极。其中玻碳电极用砂纸打磨,铂电极与Hg/Hg2SO4电极用去离子水
清洗。
3. 连接好电极,打开CHI电化学工作站,选择“循环伏安”方法。
4. 设置实验参数。初始电位为开路电位,阴极终止电位-1.5V,阳极终止电位+2V,扫描速率为10mV/s,循环次数2次。保存实验数据。
5. 换电解液,处理电极后,将扫速设置为5mV/s,阴极终止电位0.3V,阳极终止电位1.3V,循环次数为2次。保存实验数据。
6. 在扫描速度分别为50mV/s ,20mV/s ,15mV/s, 10mV/s下按照步骤5的实验条件测量循环伏安曲线。保存实验数据。
7.清洗电极和电解槽,关闭仪器和电脑。
五.实验数据处理与分析
1.作出玻碳电极在-1.5V~2.0V范围内测出的循环伏安曲线图 (选第2次扫描的曲线)。指出玻碳电极上的析氢电位、析氧电位以及另外一对氧化峰和还原峰的电位及其对应的电化学反应。
图3. 玻碳电极在-1.5V~2.0V范围内,扫速10mV/s时测出的循环伏安曲线图
析氢电位:由于扫描的电位范围比较小,还没出现析氢电位
析氢电位对应的电化学反应:2H++2e=H2 ;
析氧电位:1.555V
析氧电位对应的电化学反应:2H2O-4e=O2+4H+ ;
另一氧化峰电位:0.477V
其电化学反应为:VO2++H2O = VO2++e+2H+;
另一还原峰电位:-0.657V
其电化学反应为:VO2++2H++e= VO2++H2O.
2. 在同一张图中做出-0.3V~1.1V范围内不同扫速下的循环伏安曲线。列表总结不同扫速下的测量结果。根据ΔEp和ipa/ipc随扫描速度的变化趋势,说明扫速对
VO2+/ VO2+ 电对的可逆性的影响。
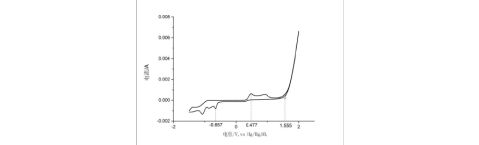
图4. 玻碳电极在-0.3V~1.1V范围内不同扫速下的循环伏安曲线
不同扫速下的测量结果数据表:
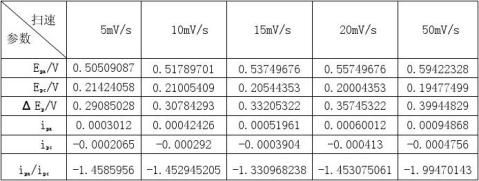
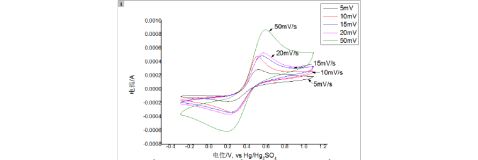

随着扫描速度的增加,ΔEp不断增大,ipa/ipc的比值也越来越偏离1,电池的可逆性随着扫描速度的增加越来越差。
3. 在同一张图中作出ipa和ipc对v1/2的曲线,并指出这两条曲线是否都是通过原点的直线。
图5. ipa和ipc对v的曲线
这两条直线都没有通过原点。
1/2
