关于黄酒成分分析及研究意义
摘 要
本文首先对黄酒的基本概述、酿造原料、酿造工艺、以及分类方法进行了介绍;并介绍了烹饪功用以及药用功能;然后简要介绍对黄酒总糖、Ph、总酸、氨基酸态氧、氧化钙、挥发酯这些成分分析的测定方法;再通过实验并处理数据得出相关成分的含量;最后讲述了黄酒成分分析的研究意义。
关键词:黄酒 成分分析 测定方法 研究意义
目录
1. 引言... 1
1.1基本概述... 1
1.2酿造原料... 2
1.3酿造工艺... 2
1.4分类方法... 3
1.4.1根据产品风格分类... 3
1.4.2根据含糖量分类... 3
1.4.3根据原材料的分类... 3
1.4.4其他习惯分类方法... 3
1.5烹饪功用... 3
1.6药用功能... 4
2. 实验概述与研究意义... 5
2.1测定方法... 5
2.2实验过程与数据处理... 5
3. 研究意义... 15
参考文献... 16
致谢... 16
附录... 16
1. 引言
1.1基本概述
黄酒是我国的民族特产,其前身是发酵米酒或者说是发醉谷物酒,在世界三大酿造酒(黄酒、葡萄酒和啤酒)中占有重要的一席。酿酒技术独树一帜,成为东方酿造界的典型代表和楷模。黄酒是世界上最古老的酒类之一,源于中国,且唯中国有之,与啤酒、葡萄酒并称世界三大古酒。约在三千多年前,商周时代,中国人独创酒曲复式发酵法,开始大量酿制黄酒。黄酒以大米、黍米为原料,一般酒精含量为14%—20%,属于低度酿造酒。黄酒含有丰富的营养,含有21种氨基酸,其中包括有特中未知氨基酸,而人体自身不能合成必须依靠食物摄取8种必需氨其酸黄酒都具备,故被誉为“液体蛋糕”。谷物酒产生的最基本条件有两个一是粮食盈余才有酿酒的可能,这是酿酒最重要的物质条件;二是从出土的陶器、瓷器、青铜器的功能角度去看,看其是否有熟化谷物、贮存、祭祀、饮用等功能,若具备则可以佐证当时具有酿造谷物酒的现实条件或技术条件.至于要做成好酒,除这两个基本条件以外,还要加上好水这一条件;当然要成为名酒,则还必须有相应的人文文化作为支撑。
1.2酿造原料
黄酒是用谷物作原料,用麦曲或小曲做糖化发酵剂制成的酿造酒。在历史上,黄酒的生产原料在北方以粟(学名:Setaria italica,在古代,是秫、梁、稷、黍的总称,有时也称为梁,现在也称为谷子,去除壳后的叫小米)。在南方,普遍用稻米(尤其是糯米为最佳原料)为原料酿造黄酒。在北方酿造黄酒主要用黄米即粟也叫小米 ,由于宋代开始,政治、文化、经济中心的南移,黄酒的生产局限于南方数省,南宋时期,烧酒开始生产,元朝开始在北方得到普及,北方的黄酒生产逐渐萎缩,南方人饮烧酒者不如北方普遍,在南方,黄酒生产得以保留,在清朝时期,南方绍兴一带的黄酒称雄国内外。目前黄酒生产主要集中于浙江、江苏、上海、福建、江西和广东、安徽等地,山东、陕西、大连等地也有少量生产。
1.3酿造工艺
我国的酿酒技术的发展可分为二个阶段,第一阶段是自然发酵阶段,经历数千年,传统发酵技术由孕育,发展乃至成熟。即使在当代天然发酵技术并未完全消失。其中的一些奥秘仍有待于人们去解开。人们主要是凭经验酿酒,生产规模一般不大,基本上是手工操作。酒的质量没有一套可信的检测指标作保证。第二阶段是从民国开始的,由于引入西方的科技知识,尤其是微生物学,生物化学和工程知识后,传统酿酒技术发生了巨大的变化,人们懂得了酿酒微观世界的奥秘,生产上劳动强度大大降低,机械化水平提高,酒的质量更有保障。
1.4分类方法
1.4.1根据产品风格分类
黄酒按产品风格可分为传统型黄酒、清爽型黄酒以及特型黄酒等三大类
1.4.2根据含糖量分类
黄酒按产品含糖量可分为干黄酒、半干黄酒、半甜黄酒和甜黄酒等四大类
1.4.3根据原材料的分类
这是黄酒最常用的分类方法之一,也是国家分类标准CB/T 17204一2008所采纳的方法。包括胭米黄酒、非稻米黄酒等
1.4.4其他习惯分类方法
1.5烹饪功用
作为常用的调味料之一的黄酒,在烹饪肉类食品时,用黄酒漫腌,可祛腥腻、提香味。较为著名有绍兴黄酒、福建沉缸酒、浙江加饭酒等。炒菜时加入一点黄酒,可增加菜的鲜味和香气,还能去除肉类膻腥。这是因为黄酒中的氨基酸能与盐反应生成氨基酸钠盐。造成鱼、虾腥味的主要原因是三甲基胺等,它能溶解在黄酒的乙醇中,加热烹调时,腥味与酒精一齐挥发,达到去除杂味的目的。 菇香黄酒鸡翅黄酒营养丰富,黄酒是中国酒中的瑰宝,它含有18种氨基酸,含量为6.624毫克/升,加饭酒含氨基酸更多,总量为7.3663毫克/升。并含人体所必需的7种氨基酸。其他营养成分有糖、有机酸、酯类、甘油和丰富的维生素。 黄酒的酯香、酮香同菜肴的香气十分和谐,用于烹饪不仅为菜肴增香,而且通过乙醇挥发,把食物固有的香气诱导挥发出来,能增进食欲。黄酒还能渗透到食物组织内部,溶解微量的有机物质,从而令菜肴质地松嫩。温饮黄酒,可帮助血液循环,促进新陈代谢,具有补血养颜、活血祛寒、通经活络的作用,能有效抵御寒冷刺激,预防感冒。中医常用黄酒来浸泡、炒煮、蒸炙各种药材,借以提高药效。一次5-15毫升即可。健康成年人可以直接饮用,以30毫升左右为宜,每日最多不超过200毫升。黄酒烫热喝更好,这样可以使黄酒中极微量的甲醇、醛。醚类等有机化合物挥发掉,同时所含的脂类芳香物蒸腾,芬芳浓郁。烹调时放黄酒的最佳时间应为炒锅温度最高的时候。 黄酒的药用价值也很大,它可用来浸泡、煎熬、冲中药,效果极好,因为中药有效成分在水中的微溶或不溶,在乙醇中却溶解度较大。白酒虽对中药溶解较好,但饮用时刺激太大,啤酒等则酒度太低,不利于药中成分的溶解。而黄酒酒度适中,是较为理想的药引子,黄酒气味苦,甘,辛,通经络,行血脉,温脾胃,养皮肤,散湿气,扶肝,除风下气,热饮更好。 值得注意的是,黄酒虽然有以上的好处,但它和其他的饮料酒一样,过量饮用也会影响人们的身体健康。
1.6药用功能
黄酒是医药上很重要的辅料或药引子;具体药用于以下方面。
用黄酒为辅料炮制药的方法很多,如酒洗、酒淬、酒蒸、酒炙、酒煮、酒垠等。黄酒炮制中药可改变这些药物的药性,提高功效及减轻不良反应,起矫臭、矫味等作用。
降低药物异味、防腐:一些具有腥味的药物如地龙、乌梢蛇、薪蛇等,经黄酒制后,其所含三甲胺和乙醇结合后,随乙醇挥发,可降低药物腥臭味,便于服用;黄酒制后有防腐作用,便于保存。
用于制药能“升腾行窜”、通脉,增强疗效,起协同作用。如川芍、白芍、当归、白花蛇等药物,一般多用黄酒制、酒炙,可增强活血化霭作用。黄酒也常代替水煎药,加强药效。如王清任《医林改错》中的通窍活血汤,用黄酒250克代水煎药,并强调“方中黄酒宁可多二两,不可少”。
酒是良好的有机溶媒:药物的有效成分如脂类、挥发油、昔类及部分生物碱,在黄酒中易于溶解。如生地性寒,为清热凉血之品,黄酒炙后则性温主补阴血,且可借酒力行散,起到行药势、通血脉作用,更有利于补血。黄酒炒白芍,使白芍所含主要成分白芍昔,在水煎剂中大量增加,提高了药物的疗效。黄酒还可缓和药性。如生大黄泻下作用峻烈,酒制大黄泻下作用稍缓,能减轻腹痛等。
黄酒能行药势:用于制药可缓和苦寒之性,能引药上行或下行。临床常用的一些苦寒药,其性降,常用于清中、下焦的湿热。如黄等、黄连、黄柏、大黄等.经黄酒制后,可缓和苦寒之性,借酒上行之力引药上行,酒炒后清上焦邪热。明·王肯堂撰《证治准绳》中的石解夜光丸,治疗阴虚血少、肝风上乘、剧烈头痛后引起的白内障。应用温黄酒送服,可引药势上行于头目。黄酒也能增强药物作用,清代《医宗金鉴》中的神授卫生汤,治外疡兼里热,如疡证在身体上部,应先饮黄酒一杯后再服药,以助药上行;疡证在身体下部,则先服药后,再饮黄酒一杯,以助药下行。
制造药酒:药酒是传统中药剂型中的主要剂型之一,系选用适宜的中药材,以发酵酒或蒸馏酒为溶媒,浸出中药里的有效成分而成。黄酒为重要溶媒之一。我国药酒历史悠久,夏禹时期已经能酿酒,同时发现了曲,开始有多种药物浸制而成的药酒。据统计有70多种药酒需用黄酒作酒基配制,如治风湿性关节痛,四肢麻木的五加皮酒;开胃健脾、顺气消食的神仙药丸酒;温补肾阳,健脾利湿的仙灵脾肉桂酒;主治反胃的松节酒等。
以酒糊丸:当以水为润湿剂致戮性太强而泛丸制困难时,常用黄酒代替;黄酒也有助于药粉中生物碱、昔类等溶出,也可使药物在加工过程中不霉变。以黄酒为薪合剂,制成丸剂。如舒筋活血之类的处方,常以酒为赋形剂泛丸,酒穿透性强,有活血通络、引药上行作用,同时酒中的乙醇能溶解药材中的树脂等成分而增加药物细粉的瀚性,是一种润湿剂。
2. 实验概述与研究意义
2.1测定方法
总糖的测定——铁氰化钾滴定法
pH的测定——pH计法
总酸的测定——中和滴定法
氨基酸态氮的测定——中和滴定法
氧化钙的测定——EDTA 滴定法
挥发酯的测定——中和滴定法
2.2实验过程与数据处理
黄酒成分分析一
总糖的测定——铁氰化钾滴定法
1范围
本方法适用于干黄酒和半干黄酒中总糖的测定。以 g/L 报告其结果,测定值保留三位有效数字。
2原理
费林溶液与还原糖共沸,在碱性溶液中将铜离子还原成亚铜离子,并与溶液中亚铁氰化钾络合而呈黄色。以次甲基蓝为指示液,达到终点时,稍微过量的还原糖将次甲基蓝还原成无色为终点,依据试样水解液的消耗体积,计算总糖含量。
3试剂
3.1 盐酸,ρ约 1.14 g/mL
3.2 盐酸溶液,6mol/L
3.3 氢氧化钠溶液,200g/L
3.4 费林甲液:称取 15.0 g 硫酸铜(CuSO4·5H2O)及 0.05g 次甲基蓝,加水溶解并定容至 1000mL,
摇匀备用。
3.5 费林乙液:称取 50g 酒石酸钾钠、54g 氢氧化钠及 4g 亚铁氰化钾,加水溶解并定容至
1000mL,摇匀备用。
3.6 葡葡糖标准溶液,1g/L
称取 1.0000g 经 103℃~105℃烘干至恒重的无水葡葡糖 (精确至 0.1mg),加水溶解,并
加 5ml 盐酸,再用水定容至 1000mL,摇匀备用。
3.7 甲基红指示液,1g/L
4操作步骤
4.1 空白试验
准确吸取费林甲、乙液各 5.00mL 于 100mL 锥形瓶中,加入 9 mL 葡萄糖标准溶液(1g/L),混匀后置于电炉上加热,在 2min 内沸腾,然后以 4~5s 一滴的速度继续滴入葡萄糖标准溶液,直至蓝色消失立即呈现黄色为终点,记录消耗葡萄糖标准溶液的总体积。
4.2 样品的测定
4.2.1 样品预处理:
吸取试样 2.00 mL~10.00mL(控制水解液总糖量为 1 g/L~2 g/L)于 100mL容量瓶中,加 30 mL 水和 5 mL 盐酸溶液(6mol/L),在 68℃~70℃水浴中加热水解 15min。冷却后,加入 2 滴甲基红指示液(1g/L),用氢氧化钠溶液(200g/L)中和至红色消失(近似于中性)。加水定容,摇匀,用滤纸过滤后备用。
4.2.2 预滴定:
准确吸取费林甲、乙液各 5.00mL 及 5.00 mL 样品水解液于 100mL 锥形瓶中, 摇匀后置于电炉上加热至沸腾, 用葡萄糖标准溶液滴定至终点,记录消耗葡萄糖标准溶液的体积。
4.2.3 滴定:
准确吸取费林甲、乙液各 5.00mL 及 5.00 mL 样品水解液于 100mL 锥形瓶中,加入比预滴定体积少 1.00mL 的葡萄糖标准溶液,摇匀后置于电炉上加热至沸腾,继续用葡萄糖标准溶液滴定至终点。记录消耗葡萄糖标准溶液的体积。接近终点时,滴入的葡萄糖标准溶液用量应控制在 0.50 mL~1.00 mL。
5结果计算
按下式计算总糖的含量,结果的表述以算术平均值报三位有效数字:
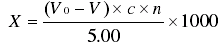
式中::X 一样品中总糖的含量,g/L;
V。一空白试验时,消耗葡萄糖标准溶液的体积,mL;
V 一样品测定时,消耗葡萄糖标准溶液的体积,mL;
c 一葡萄糖标准溶液的浓度,g/mL;
n 一样品的稀释倍数。
同一样品两次滴定结果之差不得超过 0.10 mL。
6数据处理结果
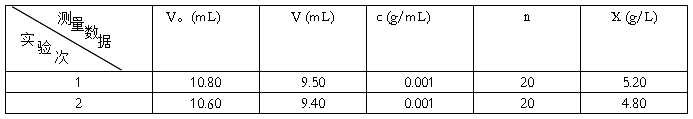
黄酒成分分析二
pH的测定——pH计法
1范围
本方法适用于黄酒pH的测定。结果表示为pH,测定值保留两位有效数字。
2原理
将玻璃电极和甘汞电极浸入试样溶液中,构成一个原电池。两极间的电动势与溶液的pH有关。通过测量原电池的电动势,即可得到试样溶液的pH。
3试剂
邻苯二甲酸氢钾标准缓冲溶液, PH=4.00
混合磷酸盐标准缓冲溶液, PH=6.86
4仪器
4.1 pH计,精度0.02pH
4.2复合电极
4.3电磁搅拌器
5操作步骤
5.1仪器校准
按仪器使用说明书校正pH计,并注意校正温度,使其与测定时保持一致。
将复合电极事先用pH 4.00标准缓冲溶液校准。校准时,先将复合电极插入PH6.86标准缓冲溶液,调节“温度” 旋钮至测定时温度,将“斜率”旋钮调至最大,调整“定位”旋钮至读数为6.86。清洗电极后将电极插入PH 4.00标准缓冲溶液中,“定位”旋钮不动,调节“斜率”旋钮至读数为4.00,再次清洗电极并用PH6.86标准缓冲溶液进行校正,反复操作直至读数稳定在4.00和6.86。
5.2样品的测定
移取适量酒样于样品杯中,并将样品杯置于电磁搅拌器上,插入复合电极,在搅拌下直接测定,直至pH计稳定1min为止,记录。同一样品两次平行测定值之差,不得超过0.05pH。
6数据处理结果
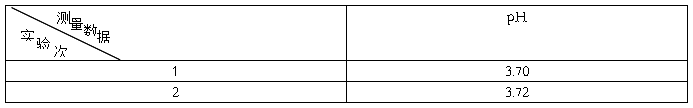
黄酒成分分析三
总酸的测定——中和滴定法
1 范围
本方法适用于各种类型黄酒中总酸量的测定,结果以乳酸计,表示为 g/L,保留两位有效数字。
2 原理
利用酸碱中和的原理,以氢氧化钠标准溶液直接滴定黄酒样品中的总酸,用 pH 计指示滴定终点,由所消耗的氢氧化钠标准溶液的体积计算黄酒中总酸的含量。
3 试剂
氢氧化钠标准溶液,c(NaOH)=0.1mol/L
4 仪器
4.1 pH 计
4.2 电磁搅拌器
4.3 分析天平,感量为 0.0001g
5 操作步骤
5.1 仪器校准
按仪器使用说明书校正 pH 计,并注意校正温度使其与测定时保持一致。
将复合电极事先用 pH 9.22 标准缓冲溶液校准。
5.2 样品的测定
吸取试样 10.0mL 于 150mL 烧杯中,加入无二氧化碳的水 50mL。烧杯中放入磁力搅拌棒,置于电磁搅拌器上,插入复合电极,在搅拌下用氢氧化钠标准溶液(c(NaOH)=0.1mol/L)滴定,开始时可快速滴加氢氧化钠标准溶液,当滴定至 pH 等于 7.0 时,放慢滴定速度,每次加半滴氢氧化钠标准溶液,直至 pH 等于 8.20 为终点,记录所消耗氢氧化钠标准溶液的体积(V1)。同时做空白试验,记录所消耗氢氧化钠标准溶液的体积(V2)
6 结果计算
按下式计算酒样中的总酸含量:
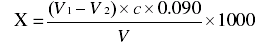
式中:X —酒样中总酸的含量(以乳酸计),g/L;
V1—测定酒样时,消耗氢氧化钠标准溶液的体积,mL;
V2—空白试验时,消耗氢氧化钠标准溶液的体积,mL;
c —氢氧化钠标准溶液浓度,mol/L;
0.090 —与 1.00mL 氢氧化钠标准溶液[c(NaOH)=0.1mol/L]相当的,以克表示的乳酸的质量;
V —吸取试样的体积,mL。
同一样品两次滴定结果之差,不得超过 0.05mL。
7数据处理结果

黄酒成分分析四
氨基酸态氮的测定——中和滴定法
1范围
本方法适用于各种类型黄酒中氨基酸态氮量的测定,结果表示为 g/L,保留两位有效数字。
2原理
氨基酸是两性化合物,分子中的氨基与甲醛反应后失去碱性,而使羧基呈酸性。用氢氧化钠标准溶液滴定羧基,用 pH 计指示滴定终点,通过所消耗的氢氧化钠标准溶液的体积计算黄酒中氨基酸态氮的含量。
3试剂
3.1 甲醛溶液,36%~38%
3.2 氢氧化钠标准溶液,c (NaOH)=0.1mol/L
4仪器
4.1 pH 计
4.2 电磁搅拌器
4.3 分析天平,感量为 0.0001g
5 操作步骤
5.1 仪器校准
按仪器使用说明书校正 pH 计,并注意校正温度使其与测定时保持一致。
将复合电极事先用 pH 9.22 标准缓冲溶液校准。
5.2 样品的测定
吸取试样 10.0mL 于 150mL 烧杯中,加入无二氧化碳的水 50mL。烧杯中放入磁力搅拌棒,置于电磁搅拌器上,插入复合电极,在搅拌下用氢氧化钠标准溶液(c(NaOH)=0.1mol/L)滴定,开始时可快速滴加氢氧化钠标准溶液,当滴定至 pH 等于 7.0 时,放慢滴定速度,每次加半滴氢氧化钠标准溶液,直至 pH 等于 8.20,加入甲醛溶液(36%~38%)10mL,继续用氢氧化钠标准溶液滴定至 pH 等于 9.20,记录加甲醛溶液后消耗氢氧化钠标准溶液的体积(V1),同时做空白试验,记录加甲醛溶液后所消耗氢氧化钠标准溶液的体积(V2)。
6 结果计算
按下式计算试样中的氨基酸态氮含量:
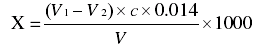
式中:X —试样中氨基酸态的含量,g/L;
V1—加甲醛后,测定试样时消耗氢氧化钠标准溶液的体积,mL;
V2—加甲醛后,空白试验时消耗氢氧化钠标准溶液的体积,mL;
c —氢氧化钠标准溶液浓度,mol/L;
0.014 —与 1.00mL 氢氧化钠标准溶液[c(NaOH)=0.1mol/L]相当的,以克表示的氮的质量;
V —吸取试样的体积,mL。
同一样品两次滴定结果之差,不得超过 0.10mL。
7数据处理结果

黄酒成分分析五
氧化钙的测定——EDTA 滴定法
1 范围
本方法适用于各类黄酒中氧化钙含量的测定,以 g/L 报告其结果,测定值保留两位有效数字。
2 原理
用氢氧化钾溶液调整黄酒试样的 pH 至 12 以上。以盐酸羟胺、三乙醇胺和硫化钠作掩蔽剂,排除锰、铁、铜等离子的干扰。在过量 EDTA 存在下,用钙标准溶液进行滴定。
3 试剂
3.1 盐酸溶液,1+4,
3.2 氢氧化钾溶液,280g/L
3.3 氢氧化钾溶液,56g/L
3.4 氯化镁溶液,100 g/L
3.5 盐酸羟胺溶液,10 g/L
3.6 三乙醇胺溶液,500g/L
3.7 硫化钠溶液,50 g/L
3.8 EDTA 溶液,0.02mol/L
3.9 钙标准溶液,0.01mol/L: 精确称取于 105℃烘至恒重的基准级碳酸钙 1.000g(精确至 0.1mg)于小烧杯中,加水50mL,用盐酸溶液(1+4)使之溶解,煮沸,冷却至室温。用氢氧化钾溶液(56g/L)中和至 pH6~pH8,用水定容至 1000 mL。
3.10 钙羧酸指示剂
4 仪器
电热干燥箱,105℃±2℃
5 操作步骤
准确吸取试样 2.00mL~5.00mL(视试样中钙含量的高低而定)于 250 mL 锥形瓶中,50mL 加水,依次加入 1mL 氯化镁溶液(100 g/L)、1mL 盐酸羟胺溶液(10 g/L)、0.5mL 三乙醇胺溶液(500g/L)、0.5mL 硫化钠溶液(50 g/L),混匀,加入 5mL 氢氧化钾溶液(280g/L),再准确加入 EDTA 溶液(0.02mol/L)5.00mL、钙羧酸指示剂一小勺(约 0.1g),摇匀,用钙标准溶液(0.01mol/L)滴定至蓝色消失并初现酒红色为终点。记录消耗钙标准溶液的体积V1。同时以蒸馏水代替样品做空白试验,记录消耗钙标准溶液的体积 V0。
6 结果计算
按下式计算氧化钙含量:
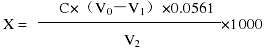
式中:X —样品中氧化钙的含量,g/L;
C —钙标准溶液浓度,mol/L;
V1 —样品测定时,消耗钙标准溶液的体积,mL;
V0 —空白试验时,消耗钙标准溶液的体积,mL;
V2 —吸取样品的体积,mL;
0.0561—1 mmoL 氧化钙的质量,g。
同一样品两次平行测定值之相对差,不得超过 5%。
7数据处理结果
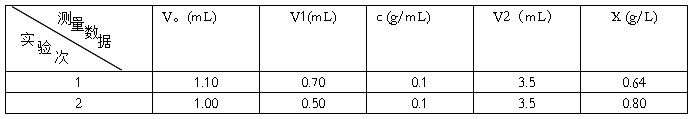
黄酒成分分析六
挥发酯的测定——中和滴定法
1范围
本方法适用于绍兴黄酒中挥发酯的测定,所得结果以 g/L 表示,保留二位小数。
2原理
黄酒通过蒸馏,酒中的挥发酯收集在馏出液中。先用碱中和馏出液中的挥发酸,再加入一定的碱使酯皂化,过量的碱再用酸反滴定,其反应式为:
R -C -OOR + NaOH → R -COONa + ROH
2NaOH + H2SO4 → Na2SO4 +2H2O
3试剂
3.1 硫酸标准溶液:0.1mol/L。
3.2 氢氧化钠标准滴定溶液,c(NaOH)=0.1mol/L。
3.3 酚酞指示液 10g/L。
3.4 溴甲酚绿-甲基红指示液
配制:
溶液Ⅰ:称取 0.1g 溴甲酚绿,溶于乙醇(95%),用乙醇(95%)稀释至 100mL。
溶液Ⅱ:称取 0.2g 甲基红,溶于乙醇(95%),用乙醇(95%)稀释至 100mL。
取 30mL 溶液Ⅰ、10mL 溶液Ⅱ,混匀。
4仪器
4.1 电炉,500W~800W。
4.2冷凝管,玻璃,直形。
4.3 250mL 全玻璃回流装置。
4.4 分析天平,感量为 0.0001g
5操作步骤
试样的制备:在约 20℃时,用容量瓶取试样 100mL,全部移入 500mL 蒸馏瓶中。用 100mL水分次洗涤容量瓶,洗液并入蒸馏瓶中,加数粒玻璃珠。装上冷凝管,通入冷水,用原 100mL容量瓶接收馏出液(外加冰浴)。加热蒸馏,直至收集馏出液体积约 95mL 时,停止蒸馏。于水浴中恒温至约 20℃,用水定容,摇匀。
吸取上述馏出液 50.0mL 于 250mL 锥形瓶中,加入酚酞指示剂(10g/L)2 滴,以 0.1 mol/L氢氧化钠标准溶液滴定至微红色,准确加入 0.1 mol/L 氢氧化钠标准溶液 25.0mL,摇匀,装上冷凝管,于沸水中回流 30 分钟,取下,冷却至室温。然后再准确加入 0.1 mol/L 硫酸标准溶液 25.0mL,摇匀,用 0.1 mol/L 氢氧化钠标准溶液滴定至微红色,30 秒内不消失为止,记录消耗氢氧化钠标准溶液的体积。
6结果计算
按下式计算试样中的挥发酯含量:
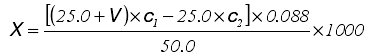
式中:X —试样中挥发酯的含量,g/L;
c1 —氢氧化钠标准溶液浓度,mol/L;
c2 —硫酸标准溶液浓度,mol/L;
V —滴定剩余硫酸所耗用的氢氧化钠标准溶液的体积,mL。
0.088—乙酸乙酯的摩尔质量,g/mol。
同一样品两次滴定结果之差,不得超过 0.01g/L。
7数据处理结果

3. 研究意义
研究黄酒的成分分析,让人们对黄酒有充分的认识,如何按种类进行购买,更好地在生活中应用它;更深一层次说,有利于提高黄酒的质量,能够更好地利用黄酒在一些领域的应用,充分发挥它的作用。
参考文献
张文学主编 《中国酒概述》 2011 第三章
孙溥泉主编 《药酒妙用205问》 20## 第5.6.7页
孙 九主编 《酒之道》 20## 第二章
谢广发主编 《黄酒》 20## 第三章
谢广发主编 《黄酒酿造技术》 20## 第一章
致谢
感谢我的孙磊老师,这片论文的每个实验细节和每个数据,都离不开你的细心指导。而你开开朗的个性和宽容的态度,帮助我能够很快的融入我们这个新的实验室。
感谢我的室友们,从遥远的家来到这个陌生的城市里,是你们和我共同维系着彼此之间兄弟般的感情,维系着寝室那份家的融洽。我们没有红过脸,没有吵过嘴,没有发生上大学前所担心的任何不开心的事情。只是我们在一起的日子,我会记一辈子的。
感谢我的爸爸妈妈,焉得谖草,言树之背,养育之恩,无以回报,你们永远健康快乐是我最大的心愿。
在论文即将完成之际,我的心情无法平静,从开始进入课题到论文的顺利完成,有多少可敬的师长、同学、朋友给了我无言的帮助,在这里请接受我诚挚的谢意。
附录
附录1 黄酒测定成分的国家标准(GB/T 13662-2000)*
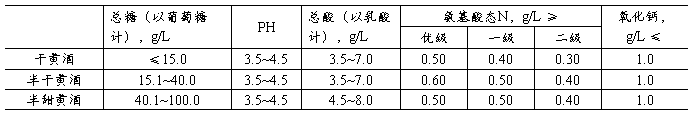
附录2 清爽型黄酒的轻工业标准(QB/T 2746-2005)*
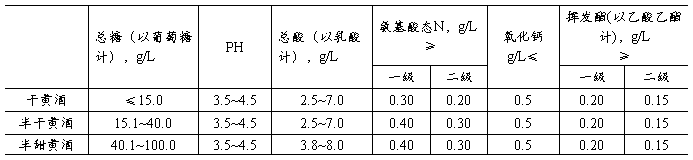
附录3 烹饪型黄酒的轻工业标准(QB/T 2745-2005)*
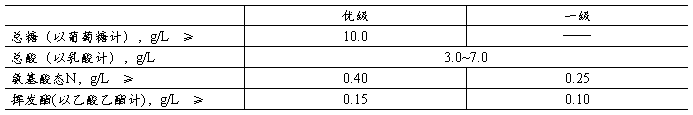
* 上述所有标准仅适用于稻米黄酒
附录4 黄酒测定样品说明

