最常见的要求书写离子方程式的化学方程式集锦
1、向氢氧化钠溶液中通入少量CO2:
2、在过量CO2通入NaOH溶液中:
3、烧碱溶液中通入过量二氧化硫:
4、在澄清石灰水中通入过量二氧化碳:
5、氨水中通入少量二氧化碳:
8、硫酸亚铁溶液中加入过氧化氢溶液:
10、氯化铁溶液中通入碘化氢气体:
11、硫酸铁的酸性溶液中通入足量硫化氢:
12、少量SO2气体通入NaClO溶液中:
13、氯气通入水中:
15、氯气通入冷的氢氧化钠溶液中:
16、FeBr2溶液中通入过量Cl2:
18、足量氯气通入碘化亚铁溶液中:
19、在FeI2溶液中滴入少量溴水:
21、钠与水反应:
22、过氧化钠和水反应:
铝片投入氢氧化钠溶液:
23、氯化铁溶液中加入铁粉:
24、FeCl3溶液与Cu反应:
26、铝片投入氢氧化钠溶液:
27、铜与浓硝酸:
28、铜与稀硝酸:
30、稀硝酸与过量的铁屑反应
31、FeS和稀硝酸反应:
32、电解饱和食盐水:
34、醋酸加入氨水:
35、氢氧化镁加入醋酸:
37、石灰乳与海水制取氢氧化镁:
38、少量氢氧化钙溶液与碳酸氢钙溶液混合:
39、向Ca(HCO3)2溶液中加入足量的氢氧化钠溶液:
40、少量氢氧化钙溶液与碳酸氢钠溶液混合:
44、NH4HCO3溶液与过量的NaOH溶液反应:
45、向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全
46、碳酸氢铵溶液中加入足量氢氧化钡溶液:
47、在亚硫酸氢铵稀溶液中加入足量的氢氧化钠稀溶液:
48、硫酸氢钠溶液中加入氢氧化钡溶液至溶液pH=7:
52、大理石与盐酸反应制CO2气体:
53、碳酸钙中滴入醋酸溶液:
54、乙酸溶液中加入少量碳酸氢铵溶液:w.w.w.k.s.5.u.c.o.m
55、硫化钠溶液中加入盐酸:
58、碳酸钠溶液中逐滴加入等物质的量的乙酸:
60、硫酸铜溶液中加入氢硫酸:
61、Na2CO3的水解:
62、硫氢化钠的水解:
63、实验室制备氢氧化铁胶体:
64、氯化铝溶液中加足量碳酸氢钠溶液:
65、NaNO2溶液中加入酸性KMnO4溶液:
相应离子方程式答案
1、CO2+ OH- CO32-+ H2O
2、CO2+ OH- HCO3-
3、 OH- +SO2 HSO3-
4、CO2+ OH- HCO3-
5、2NH3?H2O+CO2== 2NH4+ +2H2O
6、CO32-+ SO2 SO32-+ CO2↑
7、CO32-+ CO2 +H2O══HCO3-
8、2Fe 2++H2O2+ 2H+══2Fe 3++2 H2O
9、CO2+H2O+C6H5O-→C6H5OH+ HCO3-
10、2Fe3++2 H++2I- 2Fe 2++ I2+2 H+
11、2Fe3++ H2S== 2Fe 2++ S↓+2 H+
12、2ClO- +2SO2+ 2H2O══SO42-+ 2Cl-+2 H++SO42-
 13、Cl2+H2O H++Cl-+HClO
13、Cl2+H2O H++Cl-+HClO 
14、2F2+2H2O 4HF+O2↑
15、Cl2+ 2OH-══ ClO- + Cl-+ H2O
16、2Fe 2++4 Br-+ 3Cl2══2Fe3+++2 Br2+6Cl-
17、2Fe 2++2Br-+ 2Cl2══+Br2+4Cl-
18、3Cl2+2Fe 2++4I- 2Fe3++2I2
19、Br2+2I- 2Br-+ I2
20、2Fe 2++ Br2══2Fe3++2Br-
21、2Na+2H2O 2Na++2OH- +H2↑
22、2Na2O2+2H2O=4 Na++4OH- +O2↑
23、 2Fe3++Fe 3 Fe 2+
24、2Fe3++Cu Cu2++2Fe 2+
25、HS-+I2 S↓+2I-+ H+
26、2Al+2OH-+2H2O 2 AlO2- +3H2↑
2Na2O2+2H2O=4 Na++4OH- +O2↑
27、Cu+4H++2NO3- Cu2++ 2NO2↑+ 2H2O
28、3Cu+8H++2NO3- 3Cu2++ 2NO↑+ 4H2O
29、3Ag+4H++NO3- 3Ag++ NO↑+ 2H2O
30、3Fe+8H++2NO3—=3Fe3++2NO↑+4H2O
31、 FeS +4H++2NO3- Fe3++NO↑+S↓+2 H2Ow.w.w.k.s.5.u.c.o.m
32、2Cl-+2H2O C12↑+ H2↑+ 2OH-
C12↑+ H2↑+ 2OH-
33、2Cu2++2H2O 2Cu+O2↑+4H+
2Cu+O2↑+4H+
 34、CH3COOH+NH3·H2O CH3COO-+NH4++H2O
34、CH3COOH+NH3·H2O CH3COO-+NH4++H2O
35、 Mg(OH)2+2CH3COOH 2CH3COO-+Mg2++2H2O
36、Cu2++SO42-+ Ba2++2OH-══Cu(OH)2↓+ BaSO4↓
37、Mg2++2OH-══Mg(OH)2↓
38、Ca2++ HCO3-+OH-══CaCO3↓+H2O
39、Ca2++ 2HCO3-+2OH-══CaCO3↓+H2O+CO32-
40、Ca2++ 2HCO3-+2OH-══CaCO3↓+H2O+CO32-
41、Mg2++2HCO3-+2Ca2++4OH-══Mg(OH)2↓+2CaCO3↓+ 2H2O
42、Mg2++2HCO3-+Ba2++2OH-══Mg(OH)2↓+ BaCO3↓+2H2O
43、Mg2++2HCO3-+4OH-══Mg(OH)2↓+2H2O+CO32-
44、NH4++HCO3-+2OH-══CO32-+ 2H2O+NH3↑
45、NH4++H++SO42-+ Ba2++2OH-══BaSO4↓+ NH3·H2O+ H2O
46、NH4++HCO3-+ Ba2++2OH-══BaCO3↓+ NH3↑+ 2H2O
47、NH4++HSO3-+OH-══SO32-+ NH3·H2O+ H2O
48、2H++SO42-+ Ba2++2OH-══BaSO4↓ + 2H2O
49、Al3++3NH3·H2O === Al(OH)3↓+ 3NH4+
50、Al3++3NH3·H2O === Al(OH)3↓+ 3NH4+
51、3Ba2++6OH-+3Al3++3SO42-═3BaSO4↓+ 2Al(OH)3↓
52、CaCO3+ 2H+══Ca2++CO2↑+ H2O
53、CaCO3+ 2CH3COOH==2CH3COO-+Ca2++CO2↑+ H2O
54、CH3COOH十HCO3- CH3COO-+CO2↑+H2O
55、S2-+2H+ H2S↑
56、HCO3-+H+ CO2↑+H2O
57、CO32-+H+ HCO3-
58、CO32-+CH3COOH CH3COO-+HCO3-
59、[Al(OH)4]-+H+ Al(OH)3↓+H2O
60、Cu2++ H2S === CuS↓+ 2H+
61、CO32-+H2O HCO3-+OH-
HCO3-+OH-
62、HS-+ H2O H2S+ OH-
H2S+ OH-
63、Fe3++3H2O Fe(OH)3(胶体)+ 3H+
64、Al3++3HCO3- Al(OH)3↓+3 CO2↑
65、2MnO4-+5NO2-+ 6H+ 2Mn2+ + 5NO3- + 3H2O
第二篇:[化学]离子反应和离子方程式复习总结
离子反应和离子方程式复习总结
(一)离子反应
1、离子反应的概念
在反应中有离子参加或有离子生成的反应称为离子反应。在中学阶段仅限于在溶液中进行的反应,可以说离子反应是指在水溶液中有电解质参加的一类反应。因为电解质在水溶液里发生的反应,其实质是该电解质电离出的离子在水溶液中的反应。
2、离子反应的特点
离子反应的反应速率快,相应离子间的反应不受其它离子的干扰。
3、离子反应的类型
(1)离子互换反应 在溶液中酸、碱、盐之间互相交换离子的反应,一般为非氧化还原反应。
(2)离子互换反应发生的条件
①生成难溶的物质。如生成BaSO4、AgCl、CaCO3等。
②生成难电离的物质。如生成CH3COOH、H2O、NH3·H2O、HClO等。
③生成挥发性物质。如生成CO2、SO2、H2S等。
只要具备上述三个条件中的一个,离子互换反应即可发生。这是由于溶液中离子间相互作用生成难溶物质、难电离物质、易挥发物质时,都可使溶液中某几种、自由移动离子浓度减小的缘故。若不能使某几种自由移动离子浓度减小时,则该离子反应不能发生。如KNO3溶液与NaCl溶液混合后,因无难溶物质、难电离物质、易挥发物质生成,Na+、 Cl-、K+、NO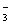 浓度都不减少,四种离子共存于溶液中,故不能发生离子反应。
浓度都不减少,四种离子共存于溶液中,故不能发生离子反应。
(3)有离子参加的氧化还原反应
①置换反应的离子反应 金属单质与金属阳离子之间的置换反应,如Fe与CuSO4溶液的反应,实际上是Fe与Cu2+之间的置换反应。非金属单质与非金属阴离子之间的置换反应,如Cl2与NaBr溶液的反应,实际上是Cl2与Br-之间的置换反应。
②其它一些有离子参加的氧化还原反应 如MnO2与浓HCl反应制取Cl2;Cu与FeCl3溶液反应生成FeCl2、CuCl2;Cl2与NaOH溶液反应生成NaCl、NaClO和水等。
这些离子反应发生的条件是:比较强的氧化剂和较强的还原剂反应,生成氧化性较弱的氧化产物和还原性较弱的还原产物。因此掌握一些常见离子的氧化性或还原性的相对强弱,是判断这一类离子反应能否发生的重要依据。
(二)离子方程式
1、离子方程式的概念
用实际参加反应的离子符号来表示离子反应的式子叫做离子方程式。
2、离子方程式的特点
离子方程式不仅表示一定物质间的某个反应,而且还表示所有同一类型的离子反应。如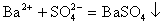 ,不仅表示BaCl2溶液与Na2SO4溶液之间的反应,还表示所有可溶性钡盐与可溶性硫酸盐溶液的反应。
,不仅表示BaCl2溶液与Na2SO4溶液之间的反应,还表示所有可溶性钡盐与可溶性硫酸盐溶液的反应。
3、书写离子方程式的四个步骤
(1)写——根据客观事实,写出正确的化学方程式。
(2)拆——把易溶于水且易电离的物质写成离子形式,把难溶于水的物质或难电离的物质以及气体、单质、氧化物仍用分子式表示。对于难溶于水但易溶于酸的物质,如CaCO3、FeS、Cu(OH)2、Mg(OH)2等仍写成分子式。
(3)消——对方程式的两边都有的相同离子,把其中不参加反应的离子,应“按数”消掉。
(4)查——检查写出的离子方程式是否符合前三项的要求,并检查是否符合质量守恒、是否符合电荷守恒。
4、书写离子方程式时应注意的几个问题
(1)注意哪些物质是难溶于水的物质,哪些物质是易溶于水的,哪些物质是微溶于水的。
在写离子方程式时难溶于水的物质必须用分子式表示,不能写成离子形式。
对于微溶物的处理,有以下三种情况:
①在生成物中有微溶物析出时,应用分子式表示。如Na2SO4浓溶液与CaCl2浓溶液反应时,其离子方程式为: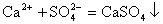
②当反应物中有微溶物并且处于澄清状态时,应将微溶物写成离子形式。如在澄清的石灰水中通入适量CO2,其离子方程式为:
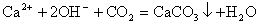
③当反应物中有微溶物,且处于悬浊液或固态时,应将微溶物写成分子式。如在石灰乳中加入Na2CO3浓溶液,其离子方程式为:
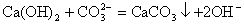
(2)注意哪些物质是强电解质,在溶液中是易电离的;哪些物质是弱电解质,在溶液中是难电离的。
常见的弱电解质有:HF、HClO、H2S、CH3COOH等弱酸;H2SO3、H2PO4等中强酸;NH3·H2O等弱碱;还有水也是弱电解质。
在写离子方程式时,难电离的物质应写成分子式。如醋酸与NaOH溶液反应的离子方程式为: 。
。
氢硫酸与硫酸铜溶液反应的离子方程式为: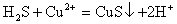 。
。
(3)注意反应是否在溶液中进行。
离子方程式只能用来表示电解质在溶液中进行的反应,不是在溶液中进行的反应,一般不用离子方程式表示。如氯化铵固体与熟石灰固体之间经加热生成氨气的反应,就不能用离子方程式表示,只能用化学方程式表示:
2NH4Cl+Ca(OH)2 CaCl2+2NH3
CaCl2+2NH3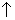 +2H2O
+2H2O
而NH4Cl溶液与NaOH溶液混合加热的反应,就可以用离子方程式表示:
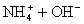

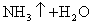
(4)注意浓酸中水的含量
浓H2SO4的浓度一般为98%,水的含量很少,其溶质基本上以硫酸分子的形式存在,所以有浓硫酸参加的一些反应,可以认为不是在溶液中进行的反应。如NaCl固体与浓硫酸、Cu与浓硫酸的反应,一般不用离子方程式表示,只能用化学方程式表示:
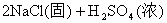




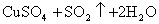
浓盐酸的浓度一般为36%,浓硝酸的浓度一般为69%,它们溶液中的溶质几乎完全以离子形式存在,所以在离子方程式中,浓HCl与浓HNO3都应写成离子形式。如:
MnO2与浓盐酸共热制取Cl2的离子方程式为:
MnO2 + 4H+ + 2Cl- Mn2+ + Cl2
Mn2+ + Cl2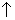 + 2H2O
+ 2H2O
Cu与浓硝酸反应的离子方程式为:
Cu + 4H+ + 2NO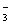 =Cu2+ + 2NO2
=Cu2+ + 2NO2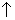 + 2H2O
+ 2H2O
Cu与稀硝酸反应的离子方程式为:
3Cu + 8H+ + 2NO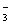 =3Cu2++2NO
=3Cu2++2NO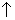 +4H2O
+4H2O
(5)注意电荷是否守恒
一个正确的离子方程式,不仅要遵循质量守恒,还要遵循电荷守恒。即反应前后各元素的原子个数要相等,方程式两边离子所带电荷也应相等。如Cl2与FeBr2反应的离子方程式,若写成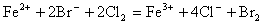 就错了。虽然反应前后各元素原子个数相等,但两边电荷数不等,因而是错误的。正确的写法是:
就错了。虽然反应前后各元素原子个数相等,但两边电荷数不等,因而是错误的。正确的写法是:
2Fe2+ +4Br-+3Cl2=2Fe3++6Cl-+2Br2。
(6)注意溶液中溶质电离出的阴离子和阳离子配比数是否正确
有些离子方程式中离子数不能任意约减,要注意电解质电离时阴、阳离子的配比。如:H2SO4与Ba(OH)2溶液反应的离子方程式,应当是
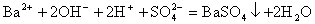
而不应写成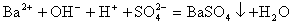 ,因为Ba(OH)2 电离时,电离出的
,因为Ba(OH)2 电离时,电离出的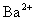 与
与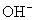 物质的量之比为1∶2而不是1∶1;H2SO4电离出的H+与SO
物质的量之比为1∶2而不是1∶1;H2SO4电离出的H+与SO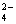 物质的量之比为2∶1而不是1∶1。
物质的量之比为2∶1而不是1∶1。
(7)注意有水参加的反应
在许多离子反应中,水是一种反应物,书写离子方程式时一定要注意这一隐含因素。如Ca(ClO)2溶液中通入CO2的离子方程式为:
Ca2++2ClO-+CO2+H2O = CaCO3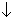 +2HClO
+2HClO
又如往溴水中通入SO2气的离子方程式为:
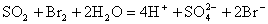
5、判断离子方程式正误的主要内容
(1)看反应能否写离子方程式。
(2)看“==”、“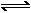 ”、“
”、“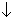 ”、“
”、“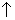 ”及必要的反应条件是否正确、齐全。
”及必要的反应条件是否正确、齐全。
(3)看表示各物质的化学式是否正确。如HCO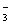 不能写成H++CO
不能写成H++CO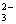 ,而HSO
,而HSO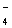 通常应写成H++SO
通常应写成H++SO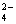 等。该用离子表示的是否拆成了离子,该用分子式表示的是否写成了分子式。
等。该用离子表示的是否拆成了离子,该用分子式表示的是否写成了分子式。
(4)看产物是否符合事实。如H2S与FeCl3反应生成FeCl2、S和HCl,而不生成FeS。
(5)看是否漏掉离子反应。如Ba(OH)2溶液与CuSO4溶液反应,既要写Ba2+与SO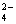 生成BaSO4的反应,又不能漏掉Cu2+与OH-生成Cu(OH)2的反应。
生成BaSO4的反应,又不能漏掉Cu2+与OH-生成Cu(OH)2的反应。
此外,还要检查是否符合质量守恒、电荷守恒;检查反应物或生成物的配比是否正确。
(三)关于溶液中离子共存问题
在溶液中离子共存问题的实质是哪些离子之间不能发生反应。能够发生反应的离子就不能共存,不能发生反应的离子才可以共存。
1、在溶液中某些离子间能互相反应生成难溶性物质时,这些离子就不能大量共存。如SO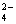 与Ba2+、Pb2+、Ag+;OH-与Cu2+、Fe3+、Mg3+、Al3+、Zn2+;Ag+与Cl-、Br-、I-、CO
与Ba2+、Pb2+、Ag+;OH-与Cu2+、Fe3+、Mg3+、Al3+、Zn2+;Ag+与Cl-、Br-、I-、CO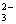 、SO
、SO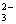 、S2-;Mg2+、Ca2+、Ba2+2+2+2+222+、与CO
、S2-;Mg2+、Ca2+、Ba2+2+2+2+222+、与CO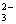 、SO
、SO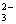 、PO
、PO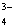 ;S2-与Cu2+、Pb2+等,不能大量共存。
;S2-与Cu2+、Pb2+等,不能大量共存。
2、离子间能结合生成难电离物质时,则这些离子不能大量共存。如H+与、OH-、ClO-、CH3COO-、HPO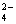 、H2PO
、H2PO ;OH-与HCO
;OH-与HCO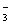 、HS-、HSO
、HS-、HSO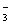 、H2PO
、H2PO 、HPO
、HPO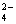 、H+等不能大量共存。
、H+等不能大量共存。
3、离子间能结合生成挥发性物质时,则这些离子不能大量共存。如H+与CO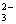 、SO
、SO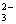 、HCO
、HCO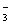 、HSO
、HSO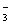 、S2-、HS-;OH-与NH
、S2-、HS-;OH-与NH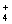 等不能大量共存。
等不能大量共存。
4、离子之间能发生氧化还原反应时,则这些离子不能大量共存。一般说来,有氧化性的离子(如MnO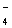 、ClO-、Fe3+、NO
、ClO-、Fe3+、NO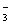 等)与有还原性的离子(如S2-、I-、Br-、SO
等)与有还原性的离子(如S2-、I-、Br-、SO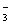 、Cl-、Fe2+等)不能大量共存。
、Cl-、Fe2+等)不能大量共存。
5、注意以下几种情况
(1)在有H+存在的情况下,MnO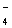 、ClO-、NO
、ClO-、NO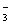 的氧化性会增强。如Fe2+、Na+、NO
的氧化性会增强。如Fe2+、Na+、NO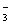 可以共存;但Fe2+、H+、NO
可以共存;但Fe2+、H+、NO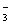 不能共存,Fe2+被氧化成Fe3+。
不能共存,Fe2+被氧化成Fe3+。
(2)Fe2+与Fe3+可以共存,因为它们之间不存在中间价态。
(3)Fe3+不能氧化Cl-。NO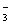 (有H+时)不能氧化Cl-.
(有H+时)不能氧化Cl-.
(4)还应注意题目是否给出溶液的酸碱性,是否给定溶液是无色的。在酸性溶液中除题给离子外,还应有大量H+;在碱性溶液中除题给离子外,还应有大量OH-。若给定溶液为无色时,则应排除Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(黄棕色)、MnO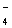 (紫色)。
(紫色)。
