《生活中两种常见的有机物——乙醇》教学反思
甘肃省岷县第二中学 陈新平
本节课的教学采取从古诗日常生活入手感受酒精,从结构到性质,从性质到用途,然后启发引导、实验探究、讨论总结。从而,使学生更加全面地认识乙醇。现在用新的教育理念去反思和对照比较这一堂课。简述几个片段如下
引入: 有关酒名句:“清明时节雨纷纷,路上行人欲断魂。借问酒家何处有?牧童遥指杏花村。”,“酒香不怕巷子深。”等诗句把学生带进中国传统酒文化,活跃课堂气氛,激发学生的学习兴趣。
多媒体展示:生活中各种酒有关的几个图片,把学生带进这堂课的研究对象。
准备好的准备好的无水乙醇,探究乙醇性质。
探究一:乙醇的物理性质
观察乙醇样品,结合已学过的知识和生活经验,总结乙醇的物理性质。
探究二:乙醇的分子结构
空间思维:请同学们根据乙醇分子式、并结合乙烷的分子结构,试推测乙醇可能的结构?
(提示:乙醇分子中C、O原子均达到8电子稳定结构)
乙醇的分子式:
乙醇的分子可能结构式:__________________________________________________
乙醇的结构式: 简写为:
探究三:乙醇的化学性质
1、乙醇与金属钠的反应
实验探究1:在盛有无水乙醇的小试管中,加入一小块新切的、用滤纸擦干表面煤油的金属钠,
迅速塞上配有医用注射针头的单孔塞。
①用小试管收集并验纯气体
②把一干燥的小烧杯罩在火焰上,片刻后,迅速倒转烧杯,向烧杯中加入少量澄清石灰水
1、完成表格内容:

2、实验猜想
①
②
③
…
思考与交流
(1)你能根据钠与水的反应原理写出钠与乙醇的化学方程式吗?
_______________________________________________________________
实验探究2: 向一支小试管中加入2mL乙醇,取一根铜丝,下端绕成螺旋状,在酒精灯上灼烧制红热,插入乙醇中,反复几次。注意观察反应现象,小心闻试管中液体产生的气味。
讨论:1、实验现象:______________________________________________
2、铜丝在此实验中起什么作用?____________________________________
2、乙醇的氧化反应
①乙醇的催化氧化:_______________________________________________
②乙醇的燃烧:___________________________________________________
以上教学过程形式活泼,从内容上有利于培养学生探索创新的精神,在乙醇的分子结构,如何定性确定乙醇的分子结构,乙醇和钠反应的实验现象的总结,乙醇与钠和水与钠反应现象不同的原因分析,乙醇催化氧化的实验等都可以给学生很大的研究和探索空间。学生积极性特别高,踊跃发言,积极做实验。无论是情景设置、实验探究还是课外活动,本课时的教学安排以学生为主体,紧紧围绕提高学生的科学探究能力,充分体现了新课标的理念。尤其是在对乙醇分子结构的分析上,运用探究实验,正反对比思想,由学生归纳总结实验现象,并得出初步结论,在性质探究方面学生亲自实践感受深刻,这样有利于激发学生的学习积极性。但对照新的课程标准,我觉得还存在很多遗憾。
一、引入的内容略显重复,实验探究过程中,醇的催化氧化探究时间分配的比例略显少了些,幻灯片中间个别地方没有实现同步,出现了个别口头语。
二、教师应把自己的角色定位在引导者上,尊重学生的差异和多样性,把培养学生积极进取,各具特色的个性作为一项重要的教育任务。这节课乙醇的可能结构教学上,应充分调动学生想象空间;乙醇作为燃料的意义;“酒精检测仪”的原理;过度饮酒的危害;乙醇与钠,氧气反应的本质等,学生都可以作出其个性回答,在学生个性思考以后,教师适时地予以引导。如果下次再有机会我会充分调动学生联系实际找出生活中的乙醇,让学生自己展示。
三、新课程强调,教学是教与学的交往、互动,师生双方相互交流、相互沟通、相互启发、相互补充,在这个过程中教师与学生分享彼此的思考、经验和知识,交流彼此的情感、体验与观念,从而达到共识、共同发展。但本节课我总觉得自己第一个讲还是有些紧张略显拘束,课堂气氛没有足够活跃,同组,组与组之间讨论不够到位。
四、在传统的应试教育模式下,由于急功近利式的应对考试,往往忽视人文教育,新课标对培养什么样的人作了较高的要求,对教育的要求不仅仅是知识的传授,而是培养全面发展的人。
本节课上在对酗酒的危害,乙醇作为燃料的意义等的人文教育是不够的。仅仅是作为科普介绍,一带而过。
第二篇:第三节 生活中两种常见的有机物(乙醇、乙酸)
人教版必修2第四章《有机化合物》
第三节 生活中两种常见的有机物(乙醇、乙酸)
练习一:乙醇
一、选择题(可能有1-2答案)
1.

下列表示乙醇分子结构的模型或结构式错误的是
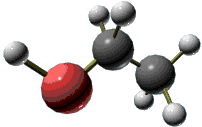
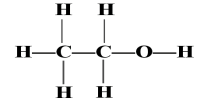
(
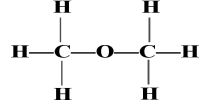
)
2.下列酒类饮品中酒精含量最高的是 ( ) A B C D
A 啤酒 B 白酒 C 葡萄酒 D 黄酒
3.下列有机物中,不属于烃的衍生物的是 ( )
A.氯丁烷 B.甲苯 C.硝基苯 D.乙醇
4.下列物质不能用于从碘水中提取碘的是 ( )
A、乙醇 B、苯 C、四氯化碳 D.汽油
5.下列有关乙醇的物理性质的应用中不正确的是
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子深”的说法
6.某饱和一元醇0.1mol,跟足量金属钠作用,能产生氢气 ( )
A.0.1mol B.0.1g C.1.12L D.0.05mol
7.向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述中正确的是 ( ) A.钠块沉在乙醇液面的下面 B.钠熔化成小球
C.钠块在乙醇的液面上游动 D.钠块表面有气泡放出
8.(20xx年全国理综)a g的铜丝灼烧变黑,立即放人下列的某种物质中发生反应,铜丝变红且反应后铜丝质量仍为a g.则该物质是 ( )
A.稀H2SO4 B.C2H5OH C.CuSO4溶液 D.NaOH溶液
9.若要检验酒精中是否含有少量水,可选用的试剂是 ( )
A.生石灰 B.金属钠 C.浓硫酸 D.无水硫酸铜
10.(20xx年上海理综)下列选项中说明乙醇作为燃料的优点的是 ( )①燃烧时发生氧化反应 ②充分燃烧的产物不污染环境 ③乙醇是一种再生能源 ④燃烧时放出大量热量 A ①②③ B ①②④ C ①③④ D ②③④
11.醇类是链烃基与—OH直连的烃的衍生物,化学性质与乙醇相似,32 g某一元醇与足量的金属钠完全反应,得到11.2 L。(标准状况)氢气,该醇的分子式是 ( ) ( ) 1
A.CH3OH B.C2H5OH C.C3H7OH D.C4H9OH
12.(06上海高考)二甘醇可用作溶剂纺织助剂,进入人体会导致急性肾衰竭危及生命。二甘醇
的结构简式是HO—CH2CH2—O—CH2CH2—OH。下列有关二甘醇叙述正确的 ( ) A.不能发生消去反应 B.能发生取代反应 C.能溶于水,不溶于乙醇 D.符合通式CnH2nO3
13..已知C4H10的同分异构体有两种:CH3-CH2-CH2—CH3、CH3-CH(CH3)-CH3则C4H9OH属于醇类的同分异构体共有( ) A.1种 B.2种 C.3种 D.4种 二、填空题
14.已知乙醇的分子结构如下图:其中①②③④⑤表示化学键的代号,用代号回答 乙醇与钠反应断裂的键是_
乙醇与氧气在铜或银作催化剂,加热条件下反应断裂的键是
15.在焊接铜漆包线时,常先把线头放在火上烧一下,以除去漆层,并立即在酒精中蘸一下再焊接,这是因为(用化学方程式表示):⑴ ; ⑵ 。
16.把一端弯成螺旋状的铜丝放在酒精灯外焰部分加热,可以看到铜丝表面变 色,这是因为生成了 。趁热将它插入盛乙醇的试管中,发现铜丝表面变成 色,并有 气味的物质生成,反应的化学方程式是 该反应属于 反应。 17.(20xx年高考)对于司机酒后驾车,可对其呼出的气体进行检验而查出,所利用的化学反应如下:2CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O
被检测的气体成分是_____,上述反应中的氧化剂是_____,还原剂是____。 三、计算题
18.科学实验测得:乙醇的相对分子质量为46,现取9.2克乙醇在足量的氧气中完全燃烧,将燃烧后的产物依次通过足量的浓硫酸和氢氧化钠溶液,测得浓硫酸增重10.8克,氢氧化钠溶液增重17.6克,求:乙醇的分子式(要写出计算过程)。
19.一定量的乙醇在氧气不足的条件下燃烧,得到一氧化碳、二氧化碳和水的总质量为27.6g,其中水的质量为10.8g。试求一氧化碳和二氧化碳的质量。
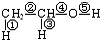
2
练习二:乙酸
一、选择题(可能有1-2答案)
1.乙酸的结构简式是CH3COOH,其官能团是 A.-CH3
B.-H
C.-OH
D.-COOH
( )
2.关于冰醋酸的说法中正确的是 ( ) A.冰醋酸是冰和醋酸的混合物 C.冰醋酸是无色无味的液体
B.冰醋酸是纯净的乙酸 D.冰醋酸易溶解于水和乙醇
( )
3.下列物质能够使紫色石蕊试液变色的是 A.甲烷
B.乙醇
C.乙酸
D.苯
4.酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是 A.酯化反应的反应物之一肯定是醇 C.酯化反应是有限度的
B.酯化反应一般需要脱水 D.酯化反应一般需要催化剂
( )
5.乙醇和乙酸发生酯化反应时,浓硫酸的作用是 ( ) A.脱水作用 B.吸水作用 C.氧化作用 D.既起催化作用又起吸水作用 6.实验室用乙酸、乙醇、浓H2SO4制取乙酸乙酯,加热蒸馏后,在饱和Na2CO3溶液上面得到无色油状液体,当振荡混合时,有气泡产生,原因是 ( ) A.产品中有被蒸馏出的H2SO4 B.有部分未反应的乙醇被蒸馏出来 C.有部分未反应的乙酸被蒸馏出来 D.有部分乙醇跟浓H2SO4作用生成乙烯 7.巴豆酸的结构简式为CH3—CH=CH—COOH。现有 ①氯化氢、②溴水、③纯碱溶液、④2—丁醇、⑤酸性高锰酸钾溶液,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆
酸反应的物质是 ( ) A、只有②④⑤ B、只有①③④ C、只有①②③④ D、全部 二、填空题
8.写出下列反应的离子方程式:
⑴醋酸除去水垢的反应 ; ⑵乙酸溶液与澄清石灰水反应 ; ⑶乙酸溶液与氧化铜反应 ; ⑷乙酸溶液与锌粒反应 ; 9.HCOOH、丙酸CH3CH2COOH均含羧基—COOH,因此的化学性质与乙酸相似,请写出下列化学方程式 ①甲酸与碳酸钠反应: ; ②丙酸、乙醇与浓硫酸混合后加热 。 10.已知在一定的条件下乙醛能发生下列反应:CH3CHO+H2→CH3CH2OH。现有有A、B、C、D、E五种有机物,分别由碳、氢两种元素或碳、氢、氧三种元素组成。五种有机物各取0.1rnol,分别完全燃烧,都能得到4.48L(标准状况下)二氧化碳。 (1)A氧化能得到B,E氧化能得到A;
(2)D在一定条件下跟水反应能得到E,D跟氢气加成得到C; (3)B易溶于水,水溶液呈酸性。
3
则这五种有机物的结构简式分别为: A______ ______ __,B_____ __________,C______ _________, D__________ _____, E_______ ________。
11.乳酸的结构简式为:CH3(1)乳酸分子含有官能团名称: ;
(2)乳酸与NaOH反应化学方程式: ;
(3)乳酸与Na反应化学方程式: ;
12.(06年全国卷II)可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空:
(1) 试管a中需要加入浓硫酸、冰醋酸和乙醇各
2mL,正确的加入顺序入操作是
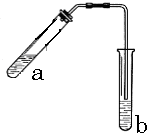
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 ;
(3)实验中加热试管的目的是:
① ; ② ;
(4) 试管b中加有饱和Na2CO3溶液 ,其作用是 ;
(5)反应结束后,振荡试管b静置,观察到的现象是 ;
三、计算题
13.某有机物含碳40.0%、氧53.3%、氢6.70%,其蒸气密度为2.68g/L(已校正至标准状况),此有机物呈酸性。
(1)通过计算,根据性质确定此有机物的结构简式。
(2)用30g此有机物跟足量碳酸钠溶液反应,所产生的气体在标准状况下的体积是多少?
4
参考答案 第三节 生活中两种常见的有机物(第1课时:乙醇) 一、选择题
1.D 2.B 3.B 4.A 5.A 6.BD 7.AD 8.B 9.D 10.D 11.A 12.B 13..D 二、填空题
14.⑤ ;③⑤
△ △ O 15.⑴2Cu+O2===2CuO ⑵C2H52
16.黑,氧化铜,红,刺激性,2CH3CH2OH+O2O 氧化
17.C2H5OH、CrO3、C2H5OH 三、计算题
18.n(C) =17.6g÷44(g/mol)=0.4 mol; m(C)=0.4 mol×12(g/mol)=4.8g
n(H)=10.8g÷18(g/mol)=1.2 mol; m(H)=1.2 mol×1(g/mol)=1.2g m(O)=9.2g—4.8g—1.2g=3.2g; n(H)=3.2g÷16(g/mol)=0.2 mol 则; n(C)∶n(H)∶n(O)=2∶6∶1
所以,可设乙醇的分子式为(C2H6O)x;根据乙醇的相对分子质量为46,得:
46x=46 即:X=1。 故,乙醇的分子式为C2H60。
19.解:设一定量的乙醇不完全燃烧产生的CO、CO2的物质的量分别为x、y
由题意可求得产物水的物质的量为:10.8g/18g·mol-1=0.6mol,
根据燃烧前后的氢原子守恒可以得出乙醇的物质的量为:(0.6mol×2)/6=0.2mol 根据碳原子守恒列等式:
x+y=0.2mol×2=0.4mol??????①
根据题意中物质质量的变化关系可以列等式: 44x+28y=27.6g-10.8g=16.8g?????②
解①、②两个方程式,可以得出x=0.35mol;y=0.05mol。 所以,CO、CO2的质量分别为1.4g.和15.4g
第三节 生活中两种常见的有机物(第2课时:乙酸)
一、选择题
1.D 2.BD 3.C 4.B 5.D 6.C 7.D 二、填空题 8.略 9.略
10.A:CH3CHO B:CH3COOH C:CH3CH3 D:CH2==CH2 E:C2H5OH 11.羟基、羧基
12.(1)先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸
(如在试管a中最先加入浓硫酸,此题得0分) (2)在试管a中加入几粒沸石(或碎瓷片) (3) ①加快反应速率
5
②及时将产物乙酸乙酯蒸出,以利于平衡向生成乙酸乙酯的方向移动
(4)吸收随乙酸乙酯蒸出的少量酸性物质和乙醇
(5)b中的液体分层,上层是透明的油状液体
三、计算题
13.⑴CH3COOH ⑵5.6L
6
