实验二十五 SDS-聚丙烯酰胺凝胶电泳
测定蛋白质相对分子质量
一、目的要求
1、掌握SDS-聚丙烯酰胺凝胶电泳法的原理。
2、巩固垂直板电泳的基本操作。
3、学会用该方法测定蛋白质的相对分子量。
二、原理
聚丙烯酰胺凝胶电泳具有较高分辨率,用它分离、检测蛋白质混合样品,主要是根据各蛋白质组分的分子大小和形状以及所带净电荷多少等因素所造成的电泳迁移率的差别。1967年,Shapiro等人发现,在聚丙烯酰胺凝胶中加入十二烷基硫酸钠(sodium dodecylsulfate,SDS)后,与SDS结合的蛋白质带有一致的负电荷,电泳时其迁移速率主要取决于它的Mr(相对分子质量),而与所带电荷和形状无关。
当蛋白质的Mr在15000~200000之间时,蛋白质的Mr与电泳迁移率间的关系可用下式表示:
lgMr=K-bm
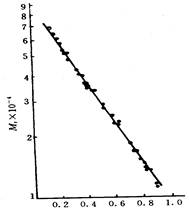
图1 37种蛋白质的Mr对数与电泳相对迁移率关系图
Mr范围为11000~70000,
10%凝胶, pH=7.2, SDS-磷酸盐缓冲系统
式中,Mr为蛋白质的相对分子质量;m为迁移率;b为斜率;K为截距。均为常数。在条件一定时,b和K将已知相对分子质量的标准蛋白质的迁移率对Mr的对数作图,可得到一条标准曲线(如图1)。将未知相对分子质量的蛋白质样品,在相同的条件下进行电泳,根据它的电泳迁移率可在标准曲线上查得它的相对分子质量。
SDS是一种阴离子型去污剂,在蛋白质溶解液中加入SDS和巯基乙醇后,巯基乙醇可使蛋白质分子中的二硫键还原;SDS能使蛋白质的非共价键 (氢键、疏水键)打开,并结合到蛋白质分子上(在一定条件下,大多数蛋白质与SDS的结合比为1.4 g SDS/g蛋白质),形成蛋白质—SDS复合物。由于SDS带有大量负电荷,当它与蛋白质结合时,所带的负电荷的量大大超过了蛋白质分子原有的电荷量,因而掩盖了不同种类蛋白质间原有的电荷差异。
SDS与蛋白质结合后,还引起了蛋白质构象的改变。蛋白质—SDS复合物的流体力学和光学性质表明,它们在水溶液中的形状,近似于雪茄烟形的长椭圆棒。不同蛋白质的SDS复合物的短轴长度都一样,而长轴则随蛋白质相对分子质量的大小成正比地变化。这样的蛋白质—SDS复合物在凝胶中的迁移率,不再受蛋白质原有电荷和形状的影响,而只是椭圆棒的长度,也就是蛋白质相对分子质量的函数。
SDS-PAGE缓冲系统有连续系统和不连续系统。不连续SDS-PAGE缓冲系统有较好的浓缩效应,近年趋向用不连续SDS-PAGE缓冲系统。按所制成的凝胶形状又有垂直板型电泳和垂直柱型电泳。本实验采用SDS-不连续系统垂直板型凝胶电泳测定蛋白质的相对分子质量。
三、试剂与器材
(一)、试剂
1.标准蛋白质纯品:根据待测蛋白质的相对分子质量大小,选择4~6种已知相对分子质量的蛋白质纯品作为标准蛋白质。本实验采用的标准蛋白质见表1所示。
表1 5种标准蛋白质的相对分子质量

2.1%(V/V)TEMED溶液:取1 ml TEMED,加蒸馏水至100 ml,置于棕色瓶中,在4℃冰箱中保存。
3.10%(W/V)过硫酸铵溶液:取过硫酸铵1 g,溶解于10ml蒸馏水中。最好现配现用。
4.0.05 mol·L-1,pH=8.0 Tris-HCI缓冲溶液:称取Tris 0.61g,加入50ml蒸馏水使之溶解,再加入3ml l mol·L-1 HCl溶液,混匀后在pH计上调pH至8.0,最后加蒸馏水定容至100ml。
5. 蛋白质样品溶解液:SDS 100mg,巯基乙醇0.1 ml,甘油1.0ml,溴酚蓝2 mg,Tris-HCl缓冲溶液2ml,加蒸馏水至总体积10ml。
6.分离胶缓冲溶液:Tris 36.3 g,加入1 mol·L-1 HCl溶液48.0 ml,再加蒸馏水到100ml,pH=8.9。
7.浓缩胶缓冲溶液:Tris 5.98g,加1 mol·L-1 HCI溶液48.0ml,加蒸馏水到100ml,pH=6.7
8.凝胶贮液:Acr 30.0g,Bis 0.8g,加蒸馏水到100ml
9. 电极缓冲溶液:SDS l g,Tris 6g,甘氨酸28.8g,加蒸馏水至1000ml,pH=8.3。
10.固定液:取50%甲醇454ml,冰醋酸46ml,混匀。
11.染色液:1.25 g考马斯亮蓝R-250,加454 ml 50%甲醇溶液和46ml冰醋酸,混匀。
12.脱色液:取冰醋酸75ml,甲醇50ml,加蒸馏水875 ml。
(二)、器材
1.垂直板型电泳槽
2.直流稳压电源(电压300~600V,电流50~100mA)
3.50或100μl的微量注射器
四、操作步骤
(一)安装垂直板型电泳装置
此种夹心式垂直板电泳装置(如图2,3)的两侧为有机玻璃制成的电极槽,两个电极槽中间夹有一个凝胶模子。凝胶模子由3部分组成;一个“U”形的硅胶框、两块长短不等的玻璃片、样品槽模板(俗称“梳子”)。电极槽由上贮槽(白金电极在上或面对短玻璃片)、下贮槽(白金电极在下或面对长玻璃片)和冷凝系统组成。凝胶模子的硅胶框内侧有两条凹槽,可将两块相应大小的玻璃片嵌入槽内。玻璃片之间形成一个2~3mm厚的间隙,将来制胶时,将胶灌入其中。灌胶前,先将玻璃片洗净、晾干、嵌入胶带凹槽中。长玻璃片下沿与胶带框底之间保持有一缝隙,以使此端的凝胶与一侧的电极槽相通;而短玻璃片的下沿则插入橡胶框的底槽内。将已插好玻璃片的凝胶模子置于仰放的上贮槽上,短玻璃片应面对上贮槽,再合上下贮槽,用4条长螺丝将两个半槽固定在一起。上螺丝时,要按一定顺序逐个拧紧,均匀用力。将装好的电泳装置垂直放置,在长玻璃片下端与硅胶框交界的缝隙内加入用电极缓冲溶液配制的1%琼脂糖溶液,待其凝固后,即堵住凝胶模板下面的窄缝(通电时又可作为盐桥)。(二)凝胶的制备
1.分离胶的制备
根据所测蛋白质的相对分子质量范围,选择某一合适的分离胶浓度。按表2所列的试剂用量配制。
将所配制的凝胶液沿着凝胶的长玻璃片的内面用细长头的滴管加至长、短玻璃片的窄缝内,加胶高度距样品槽模板下缘约1 cm。用滴管沿玻璃片内壁加一层蒸馏
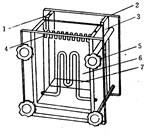
图2 夹心式垂直板型电泳槽示意图
1.导线接头 2.下贮槽 3.U形橡胶框
4.样品槽模板5.固定螺丝 6.上贮槽
7.冷凝系统
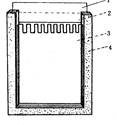 图3 凝胶模子示意图
图3 凝胶模子示意图
1.样品槽模板 2.长玻璃片
3.短玻璃片 4.U形硅胶框
表2 SDS-不连续系统不同浓度凝胶配制用量表
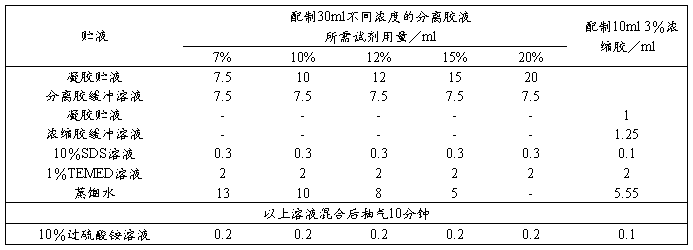
水(用于隔绝空气,使胶面平整)。约30~60分钟凝胶完全聚合,用滴管吸去分离胶胶面的水封层,并用无毛边的滤纸条吸去残留的水液。
2.浓缩胶的制备
按表2配制浓缩胶,混匀后用细长头的滴管将凝胶溶液加到已聚合的分离胶上方,直至距短玻璃片上缘0.5cm处,轻轻将“梳子”插入浓缩胶内(插入“梳子”的目的是使胶液聚合后,在凝胶顶部形成数个相互隔开的凹槽)。约30分钟后凝胶聚合,再放置30分钟。小心拔去“梳子”,用窄条滤纸吸去样品凹槽内多余的水分。
(三)蛋白质样品的处理
1.标准蛋白质样品的处理
称标准蛋白质样品各1 mg左右,分别转移至带塞的小试管中,按1.0~1.5 g/L溶液比例,向样品加入“样品溶解液”,溶解后轻轻盖上盖子(不要盖紧,以免加热时迸出),在100℃沸水浴中保温2~3分钟,取出冷至室温。如处理好的样品暂时不用,可放在-20℃冰箱保存较长时间。使用前在100℃水中加热3分钟,以除去可能出现的亚稳态聚合物。
2.待测蛋白质样品的处理
固体样品的处理与标准蛋白质相同。如待测样品已在溶液中,可先配制“浓样品溶解液”(各种溶质的浓度均比“样品溶解液”高1倍),将待测液与“浓样品溶解液”等体积混匀,然后同上加热。如待测液太稀可事先浓缩,若含盐量太高则需先透析。
(四)加样
将pH=8.3的电极缓冲溶液倒入上、下贮槽中,应没过短玻璃片。用微量注射器依次在各个样品凹槽内加样,一般加样体积为10~15/μl。如样品较稀,可加20~30/μl。由于样品溶解液中含有比重较大的甘油,故样品溶液会自动沉降在凝胶表面形成样品层。
(五)电泳
将上槽接负极,下槽接正极,打开电源,开始时将电流控制在15~20 mA,待样品进入分离胶后,改为30~50mA。待蓝色染料迁移至下端约1~1.5cm时,停止电泳,约需5~6小时。
(六)固定
取下凝胶模子,将凝胶片取出,滑入一白瓷盘或大培养皿内,在染料区带的中心插入细铜丝作为标志。加入固定液(应没过凝胶片),固定2小时或过夜。
(七)染色
倾出固定液,加入染色液,染色过夜。
(八)脱色
染色完毕,倾出染色液,加人脱色液。数小时换一次脱色液,直至背景清晰,约需一昼夜。
(九)Mr的计算
通常以相对迁移率(mr)来表示迁移率。相对迁移率的计算方法如下:
用直尺分别量出样品区带中心及铜丝与凝胶顶端的距离(如图4),按下式计算:
相对迁移率(mr)=样品迁移距离(cm)/染料迁移距离(cm)。
以标准蛋白质相对分子质量的对数对相对迁移率作图,得到标准曲线(如图1)。根据待测样品的相对迁移率,从标准曲线上查出其相对分子质量。

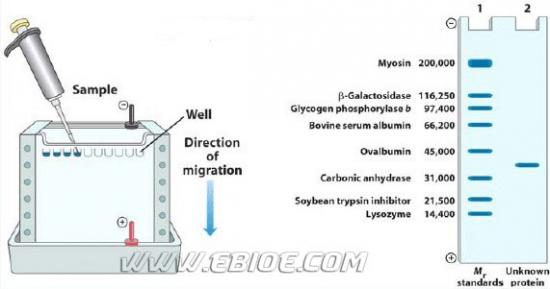
图4 标准蛋白质在SDS-凝胶上的分离示意图
a.样品迁移距离 b.染料迁移距离
1.细胞色素c 2.胰凝乳蛋白酶原A 3.胃蛋白酶
4.卵清蛋白 5.牛血清清蛋白
五、思考题
1、样品溶解液中各种试剂的作用是什么?
2、实验否需要在低温下进行?
3、该方法是否能用于所有的蛋白质相对分子量的测定?为什么?
4、本实验测得的分子量存在误差,根据你的实验分析造成误差产生的原因。
实验二十五 SDS-聚丙烯酰胺凝胶电泳测定蛋白质相对分子质量习题
一、单项选择题
1.在聚丙烯酰胺凝胶中加入下列那个成分后,蛋白质带有一致的负电荷,电泳时其迁移速率主要取决于它的Mr(相对分子质量),而与所带电荷和形状无关。
A.EDTA B.尿素 C.亚精胺 D.SDS
2.下列那个试剂具有还原性?
A.二硫苏糖醇B DEPC C. 巯基乙醇D. Tris-HCl
3.在SDS-聚丙烯酰胺凝胶电泳中,下列那个试剂常用为指示剂?
A.SDS B.巯基乙醇 C.溴酚蓝 D.甘油
4.当蛋白质的分子量在15000~200000之间时,蛋白质的分子量的对数与电泳迁移率是什么关系?
A.正相关线性关系 B 负相关线性关系 C抛物线关系 D.没有规律
5.将未知相对分子质量的蛋白质样品,在相同的条件下进行SDS-聚丙烯酰胺凝胶电泳,考马斯亮蓝染色后,根据它的电泳迁移率可在标准曲线上查得蛋白质的那个信息?
A.蛋白质的结构B.蛋白质的底物C.蛋白质的抗体D 蛋白质的分子量
二、多项选择题
1.下列那些试剂是蛋白质样品溶解液的成分?
A.SDS B三氯乙酸 C溴酚蓝 D磷酸二氢钠
2.在SDS-聚丙烯酰胺凝胶电泳中,脱色液和染色液共用的是那两个试剂?
A. TEMED B. 冰醋酸C. 甲醇 D.HCl
3.SDS与蛋白质结合后,还引起了蛋白质构象的改变,它们在水溶液中的形状,不可能是
下列那些形状?
A. 雪茄烟形 B. 长椭圆棒 C.正方体形 D.球形
4.在公式lgMr=K-bm 中,作为常数的是:
A. Mr B. K C. b D. m
5.在SDS-不连续系统垂直板型凝胶电泳测定蛋白质的相对分子质量实验中,有那些效应?A.浓缩效应 B.化学效应 C.分子筛效应 D.电荷效应
三、填空题
1.在SDS-聚丙烯酰胺凝胶电泳中,电泳时其迁移速率主要取决于它的————,而与所带电荷
和形状无关。
2.在SDS-聚丙烯酰胺凝胶电泳中,SDS与蛋白质结合后,不同蛋白质的SDS复合物的————
长度都一样,而————则随蛋白质相对分子质量的大小成正比地变化。
3.SDS是一种————离子型去污剂。
4.由于SDS带有大量————电荷,当它与蛋白质结合时,所带的电荷量大大超过了蛋白质分
子原有的电荷量,因而掩盖了不同种类蛋白质间原有的电荷差异。
5.蛋白质样品溶解液中,甘油的作用是————。
四、简答题
1、简述SDS-聚丙烯酰胺凝胶电泳测定蛋白质相对分子质量的原理。
2、在SDS-聚丙烯酰胺凝胶电泳中,试说明样品溶解液中(含有SDS、巯基乙醇、甘油、溴酚蓝、和Tris-HCl)各种试剂的作用是什么?
3、在SDS-聚丙烯酰胺凝胶电泳中,当SDS与蛋白质结合后,会引起蛋白质构象如何变化?该变化会有什么结果?
参考答案
一、单项选择题
1、D 2、C 3、C 4、B 5、D
二、多项选择题
1、AC 2、BC 3、AB 4、CD 5、ACD
三、填空题
1.Mr(相对分子质量)
2.短轴, 长轴
3.阴
4.负
5.协助蛋白质沉淀
四、简答题
1、简述SDS-聚丙烯酰胺凝胶电泳测定蛋白质相对分子质量的原理。
答案:在聚丙烯酰胺凝胶中加入十二烷基硫酸钠(sodium dodecylsulfate,SDS)后,与SDS结合的蛋白质带有一致的负电荷,电泳时其迁移速率主要取决于它的Mr(相对分子质量),而与所带电荷和形状无关,在一定的分子量范围内,二者是种线性关系。这是因为SDS带有大量负电荷,当它与蛋白质结合时(大多数蛋白质与SDS的结合比为1.4 g SDS/g蛋白质),所带的负电荷的量大大超过了蛋白质分子原有的电荷量,因而掩盖了不同种类蛋白质间原有的电荷差异。
2、在SDS-聚丙烯酰胺凝胶电泳中,试说明样品溶解液中(含有SDS、巯基乙醇、甘油、溴酚蓝、和Tris-HCl)各种试剂的作用是什么?
答案:SDS:结合蛋白质,消除蛋白质间电荷差异,同时是一种变性剂;巯基乙醇:还原剂;甘油:协助沉淀蛋白质;溴酚蓝:指示剂;Tris-HCl:缓冲剂。
3、在SDS-聚丙烯酰胺凝胶电泳中,当SDS与蛋白质结合后,会引起蛋白质构象如何变化?该变化会有什么结果?
答案:SDS与蛋白质结合后,还引起了蛋白质构象的改变。蛋白质—SDS复合物的流体力学和光学性质表明,它们在水溶液中的形状,近似于雪茄烟形的长椭圆棒。不同蛋白质的SDS复合物的短轴长度都一样,而长轴则随蛋白质相对分子质量的大小成正比地变化。这样的蛋白质—SDS复合物在凝胶中的迁移率,不再受蛋白质原有电荷和形状的影响,而只与椭圆棒的长度相关,也就是蛋白质相对分子质量的函数。
第二篇:SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE)实验原理和操作步骤
SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE)实验原理和操作步骤
实验原理:
SDS-PAGE是对蛋白质进行量化,比较及特性鉴定的一种经济、快速、而且可重复的方法。该法是依据混合蛋白的分子量不同来进行分离的。
SDS是一种去垢剂,可与蛋白质的疏水部分相结合,破坏其折叠结构,并使其广泛存在于一个广泛均一的溶液中。SDS蛋白质复合物的长度与其分子量成正比。在样品介质和凝胶中加入强还原剂和去污剂后,电荷因素可被忽略。蛋白亚基的迁移率取决于亚基分子量。
试剂和器材:
试剂:1. 5x样品缓冲液(10ml):0.6ml 1mol/L的Tris-HCl(pH6.8),5ml 50%甘油,2ml 10%的SDS,0.5ml巯基乙醇[a1] ,1ml 1%溴酚蓝,0.9ml蒸馏水。可在4℃保存数周,或在-20℃保存数月。
2. 凝胶贮液:在通风橱中,称取丙烯酰胺30g,甲叉双丙烯酰胺0.8g,加重蒸水溶解后,定容到100ml。过滤后置棕色瓶中,4℃保存,一般可放置1个月。
3. pH8.9分离胶缓冲液: Tris 36.3g ,加1mol/L HCl 48ml,加重蒸水80ml使其溶解,调pH8.9,定容至100ml, 4℃保存。
4. pH6.7浓缩胶缓冲液: Tris 5.98g ,加1mol/L HCl 48ml,加重蒸水80ml使其溶解,调pH6.7,定容至100ml, 4℃保存。
5. TEMED(四乙基乙二胺)原液
6.10%过硫酸铵(用重蒸水新鲜配制)
7. pH8.3 Tris-甘氨酸电极缓冲液:称取Tris 6.0g,甘氨酸28.8g,加蒸馏水约900ml,调pH8.3后,用蒸馏水定容至1000ml。置4℃保存,临用前稀释10倍。
8. 考马斯亮蓝G250染色液:称100mg考马斯亮蓝G250,溶于200ml蒸馏水中,慢慢加入7.5ml 70%的过氯酸,最后补足水到250ml,搅拌1小时,小孔滤纸过滤。
器材:电泳仪,电泳槽,水浴锅,摇床。
实验操作
(一)样品制备
将蛋白质样品与5X样品缓冲液(20ul+5ul)在一个Eppendorf管中混合。放入100℃加热 5-10min,取上清点样。
(二)分离胶及浓缩胶的制备1 将玻璃板、样品梳、Spacer用洗涤剂洗净,用ddH2O 冲洗数次,再用乙醇擦拭,晾干;
2 将两块洗净的玻璃板之间加入Spacer,按照Bio-Rad Mini Ⅱ/Ⅲ说明书提示装好玻璃板;
3 按如下体积配制10%分离胶8.0 ml,混匀;
ddH2O 3.0 ml
1.0 mol/LTris-HCl[a2] pH=8.8 2.1 ml
30% Acr-Bis[a3] 2.8 ml
10% SDS [a4] 80 ul
10%AP[a5] 56 ul
TEMED[a6] 6 ul
4 向玻璃板间灌制分离胶,立即覆一层重蒸水,大约20 min后胶即可聚合;
5 按如下体积配制6%浓缩胶3.0 ml,混匀;ddH2O[a7] 1.0 mol/LTris-HCl pH=6.8 30% Acr-Bis
2.0 ml 400 ul 600 ul
10% SDS 10% AP TEMED
36ul 24ul 4ul
6 将上层重蒸水倾去,滤纸吸干,灌制浓缩胶,插入样品梳;
7 装好电泳系统,加入电极缓冲液,上样20 μl;
8 稳压200V,溴酚蓝刚跑出分离胶时,停止电泳,约需45 min~1hr.
9 卸下胶板,剥离胶放入染色液中,室温染色1~2 hr;加入脱色液,置于80 rpm脱色摇床上,每20 min更换一次脱色液(10 ml 冰乙酸;45 ml乙醇;45 ml蒸馏水)至完全脱净。
打开二硫键的作用
缓冲溶液,三羟甲基氨基甲烷
甲叉双丙烯酰胺
十二烷基磺酸钠,使蛋白质变性
过硫酸铵,助氧化剂,加速胶的凝固
催化过硫酸钠产生自由基,从而加速丙烯酰胺凝胶的聚合
重蒸水
