����ˮʵ����л�ѧʵ�鼼�ܴ������ֱ�
�༶�� ������
�ڶ�ƪ������к͵ζ�ϰ��
������ѧ20xx�괺�ڸ߶���ѧ
����к͵ζ���ϰ��
�߶���1�� ������ �ܷ�
һ��ѡ����
1������������������0���̶�λ����ȷ���ǣ� ��
A. ����Ͳ���϶�
C. ��������ƽ�̶ȳߵ�����
A. 25ml��Ͳ
C. 25ml��ʽ�ζ��� B. �ڵζ����϶� D. ��������ƽ�̶ȳߵ��ұ� B. 25ml��ʽ�ζ��� D. �п̶ȵ�50ml�ձ� 2��ȷ��ȡ25.00ml KMnO4��Һ����ѡ�õ������ǣ� ��
3������ʵ���У����ڴ���������������������һ��ƫ�͵��ǣ� ��
A. ����Ͳ��ȡһ�����Һ��ʱ�����Ӷ����Ķ���
B. �ñ�����ζ�����������Һ���ҺŨ��ʱ����ʽ�ζ���ϴ����û���ñ�������ϴ��ֱ��װ������ζ���Һ��������ļ�Һ��Ũ��ֵ
C. �ⶨ����ͭ����ᾧˮ����ʱ�������¶�̫��ʹһ��������ͭ�����ֽ⣬������Ľᾧˮ�ĺ���
D. ���к��Ȳⶨʱ���ڴ�С�ձ�֮��û�е�����ĭ���ϣ���ֽ������������к�����ֵ
4������кͷ�Ӧ���ڷ��ȷ�Ӧ������к�����1molˮʱ���ų���������Ϊ�к��ȡ�������Ũ�Ⱦ�Ϊ0.1mol/L����Һ���ʱ�����˵������ȷ���ǣ� ��
A. ��NaOH��Ӧʱ��HCL���к���С��CH3COOH���к���
B. ��NaOH��Ӧʱ��HCL���к��ȴ���CH3COOH���к���
C. ��NaOH��Ӧʱ��H2SO4���к��ȴ���HCL���к���
D. ��H2SO4��Ӧʱ��Ba��OH��2���к��ȵ���NaOH���к��ȵ�2��
5�����й��ڵ��������pH��NaOH�Ͱ���Һ��˵����ȷ���ǣ� ��
A. ������Һ��OH��Ũ����ͬ
B. ��Ҫ��Ũ�ȡ�������������к�
C. �¶�����10�棬����Һ��pH�����
D. ������Һ�����ʵ����ʵ���Ũ����ͬ
6�������ȫ�к�ʱ�� ��
A�����������ʵ���һ����� C���������������
+- B���������ṩ��H�ͼ������ṩ��OH�����ʵ������ D����Һ������
7��Ҫȷ��ȡ25.00mL��ϡ���ᣬ���õ������ǣ� ��
A��25mL����ƿ B��25mL��Ͳ C��25mL��ʽ�ζ��� D��25mL��ʽ�ζ���
8����25mL�ļ�ʽ�ζ�����ʢ����Һ��Һ��ǡ����20mL�̶ȴ����ֽ��ζ�������Һȫ���ų���������Ͳ�ڣ�������Һ�����Ϊ�� ��
A��5mL B��20mL C������5mL D����5mL
9�������ʵ���Ũ����ͬ�����ᡢ���ᡢ������Һ���ֱ��к�������ͬ��Ũ����ͬ��NaOH��Һ�������Σ��������������������ǣ� ��
A��1:1:1 B��3:2:1 C��6:3:2 D��1:2:3
10���к���ͬ�������ͬpH��Ba(OH)2��NaOH��NH3��H2O����ϡ��Һ��������ͬŨ�ȵ��� 1 ��
�������ֱ�ΪV1��V2��V3�������ߵĴ�С��ϵΪ�� ��
A��V3>V2>V1 B��V3>V2=V1
C��V3=V2>V1 D��V1=V2>V3��
11����NaOH��Һ�ζ�����ʱ�����ڵζ��ٶ�̫�죬�������Һ���ʱ��֪NaOH�Ƿ�������ж����Ƿ�����ķ����ǣ� ��
A������5mL�����ٽ��еζ� B������һ�δ�������
C�����½��еζ� D�����Ϸ�����������
12�������£��ڰ�ˮ�е������ᣬʹpH=7������˵���д�����ǣ� ��
A����������������� B��������������
+--7+- C��c(H)=c(OH)=10mol/L D��c(NH4)<c(Cl)
13����10mLpH=12��ij����Һ�м���10mLpH=2�����ᣬ��ַ�Ӧ������̪��Һ����Һ��죬��˼�һ���ǣ� ��
A������ B��һԪǿ�� C����Ԫǿ�� D���κ�ǿ��
14�������Ŀ�������Һ�ֱ���pHֵΪ2��3�Ĵ�����Һ�кͣ������Ĵ�����Һ���������ΪVa��Vb��������֮��Ĺ�ϵ�ǣ� ��
A��Va>10Vb B��Vb=10Va C��Va<10Vb D��Vb>10Va
15��ij���Լ���Ʒ�к��в����ᷴӦ�����ʣ�Ϊ�˲ⶨ���ԼصĴ��ȣ�ȡ��Ʒ0.56g����ˮ�Ƴ�1L��Һ��ȡ����Һ25.00mL����0.005mol/LH2SO4��Һ�ζ�����ȥ24mL������Լص���������Ϊ�� ��
A��96% B��48% C��9.6% D��56%
16�������й��к͵ζ��IJ��������ñ�Һ��ϴ�ζ��ܣ������ζ�����ע�����Һ���ۼ��ζ����Ƿ�©ˮ���ܵζ����ݵμ�ָʾ���ڴ���Һ����ϴ�ӡ���ȷ�IJ���˳���� ( )
A���ޢۢ٢ڢݢ� B���ݢ٢ڢޢܢ�
C���ݢܢۢڢ٢� D���ۢ٢ڢܢݢ�
-117��ijѧ���ü�ʽ�ζ�����ȡ0.1mol��L��NaOH��Һ����ʼʱ����Һ�����Ϊ1.0mL�� ȡ
��������Һ����Һ�棬����Ϊ11.0mL����ͬѧ�ڲ�����ʵ��ȡ����Һ�����Ϊ ( )
A.����10.0mL B.��10.0mL C.����10.0mL D.����11.0mL
18�� ����֪Ũ�ȵ�NaOH��Һ�ⶨijH2SO4��Һ��Ũ�ȣ��ο���ͼ���ӱ���ѡ����ȷѡ� ��
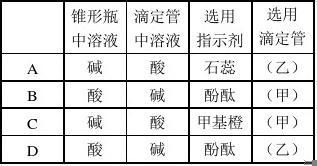

19�� ����֪Ũ�ȵ���ζ�δ֪Ũ�ȵļ�ʱ���ᵼ�´����Һ��Ũ��ƫ�͵IJ�����
����ʽ�ζ���������ˮϴ��δ�ñ�Һ��ϴ
�ڼ�ʽ�ζ���������ˮϴ��δ�ô���Һ��ϴ
�����Ƽ�Һʱ�������Ĺ������� �ܵζ�ǰ��ʽ�ζ��ܼ��첿��δ������Һ
�ݵζ��в�������ƿ��Һ��ҡ��������ƿ��
A. �٢ۢ�
-1B. �ڢ� C. �ڢۢ� D. �٢� -120����0.01mol��LH2SO4�ζ�0.01mol��LNaOH��Һ���кͺ��ˮ��100mL .���ζ�ʱ�յ�
+�ж������ٶ����1��H2SO4�����ټ���1��H2SO4(��1��Ϊ0.05mL)����ٺ͢ڣ�H��
2
֮��ֵ( )
3 4A.10 B.50 C.5��10D.10
���������
1������������������Ʒ��������̨������Ȧ���������У�������ƿ���۵ζ��ܣ���ʽ
���ʽ�������ձ������ɸ������ݲ�����������ƽ�������룩������ֽ������Ͳ��������©����������ҩƷ����NaOH���壻�ڱ�NaOH��Һ����δ֪Ũ�ȵ������Na2CO3��Һ���Իش��������⡣
��1��������к͵ζ�ʱ����ȱ�ٵ��Լ��� ��
��2������250mL0.1mol/L��Һʱ����ȱ�ٵ������� ��
��3������ʱ��Ӧѡ�����������е� �����ţ���
2���ñ�����ζ�δ֪Ũ�ȵİ�ˮʱ����ƿ��ͨ��ʢ�� ���ζ�ʱ���� ������ ��˫��ע�� ���� ʱ�Ŵﵽ�ζ��յ㡣��ζ������н������²������ֱ�ָ����������Եζ������Ӱ�죨�ƫ�ߡ�����ƫ�͡�����Ӱ�족��
��1���÷�̪��ָʾ�� ��
��2���ζ�ǰδ�ñ�������ϴ��ʽ�ζ��� ��
��3���ζ�ǰ�ð�ˮ��ϴ��ƿ ��
��4���ζ�ǰ�������dz��ڷ��õ� ��
��5���к���������ƿ�м�һЩˮ ��
��6���ζ�����ʱ���ӵζ��̶ܿ� ��
3����ȡmg��NaOH���500mL��Һ��ȡ��25mLǡ����20mL������ȫ�кͣ������������ʵ���Ũ���� ��
����mgNaOH��ʵ�ʺ����������������ƣ��������ʵ��Ũ�ȱ��������ֵҪ �� ����mgNaOH��ʵ�ʺ����������Ȼ��ƣ��������ʵ��Ũ�ȱ��������ֵҪ �� ��mgNaOH��ʵ�ʺ���������̼���ƣ��������ʵ��Ũ�ȱ�������ֵҪ ��
4���������ⶨˮ���ܽ����ķ����ǣ�
����ȡamLˮ����Ѹ�ټ���̶���MnSO4��Һ�ͼ���KI��Һ����KOH������������ƿ����������ʹ֮��ַ�Ӧ���䷴ӦʽΪ�� 2Mn+O2+4OH=2MnO(OH)2���÷�Ӧ���죩
�ڲⶨ��������Ѹ�ټ���1mL��2mLŨ���ᣨ�ṩH����ʹ֮����I2������bmol/L��Na2S2O3
��Һ�ζ����Ե���Ϊָʾ����������VmL���йط�ӦʽΪ��
MnO(OH)2+2I+4H=Mn+I2+3H2O I2+2S2O3=2I+S4O6
�Իش𣺣�1��ˮ���ܽ����ļ���ʽ�ǣ���g/LΪ��λ�� ��
��2���ζ���I2��S2O3��Ӧ���Ե���Ϊָʾ�����յ�ʱ��Һ�� ɫ��Ϊ ɫ��
��3���ⶨʱ���ζ��ܾ�����ˮϴ�Ӻӵζ���Na2S2O3��Һ�����²ⶨ�����ƫ�ߡ�ƫ�͡���Ӱ�죩 ��
��4����¼�ⶨ���ʱ���ζ�ǰ���ӿ̶��ߣ��ζ������յ�ʱ�ָ��ӿ̶��ߣ������µζ������ƫ�ߡ�ƫ�͡���Ӱ�죩 �� 2--+2+2--2-+2+-
3
5�����к͵ζ����ⶨ�ռ�Ĵ��ȣ����ռ��к��������Ӧ�����ʣ��Ը���ʵ��ش� �Ž�ȷ��ȡ��4.3g�ռ���Ʒ���250mL����Һ����Ҫ����Ҫ��������Ͳ���ձ����������⣬�������õ��������� �� ��
��ȡ10.00mL����Һ���� ʽ�ζ�����ȡ��
����0.2010mol��L-1������ζ������ռ���Һ���ζ�ʱ������ת��ʽ�ζ��ܵIJ������������ֲ�ͣ��ҡ����ƿ������ע�� ��ֱ���ζ����յ㡣 �ȸ����������ݣ��ռ�Ĵ���Ϊ ��
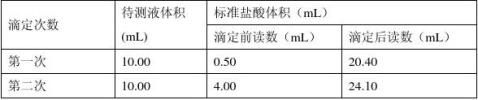
���Ա���������Һ�ζ�δ֪������������ҺΪ��,�ж����в�����������(�ƫ����ƫС�� ����Ӱ�족�����жϡ�)
�ٶ������ζ�ǰƽ�ӣ��ζ����� ��δ�ñ�Һ��ϴ�ζ��� ���ô���Һ��ϴ��ƿ �ܲ�С�Ľ���Һ������ƿ���� �ݵζ��ӽ��յ�ʱ������������ˮ��ϴ��ƿ�ڱ� 6��������ԭ�ζ�ԭ��ͬ�к͵ζ�ԭ�����ƣ�Ϊ�˲ⶨijδ֪Ũ�ȵ�NaHSO3��Һ��Ũ�ȣ�����0.1000mol/L������KMnO4��Һ���еζ����ش��������⣺
��1����ƽ���ӷ���ʽ�� MnO4-3-H+����2+42-H2O
��2���ζ������У�NaHSO3��Һ�������20.00mL������0.100mol/L������KMnO4��Һ16.00mL����NaHSO3��Һ�����ʵ���Ũ���� mol/L��
��3�����в����ᵼ�²ⶨ���ƫ�ߵ���
A��δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ��� B���ζ�ǰ��ƿδ����
C���ζ�ǰ�ζ��ܼ��첿�������� D����С�Ľ���������KMnO4��Һ������ƿ�� E���۲����ʱ���ζ�ǰ���ӣ��ζ�����
7�� �õζ��ķ������ⶨ�����Ũ�ȣ�ʵ������������ʾ��
ʵ����
1
2
3 ����HCl��Һ�� �������L 20.0 20.0 20.0 ����Na2CO3��Һ�Ī� �������L 24.8 23.1 22.9
��1���ζ������ϴ���ǣ� ����ʵ�飬�������������������ԭ���ǣ� .
��2������δ֪�����Ũ�ȣ����ݾ�ȷ��0.1����
4
