酸碱中和滴定实验报告
班级 姓名 学号 合作者 日期
一、实验目的:用已知浓度溶液(标准溶液)【本实验NaOH为标准溶液】测定未知溶液(待测溶液) 浓度【本实验盐酸为待测溶液】
二、实验用品:
1.所用仪器:酸式滴定管、碱式滴定管、锥形瓶、滴管、烧杯
2.所用试剂:0.1000mol/LNaOH溶液、待测盐酸、酚酞
三、实验原理:c(标)×V(标) = c(待)×V(待)【假设反应计量数之比为1:1】
【本实验具体为:c(H+)×V(酸) = c(OH-)×V(碱)】
四、实验操作:
(1)查:检查是否漏水和堵塞。
(2)洗:洗净后用指定的酸和碱液润洗。(锥形瓶只用蒸馏水洗净即可)
(3)盛、调:用烧杯沿漏斗注入滴定管中,放出液体,赶气泡、调起点。
(4)取:左手控制酸式滴定管的活塞,将一定体积未知浓度的酸溶液放入锥形瓶中,滴入几滴酚酞。
(5)滴定:操作要点及滴定终点的观察。
左手挤压碱式滴定管玻璃小球,右手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化。(指示剂变色,半分钟内不褪色)
(6)记和算:数据记录和处理,求出酸的浓度

C(盐酸)=
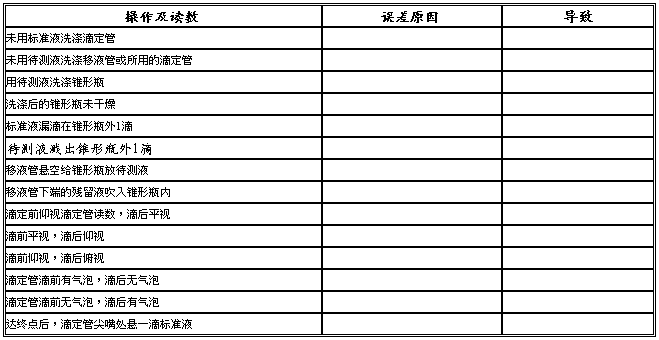
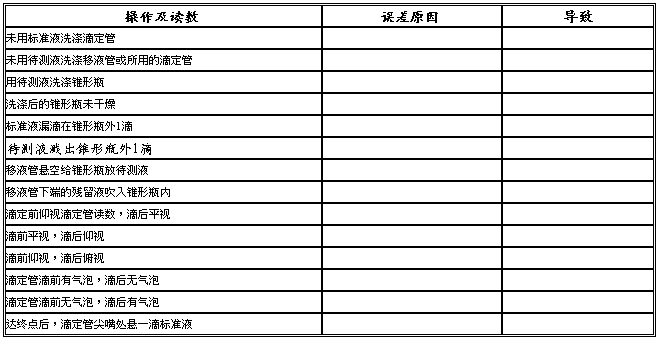
五.常见误差分析:[根据:c(H+)×V(酸) = c[(OH-)×V(碱)分析]
六、练习
1. 刻度“0”在上方的用于测量液体体积的仪器是( )
A. 滴定管 B. 量筒 C. 移液管 D. 量杯
2. 要准确量取25.00 mL稀盐酸,可用的仪器是( )
A. 25 mL碱式滴定管 B. 25 mL量筒 C. 25 mL酸式滴定管
3. 中和滴定时,用于量取待测液体积的仪器是( )
A. 胶头滴管 B. 量筒 C. 滴定管 D. 移液管
4. 进行中和滴定时,事先不应该用所盛溶液洗涤的仪器是( )
A. 酸式滴定管 B. 碱式滴定管 C. 锥形瓶 D. 移液管
5. 在25mL的碱式滴定管中盛有溶液,液面恰好在20mL刻度处,现将滴定管内溶液全部放出,流入量筒内,所得溶液的体积为( )
A. 5mL B. 20mL C. 大于5mL D. 小于5mL
6. 准确量取25.00mL KMnO4溶液可以选用的仪器是( )
A. 50mL量筒 B. 10mL量筒 C. 50mL酸式滴定管 D. 50mL碱式滴定管
7. 用标准浓度的氢氧化钠溶液来滴定未知浓度的盐酸,在滴定操作时,盐酸( )
A. 只能盛在锥形瓶中 B. 只能盛在酸式滴定管中
C. 也可用碱式滴定管取放 D. 既可盛在锥形瓶中,也可盛在酸式滴定管中w.w.w.k.s.5.u.c.o.m
8. 用标准浓度的盐酸来滴定未知浓度的氢氧化钠,若用甲基红为指示剂,滴定终点时的颜色变化应该是
A. 由黄色变成红色 B. 由黄色变为橙色 C. 由橙色变成红色 D. 由红色变为橙色
9. 用标准浓度的氢氧化钠溶液来滴定未知浓度的盐酸,使用酚酞做为指示剂,下列叙述中说明恰好达到滴定终点的是( )
A. 由红色变为深红色 B. 由无色变为深红色
C. 由浅红色变成深红色 D. 由无色变为浅红色
10. 用标准NaOH溶液滴定待测盐酸,若用甲基橙代替酚酞作指示剂,此时盐酸浓度的测定值与酚酞作指示剂的测定值相比较是( )
A. 偏大 B. 偏小 C. 无影响 D. 无法判断
第二篇:酸碱中和滴定实验操作方法--学案
酸碱中和滴定实验操作方法
一.所用仪器:酸式滴定管、碱式滴定管和锥形瓶
(1) 酸式滴定管和碱式滴定管的构造,对比不同点及其原因;
(2) 对比滴定管和量筒刻度的不同。
二.实验操作:
(1)查:检查是否漏水和堵塞。
(2)洗:洗净后用指定的酸和碱液润洗。(锥形瓶只用蒸馏水洗净即可)
(3)盛、调:用烧杯沿漏斗注入滴定管中,放出液体,赶气泡、调起点。
(4)取:将一定体积未知浓度的酸溶液放入锥形瓶中,滴入几滴酚酞。
(5)滴定:操作要点及滴定终点的观察。
左手控制滴定管的活塞或挤压玻璃小球,右手摇动锥形瓶,眼睛注视锥
形瓶内溶液颜色的变化。(指示剂变色,半分钟内不褪色)
(6)记和算:数据的记录和处理求出酸的浓度。计算时可用公式:
c(H+)= c[(OH-)×V(碱)÷V(酸)求。
[原理:c(H+)×V(酸) = c[(OH-)×V(碱)]
三、练习:
用0.1mol/L的氢氧化钠溶液测定某浓度的浓硫酸,其实验步骤如下:
1.配制稀硫酸溶液100mL,操作方法是:在____里盛适量蒸馏水,用____滴定管取1mL浓硫酸,使其缓缓沿烧杯内壁注入盛有适量蒸馏水的____中,并用____搅拌,以达____的目的。将____后的溶液沿____注入____中,用蒸馏水洗涤____和____2~3次,洗液都注入____中,振荡摇匀后,将水注入____,直至液面接近刻度线____处,改用____加水至____。盖好瓶塞,振荡摇匀后,转移至贴有标签的试剂瓶中。
2.滴定:用酸式滴定管取10mL稀硫酸,注入____中,滴入3至5滴酚酞并摇匀后,用0.1mol/L的氢氧化钠溶液滴定,直到加入最后一滴氢氧化钠,刚好使溶液____,即达滴定终点。
3.记录和计算:求:稀释前后硫酸物质的量的浓度。
4.讨论:
①碱式滴定管在盛氢氧化钠溶液前要先用____洗净再用____润洗,盛待测硫酸溶液的容器是____,容器在盛稀硫酸前,要用____洗。
②碱式滴定管未用标准碱溶液洗,只用水洗,立即注入氢氧化钠溶液,将会使测定的稀硫酸浓度____(偏高、偏低、不受影响,下同)。
③滴定前,盛稀硫酸的容器水洗后,用稀硫酸润洗,再盛稀硫酸10mL,再用标准氢氧化钠溶液滴定,将会使测定硫酸溶液的浓度结果____。
④滴定前碱式滴定管内无气泡,后因操作不当进了气泡,测定结果,使稀硫酸的浓度_。
⑤盛稀硫酸的容器内盛10mL稀硫酸后,再加入10mL水后滴定,则测定结果,硫酸溶液浓度将____。
⑥滴定前平视读数,滴定终点时,仰视读数,并记录读数,测得的硫酸溶液浓度将____。
实验报告单
时间: 地点: 同组同学:
一:实验目的:
二:实验用品:
实验仪器:
实验药品:
三:实验原理:
四:实验过程:
五.实验纪录:
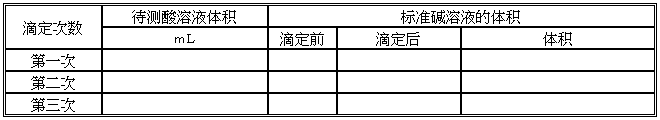
六.实验结果:
七.常见误差分析:[根据:c(H+)×V(酸) = c[(OH-)×V(碱)分析]