实验一 测定未知NaOH溶液的浓度
【实验目的】
用已知浓度的盐酸测定未知浓度的NaOH溶液,从而熟悉酸碱中和滴定实验的操作步骤。
【实验原理】
一元酸与一元碱恰好中和时:C酸 V酸 = C碱 V碱
 =
=
【实验用品】
仪器:酸式滴定管 碱式滴定管 锥形瓶 烧杯 铁架台 滴定管夹
试剂:0.1000mol/L HCl标准液 NaOH待测液 酚酞 蒸馏水
【实验步骤】
1.查漏:检查酸式、碱式滴定管是否漏水。
2.水洗:每次用5-10mL蒸馏水洗涤酸式、碱式滴定管2-3次。
3.润洗:分别用对应酸碱溶液润洗酸式、碱式滴定管2-3次,每次用5-10mL。
4.加液:分别将标准盐酸、待测氢氧化钠溶液注入酸、碱滴定管中;
赶气泡:下面接小烧杯,赶走气泡;
调液面:将液面调至0刻度或0刻度以下;
记录读数:记下初始读数。
5.取待测液:从碱式滴定管中放出20.00mL氢氧化钠溶液于锥形瓶中,滴入2滴酚酞试液,将锥形瓶置于酸式滴定管下方,并在瓶底衬一张白纸。
6.滴定:左手控制玻璃旋塞,右手不断摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化。
7.记录:当滴入最后一滴盐酸,锥形瓶中溶液由红色变为无色,且半分钟内不变色时,停止滴定,准确记下读数。
8.平行实验:重复以上操作4-7步骤2-3次。
【数据处理】

请选用其中合理的数据列式计算:
c(NaOH)=
实验二 测定酸碱滴定曲线
【实验目的】
绘制pH随NaOH溶液加入量变化的曲线,从而体会定量实验在化学研究中的作用。
【实验原理】
利用酸碱混合过程中溶液pH的变化情况,以NaOH溶液滴加量为横坐标,以溶液pH为纵坐标,绘制pH - V(NaOH)曲线。
【实验用品】
仪器:酸式滴定管 碱式滴定管 烧杯 pH计 铁架台 滴定管夹
试剂:0.1000mol/L HCl溶液 0.1000mol/L NaOH溶液 酚酞 蒸馏水
【实验步骤】
1.查漏:检查酸式、碱式滴定管是否漏水。
2.水洗:每次用5-10mL蒸馏水洗涤酸式、碱式滴定管2-3次。
3.润洗:分别用对应酸碱溶液润洗酸式、碱式滴定管2-3次,每次用5-10mL。
4.加液:分别将盐酸、氢氧化钠溶液注入酸、碱滴定管中;
赶气泡:下面接小烧杯,赶走气泡;
调液面:将液面调至0刻度或0刻度以下;
记录读数:记下初始读数。
5.取液:从酸式滴定管中放出20.00mL的盐酸于锥形瓶中,滴加2滴酚酞作指示剂,并在瓶底衬一张白纸。
6.滴定:向锥形瓶中滴加NaOH溶液,边滴加边测定溶液的pH,并将所耗NaOH溶液的体积和溶液的pH记录下表。(开始时时间可以间隔大一些,反应接近终点时,测定和记录pH的间隔要小,每加一滴测一次。)
注意:(1)准确判断酸碱恰好反应时的情况;
(2)准确判断滴定终点时的情况。
7. 记录:将pH记录填入下表:
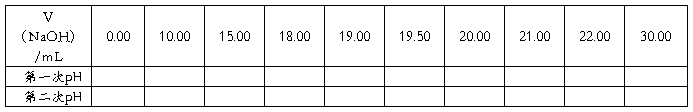
8.平行实验:重复以上操作4-7步骤2次。
【数据处理】
根据所测数据绘制溶液的pH随NaOH溶液加入量变化的曲线:
第二篇:酸碱滴定实验报告
氢氧化钠溶液的标定及盐酸溶液对氢氧化钠溶液的滴定
一.实验目的:
1.培养同学们“通过实验手段用已知测未知”的实验思想。
2.学习相关仪器的使用方法,掌握酸碱滴定的原理及操作步骤.
3.实现学习与实践相结合。
二.实验仪器及药品:
仪器:滴定台一台,25mL酸(碱)滴定管各一支,10mL移液管一支,250mL锥形瓶两个。
药品:0.1mol/L NaOH溶液,0.1mol/L盐酸,0.05mol/L草酸(二水草酸),酚酞试剂,甲基橙试剂。
三.实验原理:中和滴定是酸与碱相互作用生成盐和水的反应,通过实验手段,用已知测未知。即用已知浓度的酸(碱)溶液完全中和未知浓度的碱(酸)溶液,测定出二者的体积,然后根据化学方程式中二者的化学计量数,求出未知溶液的浓度。酸碱滴定通常用盐酸溶液和氢氧化钠溶液做标准溶液,但是,由于浓盐酸易挥发,氢氧化钠易吸收空气中的水和二氧化碳,故不能直接配制成准确浓度的溶液,一般先配制成近似浓度溶液,再用基准物标定。本实验用草酸(二水草酸)作基准物。
(1)氢氧化钠溶液标定:H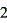 C2O4+2NaOH=Na2C2O4+2H2O
C2O4+2NaOH=Na2C2O4+2H2O
反应达到终点时,溶液呈弱碱性,用酚酞作指示剂。(平行滴定两次)
(2)盐酸溶液标定:HCl+NaOH=NaCl+H2O
反应达到终点时,溶液呈弱酸性,用甲基橙作指示剂。(平行滴定两次)
四.实验内容及步骤:
1.仪器检漏:对酸(碱)滴定管进行检漏
2.仪器洗涤:按要求洗涤滴定管及锥形瓶,并对滴定管进行润洗
3.用移液管向两个锥形瓶中分别加入10.00mL草酸(二水草酸),再分别滴入两滴酚酞.向碱式滴定管中加入药品至零刻线以上,排尽气泡,调整液面至零刻线,记录读数。
4.用氢氧化钠溶液滴定草酸(二水草酸)溶液,沿同一个方向按圆周摇动锥形瓶,待溶液由无色变成粉红色,保持30秒不褪色,即可认为达到终点,记录读数。
5.用移液管分别向清洗过的两个锥形瓶中加入10.00 mL氢氧化钠溶液,再分别滴入两滴甲基橙。向酸式滴定管中加入盐酸溶液至零刻线以上2—3cm,排尽气泡,调整液面至零刻线,记录读数。
6.用盐酸溶液滴定氢氧化钠溶液,待锥形瓶中溶液由黄色变为橙色,并保持30秒不变色,即可认为达到滴定终点,记录读数。
7.清洗并整理实验仪器,清理试验台。
五.数据分析:
1.氢氧化钠溶液浓度的标定:
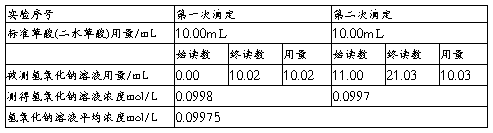
2.盐酸溶液浓度的标定:
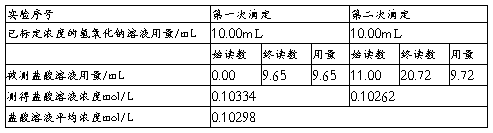
六.实验结果:
①测得氢氧化钠溶液的物质的量浓度为0.100mol/L
②测得盐酸的物质的量浓度为0.1035mol/L
七.误差分析:判断溶液浓度误差的宗旨是待测溶液的浓度与消耗标准液的体积成正比 。
引起误差的可能因素以及结果分析:①视(读数) ②洗(仪器洗涤) ③漏(液体溅漏)
④泡(滴定管尖嘴气泡) ⑤色(指示剂变色控制与选择)
八.注意事项:①滴定管必须用相应待测液润洗2—3次
②锥形瓶不可以用待测液润洗
③滴定管尖端气泡必须排尽
④确保终点已到,滴定管尖嘴处没有液滴
⑤滴定时成滴不成线,待锥形瓶中液体颜色变化较慢时,逐滴加入,加一滴后把溶液摇匀,观察颜色变化。接近终点时,控制液滴悬而不落,用锥形瓶靠下来,再用洗瓶吹洗,摇匀。
⑥读数时,视线必须平视液面凹面最低处。
