中和滴定过程中滴定曲线的测定
班级 姓名

第二篇:中和滴定实验报告单
实验一 测定未知NaOH溶液的浓度
【实验目的】
用已知浓度的盐酸测定未知浓度的NaOH溶液,从而熟悉酸碱中和滴定实验的操作步骤。
【实验原理】
一元酸与一元碱恰好中和时:C酸 V酸 = C碱 V碱
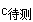 =
=
【实验用品】
仪器:酸式滴定管 碱式滴定管 锥形瓶 烧杯 铁架台 滴定管夹
试剂:0.1000mol/L HCl标准液 NaOH待测液 酚酞 蒸馏水
【实验步骤】
1.查漏:检查酸式、碱式滴定管是否漏水。
2.水洗:每次用5-10mL蒸馏水洗涤酸式、碱式滴定管2-3次。
3.润洗:分别用对应酸碱溶液润洗酸式、碱式滴定管2-3次,每次用5-10mL。
4.加液:分别将标准盐酸、待测氢氧化钠溶液注入酸、碱滴定管中;
赶气泡:下面接小烧杯,赶走气泡;
调液面:将液面调至0刻度或0刻度以下;
记录读数:记下初始读数。
5.取待测液:从碱式滴定管中放出20.00mL氢氧化钠溶液于锥形瓶中,滴入2滴酚酞试液,将锥形瓶置于酸式滴定管下方,并在瓶底衬一张白纸。
6.滴定:左手控制玻璃旋塞,右手不断摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化。
7.记录:当滴入最后一滴盐酸,锥形瓶中溶液由红色变为无色,且半分钟内不变色时,停止滴定,准确记下读数。
8.平行实验:重复以上操作4-7步骤2-3次。
【数据处理】

请选用其中合理的数据列式计算:
c(NaOH)=
实验二 测定酸碱滴定曲线
【实验目的】
绘制pH随NaOH溶液加入量变化的曲线,从而体会定量实验在化学研究中的作用。
【实验原理】
利用酸碱混合过程中溶液pH的变化情况,以NaOH溶液滴加量为横坐标,以溶液pH为纵坐标,绘制pH - V(NaOH)曲线。
【实验用品】
仪器:酸式滴定管 碱式滴定管 烧杯 pH计 铁架台 滴定管夹
试剂:0.1000mol/L HCl溶液 0.1000mol/L NaOH溶液 酚酞 蒸馏水
【实验步骤】
1.查漏:检查酸式、碱式滴定管是否漏水。
2.水洗:每次用5-10mL蒸馏水洗涤酸式、碱式滴定管2-3次。
3.润洗:分别用对应酸碱溶液润洗酸式、碱式滴定管2-3次,每次用5-10mL。
4.加液:分别将盐酸、氢氧化钠溶液注入酸、碱滴定管中;
赶气泡:下面接小烧杯,赶走气泡;
调液面:将液面调至0刻度或0刻度以下;
记录读数:记下初始读数。
5.取液:从酸式滴定管中放出20.00mL的盐酸于锥形瓶中,滴加2滴酚酞作指示剂,并在瓶底衬一张白纸。
6.滴定:向锥形瓶中滴加NaOH溶液,边滴加边测定溶液的pH,并将所耗NaOH溶液的体积和溶液的pH记录下表。(开始时时间可以间隔大一些,反应接近终点时,测定和记录pH的间隔要小,每加一滴测一次。)
注意:(1)准确判断酸碱恰好反应时的情况;
(2)准确判断滴定终点时的情况。
7. 记录:将pH记录填入下表:
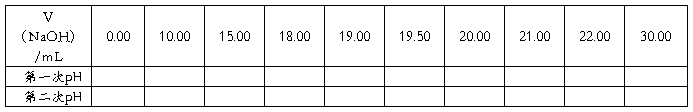
8.平行实验:重复以上操作4-7步骤2次。
【数据处理】
根据所测数据绘制溶液的pH随NaOH溶液加入量变化的曲线:
