九 年 级 化 学 方 程 式 汇 总

化学方程式练习
九 年 级 化 学 方 程 式 汇 总(下)

化学方程式练习(下册)
(6)化合反应: ,(7)分解反应: 。
第二篇:化 学 方 程 式2
化 学 方 程 式
一、选择题
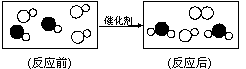
1、右下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的园球代表不同原子。下列说法错误的是 ( )
A.此反应有单质生成
B.原子在化学变化中是不可分的
C.图中生成物全部是化合物
D.参加反应的两种分子的个数比为1∶1
2、下列化学方程式中正确的是( )
A.2Fe+6HCl=2FeCl3+3H2↑ B.2NaOH+K2CO3=2KOH+Na2CO3
C.C+O2

CO D. CO+CuO CO2+Cu
3、 已知某两种物质在光照条件下能发生化学反应,其微观示意图如下:

(说明:一种小球代表一种原子)
则下列说法正确的是
A.图示中的反应物都是单质 B.图示中共有4种分子
C.该反应属于置换反应 D.该图示不符合质量守恒定律
4、 下列各组物质的溶液,不能发生复分解反应的是 ( )
A. HCl和Ca(OH)2 B. H2SO4和Na2CO3
C. AgNO3 和 BaCl2 D. KCl和CuSO4
二、填空题
1、写出下列化学方程式。
(1)木炭和氧化铜在高温下反应 ;
(2)用过氧化氢溶液制氧气 ;
(3)将硝酸银溶液滴入氯化钠溶液 ;
(4)高温煅烧石灰石 。
(5)铁在氧气中燃烧 。
(6)锌粒与稀硫酸反应 。
(7)盐酸和氢氧化钠溶液反应 。
(8)加热高锰酸钾制氧气______________________________________________;
(9)氢氧化亚铁在氧气和水的作用下生成氢氧化铁_________________________。
(10)红磷在空气中燃烧________________________________________
在上述反应中属于化合反应的是 ;属于复分解反应的是 (填序号)。
2、化学和我们的日常生活息息相关,化学科学的发展促进了人类社会文明的进步,提高了人们的生活质量。通过化学学习,我们已经认识了很多化学反应,请你用化学方程式解释下列问题:
(1)不用铁桶盛放波尔多液的原因
(2)用石灰乳粉刷墙壁能形成坚硬的墙面
(3)用盐酸除去铁制品表面的铁锈
3、根据下列要求,写出有关反应的化学方程式
(1)有黑色固体生成的化合反应
(2)检验二氧化碳气体的反应
(3)实验室用一种纯净物制取氧气
(4)用盐酸除去铁锈
(5)一种可再生能源物质的燃烧反应
(6)有单质和化合物参加的化合反应
(7)有酸生成的复分解反应
(8)有铜参加的置换反应
(9)有三种不同类别的物质生成的分解反应
(10)生成相对分子质量最小的氧化物的氧化还原反应
(11)有沉淀生成的中和反应 。
(12)农药波尔多液不能装在铁制容器中 。
4、金属钛及钛的合金被认为是21世纪重要的金属材料,地壳中的钛矿石主要是
金红石(TiO2),TiO2中钛的化合价是________。目前工业上制取钛的方法是:第一
步,在高温时,将金红石、炭粉混合并通入氯气(Cl2)制得TiCl4和一种可燃性气体,
该反应的化学方程式是 ;第二步,在氩气的环境中,用
过量的金属镁在加热条件下与TiCl4反应制得金属钛(氩气不参加反应),该反应的
化学方程式是____________________。
5、做化学实验时,不小心皮肤上沾上了硝酸银溶液,过一段时间会出现黑色痕迹,
很难洗去,这是因为硝酸银见光分解生成一种金属、一种红棕色气体(NO2)和一种
能供给呼吸的气体,请写出此反应的化学方程式___________________;该反应中
氮元素在不同物质中所显化合价_____(填“相同”或“不同”),所显化合价是_____。
6、潮湿的空气中,铜能跟氧气及空气中的另外两种物质生成铜绿[(Cu(]。2OH)2CO3)
出土的青铜制品失去了昔日的光彩,其变化的原因用化学方程式表示为
_____________________________;变色眼镜的玻璃片中含溴化银(AgBr),溴化
银见光分解为银和单质溴(Br2),眼镜片自动变暗。光线弱时,单质溴与银又化
合生成溴化银,眼镜片变亮。试写出避光时的化学方程式:_________________
__________。
7、写出下列反应的化学方程式
(1)鸡蛋进行呼吸作用会通过蛋壳表面的大量微小空隙呼出CO2,为停止鸡蛋的
呼吸作用达到保鲜的目的,常用石灰水作为鸡蛋的保鲜剂,其原理(用化学方程
式表示) 。
(2)近来,科学家通过宇宙探测仪查明金星大气层中含有一种名称为二氧化三碳
的气体,它也能燃烧。请写出二氧化三碳在氧气中燃烧的化学方程式 。
(3)“宝剑淬火”过程中,铁在高温条件下和水蒸气发生了化学反应生成四氧化
三铁和另一气体单质,此反应的化学方程式 。
(4)哥伦比亚号航天飞机的失事,并没有阻止人类探索太空的步伐,我国“神州
五号”飞船计划于今年10月升空。目前,我国运送飞船的火箭所用的燃料是偏二
甲肼(化学式为C2H8N2),火箭发射时该燃料与四氧化二氮剧烈反应,生成二氧化
碳、水和一种常见的气体单质,写出该反应的化学方程式 。
(5)氢气是一种热值高的清洁能源,也是重要的化工原料。
①写出在加热条件下,H2 与二氧化锗(GeO2)反应制备金属锗的化学方程
式 。
②如何大量、廉价地制备氢气是各国正在努力研究的课题。日本科学家最近开发出一种含镍氧化物半导体粉末,将少量这种粉末放入水中,用波长为402nm的可见光照射,能够不断地将水分解成氢气和氧气。在上述过程中,这种氧化物粉末的作用是 ;写出该反应的化学方程式 。
8、二氧化碳在化学家的眼里是可以利用的重要资源,只要有合适的条件,可以像发生光合作用那样将二氧化碳转变为所需要的产物。二氧化碳可以为化工合成提供足够的碳元素,既可以减少化工产业对煤和石油的消耗,又可以缓解大气中二氧化碳含量的增加。
⑴二氧化碳和水通过光合作用转变为葡萄糖和氧气的化学方程式为: 。
⑵化肥厂用二氧化碳与氨气在一定条件下反应生成尿素[CO(NH2)2]和水的化学方
程式为: 。
9、钛(Ti)因为具有许多神奇的性能越来越引起人们的关注,常温下钛不和非金属、强酸反应,红热时,却能与许多常见的非金属反应。钛是航空工业、军工、电工等方面的必需原料。地壳中含钛的矿石之一称金红石(TiO2),目前大规模生
产钛的方法是:
第一步:金红石、炭粉混合物在高温条件下通人氯气制得TiCl4和一种可燃性气
体,该步发生反应的化学方程式是 。 第二步:在氩气的气氛中,用过量的镁在加热的条件下与TiCl4反应制得金属钛。
①此反应的化学方程式 。
②如何从上述所得的产物中获得金属钛?简述主要的实验步骤并写出有关反应的化学方程式 。
10、做化学实验时,不小心皮肤上沾上了硝酸银溶液,过一段时间会出现黑色痕迹,很难洗去,这是因为硝酸银见光分解生成一种金属、一种红棕色气体(NO2)和一种能供给呼吸的气体,请写出此反应的化学方程式_________________;该反应中氮元素在不同物质中所显化合价_____(填“相同”或“不同”),所显化合价是_____。
11、在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应。例如:2H2+Cl22HCl,反应前后H、Cl的化合价发生了变化,该反应是氧化还原
反应。
(1)根据元素化合价发生变化的分析,下列反应属于氧化还原反应的
是 ;
①3Fe+2O4
④H2+CuOFe3O4 ②H2O+CO2=====H2CO3 ③NaOH+HCl=====NaCl+H2O Cu+H2O ⑤2KMnO4K2MnO4+MnO2+O2 ↑ ⑥CaCO3CaO+CO2↑
(2)含有高价态元素的化合物,通常具有氧化性。如:将铜片放入氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身还原成氯化亚铁。该反应的化学方程式为 。
12、 有A、B、C三种物质,已知A是一种氯化物,B是一种钠盐,C是一种碱。通过实验有以下现象:A溶液与B溶液混合无明显现象;A溶液与C溶液混合后产生蓝色沉淀;B溶液与C溶液混合后生成白色沉淀,此沉淀不溶于稀硝酸。请回答:
(1)A的化学式: 。
(2)B与C反应的化学方程式: 。
(3)A溶液与铝丝反应的化学方程式: 。
13、 生产光滑纸张使用的“钡白”有一种制法:① 用盐酸处理碳酸钡;② 向所得溶液加入硫酸。写出“钡白”的主要成分的化学式: ;写出此反应过程的化学方程式:
① ;
② 。
14、 氢氧化钾是我国古代纺织业常用作漂洗的洗涤剂,古人将贝壳(主要成分是碳酸钙)灼烧后的固体(主要成分是氧化钙)与草木灰(主要成分是碳酸钾)在水中相互作用,生成氢氧化钾。请按要求用化学方程式表述上述有关反应。
(1)分解反应 ,
(2)化合反应 ,
(3)复分解反应 。
15、按要求完成以下化学方程式:
(1)放热反应: ;
(2)属于化合反应的一个化学方程式: ;
(3)肼(N2H4)和一氧化氮(NO)燃烧反应产生的能量可以作为火箭发射的动力,
反应后生成两种物质,其中一种是空气中含量最多的气体,另一种是植物光合作用的原料之一。则反应的化学方程式为 。
16、被誉为”江南小三峡”的南京胭脂河是明代初年开凿的一条人工运河。因其“石有胭脂色”而得名。某兴趣小组的同学想知道胭脂河沿岸的那些红色石块的成分。经查阅资料得知该石块中可能含有碳酸钙、氧化铁等物质中的一种或几种,现对其成分进行实验探究,实验记录如下图所示。
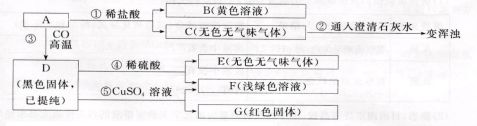
请你根据实验现象写出各步反应的化学方程式:
① A→B ____________________________________________
② ③ ④_____________________________ ⑤
