第 次课 4 学时

实验11 原电池电动势的测定和应用
一、实验目的
1. 掌握对消法测定原电池电动势的原理和方法。
2. 了解电动势测定的应用。
3. 熟悉精密电位差计和标准电池的使用。
二、实验原理
 可设计成原电池的化学反应,发生失去电子进行氧化反应的部分可作为阳极,发生获得电子进行还原反应的部分可作为阴极,两个半点池组成一个原电池。电池的书写习惯是左方为负极,即阳极,右方为正极,即阴极。符号“|”表示两相界面,液相与液相之间一般加上盐桥,以符号“ ”表示,。如电池反应是自发的,则其电动势为正,等于阴极电极电势
可设计成原电池的化学反应,发生失去电子进行氧化反应的部分可作为阳极,发生获得电子进行还原反应的部分可作为阴极,两个半点池组成一个原电池。电池的书写习惯是左方为负极,即阳极,右方为正极,即阴极。符号“|”表示两相界面,液相与液相之间一般加上盐桥,以符号“ ”表示,。如电池反应是自发的,则其电动势为正,等于阴极电极电势 与阳极电极电势
与阳极电极电势 之差,即
之差,即

以铜-锌电池为例。铜-锌电池又称丹尼尔电池(Daniell cell),是一种典型的原电池。此电池可用图示表示如下:


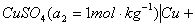
左边为阳极,起氧化反应


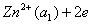
其电极电势为
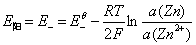
右边为阴极,起还原反应

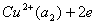

其电极电势
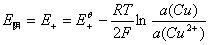
总的电池反应


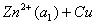
原电池电动势
 =
=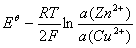

 、
、 分别为锌电极和铜电极的标准还原电极电势,
分别为锌电极和铜电极的标准还原电极电势, 和
和 分别为
分别为  和
和 的离子活度。
的离子活度。
本实验所测定的三个电池为:
 1.原电池
1.原电池 

阳极电极电势 
阴极电极电势 

原电池电动势 
 2.原电池
2.原电池 

阳极电极电势 

阴极电极电势 
原电池电动势 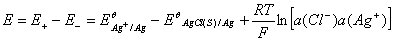
其中 
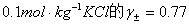
稀水溶液中 浓度可近似取
浓度可近似取 浓度的数值。
浓度的数值。
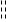 3. 原电池
3. 原电池


阳极电极电势 
阴极电极电势 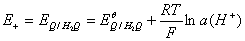

原电池电动势 
= 
即 
由此可知,只要测出原电池3的电动势,就可计算出待测溶液( 缓冲溶液)的pH值。
缓冲溶液)的pH值。
测定可逆原电池的电动势常采用对消法(又称补偿法),其原理和方法在附录1、2、3中作了详细的介绍。通过原电池电动势的测定,还可以得到许多有用的数据,如离子活度等。特别是通过测定不同温度下原电池的电动势,得到原电池电动势的温度系数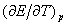 ,由此可求出许多热力学函数,如计算相应电池反应的摩尔反应吉尔斯函数变
,由此可求出许多热力学函数,如计算相应电池反应的摩尔反应吉尔斯函数变 ,摩尔反应焓
,摩尔反应焓
 及摩尔反应熵
及摩尔反应熵  等。
等。
如果电池反应中,反应物和生成物的活度均为1,温度为 ,则所测定的电动势和热力学函数即为相应电池反应的标准
,则所测定的电动势和热力学函数即为相应电池反应的标准 、
、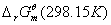 、和
、和 。
。
利用对消法可以很准确的测量出原电池的电动势,因此用电化学方法求出的化学反应的热力学函数 、
、 、
、  等比用量热法或化学平衡常数法求得的热力学数据更为准确可靠。原电池设计与制造的难度主要是电极的制备,所以对一些常用电极的制备方法作一些了解还是很有必要的(详见附录5)。
等比用量热法或化学平衡常数法求得的热力学数据更为准确可靠。原电池设计与制造的难度主要是电极的制备,所以对一些常用电极的制备方法作一些了解还是很有必要的(详见附录5)。
三、仪器和药品


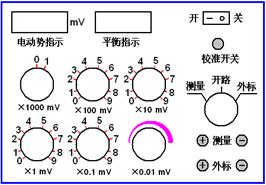
图11.1 ZD-WC数字电位差计; 左图为全图,右图为操作面板
四、实验步骤
1.完成电位差计与检流计、标准电池、工作电池的接线工作,经教师检查无误后,进行工作电流“标准化”操作,并熟悉仪器使用方法。
2.取一广口瓶 ,洗净后,用少许0.01 mol.dm-3 AgNO3溶液连同银电极一起淌洗, 然后装入0.01 mol.dm-3 AgNO3溶液约1/3,插入银电极 ,作为阴极。插在装有飽和氯化钾溶液的广口瓶中的甘汞电极作为阳极,将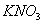 盐桥(1)插入构成二电极的溶液中,组合成一个原电池。接入电位差计(注意+、-),测原电池的电动势。测完后,银电极(阴极)的电池溶液不要倒掉,留作制备下一个电池(2)使用。
盐桥(1)插入构成二电极的溶液中,组合成一个原电池。接入电位差计(注意+、-),测原电池的电动势。测完后,银电极(阴极)的电池溶液不要倒掉,留作制备下一个电池(2)使用。
3.在淌洗过的广口瓶中装入约1/3的0.1 mol.dm-3 KCl溶液,并插入银-氯化银电极,作为阳极。用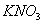 盐桥(2)将银-氯化银电极(阳极)和电池(1)中已制备好的银电极(阴极)组合成一个原电池。测其电动势。
盐桥(2)将银-氯化银电极(阳极)和电池(1)中已制备好的银电极(阴极)组合成一个原电池。测其电动势。
4.取10 ml 0.2 mol.dm-3 HAc溶液及10 ml 0.2 mol.dm-3 NaAc溶液放入淌洗过的广口瓶中,再加入少量的 醌氢醌固体粉末(黑色),而后插入光铂电极,作阴极。架上KNO3盐桥(3),同饱和甘汞电极(阳极)组合成一个原电池。测其电动势。
五、注意事项
1.测定时特别注意标准电池不要摇动、倾斜,以防液体互混使电动势变化。
2.在工作电流“标准化”或测定未知电动势时,要瞬时按下电键而不能长时间按。
3.测原电池的电动势时,注意随时进行工作电流“标准化”的校正。
六、实验记录
室温 22.0 ℃, 大气压 100.20 
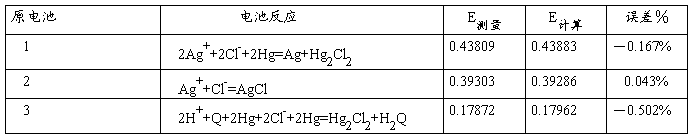
七、数据处理
1. 计算待测电池电动势:
E1=E+-E-= [E+q-RT/F·lna(Ag+)]- E-
=0.799-0.00097´(22-25)+8.314/96485´(22+273.15)´ln(0.9´0.01)-(0.241-0.00076´(22-25))=0.43883 V
误差%=(E测量-E计算)/E计算´100%=(0.43809-0.43883)/0.43883´100%=-0.167%
E2= E+-E-= [E+q-RT/F·lna(Ag+)]- [E-q-RT/F·lna(Cl-)]
=0.799-0.00097´(22-25)+8.314/96485´(22+273.15)´ln(0.9´0.01)-(0.2221-0.000645´(22-25)-8.314/96485´(22+273.15)´ln(0.77´0.1))=0.39286 V
误差%= (0.39303-0.39286)/0.39286´100%= 0.043%
在0.1 M HAc与0.1 M NaAc溶液中,设电离平衡时[H+]=x,则
HAc = H+ + Ac-
电离平衡时 0.1-x x 0.1+x
Kcq=1.74´10-5=x(0.1+x) / (0.1-x),解得 x=1.74´10-5,
所以 pH=-log a(H+)=-log(1.74´10-5)=4.759
E3=EqQ/H2Q+RT/F·lna(H+)- E-
=0.6994-0.00074´(22-25)+8.314/96485´(22+273.15)´ln(0.0000174)-[0.241-0.00076´(22-25)]=0.179622 V
误差%= (0.178720-0.179622) / 0.179622´100%=-0.502%
3 待测溶液pH值:
pH={EqQ/H2Q-0.00074´(t-25)- [E-q-0.00076´(t-25)]}/(2.303RT/F)=4.77
八、思考题
1. 用测电动势的方法求热力学函数有何优越性?
答:电动势测定法比其它方法(例如量热法)更精确,误差更小。
2. KNO3盐桥有何作用,如何选用盐桥以适应各种不同的原电池?
答:将液接电势降低到最小的作用。盐桥中的盐浓度尽量大(一般用饱和溶液),正负离子迁移数接近,与电池中的电解质不发生反应。KNO3的在水中的溶解度很大,正负负离子迁移数接近,与大多数电解质不发生反应。
3. 在工作电流“标准化”和测量电动势过程中,为什么按键不能长时间按下?
答:因为接通电路后就会有电流通过,则电极就会发生极化,电极电势与电池电动势就会偏离平衡值,而实验需要测定的是平衡电动势,所以不能长时间接通电路。
4. 本实验中,甘汞电极如果采用0.1或1.0 mol.dm-3的KCl溶液,对原电池电动势的测量有否影响?为什么?
答:有。根据Nernest方程,电解质浓度对电池电动势有影响。
5. 标准电池有什么用途?
答:工作电流标准化。
6. 参比电池应具备什么样的条件?
答:电动势稳定,在大电流下也不任意极化。
九、对消法原理
 原电池的电动势不能直接用伏特计来测量,因为原电池与伏特计相接后,便成了通路,有电流通过,使电极产生极化,破坏了原电池的电化学可逆状态,使原电池的电动势不能保持稳定,且原电池本身有内阻,所以伏特计所测量得的只是原电池的端电压,而非原电池的电动势。只有在通过原电池的电流无限小时(无液体接界电位),所测得两极的电势差才是该原电池的电动势。
原电池的电动势不能直接用伏特计来测量,因为原电池与伏特计相接后,便成了通路,有电流通过,使电极产生极化,破坏了原电池的电化学可逆状态,使原电池的电动势不能保持稳定,且原电池本身有内阻,所以伏特计所测量得的只是原电池的端电压,而非原电池的电动势。只有在通过原电池的电流无限小时(无液体接界电位),所测得两极的电势差才是该原电池的电动势。
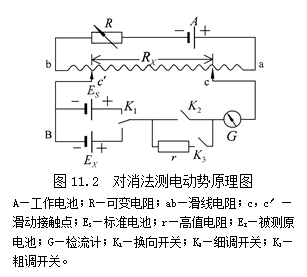
测定可逆原电池电动势常用对消法(又称补偿法)。原理如图11.2所示。
图11.2中ARbaA为工作电路,c′BGcc′为测量电路。在工作电路中以工作电池A供给电流I,通过滑线电阻ab。若将待测原电池之电动势EX(其电动势必须较A的电动势小些)与移动点c、c′间滑线电阻并联,移动c、c′点,直到检流计G的光点不发生偏转,即原电池EX中无电流通过。此时

式中RX为cc′段电阻。
如果事先使电流I调为某定值,则 。在电位差计中,ab由一系列阻值准确的电阻组成,只要滑动点c、c′位置确定,RX的阻值就确定可知,则EX可得知。
。在电位差计中,ab由一系列阻值准确的电阻组成,只要滑动点c、c′位置确定,RX的阻值就确定可知,则EX可得知。
为使工作电流等于给定值,须要利用标准电池ES。标准电池的电动势是已知的。例如某标准电池在实验温度下的电动势为1.01863V,要求工作电流I为0.100000 mA,我们将滑动点c、c′之间的阻值调为10186.3Ω,将换向开关K1扳到ES一边,如果检流计光点不动(示零),则工作电流恰为0.100000 mA。如果检流计光点偏转,则调节可变电阻R,直到光点不偏转。这一步骤称为标定工作电流,即工作电流的“标准化”。
用补偿法原理测电动势所用仪器称为电位差计。电位差计根据其测量范围和精度,有多种型号。
第二篇:原电池电动势的测定
实验报告
课程名称: 大学化学实验(P) 指导老师: 成绩:_______________
实验名称: 原电池电动势的测定及其应用 实验类型: 测量型实验 同组学生姓名: 无
【实验目的】
1. 掌握补偿法测定电池电动势的原理和方法。
2. 掌握电位差计、检流计和标准电池的使用方法。
3. 掌握通过测量原电池电动势计算热力学函数变化值的原理、方法及其他应用。
【实验原理】
1. 补偿法测量电动势原理
采用补偿法测定原电池电动势,其原理为:严格控制电流在接近于零的情况下来决定电池的电动势,其电路图如下:
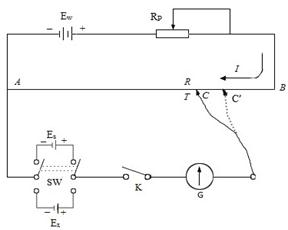
工作电流回路:工作电流由工作电池Ew的正极流出,经可变电阻RP、滑线电阻R返回Ew的负极,构成一个通路,调节RP,使均匀滑线电阻AB上产生一定的电势降。
标准回路:开关SW合向Es,对工作电流进行标定。从标准电池的正极开始,经检流计G,划线电阻上的CA段,回到标准电池的负极。其作用是校准工作电流以标定AB上的电势降。调节Rp使G中的电流为零,CA段上的电势降UCA与标准电势ES相对消。
测量回路:SW合向EX,从从待测电池的正极开始,经检流计G,划线电阻上的C’A段,回到待测电池的负极。其作用是用校正好的划线电阻CA上的电势降来测量未知电池的电动势。在保持标准后的工作电流I不变的情况下,在AB上寻找C’点使得G中电流为零,C’A段上的电势降UC’A与标准电势EX相对消。
2. 电动势与热力学函数的关系
测定某一原电池在不同温度下的电动势E,即可求得电动势的温度系数 ,由E和
,由E和 并结合下列公式计算
并结合下列公式计算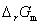 、
、 和
和 。
。
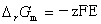

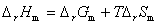
式中:z为反应的电荷数;F为法拉第常量。
【试剂与仪器】
仪器: UJ-25型电位差计1台;检流计1台;惠斯登标准电池1只;3V电源1个;饱和甘汞电极1支;银—氯化银电极1支; 100mL容量瓶5只;50mL酸式滴定管1支;洗瓶1只;废液搪瓷杯1只;恒温槽1套;饱和KCl盐桥和饱和KNO3盐桥。
试剂: 0.200mol·L-1 KCl溶液。
【实验步骤】
本实验测定电动势的电池为:
Hg|Hg2Cl2,KCl(饱和)|| KCl(c)|AgCl|Ag
c=0.0100mol·L-1,0.0300mol·L-1,0.0500mol·L-1,0.0700mol·L-1,0.0900mol·L-1
电动势的的定:
1. 配制溶液:用滴定管和容量瓶,将0.200mol·L-1 KCl溶液分别稀释成0.0100mol·L-1、0.0300mol·L-1、0.0500mol·L-1、0.0700mol·L-1和0.0900mol·L-1各100mL。
2. 根据补偿法原理接好测量线路,恒温槽设定温度为25℃。
3. 校正工作电流。先读取环境温度,根据惠斯登标准电池电动势与温度的关系
Et/V = 1.018625-[39.94(t/℃-20)+0.929(t/℃-20)2 -0.0090 (t/℃-20)3+0.00006 (t/℃-20)4]×10-6
4. 计算出环境温度下的标准电池电动势,调节标准电池的温度补偿旋钮至计算值;将开关拨至“N”处,转动工作电流调节旋钮粗、中、细,依次按下电计旋钮“粗”、“细”,直至检流计指示为零。
5. 测量待测电池电动势。将电位差计换向开关指“X1”或“X2”,从大到小旋转测量旋钮,按下电计按钮,直至检流计指向零点,6个小窗口内读数即为待测电池的电动势。
【数据记录与处理】
1. 25.00℃电池电动势的测定
室温:18.0℃; 大气压:102.00kpa。
(1) 工作电流校正(18.0℃):
Et/V = 1.018625-[39.94(t/℃-20)+0.929(t/℃-20)2 -0.0090 (t/℃-20)3+0.00006 (t/℃-20)4]×10-6
=1.018701
温度补偿旋钮调节值:70
(2) 原电池分析:Hg|Hg2Cl2,KCl(饱和)|| KCl(c)|AgCl|Ag
正极(银电极)的反应为: 2AgCl+2e-→2Ag+2Cl—
负极(甘汞电极)的反应为: 2Hg+2Cl—→Hg2Cl2+2e-
E/V = φ+—φ_=E(Cl—/AgCl)—E/V(甘汞)
甘汞电极电动势E/V(甘汞)= 0.2415V-7.6×10-4 (t/℃-25)
则有:25.00℃时E(Cl—/AgCl)= E/V + 0.2415V
(3) 
本实验中,以氯离子的浓度代替其活度
表1 25℃电池电动势测定结果

2. 以 E(Cl—/AgCl)对lnαCl—作图
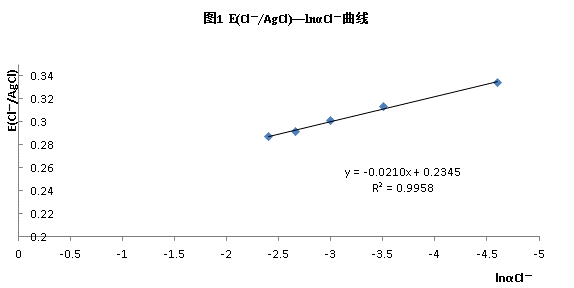
3. 根据图1 E(Cl—/AgCl)—lnαCl—曲线,外推得到
 = 0.2345V
= 0.2345V
 文献值为0.2222V[①]
文献值为0.2222V[①]
实验误差e = |0.2345—0.2222|/ 0.2222 = 5.5%
【分析与讨论】
1. 误差分析
本次试验得到的标准电极电势的误差为5.5%,线性回归的相关程度较高,由于实验条件及实验要求所限,可能产生误差的原因很多,主要原因有
(1) 配置的溶液浓度本身存在误差,且电极与盐桥在移动过程中会使各个溶液的浓度发生变化;
(2) 按电计旋钮按的时间过长,使得电路长时间导通,电极表面极化现象会使平衡状态发生改变;
(3) 甘汞电极由于使用时间较长,电动势会存在一定的误差。
2. 实验中需要注意的一些问题
(1) 测定过程中,选择由稀到浓的电解质溶液进行测量,且盐桥放在饱和溶液的一段不要改变,以减小对溶液浓度的影响。
(2) 为了降低极化现象的影响,测量前先估算待测电动势的大小再进行调节,且注意指针分别向左右偏时是偏大还是偏小,方便调节,同时保护电路。
(3) 测量前要确定盐桥与电极内没有存在气泡,使用前要先清洗。
(4) 测量过程中,检流计受到冲击,应迅速按下短路按钮,保护检流计。
3. 思考题
(1)电位差计用来精确测量待测电动势,并调节工作回路电流、电势降;工作电源为工作回路提供电势降;标准电池用以对消待测电池电动势,使电路中无电流通过,这时测出的两极的电势差就等于该电池的电动势;检流计是检测微弱电量用的指零仪表,确定电路对消的平衡点。测量过程中,检流计受到冲击,应迅速按下短路按钮,保护检流计。使用检流计时,按按钮的时间要短,以防止过多的电量通过标准电池或被测电池,造成严重的极化现象,破坏被测电池的可逆状态。
(2)测定过程中,检流计一直向一边偏转,可能是正负极接错,或者导线有断路,也有可能是工作电源电压不够或者量程不够造成,应进行检查。
(3)在两种溶液之间插入盐桥以代替原来的两种溶液的直接接触,减免和稳定液接电位,使液接电位减至最小以致接近消除。防止试液中的有害离子扩散到参比电极的内盐桥溶液中影响其电极电位。作为盐桥使用的电解质的要求:
①盐桥电解质不能与两端电极溶液发生化学反应;
②盐桥电解质溶液中的正、负离子的迁移速率应该极其接近;
③盐桥电解质溶液的浓度通常很高,甚至达到饱和状态。
(4)可逆电池应满足如下条件:
①电池反应可逆,亦即电池电极反应可逆。
②电池中不允许存在任何不可逆的液接界。
③电池必须在可逆的情况下工作,即充放电过程必须在平衡态下进行,亦即允许通过电池的电流为无限小。
因此在制备可逆电池、测定可逆电池的电动势时应符合上述条件,在精确度不高的测量中,常用正负离子迁移数比较接近的盐类构成“盐桥”来消除液接电位。用电位差计测量电动势也可满足通过电池电流为无限小的条件。
[①]数据来源:CRC Handbook of Chemistry and Physics,87版,20##—20##年。
