建曲炮制工艺验证报告
1. 验证概述
随着生产规模的扩大和增添较先进的设备,原有的生产工艺已不能适应产量的扩大,且手工操作的工艺参数难以控制,因此,我们对工艺过程和工艺条件进行了全面研究,得到了满意的结果。现对修改后的建曲生产工艺进行验证,以确定生产过程的规范性、可控性、稳定性,保证在规定的条件下始终如一地生产出质量稳定的产品,特制定了《建曲炮制工艺验证方案》。
生产工艺包括工艺条件、操作程序和设备使用三个方面,文件执行依据是《建曲工艺规程》、相关设备操作、维护保养SOP、岗位操作SOP、清洁SOP、批生产记录。工艺验证的目的是证明上述文件规定的工艺条件、操作程序、设备、原药材能适应生产实际,能生产出符合质量要求的产品,并有良好的重现性及可靠性。
我们把生产工艺流程划分为8个单元操作,即:混合粉碎、配料、混合、总混、制型、发酵、干燥、包装。每个单元操作作为一个验证小节,每项小节包括概述、执行文件、验证实施项目,验证实施又包括样品采集、检验方法、评估项目及标准。批生产记录作为原始操作记录备查,最后对成品质量进行检验,以判断工艺连续完成后的成品质量。验证方案中只记录重点控制项目、重点数据。在完成连续3批工艺验证后,经过归纳总结,再对建曲工艺规程进行修订。
2. 职责
车间主管:负责验证方案的起草及具体实施。
验证管理员:由QA负责验证工作的组织及协调。
QC检验员:负责验证方案中检验方法的审核及检验操作的准确执行。
生产技术部经理:负责验证方案组织实施。
验证小组质量负责人:负责验证方案的审核。
验证小组组长: 负责验证方案的批准。
3. 建曲饮片生产工艺简介
3.1 规格:
3.1.1 包装规格:50块/包×40包/件
3.1.2批量:
建曲每批3000Kg
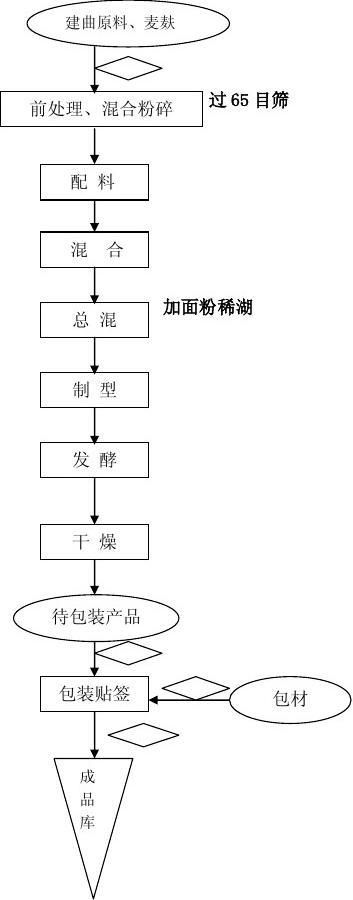
3. 2工艺流程图

物料

工序
检验

入库
4. 验证实施
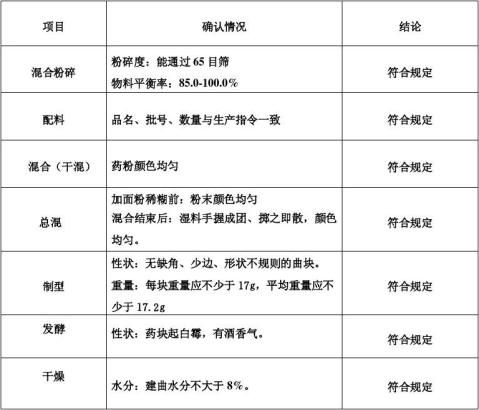
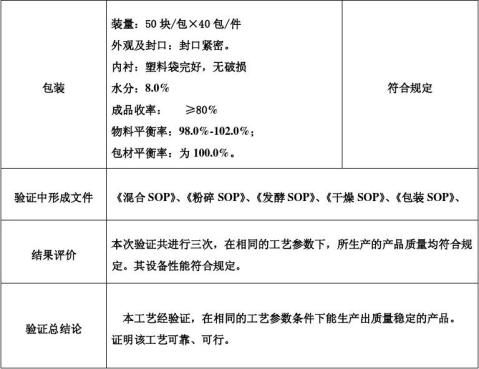
在20xx年5月20日-20xx年6月5日按《建曲炮制工艺验证方案》进行实施:对建曲混合粉碎、配料、混合(干混)、总混、制型、发酵、干燥、包装等工序生产情况进行确认,对产品进行取样、检测。
6. 再验证周期:一年
第二篇:注塑工艺验证报告1
注:
1、 本报告仅为样本,请依据公司的实际情况予以修订;
2、 修订时,请特别注意红色斜体部分;
3、 正式报告发布时请将文中的红色斜体部分删除;
4、 过程确认是一项复杂、耗时的研究工作,目的在于保证生产设备、生产工艺、检验技术
能确保提供稳定的、安全性高的产品,特别适用于一些高风险的工艺,产品性能检测成本高的过程,如灭菌过程、无菌医疗器械的封口过程等;
5、 过程确认本身是一种过程,通常应依据PDCA执行。
6、 过程确认需要判断该过程是否稳定,通常需要使用一些统计技术,如Cpk计算、控制图、
直方图、回归分析、正交表等,请依据公司的实际情况选择。

一、 验证目的:
1. 医疗器械数据传输线生产中,注塑是生产过程中影响产品质量的主要环节之一。注塑
质量影响到产品整体的性能和外观,配合等方面因此,对注塑工艺进行有效的控制并验证,以保证实现在正常的生产条件下,生产出符合标准的医疗器械产品。
2. 本报告的目的在于为评价注塑工艺参数的状况对注塑产品的外观及尺寸的影响,以确
认最佳的注塑工艺参数。
二、 报告验证小组成员:
技术部: 韦 克
品管部: 梁淑梅
模具部: 韦 敏
注塑车间:吴健先
本报告的由技术部编制,由品管部、技术部协同努力设计完成,由工程师审核批准。
三、 验证依据:产品工程图纸(GED-E-M- 11249 )和相关作业参数(SOP)。
四、 验证项目:注塑设备性能,注塑压力、温度、成型周期对产品质量的影响。
设备编号:GTL-AM-066
验证条件设置:
1.注塑区环境条件:
a) 温度:18-28 ℃
b)湿度:50-65%RH
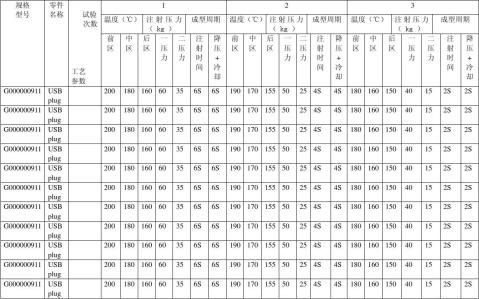
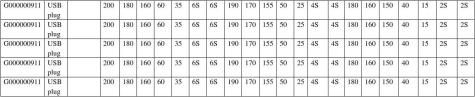
2.注塑工艺参数:
a) 温度
推杆类:前区:180℃――200℃
中区:160℃――180℃
后区:150℃――160℃
模温:55 ℃---65 ℃
b)注射压力:
一压力:50±10kg
二压力:25±10kg
注塑时间: 4±2 Sec
保压+冷却:4±2 Sec
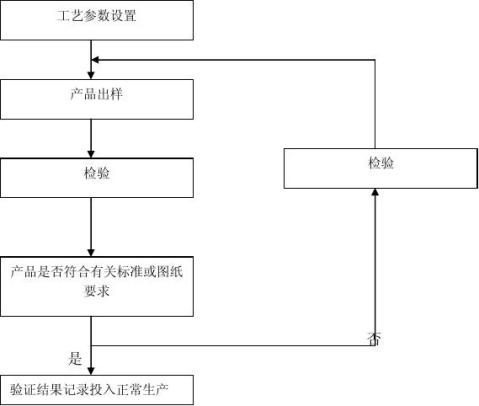
五、 验证方法
OQ:
1、参数设置:设置好各类参数: 温度、时间、压力,使机器预热升温至额定值。
2、出样:空注出模头样,手动闭模,注塑2-3模产品。
3、检验:检验产品外观及尺寸是否符合有关要求及图纸,如果全部合格,则投入正常生产,如果一项或某几项不合格,则需回到第一步,进行参数调整,重新进行验证。 PQ:
4、连续运行:在OQ取得的工艺基础上,连续运行3批,每批至少生产15模产品。 5、工艺记录:运行过程中,读取每模的工艺运行的参数,
6、产品测试:品质部对取得的全部产品按有关图纸或检验规程检验产品外观及尺寸,并做好记录。
六、 结果分析和评价:
1、运用统计技术分析工艺参数和产品性能之间的关系。确定关键工艺。并评价其稳定性。
2、经计算:
关键工艺为:
a) 温度
推杆类:前区:180℃――200℃
中区:160℃――180℃
后区:150℃――160℃
模温: 60 ℃
b)注射压力:
一压力:50±10kg
二压力:25±10kg
注塑时间:4±2 Sec
保压+冷却:4±2 Sec
3、对取得的结果进行数据分析:
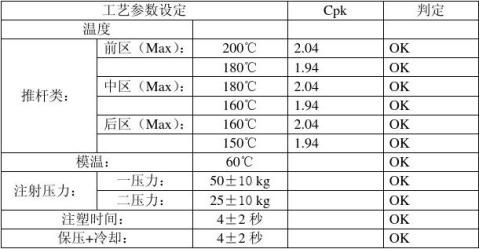
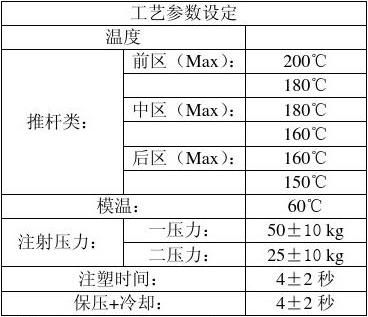

七、 结论:本次验证结果表明以下的工艺满足注塑过程的要求。
八、 最终批准:验证小组审阅上述所有结果及评价分析意见,同意验证结果,并按此结论编
制注塑工艺过程卡。
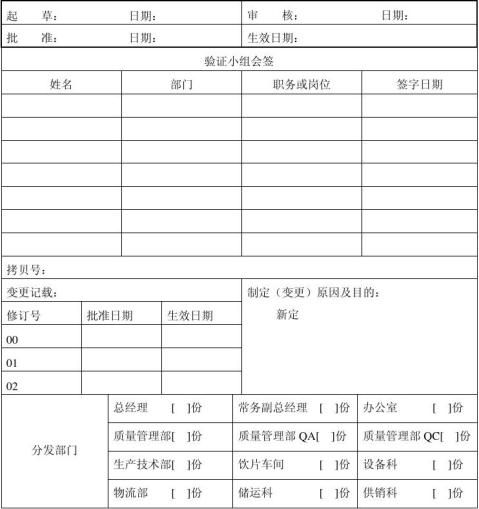
验证报告审核会签表:
九、 工艺验证流程图