环氧乙烷灭菌工艺验证报告
验证目的;对我公司环氧乙烷灭菌器年度审核,现对进行灭菌的有效性及安全性进行验证。 1. 验证安排: 验证组员 组长:XXXX
操作人员:XXXX XXXXX
微生物检验员:送检(XXXXX公司) 1.2验证时间:XXXX-X-XX
1.3验证设备:环氧乙烷灭菌柜(XXXX—XXX) 1.4验证步骤:
环氧乙烷残留确认 微生物性能确认 2操作人员资格
灭菌人员经过了灭菌柜的操作,维护,安全方面的培训,考核通过并取得上岗证,符合要求。
2.1
物理运行确认:
性能物理确认包括真空速率实验、真空(负压)泄漏实验、空载温、湿度均匀性实验和满温、湿度均匀性实验,实验结果如下:
2.2本套设备真空度达到-15kpa的时间为5min;真空速率-3Kpa;灭菌器真空度到达-50kpa的时间为18min;真空速率-2.7Kpa符合说明书中灭菌器真空度到达-50kpa的时间规定的≤30min的真空速率要求。 2.3真空(负压)泄漏实验系在-50kpa条件下,保压60min时间,符合泄漏速率≤0.1kpa/min的要求; 2.4真空(正压)泄漏实验系在+50kpa条件下,保压60min时间,符合泄漏速率≤0.1kpa/min的要求; 2.5温度均匀性;
温度传感器数25个,测试空载温度为50℃检测结果为≤±1.5℃,符合要求空载温度均匀≤±3℃.
3.化学及微生物性能确认
使用的化学指示剂是天津大学生产的。每车三层,每层各贴4片(每个边贴一片) 枯草芽刨杆菌片是北京鑫四环消毒技术开发有限公司生产的,使用菌片数为20枚。(化学指示剂及枯草芽孢杆菌菌片放置操作规程,具体位置见附件) 3.1纯环氧乙烷气体,每瓶20kg,每次灭菌使用13kg;
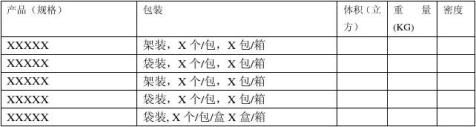
3.2测试产品为 6板,离心管、吸头、微量离心管、乳胶手套
1
XXX产品密度最大,客户对XXX产品灭菌要求也很高,所以密度紧
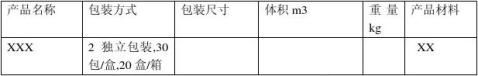
随其后的,XX1,XXX2,XXX3也一并考虑进去.
3.3本次验证将三个半时循环的完整微生物绩效评估,在验证过程中每个菌片将放在10ml的离心管内,产品拧上盖子并用0.05mm厚是塑料热封袋包装。

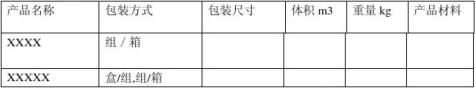

15个温控点温度范围在46.2℃-51.2℃,最大温差5度,符合小于10度的要求.
3.5第2个半周期
2

15个温控点温度范围在44.3℃-50.4℃,最大温差4.9度,符合小于10度的要求.
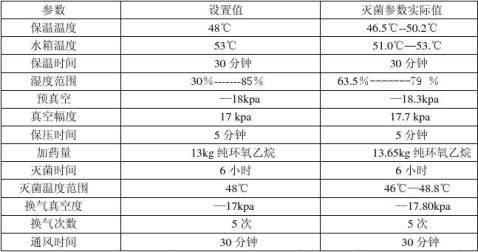
15个温控点温度范围在45.4℃-50.3℃,最大温差4.9度,符合小于10度的要求. 4.1结论:
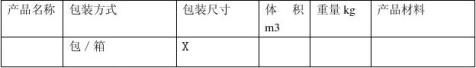
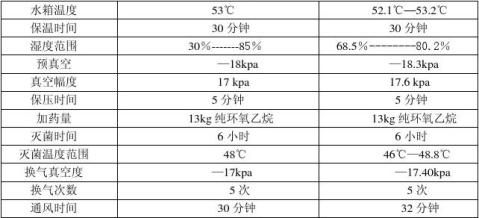
通过本次确认,灭菌过程的温度,湿度,保温,预真空压力,灭菌时间,加药量等参数都在可允许范围,芽孢杆菌片检测全部合格,见附件《芽孢杆菌片检测报告》 4.2本次验证过程符合制定的方案要求;参数确认如下; 表4
3
4

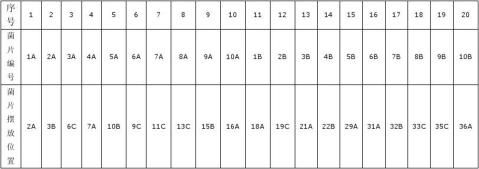
菌片摆放位置
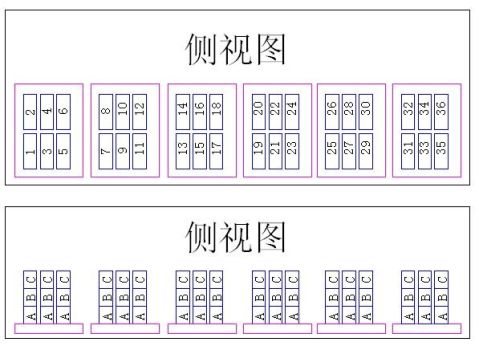
1. 每次放菌片20个
5
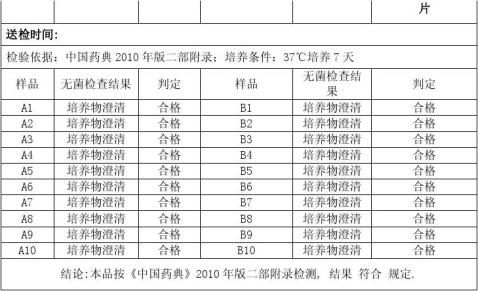
无菌检查报告-检验时间:2012.08.13
受XXXXX公司委托,我部对XXXX公司的三个不同批次样品共60个样品经环氧乙烷灭菌后取菌片进行无菌检测(菌片批号: 120701.120702.120703) 1. 生化培养箱培养箱 型号: XXXX 厂家:XXXXXX有限公司 2. 检验方法:取菌片直接放入肉汤培养基中于37℃培养7天 3. 每天观察记录:逐日观察培养物均澄清 4

6
检测人:XXXX
201X XX.XX
7
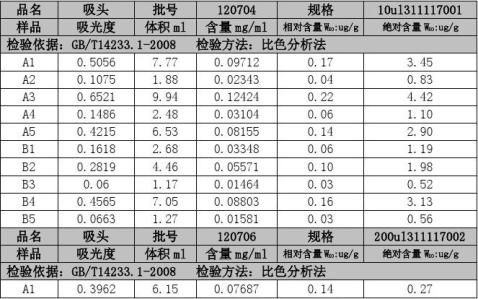
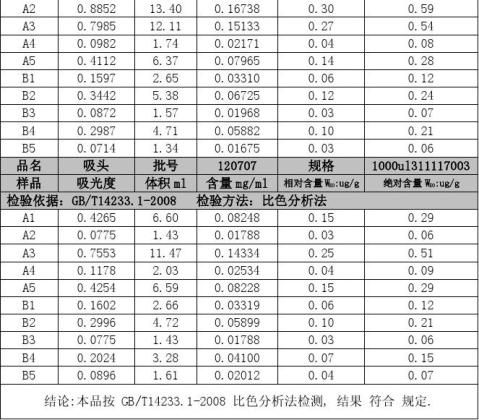
环氧乙烷残留含量测定-检验时间:2012.08.13
受XXXXX公司委托,我部对XXX公司生产的吸头(批号:110704、110706、110707)共30个样品进行环氧乙烷残留检测。
1. 检验设备:紫外分光度计 型号:XXXX 厂家:XXX公司
2. 检验方法:比色分析法测定方法
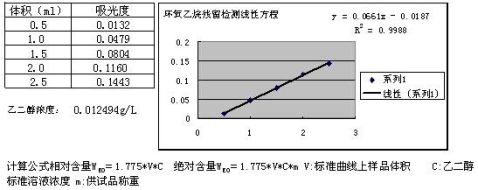
1).取五支纳氏比色管,分别加入0.1mol /L盐酸2ml,再精确加入0.5ml、1.0ml、
1.5ml、2.0ml、2.5ml乙二醇标准溶液。另取一支纳氏比色管,精确加入0.1mol/L盐酸2ml作为空白对照。
2).于上述各管中分别加入0.5%高碘酸溶液0.4ml,放置1小时,再分别滴加硫代硫酸钠溶液至出现的黄色恰好消失(除去剩余的高碘酸)。再分别加入品红-亚硫酸试液0.2ml,用蒸馏水稀释至10ml,室温放置1小时,于560nm波长处以空白液作参比,测定吸光度。绘制吸光度-体积标准曲线。
3).精密移取样品试液2.0ml于纳氏比色管中,按2步骤操作,以测得的吸光度从标准曲线上查得试液相应的体积。
3. 检测单位:
XXXXXXX
8
检测人:XXXX
201X.0X.XX
9
第二篇:验证方案(环氧乙烷灭菌确效)
_________________________________(公司)
确效主计划Validation Master Plan 文件编号VMP-01
生效日期20xx年08月01日

目 录
1、目的 ......................................................................... 2
2、本主计划书适用范围 ........................................................... 2
3、计划推行程序 ................................................................. 2
4、确效作业概述及目标 ........................................................... 2
4.1安装验证 .................................................................... 2
4.3性能验证 .................................................................... 4
4.4灭菌程序确效验证 ............................................................ 5
4.5其它规定事项 ................................................................ 6
5、文件之保存、取用及档案系统 ................................................... 6
6、计划书、标准作业程序及文件之核定 ............................................. 7
1、目的
本主计划书之订定,系根据「环氧乙烷灭菌确效及例行管制指导手册」之内容要旨为蓝本,整体规划本公司于执行环氧乙烷灭菌确效作业的所有相关事宜,作为本公司无菌医疗器材产品在实施环氧乙烷气体灭菌程序的确效及例行管制之要求准则,以期灭菌确效作业能顺利完成,据此确保本公司产制的无菌医疗器材质量及安全性。
2、本主计划书适用范围
2.1本主计划书适用于本公司整体规划环氧乙烷灭菌确效作业之指导原则及基本方法。其中所列载之事项除符合本公司各种标准及规格外,以符合我国医疗器材优良制造规范(卫署药字第八七○四二四七○号暨经(八七)第八七二六一七五七号公告)之规定及环氧乙烷灭菌确效及例行管制指导手册有关规定为准。
2.2本公司环氧乙烷灭菌确效作业推行小组为本主计划之制作、修订、核定及颁行之权责单位。
2.3本主计划所列载之各种事项为本公司对于环氧乙烷灭菌之各种确效等事项之基本原则。
2.4外销用产品之有关环氧乙烷灭菌确效事宜,除依本主计划之规定外,得依外销目的地区之规定处理。
3、计划推行程序
组成环氧乙烷灭菌确效作业推行小组?取得相关信息(法规、技术、设备调查) ?任务分配?教育训练?各类计划书/记录书、确效标准作业程序书之起草与核定?计划实施排程?准备?※计划实施前会商讨论准备是否齐全?实施?报告提出?审核检讨?再确效时间表之决定。
【※确效实施前的准备】
◎【validation schedule】
○validation project之构成与组织
○validation list
○validation 必要之SOP list
○validation protocol之概要
○教育计划之立案
○必要计测计器之决定
○机器校正计划之立案
○设备保全list
○必要人员计划
○validation必备品list及购买
○validation SOP之作成
○protocol与纪录书样式之作成
○计器类校正方法之制定
○灭菌全过程之概要描述
○试验法之制定
以上是确效实施前应具备或完成的事项。
4、确效作业概述及目标
4.1安装验证
确认已获得及保存文件以证明设备已符合其规格所提供的功能并安置妥善,同时若依照操作说明进行操作,可在一预期的限制范围内正常工作。
4.1.1验证范围:
该设备于本次开始确效作业前即已购置,故安装验证之确认以设备之电源配备、设备或系统之鉴别、基本数据复查及其它外围需求为主。
4.1.2设备或系统之鉴别
目的:确定设备或系统之识别标示以便正常运用时之识别。
合格标准:设备或系统上应贴有适当之识别标示。
验证方法:目测识别标示。
4.1.3基本数据复查
目的:确定备有各项书面资料,以利日常运用及必要时之参考依据。
合格标准:本设备应备有之书面数据都备齐。
验证方法:检查核对相关各项书面资料。
4.1.4.设备安装规格之复查
目的:确定安装时所需之共享设施是否适当,以确保设备得到充分之支持。
合格标准:本设备各组件、需用之共享设施皆符合原设计所需,设备于供操作验证前,已完成安装规格之核对。
验证方法:(1) 核查电源配备是否符合设备原设计规定之电压及电流量须求,电压及电流强度各测三次,分别记录之。
(2) 目测比较设备现况与原设计图,观察各机件及配备品是否仍处于正常组合及是否有损坏,如有异常时,应先予调整或修复。
(3) 检查本设备应附之辅助器材,并列出清单。
设备结构之材质及实检结果
目的:确定本设备之基本结构及材质规格之适当性。
合格标准:
(1) 本设备之主要部位之材质皆符合原设计。
(2) 基本结构及主组件适当。
验证方法:
(1) 检查供货商提供之原始文件(附该等数据之影印本)。
(2) 实检核对。
4.2操作验证
确认设施或设备于其操作极限范围与正常范围内能适当运转,验证以预热预湿装置、环氧乙烷气化器、灭菌机本体、调温调湿装置、温度计器、湿度计器、压力计器、计时计器、记录器、预减压装置、安全阀、通气用无菌过滤器、排气装置、气体置换/通气(Aeration)装置及气洗(flushing)装置为对象。
4.2.1供计量之刻度仪器配件之操作验证
目的:确认各主要刻度仪器显示之正确性
方法:检查各主要刻度仪器之背景数据及校正记录
合格标准:各主要刻度仪器之背景数据及校正记录皆显示符合正确性之要求
4.2.2控制器等之操作验证
目标:确定各电源开关、控制器、感应器、定时器、记录器及调节器皆能正常发挥功能。 合格标准:启动各电源开关、控制器、感应器、定时器、记录器及调节器时,能得到应有之响
应。
试验方法及记录:参照另册『预湿预热装置标准操作程序书』(登录No.SOP EO-01)及『环氧乙烷灭菌机标准操作程序书』(登录No.SOP EO-02)并依另订之试验方法逐项实施验证并记录之。
4.3性能验证
确认设施或设备能持续稳定的表现其应有之性能,验证随操作验证之后执行,以模式处方行之。 合格标准:包括物理性性能验证与微生物性能验证各验证要项结果皆能达成预期的要求
验证要项:验证研究旨趣在确认或建立包括下列事项:
4.3.1前置处理与产品的兼容性:
(1) 时间、温度及湿度;
(2) 允许产品进入前置处理的最低温度;
(3) 在前置处理区域的装载型态及产品分离的适当化;
(4) 自前置处理区域移除装载到灭菌周期正式开始之间所允许的最长时间;
(5) 证实在指定的前置处理时间终止时,灭菌装载的温湿度都在前置处理文件规定的范围内;
(6) 监测与记录温度及湿度最难达到规定状态的相关位置;
(7) 前置处理的必要性、可行性与经济性之综合评估。
4.3.2灭菌与产品的兼容性:
(1) 物理性性能验证确能提供证明:
a) 在指定的前置处理时间终止时,灭菌装载的温湿度都在前置处理文件规定的范围内;湿度与加入蒸气后压力增加间的相关性;
c) 在加入灭菌剂到灭菌舱时,灭菌装载的温湿度都在灭菌程序文件规定范围内;灭菌气体确已加入灭菌舱中;
温湿度及其它适用的参数都在灭菌程序规定范围之内;
在整个暴露时间内,维持所有灭菌装载实体状况的规格。
在通气期间,灭菌装载维持在规定温度范围内。
(2) 微生物性性能验证确能提供证明:
a) 依ISO 11138-1由生物指示剂的不活性化证实产品灭菌程序的适合性
b) 生物指示剂确实放置在致死性较低的代表性位置且是在前置处理前置入灭菌装载并在灭菌周期中保持原位
c) 产品包装、装载型态的组合、设备或程序参数确与例行管制相同。
d) 使用的生物指示剂之适用性,确依制订的文件证实无误。
4.3.3通气(含气体置换与气洗)与产品的兼容性:
(1) 时间及温度
(2) 舱室中压力的改变
(3) 气体交换速率
(4) 灭菌装载的温度
(5) 舱室内装载型态的承受性
(6) 不同产品的区隔
(7) 排毒效果
4.3.4验证方法与预期目标概述
按照例行灭菌方式的产品包装、同样的装载型态之组合与数量作为对象,将12支温.湿度Sensor
参照『EOG灭菌确效BI、CI、温.湿度Sensor设置位置图标1』所指定之设置位置妥适固定置放。
依照既定设定条件及『环氧乙烷灭菌机标准操作程序书』(登录No.SOP EO-02)进行操作;从中证实下列事项或取得信息及建立标准:
(1) 物理性性能:
在指定的前置处理时间终止时,灭菌装载的温湿度都在前置处理文件规定的范围内;
b) 湿度与加入蒸气后压力增加间的相关性;
c) 在加入灭菌剂到灭菌舱时,灭菌装载的温湿度都在灭菌程序文件规定范围内;
d) 灭菌气体确已加入灭菌舱中;
e) 温湿度及其它适用的参数都在灭菌程序规定范围之内;
f) 在整个曝露时间内,维持所有灭菌装载实体状况的规格。
(2) 微生物性性能:
a) 依ISO 11138-1由生物指示剂的不活性化证实产品灭菌程序的适合性:生物指示剂确实放置在致死性较低的代表性位置且是在前置处理前置入灭菌装载并在灭菌周期中保持原位;
c) 产品包装、装载型态的组合、设备或程序参数确与例行管制相同;
d) 使用的生物指示剂之适用性,确依制订的文件证实无误。
4.3.5性能验证之起始与终止
起点:自前置处理区域移除装载到灭菌舱内正式开始
终点:完成气洗程序
4.4灭菌程序确效验证
灭菌程序包括预设条件及设定条件、灭菌周期及通气/气洗
4.4.1计划
灭菌程序确效验证之计划由工程责仕者或其代理人拟定。工程责任者或其代理人作成确效之实施计划书后,经各权责单位审议后,发行给各关系部门及相关人员。
4.4.2实施
(1) BI之性能试验、培养、判定由品管部门负责担任
(2) EOG之浓度测定由品管部门负责担任
(3) EOG之残留物由品管部门负责担任
(4) 其它灭菌工程相关事宜由工程责仕者或其代理人负责实施
(5) 必要时工务部门或其它有关单位协同执行
4.4.3试验频度
初期评价须连续成功实施三次。而定期再确效(Revalidation)规定为一年实施一次以上。但是如果踫到layout 变更、产品设计变更、品目变更、数量增加、装载型式或组合变更、设备改造或更新致机能变更等大幅度异动而可能影响灭菌效率之顾虑时,应比照初期评价之基准次数,重新实施确效。
4.4.4方法
灭菌关键重点在于正确掌控影响EOG灭菌效果的5大因素:EOG浓度、温度、湿度、压力、处理时间,本于此认知为前提,以日常灭菌装载之产品为对象,依日常灭菌条件为准则,进行预热预湿装置及灭菌机中舱室内状态之评价,由此取得灭菌确效证明。
4.4.5测定项目
(1) 热分布热渗透(热探测器sensor温度记录)
(2) 灭菌cycle确认(灭菌工程时间之记录)
(3) 灭菌条件之确认(jacket压力、jacket温度、舱内压力、舱内温度、舱内湿度、灭菌装载产品温度及湿度之记录)
(4) 生物指示剂(Biological Indicator)灭菌效果之确认试验
(5) 化学指示剂(Chemical Indicator)灭菌效果之确认试验
(6) 灭菌机机内EOG浓度测定
(7) 灭菌完了品EO残留测定及二次生成物有无确认
4.4.6BI之培养、监测与判定
(1) 培养(Incubation)
依照生物灭菌确效指示剂使用说明(Biological Indicator Instructions for Use)所示,将灭菌后收回的BI携带体,以无菌操作移植于适当之生长培养基(如soybean-casein digest broth)内培养,并以最适宜之生长温度培养至少72小时(通常30~35℃恒温箱内,连续培养7天)。
(2) 监测(Monitoring)
在连续培养的时段中,应每天检查生长培养基内的BI,记录所观察的结果。
(3) 判定(Interpretation)
(3)-1 比对(Control):对照用检品呈混浊或变色,则本试验为有效。
(3)-2 试验(Test):灭菌后试验检体保持原来的颜色没有混浊物或颜色改变的话,判定BI死亡。灭菌后试验检体呈混浊或变色时,依微生物检验法鉴定是否为原来的指标菌(Bacillus Subtilis var. niger),其结果若与BI为同一菌种,则判定BI未死亡。
(4) 判定基准
所有参与灭菌的BI检体,应皆呈现死亡。
有任一BI未死亡者,判定灭菌Cycle失败。
4.4.7. BI之性能试验
依另件『生物指示剂质量鉴定试验法』实施,鉴定出来的Bacillus Subtilis菌数,应与标示值相符。
4.5其它规定事项
4.5.1 采用新的或变更的产品、包装、装载型态、灭菌设备或灭菌参数有异动时,应依本公司「异动事项之管制措施」之规定处理。
4.5.2 各种确效作业应依核定过之计划书及标准操作程序(SOP)执行。任何与既定方法有偏差之事项均应登录于书面记录中并列入文件管理。
4.5.3 各种确效计划书、验证计划书及标准操作程序于拟订或修订后,均应经本公司确效作业推行小组之核定后方可应用及实施。
4.5.4于每一确效作业完成后,应提出书面确效报告。确效报告应经本公司确效作业推行小组之核定后方可归档及应用。
4.5.5有任何变更需作再确效时,均应经本公司确效作业推行小组之核可。
5、文件之保存、取用及档案系统
5.1.本公司各种涉及确效之记录、文件及档案,均依本公司文件及档案管理办法管理。
各记录、文件、及档案均依文件编号办法编号纳管。
5.2各现场用记事本、设备使用及维护记录、设备校正记录等,每年归档一次。
5.3全部档案正本由本公司档案室管理。各档案至少备有一份副本,各副本首页右上角加注「副
本COPY」字样及副本之编号,如「COPY 3-1」代表共三份副本中之第一份。档案原件与副本应分置不同处所,但两者之取用均依照同样方法管制。
5.4. 档案本身如为由若干作业单位之记录及文件组合而成者,则各作业单位应设单位内档案管理员,保管与本单位有关之一份副本。
5.5档案之调阅应循档案管理制度,向各档案管理员登记借出及归还。
5.6. 档案管理员应有代理人。
6、计划书、标准作业程序及文件之核定
6.1. 本公司各种确效文件包括主计划书、各种确效及验证计划书、标准作业程序、确效记录及报告等,均应有编写人或记录人、复核人及核定人之全名签署并签注日期才生效。
6.2. 参与确效作业之所有人员之全名签字及缩写签字式,应存档备查。
6.3. 确定或核定各行动或文件之签名方式如下:
6.3.1确定完成标准作业程序中某一行动时:用缩写式;
6.3.2确定一记录时:用缩写式;
6.3.3于记录中作旁注或说明时:用缩写式;
6.3.4确定计划书、标准作业程序、确效报告之编写时:用全名式;
6.3.5核定时:用全名式。
6.4. 文件之核定
核定时依下列三级处理:
6.4.1.1. 技术面适当性Technically Acceptability
本类核定事宜为有关文件内容是否包括应加处理之关键性指针及必要事项。如未适当包括,则会因缺少证据而无法显示系统之功能及运作是否能符合既定目标。偏差及矫正事项亦应列入评估。
A 品管及品保面适当性QC/QA Acceptability
本类核定主要针对确效之执行是否符合GMP之规定。例如确效作业之执行是否全都符合确效计划书及确效标准作业程序之规定,确效试验结果是否在合格标准范围内,偏差及矫正事项是否有加以记录,结论是否是准确叙述等。
B确效适当性 Validation Acceptability
本类核定旨在评估一确效作业是否符合本公司之确效策略、标准、及程序方法,也兼评估是否符合主管机关之规定。
6.5. 定期评估计划
6.5.1本确效事项既经完成后,均纳入定期评估操作系统。每年作一次年度检讨为原则。经确效过之系统如发生有需要修改系统内容时,均应依据「异动事项之管制措施」之规定办理。
