? 肿瘤是机体在各种致瘤
因素作用下,局部组织
和细胞异常增生而形成
的新生物。
? 常表现为局部肿块。
? 肿瘤细胞具有异常的形态、
代谢和功能,生长旺盛,
常呈持续性生长。
肿瘤生物学特征 机制举例
自主性的生长信号 H-RAS癌基因活化
对抑制生长信号耐受 Rb抑制因子缺失
凋亡逃避 产生IGF生长因子
无限复制 端粒酶开启
持续性血管生成 产生VEGF诱导因子
浸润转移 E-cadherin失活
浸润(直接蔓延)
肿瘤细胞破坏周围组织,并从原发部位连续不断地沿着组织间隙、淋巴管、血管或神经束衣侵入周围组织或器官并继续生长,称为直接蔓延(浸润)。如胃癌从粘膜层浸润至粘膜下层?肌层?浆膜层,晚期子宫颈癌可蔓延到直肠和膀胱。
转移
肿瘤细胞从原发部位侵入淋巴管、血管或体腔,被带到其它部位继续生长,形成与原发瘤同样类型的肿瘤,这个过程称为转移。
淋巴道转移
肿瘤细胞侵入淋巴管后,随淋巴流首先到达
局部淋巴结。局部淋巴结发生转移后,继续转移
到下一站淋巴结,最后可经胸导管进入血流,继
发血道转移。
? 血道转移
瘤细胞多经小静脉入血。血道转移的运行途
径与血栓栓塞过程相同,即侵入体循环静脉的肿
瘤细胞经右心到肺,在肺内形成转移瘤,如肉瘤
的肺转移。
转移的过程和机制
? 癌细胞附着于基底膜
? 细胞外基质降解
?
?
?
?
?
?
?
?
?
?
?
?
?
?
?
癌细胞的移出 癌细胞进入血管 癌细胞与血小板等凝集 癌细胞栓子随血流运行 癌细胞附着于血管壁 癌细胞穿过血管壁 癌细胞继续增殖,建立间质,形成转移瘤。 种植转移 体腔内器官的肿瘤蔓延至器官表面 瘤细胞可以脱落 种植在体腔和体腔内各器官的表面 形成多数的转移瘤 浆膜腔的种植性转移常伴有血性积液 积液内可查找癌细胞 手术也可以造成种植性转移
? 侵入门静脉系统的肿瘤细胞,首先形成肝内转移,
如胃肠道癌的肝转移等。
? 侵入肺静脉的肿瘤细胞或肺内转移瘤通过肺毛细
血管而进入肺静脉的瘤细胞,可经左心随主动脉
血流到达全身各器官,常见转移到脑、骨、肝等
处。因此这些器官的转移瘤常发生在肺已有转移
之后。
? 侵入胸、腰、骨盆静脉的肿瘤细胞,也可以通过
吻合支进入脊椎静脉丛,例如前列腺癌可通过此
途径转移到脊椎,进而转移到脑,这时可不伴有
肺的转移。
? 转移的器官倾向性
“种子和土壤”学说,器官亲合性。
甲状腺?骨
肺癌?脑
乳腺癌?肺、肝、骨 等等。
在某些器官和组织内不易形成转移瘤,如心肌、
横纹肌、脾等。
? 上述的每一个特征都是在肿瘤发生过程中新获得的一种能力,同时都代表了对人体
原有防御肿瘤机制的破坏。
? 肿瘤生物学和肿瘤治疗是细胞生物学、遗传学、组织病理学、生物化学和药理学的
组合,将来将成为一个有机的整体学科。
肿瘤的组织结构
肿瘤的实质 肿瘤的间质
肿瘤细胞的总称 纤维结缔组织
肿瘤组织的主要成份 血管淋巴管
生物学特点以及每种 炎细胞
肿瘤的特殊性 支持和营养肿瘤实质
识别各种肿瘤的组织来源 生长、浸润、转移
肿瘤的分类、命名
组织学诊断
确定肿瘤的良恶性
? 肿瘤细胞的主要特点
细胞的异型性
细胞的多形性 核的多形性 胞浆的改变
组织分化程度 良性肿瘤 恶性肿瘤 分化好,异型性小,与原有组织分化不好,异形性大,与原有
的形态相似。 组织的形态差别大。
无或稀少,不见病理核分裂象 多见,可见病理核分裂象
缓慢 较快 核分裂 生长速度
生长方式 膨胀性和外生性生长,前者常有浸润性和外生性生长,前者无
包膜形成,与周围组织分界清包膜,一般与周围组织分界不
楚,故通常可推动 清楚,通常不能推动,后者每
伴有浸润性生长
组织来源 癌 上皮组织 肉瘤 间叶组织
发病率 较常见,约为肉瘤的9倍,多较少见,多见于青少年
见于40岁以上成人
大体特点 质较硬,灰白色,较干燥 质软、灰红色、湿润、鱼肉状 癌 肉瘤
组织学特点 多形成癌巢,实质与间质分界肉瘤细胞多弥漫分布,实质与间
清楚,纤维组织每有增生 质分界不清,间质内血管丰富,
纤维组织少
癌细胞间多无网状纤维 肉瘤细胞间多有网状纤维 网状纤维
转移 多经淋巴道转移 多经血道转移
? 癌前疾病
临床概念,从统计学上,该疾病患者发生肿
瘤的危险性明显高于正常人。如萎缩性胃炎、
溃疡性结肠炎、乳腺腺病等。
? 癌前病变
病理概念,非典型增生(异型增生)、上皮
内瘤病(CIN),上皮细胞的增生、分化、排列结构异常。根据异型性程度,分为轻、中、重度。有多倍体或非整倍体。
癌前病变的转归:进展,长期不变,逆转。
? 原位癌
非典型增生累及上皮的全层,癌细胞局限于上皮
层内,未侵入间质。
- 宫颈、食管、皮肤的原位癌。
- 乳腺小叶原位癌、导管内癌。
- 原位癌属于最早期的癌,从理论上,应不会扩
散。
活检组织的要求
? 病变越大,越应切取更多的组织,因组织形态变
异,而且可能只有局部区域病变具有诊断意义。
? 在溃疡性肿瘤,溃疡中心的活检组织可能仅显示
坏死和炎症。最有意义的是取溃疡周围包括正常
组织的部位。太靠周围可能只取到正常组织。
? 活检深度要够,这样才能正确分析肿瘤和间质的
关系,有无浸润。
? 位于深部的病变,有时伴有明显的反应性改变,
炎症、充血、纤维化、钙化、骨化生等。如果活
检太靠周围,得到的可能仅仅是反应性改变的组
织。
? 切取的活检组织应全部作病理检查。有时较小的、
肉眼改变不明显的组织,却是唯一会有诊断价值
的组织。
? 取活检时,尽量避免造成组织挤压。
? 活检组织立即放入有足够固定液的容器内,不要
拨动、冲洗、擦拭,造成人工假象。
? 固定液必须是中性缓冲的福尔马林!
? 应考虑到特殊检查的需要,如电子显微镜、细胞
遗传学、分子病理学、流式细胞学等,而及时对
标本作相应的特殊处理。
常用诊断性免疫组化抗体
? 上皮性标志 各种CK、EMA
? 间叶组织标志 Vim、SMA
? 淋巴造血细胞标志 各种CD
? 神经内分泌标志 Syn、CgA、CD56、 Map-2
? 器官特异性标志 TTF-1、PSA、Napsin A、
CDX2
乳腺肿瘤:
终末导管小叶单位(TDLU)
TDLU:小叶间导管-小叶内导管-末梢导管(腺泡), 乳腺组织的基本结构单位
导管及腺泡结构:
EMA,CK7,CK19 ,GCDFP-15, mammoglobin ER,PR(+);AR(-)
肌上皮:
光镜:单层,椭圆形,细胞核长轴与基底膜平行 SMA, calponin, caldesmon, myosin p63
CD10
CK5,14,17
电镜:
基底膜:laminin, IV型胶原 弹力纤维:
非典型性大汗腺化生与大汗腺癌细胞的特点是:
? 明显多形性的核仁
? 胞核上移
病理完全缓解的定义有两种: (1)一般是指乳腺原发灶中找不到恶性肿瘤的组织学证据,或仅存原位癌成份; (2)严格意义上是指乳腺原发灶和转移的区域淋巴结均达到病理完全缓解。
② 病理完全缓解的确定应当由病理医生完成,但临床医生有责任协助病理医生找到原病灶部位,经过多点取材检查后,才能确定。
浸润性导管癌,NOS/NST
(NOS, not otherwise specified)
(NST, no specific type)
? 最常见的乳腺癌,占40-75%
? 诊断标准:NOS>=50%
*10%=<NOS<=49%+某种特殊类型 混合型
* NOS <10% +某种特殊类型 某种特殊类型
? 80%伴DCIS
? 家族性乳腺癌:BRCA1(非典髓)
? 遗传学上有异质性
? 70-80%:ER(+); 15-30%:ERBB2(+)
? 35-50%(10y)
? 最常见的乳腺癌,占40-75%
? 诊断标准:NOS>=50%
*10%=<NOS<=49%+某种特殊类型 混合型
* NOS <10% +某种特殊类型 某种特殊类型
? 80%伴DCIS
? 家族性乳腺癌:BRCA1(非典髓)
? 遗传学上有异质性
? 70-80%:ER(+); 15-30%:ERBB2(+)
? 35-50%(10y)
?
? 多形性癌
? (Pleomorphic ca)
? 本质是高度恶性的NOS,均为3级
? 诊断标准:多形性怪异瘤巨细胞占肿瘤细胞50%以上
? EMA (+) , AE1/AE3 (+), 1/3S-100(+)
? ER(-) , PR(-), bcl2(-), 2/3p53(+)
? 淋巴结转移率高
? 浸润性小叶癌
? (invasive lobular carcinoma, ILC)
? 占5-15%
? 双侧性(13.3%)?; 多中心性?
? 大体上肿瘤范围不易界定
? 组织学特点:细胞松散,粘附力差,单排浸润,靶样结构;
常伴LCIS
? 80-100%ILC: E-cadherin(-)(16q22,截断pr)
? 70-95%:ER(+);HER2表达较低
? 淋巴结转移率:3-10%;易转移到骨、胃肠道、子宫、脑膜、
卵巢及弥漫浆膜
? 预后?
? 组织学特点(经典型):
(1) 肿瘤细胞单个散在或单行排列于纤维结缔组织中
(2) 围绕导管形成同心圆或靶样结构
(3) 肿瘤细胞小,细胞核圆形或卵圆形,常含粘液滴
(4) 90%可见小叶原位癌结构
小管癌
(tubular carcinoma)
? 少见(<2%)
? 肿瘤一般较小(<=1cm)
? 组织学特点:单层上皮构成的空心小管;瘤细胞小而一致,多形性不明显;富细胞
性促纤维增生性间质。>90%
? 常伴原位癌(DCIS,L)、上皮增生性病变
? 几乎100%:ER(+),PR(+),HER-2(-),EGFR(-)
? 16q-,1q+,8p-
? 淋巴结转移率低,长期预后很好(保乳手术
髓样癌
Medullary carcinoma)
? 少见(1-7%)
? 肿物境界清楚,2.0-2.9cm
? 组织学特点:
(1) 合体样生长方式(4-5排细胞),>75%
(2) 无腺管状结构
(3) 弥漫淋巴浆细胞浸润,中-重度
(4) 细胞核中到重度异型性,分裂像多
(5) 低倍镜下肿瘤境界清楚
*原位癌?
? ER(-); ERBB2多(-);
? 高增生指数,黏附分子表达
? 11%:胚系BRCA-1突变;61-87%:p53
? EBV(-)
? 预后较好(淋巴结转移率<10%)
? 鉴别诊断:
、
粘液癌
? 少见(2%)
? 平均年龄63岁
? 组织学特点:
(1)含有大量细胞外上皮性粘液
(2)肿瘤细胞团漂浮于粘液中
(3)常有嗜银细胞
? 预后较好(80-100%,10y)
(细胞成分越少,预后越好)
神经内分泌癌
(neuroendocrine tumors)
? 实性神经内分泌癌
? 非典型性类癌
? 小细胞/燕麦细胞癌
? 大细胞神经内分泌癌
? 2-5%
? 60-70y
? 诊断指标:50%以上瘤细胞表达神经内分泌标记
? 组织学特点:腺泡状或实性片状(*导管内乳头状癌,腺泡状小叶癌); CgA比Syn
敏感;20%TTF-1(+)
? 预后:分级(85%为高中分化)、粘液
? 鉴别诊断:
-转移性神经内分泌癌
浸润性微乳头状癌
(invasive micropapillary carcinoma
? <2%
? 见于3-6%乳腺浸润癌
? 淋巴结转移率高(72-77%)
? 组织学特点:
-肿瘤细胞形成小簇状桑葚样结构,细胞团周围呈锯齿状,中央可有腔
-肿瘤细胞团之间为疏松的纤维胶原性间质形成的网状支架,与细胞团分离 -肿瘤细胞腺腔面和邻近间质面均可见胞浆顶端突起(即呈双极性,“inside out”)
大汗腺癌
(apocrine carcinoma)
? 诊断指标:90%瘤细胞在细胞学和免疫组化上显示大汗腺细胞特点
? ER(-),PR(-),AR(+)
?
? 占乳腺癌0.3-4% 无预后价值
化生性癌
(metaplastic ca)
单纯上皮化生性癌
鳞状细胞癌(CK5,34BetaE12)
腺癌伴梭形细胞化生(CK7)
腺鳞癌
粘液表皮样癌
上皮/间叶混合性化生性癌
富于脂质癌
(lipid-rich carcinoma)
? 90%以上肿瘤细胞胞浆富含中性脂质的乳腺癌(分泌脂质癌)
? 很少见,约占1-6%,不要轻易诊断
? 多不表达ER及PR
? 肿瘤细胞较大,空泡状或透明或泡沫状,缺乏粘液,脂肪染色阳性
? 多认为其属于高级别的乳腺癌
分泌型癌
(secretory carcinoma)
? 又称幼年性乳腺癌
? 占0.15%以下,常见于女性
? 分化较好的腺癌,并有明显细胞外及腺管内乳汁样分泌物
? 生长较缓慢,很少转移
富于糖原的透明细胞癌
? 1-3%
? 组织学特点:90%以上瘤细胞为富于糖原的透明细胞
? 预后较NOS差
? 鉴别诊断:富于脂质癌、大细胞性神经内分泌癌、腺肌上皮瘤、透明细胞汗腺瘤以
及转移性透明细胞癌(肾)
乳头派杰病
? 多伴发于浸润性导管癌或导管原位癌
?
鉴别诊断:
1. 乳腺癌直接浸润表皮
2. 表浅播散型恶黑
乳腺癌病理组织学类型与预后的关系 预后极好:
小管癌 筛状癌 粘液癌 预后好:
混合型小管癌
混合型导管癌(非特殊类型导管癌与其它特殊类型混合) 经典型小叶癌 预后一般:
混合型小叶癌(经典型小叶癌与其它类型小叶癌混合) 髓样癌
非典型性髓样癌 预后差:
非特殊类型导管癌 导管和小叶混合性癌 实性小叶癌
乳腺癌组织学分级(Elston and Ellis分级) 组织学特评 分 小管形成* 占大部分(>75%1
中等量(10-75%2
很少量或无(<10%3
细胞核多形性 细胞核小而一1
细胞核有一定多形2
细胞核多形性明3
分裂相(/10HPF)*
Nikon Labophot Leitz Diaplan
点 ) ) ) 致 性 显
X40 X40
直径为0.44mm 直径为0.63mm
0-5 0-11 1
6-10 12-22 2
>11 >23 3
1级 分化好 3-5分
2级 中等分化 6-7分
3级 分化差 8-9分
? Er /pR 及PS2
?
? 雌激素受体及其下游基因,与乳腺的发生、生长、分化及肿瘤发生相关,
PR与PS2均为ER下游基因,可以反应ER的功能状况
? 常用免疫组化或放射免疫法检测(符合率为85%)
? ER、PR阳性信号在核上,PS2在胞浆,要具体报告阳性细胞百分比
? ER约70%乳腺癌阳性,PR约60-65%阳性
? 用途:
? 预后价值有限,未治疗阳性者的存活率稍高(约高10%)
? 主要用于预测雌激素阻断治疗可否有效,使死亡率降低50%
? Her-2
? 一种原癌基因表达的蛋白,为跨膜酪氨酸激酶受体,属生长因子受体家族,与细胞
增生、细胞分裂、浸润及癌的存活相关。
? 最常用的检测技术是免疫组化,荧光原位杂交技术(FISH)更准确地反应基因扩
张状况。在严格质控下两者符合率高达90%。
? IHC阳性标准:至少10%细胞显示中到强的全细胞膜反应(+++),否则须FISH
验证
? 10-34%浸润性乳腺癌过表达
? 用途:
? 高表达与组织学高级别及浸润进展有关,是重要预后指标
? 是抗肿瘤药(如阿霉素)是否敏感的标记物,阳性者较敏感
? 是靶向治疗(人源化HER-2抗体)的目标物适应证: Her22 /neu基因过表
?
?
?
?
?
达的各期可手术乳腺癌。 ① Her22 /neu基因过表达是指:免疫组化法( IHC)3 + ,或荧光原位杂交法( F ISH)阳性,或者色素原位杂交法(CISH)阳性。 ② Her22 IHC法2 +的患者值得进一步F ISH 或CISH明确是否有基因扩增。
? 细胞进入分裂周期的一种标记蛋白,表达于分裂周期各时相(G0期除外),是细胞
增值活性的重要指标
? 常用免疫组化法检测
? 阳性信号在细胞核,计数500-1000个细胞,得出阳性细胞百分数
? 目前尚无通一的阈值
? 高增生指数提示预后差,但可能辅助治疗有效
?
?
?
?
? 阳性信号在细胞核
? 强阳性预后较差,化疗敏感性低,易复发,转移及死亡率较高
? E-cadherin
? VEGF、CD31、CD34、F8等,检测内皮细胞,计算微血管密度(MVD)
? 血管密度大,血管生成因子过表达者预后较差
? 一种细胞粘附相关的蛋白,阳性者提示细胞粘着力较强,最常用于导管癌和
小叶癌的诊断及鉴别诊断
?
?
?
? SMA(胞浆): SMA除肌上皮外还标记血管及肌纤维母细胞 Calponin(胞浆) P63(核): p63大约10%浸润性癌有表达 SMMHC(平滑肌动蛋白重链,胞浆着染) P53 是重要抑癌基因蛋白,它与细胞周期调节、DNA修复及细胞凋亡有关
? CD10
推荐联合使用数种抗体标记肌上皮,以利于正确判断
GCDFP-15(巨大囊肿性疾病液体蛋白-15)
? 汗腺及乳腺癌的标记抗体
? 乳腺癌分化较低时阴性
? 转移性乳腺癌:约50-75%病例GCDFP-15阳性
? 乳腺癌基因表型分型
?
?
?
?
?
?
?
?
?
? 淋巴瘤: 淋巴组织起源的肿瘤,常表现为淋巴结肿大 目前认为淋巴瘤是特定的细胞在某一分化阶段的克隆性增生 腺腔型(luminal subtype) 正常乳腺样型(normal breast-like subtpe) *Her-2高表达型(Her-2 over-expressing subtype) *基底细胞样型(basal-like breast carcinoma,BLBC)基因表型分类成为继形态学分类后的重要分类方法。 ?
弥漫大B细胞淋巴瘤-病理形态
? 多数病例诊断不难
-大的淋巴样细胞肿瘤
-B细胞标志阳性
? 生长方式
-弥漫 +/- 硬化
-可以成片,酷似癌
? 核分裂像常容易找到
? 背景中有数量不等的小淋巴细胞
免疫组化特点
? 肿瘤性大细胞
CD20+
CD10-
Bcl-6-
MUM1+
TDT-
Ki67+50-75%
?
? 反应性小淋巴细胞
CD3+
? 其它鉴别诊断抗体
CK- (除外癌)
Syn, CD56, CgA-等
(除外神经内分泌肿瘤)
CD99- (除外PNET/Ewing肉瘤)
生发中心性(GCB):
1. CD10+
2. CD10-, Bcl-6+, MUM1-
非生发中心性(non-GCB):
1. CD10-, Bcl-6+, MUM1+
2. CD10-, Bcl6-
滤泡性淋巴瘤
? 分级
1级:0~5个中心母细
胞/HPF
2级:6~15个中心母细
胞/HPF
3级:>15个中心母细胞
/HPF
3a:可见一些中心细胞
3b:中心母细胞呈实性片
状
? 免疫表型
CD19、CD20、CD22、CD79a、CD10、
Bcl-6 阳性
Bcl-2 阳性,与反应性滤泡鉴别,但3级FL和皮肤型FL可能阴性
? 细胞遗传学
t(14;18)(q32;q21) Bcl-2 IGH
70~95%的病例存在Bcl-2基因重排
套细胞淋巴瘤
颈淋巴结活检外院免疫组化:
CD20 +++, PAX5 +++, CD3-, CD10-,
Bcl-6-, Mum少数+, Ki-67+>50%, EBER-
补做免疫组化:
CyclinD-1+++, CD5-
? 免疫表型
表达B细胞标志
CD5、CD43、Bcl-2、Cyclin D1阳性,CD10、
Bcl-6阴性,Cyclin D1表达于70~80%的病例
? 细胞遗传学
t(11;14)(q13;q32) CCND IGH
70~95%的病例存在Bcl-2基因重排
结外粘膜相关淋巴组织边缘带B细胞
淋巴瘤(MALT淋巴瘤)
? 细胞遗传学
近年发现有四种染色体易位
?t(11;18)(q21;q21): API2/ MALT1 ~30%
对清除幽门螺杆菌治疗无效
?t(1;14)(p22;q32): BCL10/ IGH
?t(14;18)(q32;q21): IGH/ MALT1 ~15%
?t(3;14)(p14.1;q32): FOXP1/ IGH
其他染色体异常
Trisomy 3(60%病例),12, 18 染色体三体
l 病理诊断
l (鼻腔)粘膜组织中见有弥漫浸润的中等大小的异型淋巴细胞浸润,免疫组化染色
显示异型细胞:CD56(+++),CD3(少数+) ,Grazyme B (+++) ,TIA-1(+++) ,Ki-67(+>75%),CD20(-),符合NK/T细胞淋巴瘤。
? 临床表现为“中线致死性肉芽肿”
? 好发生于鼻中隔、上颚和面部中线部位, 眼眶,胃肠道,
皮肤和皮下组织以及睾丸
? CD2 +
? 表面 CD3/Leu4 ?; 胞浆 CD3 + (polyclonal CD3; PS1)
? CD56 +, CD16 和 CD57 ?
?
?
?
?
?
?
?
?
?
?
?
?
? 老年患者, 广泛的淋巴结病变 肝脾肿大 皮疹、渗出、发热 多克隆高?球蛋白血症、溶血性贫血 产生不同的症状和体征 临床过程呈侵袭性,治疗后感染并发率高 增生的分支状血管 透明胞浆的非典型T细胞 CD4, CD5, CD7, CD8: ? CD43, CD45RO: + Cytotoxic molecules + Proliferative fraction (Ki67 index): high Occasionally positive for CD25 and CD30
? 散在B免疫母细胞
? 浆细胞增多, 嗜酸性粒细胞浸润
? 大多数病例滤泡萎缩或消失
? 极少数病例滤泡增生
? CD4+、CD10+、BCL-6+ T细胞
? 表达 CXCL 13
?CXCL 13 引起滤泡树突状细胞的诱导和增殖
?CXCL 13 参与B细胞在淋巴结的聚集并激活B细胞
?B细胞在HEV表面的粘附和附着的过程需要CXCL13
? 高内皮微静脉(HEV)周围的广泛CD21+ 的FDC 网 ? 散在B 免疫母细胞,通常EBV+
? 多克隆浆细胞
? > 90% TCR 重排;10-15% IgH 重排
子宫体肿瘤:
? 子宫内膜:腺体、间质和螺旋小动脉。基底层和功能层。 子宫内膜的生理周期:增殖期、分泌期和月经期。 子宫下段和宫颈内口移行部的组织学。
? 平滑肌层
? 外膜(浆膜层)
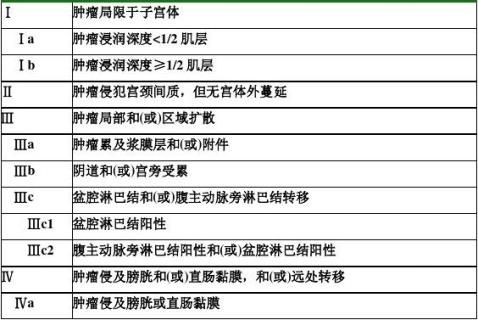

子宫内膜癌
子宫内膜样癌 (1型内膜癌)
粘液性腺癌 鳞状细胞癌
浆液性腺癌 移行细胞癌
透明细胞腺癌 ( 2型内膜癌) 小细胞癌
混合性腺癌 未分化癌
其他
参数 1型 2型
年龄 50-60岁 60-70岁 肥胖 常见 不常见
雌激素刺激 常见 不常见 子宫内膜 不排卵 萎缩
前期病变 EIN 不清 转变 缓慢 迅速 类型 子宫内膜样 浆液乳头状或混合型
分子遗传学 MIS,PTEN突变 P53突变,1p缺失 家族性 HNPCC
扩散 淋巴结 腹膜 同时伴发卵巢病变 常见 不常见
预后 好 差
? 子宫内膜样癌
? 女性生殖系统最常见的肿瘤,以雌激素依赖性为主,肥胖、糖尿病、未经产、高血
压和绝经晚。临床预后较好。
? 雌激素依赖性肿瘤(I型)多为低级别,常伴子宫内膜增生病变,特别为非典型增生。
患者可为无排卵或多囊卵巢综合症的年轻病例,以及绝经期无排卵患者。与PTEN
突变有关。
? 临床表现不规则出血,以绝经后妇女为主
形态特征为由管状或绒毛状腺体组成,腺体被覆单层或假复层柱状上皮,核垂直于基底膜,细胞核轻度增大并有一定极向。
? 组织学:以分化的腺体比例多少分为高-中-低分化(5%、6-50%和50%)。还有伴鳞状
分化、绒毛腺型、分泌型和纤毛细胞型。
? 强调点:
1.当细胞核异型明显时,要考虑II型内膜癌的可能。
2.高分化内膜样癌与内膜非典型增生鉴别:间质消失伴筛状或
绒毛腺体结构。此外间质纤维化和/或肿瘤性坏死,以及间质 的泡沫细
胞浸润。
浆液性(乳头状)腺癌
? 此类型于80年代被认识,属于II型内膜癌,它与雌激素刺激无关,与内膜增生症
无关,常为年龄大的老人,肿瘤进展较快,预后差。
? 发病机制与P53突变相关。
? 组织形态上与分化差的内膜样癌不易鉴别,但二者的鉴别临床上尤其重要。
? 以宽纤维血管轴的2-3级分支乳头为特征,可见脱落的细胞簇。细胞核圆形,无极
向,核位于顶部,核仁和核异型明显,30%沙粒体。当腺样时结构复杂呈“迷宫样”。 ? 它为高级别癌,故不再分级。
? 它与低分化内膜样癌不易鉴别,此时P53突变有意义,免疫染色可帮助鉴别诊断。
子宫内膜腺癌的免疫组化
CK7+, CK20-,
? CA125+(除粘液腺癌外)
? 雌激素依赖性:ER,PR
? P53和PTEN突变。
混合性腺癌由I型(子宫内膜样腺癌,包括了它的各种亚型或粘液腺癌)和II型癌(浆液性或透明细胞性)组成。其中较少的肿瘤成分≥ 10%,肿瘤成分所占比例在报告写出。一般认为II型≥25%时提示肿瘤预后差。
子宫间质结节和低级别间质肉瘤
? 年龄广,以中年妇女(45岁)多见。临床表现为阴道出血,子宫增大。
? 分化好的子宫间质肿瘤由类似增殖期的子宫内膜间质细胞(卵圆形或短梭形)组成,
并且可见特征性多数的螺旋小动脉。通常核异型不明显。
? 免疫染色:CD10+, Vim+, ER+, PR+, desmin-, h-caldesmon-, 伴性索结构:ɑ-inhibin、
CD99、CK和灶状desmin阳性。
?
? 子宫间质结节:
? 为孤立的、界限清楚的圆形结节,切面黄色到深棕色。大小(0.8-15cm)。
? 形态似分化好的子宫间质肉瘤由类似增殖期的子宫内膜间质细胞组成,但无边缘的
浸润。罕见浸润时呈指状突起,但<3mm。局灶可有平滑肌、骨骼肌和性索分化。 ? 为良性病变,预后好。
?
? 未分化子宫内膜肉瘤
? 高度恶性子宫内膜肉瘤,一个或多个息肉样鱼肉样、灰黄色,伴出血和坏死。 ? 形态上:明显的核异型和丰富的核分裂,无间质分化和血管发布,浸润为替代子宫
肌层。
? 预后差,多数3年内死于肿瘤扩散。
子宫平滑肌肿瘤
? 平滑肌瘤为多发圆形质韧肿物,灰白或棕色,编织状,伴出血、囊性变胶原变等。 ? 平滑肌肉瘤为孤立肿物,平均8cm,边界不清和鱼肉状,伴出血和坏死区。
? 平滑肌形态梭形,富于红色胞浆,核纺锤形两端顿圆,束状排列。免疫染色:
SMA+,desmin和h-caldesmon+,CD10-。
? 良性和肉瘤的鉴别以是否伴凝固性肿瘤细胞坏死,细胞核异型程度和核分裂象的多
少多项指标鉴别,但其中凝固性肿瘤细胞坏死最为重要。
平滑肌肉瘤的诊断指标
WHO子宫颈肿瘤分类
上皮性肿瘤
鳞状上皮肿瘤及其癌前病变
腺上皮肿瘤及其相关病变
其它
间叶性肿瘤
上皮间叶混合型肿瘤
黑色素细胞肿瘤
生殖细胞型肿瘤
淋巴造血组织肿瘤
转移瘤
子宫颈解剖
子宫峡部---宫颈---阴道
圆柱体, 长约2.5—3.5cm
子宫颈阴道部
子宫颈阴道上部(子宫颈管)
子宫颈组织结构
从内至外分
1. 粘膜层(上皮——鳞柱交界处)
宫颈阴道部 -- 非角化鳞状上皮
宫颈管内膜 -- 单层粘液柱状上皮
(宫颈腺体)
2. 肌层--平滑肌(10-15%)
致密纤维结缔组织(85-90%)
3. 外膜层--纤维膜
鳞柱交界
原始鳞-柱状交界
生理鳞-柱状交界
雌激素→颈管内膜组织(柱状上皮及腺体)外移;
移行区(转化区)——上皮性肿瘤易发区
原始鳞-柱状交界处和生理鳞-柱状交界处之间
的区域(即宫颈柱状上皮发生鳞化的部位)
阴道酸性环境、致病菌等→鳞状上皮化生
未成熟的化生鳞状上皮
代谢活跃—↓—→宫颈上皮内肿瘤—↓—→鳞状细胞癌
(细胞分化不良、异型性、核分裂增加)
鳞柱交界
原始鳞-柱状交界
生理鳞-柱状交界
雌激素→颈管内膜组织(柱状上皮及腺体)外移;
移行区(转化区)——上皮性肿瘤易发区
原始鳞-柱状交界处和生理鳞-柱状交界处之间
的区域(即宫颈柱状上皮发生鳞化的部位)
阴道酸性环境、致病菌等→鳞状上皮化生
未成熟的化生鳞状上皮
代谢活跃—↓—→宫颈上皮内肿瘤—↓—→鳞状细胞癌
(细胞分化不良、异型性、核分裂增加)
储备细胞——柱状上皮与基底膜之间,具有双向分化潜能→柱状上皮或鳞状上皮(化生)
宫颈鳞状上皮内肿瘤(CIN)
介于正常鳞状上皮与鳞状细胞癌之间的病变,其生物学性质相同、程度不同,发生发展具有连续性。
CIN I ——轻度不典型增生
CIN II ——中度不典型增生
CIN III——重度不典型增生/原位癌
CIN划分标准(WHO)
依据 细胞成熟 异型性(可全层) 核分裂(病理)
CINI 上2/3 轻度异型性 下1/3(罕见)
CINII 上1/2 中度异型性 下2/3(可有)
CINIII 无或浅表层 重度异型性 全层(常见)
/原位癌
低度鳞状上皮内病变(Low-grade squamous
intraepithelial lesion——LSIL)
CIN I和湿疣,低危型HPV(6/11)感染,
大多自然消退
高度鳞状上皮内病变(High-grade squamous
intraepithelial lesion——HSIL)
CIN II和III,高危型HPV(16/18/31/33),
易进展为癌
宫颈鳞状细胞癌
由不同分化程度的鳞状上皮细胞构成的浸润性癌
大体类型 外生型:息肉状、乳头状、结节状
侵润型:溃疡、宫颈弥漫增大桶状
镜下表现
排列成不规则巢团状、条索状,边缘呈浸润性生长
癌细胞具有异型性(细胞大小不等、核/浆↑;核大、深染、
核仁明显、核分裂多见;染色质粗糙) 组织学分型
高分化型 (角化型):角化珠、细胞间桥
中分化型
低分化型(非角化型) :细胞内角化、较多核分裂像
基底细胞样癌
淋巴上皮瘤样癌
疣状癌
湿疣状癌
乳头状鳞状细胞癌
淋巴上皮瘤样癌:
癌细胞界限不清、合体状
细胞核空泡状,核仁明显
间质大量淋巴细胞(T细胞)浸润
预后较好
疣状型——高分化鳞状细胞癌
癌细胞分化良好
胞浆丰富、异型性较小(不像癌的癌)
“侵润”生长
底部上皮脚呈膨胀性(杵状或推进性)生长
表面角化亢进、疣状
不转移、易复发
微小浸润性鳞状细胞癌
定义:
侵润深度<5mm、宽度< 7mm的显微镜下发现的浸润性鳞状细胞癌,无脉管累及 注: 深度<1mm时按原位癌处理
组织学特征
出现弥漫的CIN/和宫颈腺体的广泛受累、膨胀
细胞出现上皮内鳞状细胞成熟现象,边界极不规则
癌巢周纤维组织增生、间质水肿、淋巴细胞反应
宫颈良性鳞状上皮肿瘤
鳞状上皮乳头状瘤
乳头状、乳头单个分离,棘层肥厚
纤维上皮性息肉
息肉状、鳞状上皮+纤维血管间质
尖锐湿疣(炎性)
成簇的细小乳头状、棘层肥厚、挖空细胞
原位腺癌(adenocarcinoma in situ, AIS)
常无症状,筛查发现
细胞学辨认存在困难
好发于鳞柱交界处,常伴CIN,与HPV有关
组织学改变:腺上皮被恶性上皮取代
上皮复层、极向消失、核明显异型、核分裂常见
乳头及筛状结构、正常到肿瘤突然转化
恶性腺体位置正常,轮廓平滑清晰,基底膜完整
80%CEA(+),Ki67高,高危型HPV16/18(+)
原位腺癌(adenocarcinoma in situ, AIS)
常无症状,筛查发现
细胞学辨认存在困难
好发于鳞柱交界处,常伴CIN,与HPV有关
组织学改变:腺上皮被恶性上皮取代
上皮复层、极向消失、核明显异型、核分裂常见
乳头及筛状结构、正常到肿瘤突然转化
恶性腺体位置正常,轮廓平滑清晰,基底膜完整
﹡80%CEA(+),Ki67高,高危型HPV16/18(+)
微小侵润性腺癌
标准 (尚有争议)
侵润深度<5mm(从肿瘤性被覆上皮向下/深部间质浸润深度)
显微镜下发现的浸润性腺癌,无脉管累及
预后良好、不发生(很少)LN转移
处理与鳞状细胞的微小浸润癌相同
Kurian——121例宫颈腺上皮肿瘤:
L-CGIN→H-CGIN→微小浸润性腺癌→腺癌(年龄分别38、43、43、48岁)是一个发展过程
宫颈腺癌
具有腺体分化的侵润癌
占宫颈浸润癌的20-25%
近年发病率↑(相对、绝对)
大多与HPV有关
大体类型 外生型:息肉状、乳头状、结节状
侵润型:宫颈弥漫增大桶状、溃疡
宫颈内膜型腺癌(普通型)
占宫颈腺癌70-80%,5年生存率50-60%
阴道出血,宫颈肿块
大多数与高危型HPV(16、18)感染有关
癌细胞类似宫颈内膜上皮,胞浆嗜酸性/粘液性
宫颈粘液腺癌——宫颈内膜型腺癌
常伴原位腺癌结构
高、中、低分化
微小偏离性腺癌(恶性腺瘤)
罕见,占宫颈腺癌1-2%
阴道排液,宫颈增大变硬
高分化粘液性肿瘤(恶性腺瘤),活检——癌?
细胞形态——癌细胞分化极好,貌似宫颈粘液柱 状上皮,偶见核分裂
组织结构——腺体楞角状、排列杂乱,间质硬化 侵润————癌性腺体超过正常腺体深度、 伴血管及神经周浸润
55%有STK11基因突变,常伴发卵巢肿瘤(转移?) 大多与HPV感染无关,CEA阳性
肠型腺癌:出现肠分化——杯状、潘氏、印戒细胞 诊断前需除外胃肠道转移癌
绒毛管状腺癌:类似结肠绒毛管状腺瘤,核分裂活跃 外生性肿物,阴道出血,与HPV有关
子宫内膜样腺癌:类似子宫内膜腺癌,可伴鳞化 癌细胞不含粘液、排列密集、复层明显
问题:原发部位(宫颈内膜——子宫内膜) 肿物部位、年龄(40/50)、VIM/ER/PR、HPV 透明细胞腺癌:透明或鞋钉状癌细胞
浆液性腺癌:复杂的分支状乳头,伴沙砾体
诊断前需除外转移,尤其老年患者,HPV 中肾管腺癌:源于退化的中肾管
形态复杂,囊状、管状、网状、实性、梭形、性索样
宫颈良性腺上皮肿瘤
宫颈息肉(炎性病变,非肿瘤)
良性宫颈上皮(储留囊肿)+纤维血管间质
细胞无异型性,间质炎症,表面上皮鳞化
米勒上皮乳头状瘤
2-5岁儿童,<2cm,
复杂分支乳头——粘液上皮+纤维血管轴心 细胞无异型性,间质炎症
子宫颈肿瘤(WHO)分类
间叶性肿瘤
术后梭形细胞结节
平滑肌瘤、平滑肌肉瘤
生殖道横纹肌瘤、胚胎性横纹肌肉瘤(葡萄状肉瘤) 低级别子宫内膜样间质肉瘤、未分化肉瘤
腺泡状软组织肉瘤
恶性神经鞘瘤
其它
上皮间叶混合型肿瘤
腺纤维瘤、腺肌瘤
腺肉瘤
癌肉瘤(恶性中胚叶混合瘤)
黑色素细胞肿瘤(恶黑、蓝痣)
生殖细胞肿瘤(卵黄囊瘤、畸胎瘤)
淋巴造血组织肿瘤(淋巴瘤、白血病)
转移瘤(宫内膜、卵巢、阴道、输卵管;乳腺、胃肠道)
卵巢:
? 分期:
? Ⅰ肿瘤位于卵巢:A单侧卵巢内;B双侧卵巢内;C一侧或双侧卵巢,被膜破裂,
腹水+。
? Ⅱ肿瘤位于一侧或双侧伴盆腔内蔓延
? Ⅲ肿瘤位于一侧或双侧伴盆腔外腹膜转移;和/或淋巴结转移
? Ⅳ远处转移包括腹膜转移
浆液性肿瘤
(类似输卵管上皮为特征的卵巢肿瘤)
良性浆液性肿瘤
? 又称:浆液性-囊腺瘤、乳头状囊腺瘤、表面乳头状瘤和腺纤维瘤。
? 占卵巢上皮性肿瘤的16%,发病年龄广,单侧或双侧
? 肉眼:大小1-10CM,单房或多房,透明光滑,小乳头,囊实性
? 组织学:具有纤毛的细胞,单层立方或扁平
浆液性腺癌
? 大小不等,2/3伴双侧,囊实性,乳头糟脆
? 组织学:破坏性浸润性生长,腺管状(裂隙状不规则),乳头状,小的细胞簇,实性,
纤维间质可多或少,可伴有其他上皮成分<10%。
? 沙砾体癌,沙砾体>70%,上皮少轻度异性
? 组织学分级:低级别或高级别,G1,G2,G3
? 免疫染色:CK7,EMA,CAM5.2,panCK,85% CA125阳性;CK20-和间皮细胞标
记阴性。
浆液性交界性肿瘤(背景)
? 定义:卵巢潜在低度恶性浆液性肿瘤,形态界于良性和恶性肿瘤之间,其上皮细胞
的非典型性比良性明显,但无间质浸润。
? 组织学标准:上皮呈复层、从状、筛状和微乳头状,细胞轻度-中度不典型,分离细
胞簇,通常较少核分裂,缺乏破坏性浸润。
? 微乳头型浆液性交界性肿瘤:占5-10%,乳头细长,轴心少5倍宽度,或较少被覆
乳头表面筛网状,>5mm。1/3发生卵巢表面,2/3腹膜种植。
? 伴微浸润的浆液性交界性肿瘤:早期间质浸润以单个细胞或微小细胞巢(细胞无明
显异性),可以单一灶或多个灶,但任何一个<10mm?或≤3mm。
? 腹膜种植:非浸润性种植和浸润性种植,对于II-III期患者预后不同。二者鉴别困难,
广泛取材。
? 淋巴结受累情况:20%伴盆腔和主动脉旁淋巴结受累,无意义。因为可能为真性的
淋巴结转移,可能为淋巴结内的苗勒氏上皮的肿瘤(25-30%)。
黏液性肿瘤
由部分或全部含细胞内黏液的瘤细胞构成,瘤细胞类似宫颈内膜、胃幽门和小肠上皮,有时散在杯状细胞,其他细胞不含黏液。
良性黏液性肿瘤
? 黏液性囊腺瘤和黏液性腺纤维瘤,肿瘤较大,囊性,单侧性单房或多房,粘稠物,
囊实性小囊。
? 单层黏液性柱状上皮,核位于基底,无异性,可有黏液外渗。
黏液性腺癌
? 肿瘤较大,单侧,单房或多房,囊实性,恶性部分有时局限,可疑区域多取材。 ? 组织学:伴明显的间质浸润。当无明显的间质浸润时,腺体复杂呈乳头状、背靠背,
极少间质;明显异性性也被认为浸润, >10mm?或>3mm。多数伴良性、交界性。
黏液性交界性肿瘤
? 卵巢潜在低度恶性粘液性肿瘤,形态界于良性和恶性肿瘤之间,其上皮细胞的非典
型性比良性明显,但无间质浸润。
? 肠型:≥3层,轻度异性,可见核分裂,当上皮恶性实性、筛状称为上皮内癌。 宫颈管上皮型:呈粗乳头状,复层或簇状;当临床为II-III期时(假黏液瘤改变),肠型预后较颈管型差。
? 微浸润型≤3mm, ≤10mm?;
腹膜假黏液瘤为临床术语,指被纤维包饶大量黏液,可有或无上皮的黏液瘤病变。上皮可为良性、交界性和恶性,黏液湖位于表面或浸润性不同。当良性或交界性“播散性腹膜黏液瘤”;恶性“腹膜黏液性癌”,多为阑尾或肠道原发。
? 卵巢黏液性肿瘤,伴腹膜的种植时,多为CK7+,与肠道的CK20+不同,此外仔细
检查阑尾有时原发灶小。
子宫内膜样肿瘤
? 发生于卵巢的良性、交界性(无间质浸润)或恶性肿瘤,瘤细胞与发生在子宫体的
相应类型子宫内膜样肿瘤相似,部分于内膜异位症后。免疫染色:Vim, CK, EMA, CA125, ER, PR阳性,inhibin-。良性罕见,交界性如:腺纤维瘤,判断浸润较难。 ? 同时发生于卵巢和子宫的子宫内膜样癌:
概念同时发生不同的两个部位(苗勒上皮)肿瘤,预后好。与单一肿瘤伴转移的临床分期不同。非整倍体DNA检测支持同时发生的多见,仔细检查子宫和卵巢。
腹膜的苗勒上皮肿瘤
? 原发性腹膜癌,62岁,占5%的卵巢上皮癌。最常见为浆液性癌,其他类型也有报
道。
? 诊断条件:
1 双侧卵巢大小正常或为良性病变增大
2 卵巢外病变比任何一侧卵巢表面病灶大
3 病变未浸润卵巢间质,或卵巢皮质灶 <5X5mm。
Krukenberg瘤定义:为胃肠道的转移性粘液腺癌/印戒细胞癌。
转移癌的特点:双侧、小、浅、多结节;脉管浸润;促纤维增生;广泛卵巢外病变;临床病史。
? 食管胃交界(Oesophagastric Junction, OG)是食管进入胃的解剖学区域。鳞柱交
界在其上方,胃贲门为胃临近食管的区域,起始于胃食管交界处,其远端很难明确界定。
早期胃癌:定义:癌组织浸润不超过粘膜下层,不管肿瘤大小或是否有淋巴结转移 ? 大体形态:
? I型——隆起型
病变明显高于周围正常粘膜,隆起高度超过 正常粘膜厚度的2倍以上。少见,约占4%。
? II型——表浅型
病变无明显隆起或凹陷,较平坦。进一步分为三个亚型:IIa,IIb,IIc
IIa —表浅隆起型
呈平盘状,稍高于周围正常粘膜,不超过正常粘膜高度的2倍,约占7.3%
IIb—表浅平坦型
无肉眼可见的隆起或凹陷,病变可稍显粗糙或色泽异常,易漏诊,约占10%
IIc—表浅凹陷型
病变呈边缘不规则的浅凹陷,深度不超过粘膜层,最常见,约占39.5%
? III型——凹陷型
病变呈明显凹陷,形成达粘膜下层的溃疡,约占23%
? 复合型,如III+IIc,IIa+IIc等。
进展期胃癌:
? Borrmann分型
? I型 息肉型,向胃腔内生长,呈息肉状,浸润不明显,界限较清楚,转移发生较晚 ? II型 溃疡限局型,溃疡明显,向周围浸润不明显
? III型 溃疡浸润型,有明显溃疡形成,浸润明显,界限不清楚
? IV型 弥漫浸润型,无明显溃疡或隆起,弥漫浸润生长,胃壁增厚僵硬,皱襞消失
不规整,富于纤维间质
? 特殊类型
浅表扩散型,浸润较浅,范围较大;Borrmann O型;不能归入以上类型者,称Borrmann II型。
?
胃癌的组织病理分型
? WHO分型
管状腺癌 高、中、低分化
乳头状腺癌
粘液腺癌
印戒细胞癌
? 少见的亚型
腺鳞癌
鳞状细胞癌
未分化癌
肝样腺癌
小细胞癌
绒毛膜癌等
? Lauren分型
? 肠型胃癌
形成腺样结构,高-中分化,也可有低分化成分
? 弥漫性胃癌
癌细胞粘着性差,弥漫浸润,有少量腺体或无腺体形成
? 混合型
? 不确定型
? 癌前病变
? 慢性萎缩性胃炎和肠上皮化生
? 上皮内肿瘤(不典型增生)(Intraepithelial neoplasm,Dysplasia):低级别,高级别.
可发生自胃上皮细胞或肠化生细胞,约80%的上皮内肿瘤可进展为浸润性胃癌。
预后因素
? TNM分期
进展期胃癌常可见脉管癌栓,这是预后差的一个重要原因
? 淋巴结转移数与5年生存率显著相关
? 1-6个(PN1) 5年生存率 44%
? 7-15个(PN2) 30%
? >15个(PN3) 11%
浸润深度
? 粘膜及粘膜下层 95%
? 肌 层 60-80%
? 浆 膜 层 50%
? 侵犯十二指肠
? 浸润并跨越出门环 8%
? 浸至出门环 22%
? 无明显十二指肠浸润 58%
组织病理学分型与预后的相关性有争议
与HP感染关系:
? 实际上,在HP感染的人群中,只有1%左右会增加胃癌的发病风险,80-90%的感染
者并没有明显的临床症状,也不会发生严重的胃肠疾病。HP感染的临床表现有三种类型
单纯型或轻度胃炎型
1. 最常见的类型,约占感染人群的80-90%,表现为轻度的广泛性胃炎,轻度胃酸降低,没有临床症状或轻微,不会发生严重的胃肠疾病。HP感染与胃癌的类型(肠型、弥漫型)无关,而与胃癌的部位有关(与近端胃癌无关,而与远端胃癌有关)。
? 是胃肠道最常见的间叶性肿瘤。
? 定义:GIST是一类特殊的、通常为CD117阳性的胃肠道最常见的间叶组织发生的
肿瘤。 CD117是c-kit基因的蛋白产物。该肿瘤的发生是由c-kit基因突变或血小板生长因子受体(PDGFRA)基因突变驱动。过去诊断的胃肠道平滑肌肿瘤和神经源性肿瘤大部分为GIST。
? 部位:胃最常见(60-70%),其次是小肠(20-30%),结直肠和食管(总共<10%)。
在肠系膜和网膜等部位也可发生。
? 组织来源:可能起源于多分化潜能的前驱细胞。
? 组织形态:梭形细胞型(70%),上皮样细胞型(20%),梭形细胞/上皮样细胞混合
型(10%)
? 免疫组化:CD117(+)(95%),CD34 (+)(70%),局灶性SMA (+)(40%),
S-100 (+)(95%)。
? 对于组织形态符合典型GIST、CD117阴性的肿瘤,必须经检测证实存在c-kit或
PDGFRA基因突变,才能诊断为GIST。
? 粘膜相关淋巴瘤 (mucosa associated lymphoid tissue, MALT),细胞的形态及免疫表型
属于边缘带B细胞淋巴瘤。
? 低变恶性
? 与HP感染显著相关
? 部分病例清除HP,肿瘤可消退
? 部分病例可转化为高度恶性的弥漫大B细胞淋巴瘤
? 其他类型:弥漫大B细胞型,套细胞淋巴瘤,T细胞淋巴瘤等。
标准平滑肌分化 上皮样分化 粘液样分化
组织学 雪茄形梭形细胞束,细胞具有 圆形细胞具有中位细胞核及 梭形细胞位于丰富的 稀少到丰富的嗜酸性胞浆 透明到嗜酸性的胞浆 粘液样基质中
凝固性肿瘤细胞坏死 凝固性肿瘤细胞坏死 凝固性肿瘤细胞坏死
无坏死时,弥漫的中度以上 无坏死时,弥漫、中度 无坏死时,弥漫、中 滑肌肉 的细胞不典型和核分裂象 以上的细胞不典型和核 度以上的细胞不典型 瘤的 ≥10/10HPF 分裂象≥5/10HPF 和核分裂象≥5/10HPF
标准 当分裂象<10/10HPF时
“不典型平滑肌瘤具有低度
复发风险”
注释 A 无凝固性肿瘤细胞坏死和明显 局部上皮样分化可类似 结节周围的水肿变性 的不典型核和高的核分裂,此 标准平滑肌束的横切面 不包括在内
为良性
B 当核分裂>15/10HPF时“分裂相活跃的平滑肌瘤,经验有限”
C 当核不典型中度-重度时“非典型
平滑肌瘤,经验有限”
标准平滑肌分化 上皮样分化 粘液样分化
组织学 雪茄形梭形细胞束,细胞具有 圆形细胞具有中位细胞核及 梭形细胞位于丰富的 稀少到丰富的嗜酸性胞浆 透明到嗜酸性的胞浆 粘液样基质中
凝固性肿瘤细胞坏死 凝固性肿瘤细胞坏死 凝固性肿瘤细胞坏死
无坏死时,弥漫的中度以上 无坏死时,弥漫、中度 无坏死时,弥漫、中 滑肌肉 的细胞不典型和核分裂象 以上的细胞不典型和核 度以上的细胞不典型 瘤的 ≥10/10HPF 分裂象≥5/10HPF 和核分裂象≥5/10HPF
标准 当分裂象<10/10HPF时
“不典型平滑肌瘤具有低度
复发风险”
注释 A 无凝固性肿瘤细胞坏死和明显 局部上皮样分化可类似 结节周围的水肿变性 的不典型核和高的核分裂,此 标准平滑肌束的横切面 不包括在内
为良性
B 当核分裂>15/10HPF时“分裂相活跃的平滑肌瘤,经验有限”
C 当核不典型中度-重度时“非典型
平滑肌瘤,经验有限”
