第一学期化学方程式汇总
 1
、镁带在空气里燃烧
1
、镁带在空气里燃烧
 Mg + O2 现象:发出耀眼的白光,留下白色粉末
Mg + O2 现象:发出耀眼的白光,留下白色粉末
2 碳在空气中完全燃烧

 C + O
2
现象:在氧气里燃烧发出白光
C + O
2
现象:在氧气里燃烧发出白光
 3
碳在空气中不完全燃烧
3
碳在空气中不完全燃烧
2C + O2—→
 4
硫在空气(或氧气)里燃烧
4
硫在空气(或氧气)里燃烧
 S + O2 现象: 在空气里燃烧发出淡蓝色火焰
S + O2 现象: 在空气里燃烧发出淡蓝色火焰
在氧气里燃烧发出明亮的蓝紫色火焰
 5
铁丝在氧气里燃烧
5
铁丝在氧气里燃烧
 Fe + O2 现象:剧烈燃烧,火星四射。
Fe + O2 现象:剧烈燃烧,火星四射。
 6
氢气在空气(或氧气)里燃烧
6
氢气在空气(或氧气)里燃烧
 H2 + O2 现象:发出淡蓝色火焰
H2 + O2 现象:发出淡蓝色火焰
 7
磷在空气(或氧气)里燃烧
7
磷在空气(或氧气)里燃烧
 P + O2 现象:产生大量的白烟
P + O2 现象:产生大量的白烟
 8
一氧化碳在空气中燃烧
8
一氧化碳在空气中燃烧
CO + O2—→ 现象:产生蓝色火焰
 9
甲烷在空气中燃烧
9
甲烷在空气中燃烧
CH4 + 2O2—→ 现象:产生蓝色火焰
 10
水通电分解
10
水通电分解
 H2O
H2O
现象:两极有气泡产生,(正氧负氢,氢气氧气体积比2:1,质量比1:8)
11 氧化钙和水反应
 CaO + H2O 现象:使紫色石蕊变蓝色,使无色酚酞变红色
CaO + H2O 现象:使紫色石蕊变蓝色,使无色酚酞变红色
12 白色的无水硫酸铜中加入水
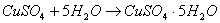 现象:白色变蓝色
现象:白色变蓝色
13 二氧化碳和水反应(二氧化碳通入紫色石蕊试液)
 H2O + CO2 H2CO3 现象:使紫色石蕊试液变红色
H2O + CO2 H2CO3 现象:使紫色石蕊试液变红色
 碳酸受热分解 H2CO3 H2O + CO2 ↑ 红色变紫色
碳酸受热分解 H2CO3 H2O + CO2 ↑ 红色变紫色
14 二氧化碳通入澄清石灰水中
 Ca(OH)2 + CO2 现象:石灰水变浑浊 ,产生白色沉淀
Ca(OH)2 + CO2 现象:石灰水变浑浊 ,产生白色沉淀
继续通入二氧化碳, 现象:沉淀消失
现象:沉淀消失
15木炭还原氧化铜
 C + 2CuO—→ 现象:黑色粉末变红色,澄清石灰水变浑浊
C + 2CuO—→ 现象:黑色粉末变红色,澄清石灰水变浑浊
 1
6
灼热的碳与二氧化碳反应
1
6
灼热的碳与二氧化碳反应
CO2 + C —→
 17
一氧化碳还原氧化铜
17
一氧化碳还原氧化铜
CuO + CO—→ 现象:黑色固体变红色,澄清石灰水变浑浊
 18
氢气还原氧化铜
18
氢气还原氧化铜
 H
2 + CuO—→ 现象:黑色固体变红色,试管口有水滴产生
H
2 + CuO—→ 现象:黑色固体变红色,试管口有水滴产生
 19
一氧化碳还原氧化铁(
工业炼铁
)
19
一氧化碳还原氧化铁(
工业炼铁
)
Fe2O3 + CO —→
20 加热氯酸钾和二氧化锰的混合物制氧气


 KClO
3 , 二氧化锰作催化剂
KClO
3 , 二氧化锰作催化剂
21 用过氧化氢溶液(双氧水)和二氧化锰制氧气


 H
2O
2 ,二氧化锰作催化剂
H
2O
2 ,二氧化锰作催化剂
22碳酸钙与稀盐酸反应(实验室制二氧化碳)
CaCO3 + HCl—→
 2
3
碳酸钙高温分解(高温煅烧石灰石)
2
3
碳酸钙高温分解(高温煅烧石灰石)
CaCO3—→ 用途:工业上制取生石灰
24 氢氧化钠溶液和硫酸铜溶液混合
 NaOH + CuSO4 现象:产生蓝色沉淀
NaOH + CuSO4 现象:产生蓝色沉淀
25 镁在二氧化碳中燃烧
镁燃烧不能用二氧化碳灭火器灭火,改用干粉灭火器
铁和盐酸反应
铝和盐酸反应
用盐酸除铁锈
用氢氧化铝治疗胃酸(含盐酸)过多
氢氧化铁溶于稀盐酸
碳酸钠和盐酸反应
硝酸银和盐酸反应
锌和硫酸反应
硫酸除铁锈
用氢氧化钠中和硫酸
氢氧化铜溶于硫酸
硫酸和氯化钡反应
硫酸和硝酸钡反应
硫酸和氢氧化钡反应
氢氧化钠在空气中变质
用氢氧化钠溶液吸收二氧化硫
氢氧化钠和氯化铁反应
氢氧化钙和硫酸铜溶液混合制波尔多液
石灰水和纯碱溶液反应
氯化钠溶液和硝酸银溶液反应
硫酸钠溶液和氯化钡溶液反应
氢氧化钠和稀硝酸反应
碳酸钡溶于稀硝酸
碳酸氢铵受热分解产生氨气
氯化铵不能和熟石灰一起使用
(1)金属单质 + 酸 -------- 盐 + 氢气 (置换反应)
33、镁和稀盐酸反应:Mg + 2HCl→ 有大量气泡产生 金属颗粒逐渐溶解
34、铝和稀盐酸反应: Al + HCl → 有大量气泡产生 金属颗粒逐渐溶解
35、锌和稀盐酸反应:Zn + HCl → 有大量气泡产生 锌粒逐渐溶解 实验室制备氢气
36、铁和稀盐酸反应:Fe + HCl→ 有大量气泡产生 金属颗粒逐渐溶解
37、 镁和稀硫酸:Mg + H2SO4 → 有大量气泡产生 金属颗粒逐渐溶解
38.、铝和稀硫酸: Al + H2SO4 → 有大量气泡产生 金属颗粒逐渐溶解
39、 锌和稀硫酸反应:Zn + H2SO4 → 有大量气泡产生 锌粒逐渐溶解 实验室制备氢气
40、 铁和稀硫酸:Fe + H2SO4 → 有大量气泡产生 金属颗粒逐渐溶解
(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐
41、铁和硫酸铜溶液反应:Fe + CuSO4 → 银白色金属表面覆盖一层红色物质 湿法炼铜 镀铜
42、铜和硝酸银溶液反应:Cu + 2AgNO3 → 红色金属表面覆盖一层银白色物质 镀银
43、锌和硫酸铜溶液反应:Zn + CuSO4 → 青白色金属表面覆盖一层红色物质 镀铜
45、盐酸和烧碱起反应:HCl + NaOH →
46、盐酸和氢氧化钾反应:HCl + KOH →
47、盐酸和氢氧化铜反应: HCl + Cu(OH)2 → 蓝色固体溶解
48、盐酸和氢氧化钙反应: HCl + Ca(OH)2 →
49、盐酸和氢氧化铁反应: HCl + Fe(OH)3 → 红褐色固体溶解 溶液呈黄色
50、氢氧化铝药物治疗胃酸过多: HCl + Al(OH)3 →
51、盐酸与氢氧化镁反应:Mg(OH)2 + HCl → 白色固体溶解
52、硫酸和烧碱反应:H2SO4 + NaOH →
53、硫酸和氢氧化钾反应:H2SO4 + KOH →
54、硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 → 蓝色固体溶解
55、硫酸和氢氧化铁反应: H2SO4 + Fe(OH)3 → 红褐色固体溶解 溶液呈黄色
56、硫酸和氢氧化钙反应:Ca(OH)2 + H2SO4 → 中和酸性土壤
57、硫酸和氢氧化钡反应:Ba(OH)2 + H2SO4 → 生成白色沉淀 不溶解于稀硝酸 这是检验H2SO4的原理
58. 硝酸和烧碱反应:HNO3 + NaOH →
59、硝酸和氢氧化铜反应:Cu(OH)2 + HNO3 → 蓝色固体溶解
60、硝酸和氢氧化镁反应:Mg(OH)2 + HNO3 → 白色固体溶解
61、硝酸和氢氧化铝反应:Al(OH)3 + HNO3 → 白色固体溶解
62、硝酸和氢氧化钙反应:Ca(OH)2 + HNO3 →
63、硝酸和氢氧化铁反应:Fe(OH)3 + HNO3 → 红褐色沉淀溶解 溶液呈黄色
65、碳酸钠与稀盐酸反应:Na2CO3 + 2HCl→ 固体逐渐溶解 有使澄清石灰水变浑浊的气体 泡沫灭火器的原理
66、碳酸钠与稀硫酸反应:Na2CO3 + H2SO4 → 固体逐渐溶解 有使澄清石灰水变浑浊的气体 泡沫灭火器原理
第二篇:初三化学方程式汇总默写版
初三化学方程式之【四大基本反应类型】
一、化合反应:由二种或二种以上的物质生成一种物质的反应(多变一)
1、二氧化碳和水反应:、二氧化硫和水反应 3、三氧化硫和水反应 4、氧化钙和水反应
5、氧化钠和水反应 、碳在高温下和二氧化碳反应7、碳在空气中燃烧、一氧化碳燃烧
9、硫燃烧、磷燃烧11、铁在氧气中燃烧、铝在氧气中燃烧13、镁在空气中燃烧、铜在空气中加热二、分解反应:由一种物质生成二种或二种以上的物质的反应。(一变多)
1、高锰酸钾加热分解 2、双氧水和二氧化锰混合3、氯酸钾和二氧化锰加热分解
4、水通电分解氧化汞受热分解
6、碳酸分解
7、氢氧化铜受热分解:
8、石灰石高温分解 9、水通电分解10、碳酸氢铵受热分解
三、置换反应:一种单质和一种化合物生成另一种单质和另一种化合物的反应。
(一)金属和酸反应,可制氢气
1、锌和稀硫酸反应
2、锌和稀盐酸反应
3、铁和稀硫酸反应(注意: )
4、铁和稀盐酸反应(注意: )
5、铝和稀硫酸反应6、铝和稀盐酸反应7、镁和稀硫酸反应8、镁和稀盐酸反应
你能把上面这四种和酸反应的金属和酸反应时的激烈程度按由大到小排列一下吗:
你做出这样的排列的理由是:( )
(二)金属氧化物和氢气或碳反应,可治炼金属
1、氢气还原氧化铜 2、氢气还原氧化铁:5、氢气还原氧化铜 、碳高温还原氧化铜 7、碳还原氧化铁 、碳还原氧化亚铁注意:一氧化碳还原氧化铜这个反应不是置换反应,因为,一氧化碳不是单质,它不满足置换反应的定义。 Co+CuO=Cu+Co2 (不是置换反应)
(三)金属与某些盐溶液反应,可治炼金属
(1)铁和硫酸铜反应 (2)铝和硫酸铜反应
(3)铜和硝酸汞反应 (4)铜和硝酸银反应
注意:金属与某些盐溶液能否发生置换反应的条件是:金属活动性顺序表中,排在前面的金属能把排在后面的金属从他的盐溶液中置换出来。
Mg+Al2(SO4)3= (可以反应) Fe+AlCl3= (不反应)
四、复分解反应:两种化合物相互交换成分生成两种新的化合物的反应。(通式:)
(一)酸+某些金属氧化物 === 盐+水
(1)盐酸与氧化铁反应
(2)硫酸与氧化铁反应
(3)硫酸与氧化铜反应
(4)盐酸与氧化铜反应
(二)酸+碱 === 盐+水(中和反应)
1、氢氧化钠和稀盐酸反应
2、氢氧化铜和盐酸反应 3、氢氧化铜和硫酸反应
4、氢氧化钠和硫酸反应 5、氢氧化钡和硫酸反应(三)盐+酸 === 新盐+新酸(生成物中有气体、沉淀或水)
1、大理石(石灰石)和稀盐酸反应
2、碳酸钠和稀盐酸反应3、硝酸银和盐酸反应
4、氯化钡和稀硫酸反应 (四)盐+碱 === 新盐+新碱(反应物均溶于水,生成物中有沉淀)
1、硫酸铜和氢氧化钠反应
2、氯化铁和氢氧化钠反应
3、碳酸钠和氢氧化钙反应4、硫酸铜和氢氧化钡反应5、硫酸镁和氢氧化钡反应6、氯化铵和氢氧化钙反应
(五)盐+盐 两种新盐(反应物均溶于水,生成物中有沉淀)
1、 氯化钾和硝酸银反应
2、氯化钠和硝酸银反应3、硫酸钠和氯化钡反应4、碳酸钠与氯化钡反应
五、不属基本反应类型的反应
(一)某些非金属氧化物与碱的反应
1、二氧化碳与澄清石灰水反应2、二氧化碳与氢氧化钠反应
3、二氧化硫与氢氧化钠反应
(二)一氧化碳与某些金属氧化物的反应
1、一氧化碳还原氧化铜2、一氧化碳还原氧化铁3、一氧化碳还原氧化亚铁
4、一氧化碳还原四氧化三铁(三)甲烷、酒精等有机物的燃烧
1、 甲烷(天然气、沼气、瓦斯气)燃烧
2、酒精(乙醇)燃烧
化学方程式的运用
写出下列化学方程式
(一) 化合反应:由二种或二种以上的物质生成一种物质的反应。
A + B === AB
4、 碳在氧气中完全燃烧5、 碳在氧气中不完全燃烧6、 硫在氧气中燃烧
7、 磷在空气中燃烧8、 氢在氧气中燃烧生成水9、 镁在空气中燃烧生成氧化镁10、铁在氧气中燃烧生成四氧化三铁11、铝在氧气中燃烧生成氧化铝
12、铜在空气中加热生成氧化铜
13、碳在高温下和二氧化碳反应生成一氧化碳
14、一氧化碳在氧气中燃烧生成二氧化碳
1、 二氧化碳和水反应生成碳酸(二)分解反应:由一种物质生成二种或二种以上的物质的反应。AB?A+B
1、 氯酸钾和二氧化锰加热分解生成氯化钾、氧气 2、高锰酸钾加热分解生成锰酸钾、二氧化锰、氧气
3、碱式碳式铜加热分解生成氧化铜、水、二氧化碳。
4、氧化汞加热分解生成汞和氧气
1、 碳酸氢铵加热分解生成氨气、水、二氧化碳。
6、水通电分解生成氢气、氧气
7、碳酸分解生成二氧化碳和水
8、石灰石高温分解生成氧化钙和二氧化碳 (三)置换反应:一种单质和一种化合物生成另一种单质和另一种化合物的反应。A+BC?B+AC
(A) 金属和酸发生的置换反应:
15、锌和稀硫酸反应生成硫酸锌和氢气 16、锌和稀盐酸反应生成氯化锌和氢气 17、铁和稀硫酸反应生成硫酸亚铁和氢气18、铁和稀盐酸反应生成氯化亚铁和氢气19、铝和稀硫酸反应生成硫酸铝和氢气铝和稀盐酸反应生成氯化铝和氢气
