EDTA标准溶液的配制和标定
一、目的要求
1.了解EDTA标准溶液标定的原理。
2.掌握配制和标定EDTAB标准溶液的方法。
二、原理
乙二胺四乙酸二钠盐(习惯上称EDTA)是一种有机络合剂,能与大多数金属离子形成稳定的1∶1螯合物,常用作配位滴定的标准溶液。
EDTA在水中的溶解度为120g/L,可以配成浓度为0.3mol/L以下的溶液。EDTA标准溶液一般不用直接法配制,而是先配制成大致浓度的溶液,然后标定。用于标定EDTA标准溶液的基准试剂较多,例如Zn、ZnO、CaCO3、Bi、Cu、MgSO4·7H2O、Ni、Pb等。
用氧化锌作基准物质标定EDTA溶液浓度时,以铬黑T作指示剂,用pH=10的氨缓冲溶液控制滴定时的酸度,滴定到溶液由紫色转变为纯蓝色,即为终点。
三、试剂
1.乙二胺四乙酸二钠盐(EDTA)。
2.氨水-氯化铵缓冲液(pH=10):称取5.4g氯化铵,加适量水溶解后,加入35mL氨水,再加水稀释至100mL。
3.铬黑T指示剂:称取0.1g铬黑T,加入10g氯化钠,研磨混合。
4.40%氨水溶液:量取40mL氨水,加水稀释至100mL。
5.氧化锌(基准试剂)。
6.盐酸
四、步骤
1. 0.01mol·L-1EDTA溶液的配制
称取乙二胺四乙酸二钠盐(Na2H2Y·2H2O)4g,加入1000mL水,加热使之溶解,冷却后摇匀,如混浊应过滤后使用。置于玻璃瓶中,避免与橡皮塞、橡皮管接触。贴上标签。
2. 锌标准溶液的配制
准确称取约0.16g于800℃灼烧至恒量的基准ZnO,置于小烧杯中,加入0.4mL盐酸,溶解后移入200mL容量瓶,加水稀释至刻度,混匀。
3. EDTA溶液浓度的标定
吸取30.00~35.00mL锌标准溶液于250mL锥形瓶中,加入70mL水,用40%氨水中和至pH为7~8,再加10mL氨水-氯化铵缓冲液(pH=10),加入少许铬黑T指示剂,用配好的EDTA溶液滴定至溶液自紫色转变为纯蓝色。记下所消耗的EDTA溶液的体积,根据消耗的EDTA溶液的体积,计算其浓度。
思 考 题
1.用铬黑T指示剂时,为什么要控制pH=10?
2.配位滴定法与酸碱滴定法相比,有哪些不同?操作中应注意哪些问题?
附:0.05mol·L-1EDTA滴定液的配制与标定(药典方法)
一、试剂
a) 稀盐酸:取盐酸234mL,加水稀释至1000mL。
b) 0.025%甲基红的乙醇液:取甲基红0.025g,加无水乙醇100mL,即得。
c) 氨试液:取浓氨水400mL,加水使成1000mL。
d) 氨-氯化铵缓冲液(pH=10.0):取氯化铵5.4g,加水20mL溶液后,加浓氨水溶液35mL,再加水稀释至100mL,即得。
e) 铬黑T指示剂:取0.1g铬黑T,加氯化钠10g,研磨均匀,即得。
二、步骤
1.配制:称取乙二胺四醋酸二钠盐(Na2H2Y·2H2O)19g,加适量的水使溶解成1000mL,摇匀。
2.标定:取于800℃灼烧至恒重的基准氧化锌约0.12g,精密称定,加稀盐酸3mL使溶解,加水25mL,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25mL与氨-氯化氨缓冲液(Ph=10.0)10ml,再加铬黑T指示剂少量,用本液滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验校正。每1ml乙二胺四醋酸二钠滴定液(0.05mol/L)相当于4.069mg的氧化锌。根据本液的消耗量与氧化锌的取用量,算出本液的浓度,即得。
3.贮藏:置玻璃塞瓶中,避免与橡皮塞、橡皮管等接触。
第二篇:EDTA标准溶液的配制和标定 水的总硬度的测定
实验九 EDTA标准溶液的配制和标定水的总硬度的测定
一、实验目的
1、掌握EDTA的配制及用硫酸镁标定EDTA的基本原理与方法;
2、了解水的硬度的概念及其表示方法;
3、掌握容量瓶、移液管的正确使用。
二、实验学时:4学时
三、基本操作
1、电子天平的使用
2、容量甁的使用
3、滴定管的使用
四、仪器与试剂
1、仪器
电子天平(0.1mg) 容量瓶(100mL)
移液管(20mL) 酸式滴定管(50mL)
锥形瓶(250mL)
2、试剂
0.2mol ·L-1EDTA (Na2H2Y·2H2O) MgSO4 · 7H2O基准试剂
NH3-NH4Cl缓冲溶液(pH=10.0) 1mol·L-1NaOH
铬黑T指示剂 钙指示剂
五、实验原理
乙二胺四乙酸二钠盐(习惯上称EDTA)是有机配位剂,能与大多数金属离子形成稳定的1:1 型的螯合物,计量关系简单,故常用作配位滴定的标准溶液。
通常采用间接法配制EDTA标准溶液。标定EDTA溶液的基准物有Zn、ZnO、CaCO3、Bi、Cu、MgSO4 · 7H2O、Ni、Pb 等。选用的标定条件应尽可能与测定条件一致,以免引起系统误差。如果用被测元素的纯金属或化合物作基准物质,就更为理想。本实验采用MgSO4 · 7H2O作基准物标定EDTA,以铬黑T(EBT)作指示剂,用pH ≈10 的氨性缓冲溶液控制滴定时的酸度。因为在pH ≈10 的溶液中,铬黑T 与Mg2+ 形成比较稳定的酒红色螯合物(Mg—EBT),而EDTA与Mg2+
能形成更为稳定的无色螯合物。因此,滴定至终点时,EBT 便被EDTA 从Mg—EBT中置换出来,游离的EBT 在pH = 8~11 的溶液中呈蓝色。
滴定前: M + EBT M—EBT
M—EBT
(酒红色)
主反应: M + EDTA  M—EDTA
M—EDTA
终点时: M—EBT + EDTA  M—EDTA + EBT
M—EDTA + EBT
酒红色 蓝色
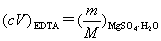
含有钙、镁离子的水叫硬水。测定水的总硬度就是测定水中钙、镁离子的总含量,可用EDTA配位滴定法测定。滴定时,Fe3+、Al3+等干扰离子可用三乙醇胺予以掩蔽;Cu2+、Pb2+、Zn2+等重属离子,可用KCN、Na2S或巯基乙酸予以掩蔽。
水的硬度有多种表示方法,本实验要求以每升水中所含Ca2+、Mg2+总量(折算成CaO的质量)表示,单位mg·L-1。
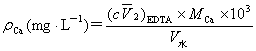
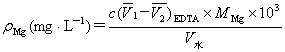

六、实验步骤
1、0.01mol ·L-1 EDTA 标准溶液的配制:
取30mL 0.1mol ·L-1的EDTA于试剂瓶中,加水稀释至300 mL,摇匀,备用。
2、0.01 mol ·L-1镁标准溶液的配制:
准确称取MgSO4 · 7H2O基准试剂0.25~0.3g,置于小烧杯中,加30 mL蒸馏水溶解,定量转移到100mL 容量瓶中,加水稀释至刻度,摇匀。计算其准确浓度。
3、EDTA 标准溶液浓度的标定:
用移液管吸取镁标准溶液20.00mL 置于250mL 锥形瓶中,加5mL pH ≈10 的NH3-NH4Cl缓冲溶液,加入铬黑T指示剂少许,用EDTA 标准溶液滴定至溶液由酒红色恰变为蓝色,即达终点,平行测定三次。根据消耗的EDTA标准溶液的体积,计算其浓度。
4、水的总硬度测定:
用100mL移液管或量筒取100mL水样于250mL锥形瓶中,加氨性缓冲溶液5mL, EBT指示剂少许,用EDTA标准溶液滴定,至溶液由酒红色变为蓝色即为终点,记录所消耗EDTA的体积V1。平行测定3次。
5、钙的测定:
取与步骤4等量的水量于250mL锥形瓶中,加5mL 1mol·L-1NaOH, 钙指示剂少许,用EDTA标准溶液滴定至溶液由酒红色变为蓝色即为终点,记录所消耗EDTA的体积V2。平行测定3次。
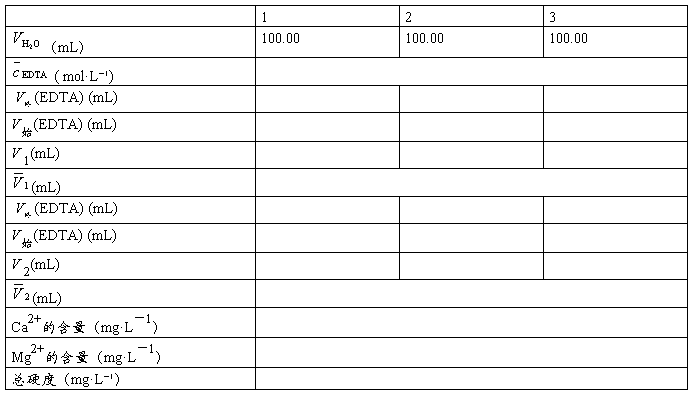
七、数据记录与处理
1、EDTA的标定

2、水的硬度的测定
八、注意事项
1、络合滴定速度不能太快,特别是近终点时要逐滴加入,并充分摇动。因为络合反应速度较中和反应要慢一些;
2、在络合滴定中加入金属指示剂的量是否合适对终点观察十分重要,应在实践中细心体会;
3、络合滴定法对去离子水质量的要求较高,不能含有Fe3+、Al3+、Cu2+、Mg2+等离子。
九、思考题
1、用铬黑T 指示剂时,为什么要控制pH ≈10?
2、配位滴定法与酸碱滴定法相比,有哪些不同?操作中应注意哪些问题?
3、用EDTA滴定Ca2+、Mg2+时,为什么要加氨性缓冲溶液?
