��������� ѧ�ţ�5603111040 ����ʱ�䣺�ڰ��ܣ�����3 ��14��
ʵ��� EDTA����Һ�����ƺͱ궨
һ�� ʵ��Ŀ�ģ�
1.��һ�����շ�����ƽ����ȷʹ�ã�
2.������ȷ�ĵζ�����������
3ѧϰEDTA ����Һ�����ƺͱ궨������
4.������λ�ζ�ָʾ����ָʾԭ�����յ���жϡ�
5. ���ն�������ʵ�鱨�����ȷ��ʾ����ʽ�����ݡ���Ч���ֵȣ�
����ԭ��
�Ҷ�����������Ƽ��EDTA������EDTA���������������γ��ȶ���1��1��������ʳ�������ϵζ��ı���Һ��
�궨EDTA��Һ�Ļ�����:Zn��ZnO��CaCO3��Cu��Bi ��Ni��Pb MgSO4·7H2O���ȡ�ͨ��ѡ�õı궨����Ӧ��������ⶨ����һ�£���������ϵͳ������ñ���Ԫ�صĴ����������������ʣ���Ϊ���롣
���EDTA��Һ���ڲⶨpb2+,Bi3+,�����ô�����п������궨EDTA���ø���T��ָʾ�����ð�������Һ����pH=10���б궨��Ҳ���ö��ӳ���ָʾ���������μ��İ�������ȣ���pH=5��6���б궨��
��ʵ����CaCO3�������pH�R12��NaOH����Һ�У��Ը�ָʾ���� �궨EDTA����Һ�ɾƺ�ɫ��Ϊ����ɫΪ�յ㡣��Ӧ���£�
�ζ�ǰ : Ca2++ HInd2-(����) CaInd-(�ƺ�)+ H+
�ζ���ʼ���յ�:
Ca2+ + H2Y2- CaY2- + H+
pH�R12
�յ�:
CaInd-���ƺ죩+H2Y2- CaY2- + HInd2-(������
pH�R12
����EDTAŨ��
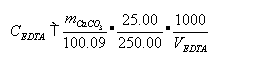
�����Լ�
1���Ҷ�����������ƣ�Na2H2Y·2H2O��
Ħ������Ϊ372.2��1g/2�ˡ�
2�� CaCO3 ��A·R��
3��NH3-NH4Cl������Һ
4����ָʾ��
�ġ���Ҫ����
��0.005mol/L EDTA ��Һ�����ƣ�1g �Ҷ�����������ơ���500mL ���ձ��У���ˮ�ܽ⣨��Ҫʱ�������ȣ��Լӿ��ܽ��� 200mL ��ˮ���ò���������ȡ����500mL��Һ��ÿ������һ�ݣ�
��0.005mol/L EDTA ��Һ�ı궨��
ȷ��ȡ0.15-0.20g CaCO3(100�ձ���)������ˮ��ʪ,���ϱ������5mL1��1HCl�ӱ�����μ���?����ȫ�ܽ��������?��������250mL �� ��ȡ25.00mL �Ʊ���Һ����Լ25mLˮ��10mL10%NaOH�����������ָʾ������EDTA�ζ�����Һ���Ϻ�ɫ������ɫΪ�յ㡣
ƽ�вⶨ���ݡ�
�塢���ݼ�¼������
����������һ��������Һ������

������EDTA��Һ�ı궨
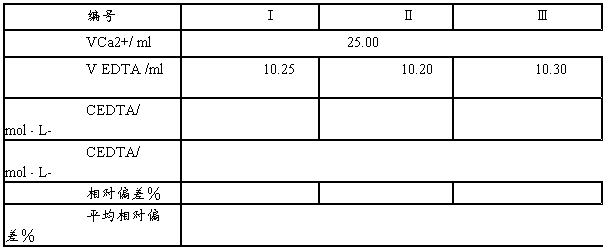
���� ˼���⣺
1. EDTA����Һ��Zn��CaCO3����Һ���Ʊ������кβ�ͬ��
2. ��λ�ζ���ΪʲôҪ���뻺����Һ?��
�ڶ�ƪ��EDTA����Һ��������궨
EDTA����Һ��������궨��3ѧʱ��
һ��Ŀ��Ҫ��
1������EDTA����Һ�����ƺͱ궨����
2��������λ�ζ���ԭ������ζ��ص�
3��ѧ���ö��ӳ�ָʾ����ָʾ���жϷ�Ӧ�յ�
����ʵ��ԭ��
�Ҷ��������ᣨ���EDTA������H4Y��ʾ��������ˮ��������ѧ��ͨ��ʹ��������Ρ��Ҷ�������������ε��ܽ��Ϊ120g?L-1��������0.3mol?L-1���µ���Һ��ͨ���Լ�ӷ����Ʊ���Һ��
�궨EDTA��Һ���õĻ�����Zn��ZnO��CaCO3��Bi��Cu��MgSO4?7H2O��Hg��Ni��Pb�ȡ�ͨ��ѡ�������뱻���������ͬ��������Ϊ����������ζ�����һ�£��ɼ���ϵͳ����ʵ����ҪѧϰCaCO3��Zn��ZnO��Ϊ����Ը�ָʾ���Ͷ��ӳ�ָʾ��Ϊ����ָʾ���궨EDTA����Һԭ����������
����ָʾ����һЩ��ɫ���л���ϼ�����һ��������������������γ���ɫ��������ɫ������ָʾ������ɫ��ͬ�����������ָʾ�ζ������н�������Ũ�ȵı仯�������������Ҫ�ʵ�����λ��Ӧ����Ӧ���������ڵζ������У�EDTA��Һ�μ��ٶȲ���̫�죬������յ�ʱ��Ӧ��μ��룬���ҡ����
��CaCO3Ϊ����ʱ���ø�ָʾ����Ϊָʾ������pH��12�����£�����ĸ�ָʾ��Ϊ����ɫ��Ca2+���ָʾ��������H3In��ʾ������γɱȽ��ȶ��ľƺ�ɫ��CaIn-��λ���ӣ�ʹ��Һ���־ƺ�ɫ������EDTA����Һ�ζ�ʱ������EDTA����Ca2+�γɱ�CaIn-���Ӹ��ȶ�����ɫ��CaY2-���ӣ���Ӧ���ﻯѧ������ʱ�ͷų�����ĸ�ָʾ������Һ����ɫ�ɾƺ�ɫ��Ϊ����ɫ����Ӧ����ʽΪ��
CaIn-(�ƺ�ɫ)+H2Y2-CaY2-(��ɫ)+HIn2-(����ɫ)+H+
����Mg2+���Ӵ���ʱ����ɫ�仯�����������ֻ��Ca2+����ʱ��������������Mg2+���ӡ��ô˷����궨��EDTA����Һ�������ڲⶨʯ��ʯ�����ʯ��CaO��MgO

������Ҳ����
���ڲⶨˮ�и�Ӳ�ȡ�
��Zn��ZnOΪ����ʱ���ö��ӳ���Ϊָʾ������pH=5��6�����£�����Ķ��ӳ�Ϊ��ɫ��Zn2+����ӳȽ���γɱȽ��ȶ����Ϻ�ɫ������ӣ�ʹ��Һ�����Ϻ�ɫ������EDTA����Һ�ζ�ʱ������EDTA����Zn2+�γɸ��ȶ�����ɫCaY2-���ӣ���Ӧ���ﻯѧ������ʱ�ͷų�����Ķ��ӳ�ָʾ������Һ����ɫ���Ϻ�ɫ��Ϊ����ɫ��
�ô˷����궨��EDTA����Һ��������Ǧ������Һ��Ǧ���麬���IJⶨ��Ҳ��������ˮ��Ӳ�Ȳⶨ��
�����������Լ�
1������
������ƽ��50mL��ʽ�ζ��ܣ�25mL��Һ�ܣ�250mL����ƿ�����ò����������ɡ�
2���Լ�
��1����CaCO3Ϊ����ʱ�����Լ�
�Ҷ������������(���壬������)��CaCO3�����Լ�����NaOH��Һ��10%����
��������Һ��pH��10������ָʾ�������壩����ˮ(1:1)��
þ��Һ���ܽ�1gMgSO4?7H2O��ˮ�У�ϡ����200mL��������T
��2����ZnO����Zn��Ϊ����ʱ�����Լ�
�Ҷ�����������ƣ����壬����������ZnO�����Լ�������ˮ(1:1)�����μ��İ���20%�������ӳ�ָʾ����0.5%��������(1:1)
�ġ��ο�����
1��0.02mol?L-1EDTA����Һ������
��̨���ϳ�ȡ3.8g�Ҷ�����������ƣ�����100mLȥ����ˮ�У����ܽ��ת�Ƶ�500mL�Լ�ƿ�У��ټ���400mLȥ����ˮ��ҡ�ȡ����л��ǣ�Ӧ���ˡ�
2����CaCO3Ϊ����궨EDTA��Һ
��1��0.02mol?L-1�Ʊ���Һ������
ȷ�س�ȡ��110������CaCO3����0.3��0.4g��ȷ��0.1mg����С�ձ��У����Ա���������ȥ����ˮ��ʪ�����صμ�1:1��HCl3��5mL����ˮ�ѿ��ܽ����������ϵ���Һ��ϴ���У���������ȫ�ܽ⡣��ȴ����Һ����ת�Ƶ�250mL����ƿ�У�ϡ
�����̶ȣ�ҡ���ȡ�
��2���궨
a��ǿ���Խ������ô˷�
��25mL��Һ����ȡ�Ʊ���Һ25.00mL��250mL����ƿ������25mLˮ��2mLþ��Һ��5mL10%NaOH��Һ���̶���С�ĸ�ָʾ����ҡ���Ⱥ���EDTA��Һ�ζ�����Һ�ɺ�ɫ��Ϊ��ɫ����Ϊ�յ㣬��¼����EDTA��Һ�������ƽ�����Σ�Ҫ����������ļ���С��0.05mL������CaCO3������������EDTA��Һ�����������EDTA����Һ��ȷŨ�ȡ�
b.���Ի�����Һ���ô˷�
��25mL��Һ����ȡ�Ʊ���Һ25.00mL��250mL����ƿ������10mLpH��10��������Һ��2�θ���Tָʾ����ҡ���Ⱥ���EDTA��Һ�ζ�����Һ���Ϻ�ɫ��Ϊ����ɫ����Ϊ�յ㣬��¼����EDTA��Һ�������ƽ�����Σ�Ҫ����������ļ���С��0.05mL������CaCO3������������EDTA��Һ�����������EDTA����Һ��ȷŨ�ȡ�
3����ZnOΪ����궨EDTA��Һ
��1��0.02mol?L-1п����Һ������
ȷ��ȡ��800��1000�����չ���ZnO����0.2��0.3g��ȷ��0.1mg����С�ձ��У�������ȥ����ˮ��ʪ�����صμ�1:1��HCl5mL��ͬʱ��������ȫ�ܽ⡣Ȼ����Һ����ת�Ƶ�250mL����ƿ�У�ϡ�����̶Ȳ�ҡ���ȡ�
��2���궨
��25mL��Һ����ȡп����Һ��250mL����ƿ������Լ30mLˮ��2�ζ��ӳ�ָʾ����ҡ���Ⱥ��ȼ�1:1�İ�ˮ����Һ�ɻ�ɫ�ձ��ɫ��Ȼ��μ�20%���μ��İ�����Һ���ȶ����Ϻ�ɫ���ٶ��3mL����EDTA��Һ�ζ�����Һ���Ϻ�ɫ��Ϊ����ɫ����Ϊ�յ㣬��¼����EDTA��Һ�������ƽ�����Σ�Ҫ����������ļ���С��0.05mL������ZnO������������EDTA��Һ�����������EDTA����Һ��ȷŨ�ȡ�
�塢ʵ�����ݼ�¼�봦����ZnOΪ����궨EDTA��Һ
���
ʵ����Ŀ
(����ƿ+����)����
�����(����ƿ+����)����
ȡ�����������
����ƿ�����
��ȡ��Һ�����
��Һ�ն���
��Һ������
EDTA��Һ���
��Һ��Ũ��
��Һ��ƽ��Ũ��
���ƽ��ƫ��
����������˼��
1����ZnOΪ����Զ��ӳ�Ϊָʾ���궨EDTA��ҺŨ�ȵ�ԭ����ʲô����Һ��pHֵӦ������ʲô��Χ������ҺΪǿ���ԣ�Ӧ�������ڣ�
2����λ�ζ��������ζ�����ȣ�����Щ��ͬ�㣿�ζ�����������Ӧע����Щ���⣿
�������֣�
