发酵工程实验指导书
辽宁石油化工大学环境与生物工程学院主编
《发酵工程》实验指导书
实验学时:24学时
适用专业:生物工程
生物技术是当前优先发展的高新技术之一,本课程是为了和生物工程专业理论教学相配合,通过实践教学,培养学生对生物工程专业知识的具体实际应用的能力。
发酵工程实验是以实验操作为主的技能课程,是生物工程专业学生的必修课,是在学生学习了《生物化学及实验》、《微生物学及实验》等专业基础课及专业实验课的基础上开设的,课程目的在于通过本课程的实验训练,使学生对整个微生物生产过程有一个全面的认识和理解,既可培养他们实际操作的技能,又可达到提高他们理论联系实际能力的目的。通过学习,使学生能掌握发酵工程常用的实验方法和常见的发酵工程设备,为以后的学习和科研工作打下良好的基础。
本实验指导书包括:
实验一、细菌增殖曲线的测定(6学时)
实验二、土壤中放线菌的分离与纯化(6学时)
实验三、发酵菌株的初筛
实验四、枯草芽孢杆菌的紫外线诱变选育(6学时)(必做)
实验五、 淀粉酶的固态发酵(6学时)
实验六、发酵过程中糖的利用(6学时)
实验七、玉米淀粉液化和糖化(6学时)
实验八、淀粉酶的固定化生产(6学时)
实验九、摇床培养确定酵母菌体的培养和营养条件(6学时)(必做)
实验十、小型连续发酵实验(6学时)
实验十一、甜酒酿的制作(6学时)
备注:实验一至实验七为基础实验,实验八至实验十一为设计性和综合性实验,除必做实验外,其他可选做。
实验总时间为24学时,包括设计实验、准备实验、进行实验、书写实验预习及最终报告及所需仪器药品清单等。
实验一 发酵菌株的初筛
一、实验目的与要求
目的:
1、从已分离到的细菌或真菌中筛选出能产生生理活性物质的菌株。
2、学习淀粉酶、蛋白酶产生菌的筛选方法。
要求:
1、复习微生物学及实验过程所学到的微生物培养的方法和过程,了解影响微生物生长各种条件因素。
2、独立查阅相关资料,设计实验方案,并对实验所需的各种药品、玻璃仪器及分析设备列出清单,写出详尽的试验过程及需要。
3、三人一组,互相配合,开展实验,动手完成实验,并记录并分实验中的实验现象、数据,必要时及时修改试验计划。
4、总结试验数据,经教师认定后,撰写实验报告。
二、实验原理
淀粉酶是一类淀粉水解酶的统称,它能将淀粉水解成糊精等小分子物质并进一步水解成麦芽糖或葡萄糖,淀粉被水解后,遇碘不再变蓝色,因此可以根据淀粉培养基上透明圈的大小来判断所选菌株的淀粉酶活力。
蛋白酶也是一类重要的工业用酶制剂,它能将蛋白质分解成短肽甚至氨基酸。根据三氯乙酸能将酪蛋白变性从而产生沉淀这一原理,可在平板培养基上直接筛选蛋白酶产生菌株。产酶菌株能将酪蛋白水解成小分子物质,菌落周围不形成沉淀蛋白而出现透明圈,根据透明圈大小还能判断产酶活力。
本实验以淀粉酶或蛋白酶产生菌株的筛选为例,介绍发酵菌种的初步筛选方法。
三、实验主要仪器设备及材料
1.菌株:自然界中分离到的目的菌株
2.淀粉酶产生菌筛选培养基:蛋白胨1%,牛肉膏0.3%,氯化钠0.5%,可溶性淀粉0.2%。琼脂2%,pH 7.2-7.4。
3.蛋白酶产生菌筛选培养基:葡萄糖0.05,氯化钠0.5%,磷酸氢二钾0.05%,磷酸二氢钾0.05%,酪蛋白1%,琼脂2%,pH 7.5。
4.器材:培养皿、吸管、250ml三角瓶、无菌水(含灭菌玻璃珠)、标签纸、三氯乙酸、碘液、玻璃刮铲、吸管、电炉、天平等。
四、实验方法、操作步骤
1、配制淀粉酶或蛋白酶的筛选培养基,分别装于三角瓶中,121摄氏度灭菌30分钟,冷却至60摄氏度时倒平板,每皿约20毫升。
2、配制指示菌菌悬液,以无菌操作法挑取3环细菌或酵母指示菌菌苔装到有3ml无菌水的试管中,制成菌悬液,吸取0.1ml涂布在相应培养基的平板上。注意:用淀粉酶产生菌筛选培养基来分离产生淀粉酶的细菌,将分离纯化的菌株点种于淀粉培养基平板上,每皿点种5点。
3、将平板放在培养箱中培养1-2天,观察菌落的生长情况。
4、淀粉酶产生菌培养基上形成菌落后,在平板上滴加碘液,以铺满平皿为度,如果菌落周围有透明圈出现,说明淀粉被水解,该菌能产淀粉酶,透明圈与菌落直径之比越大,说明产淀粉酶活力越强。
5、蛋白酶产生菌培养基上形成菌落后,可在平板上滴加2.5%三氯乙酸溶液,以刚铺满平皿为度,菌落周围如有无色透明圈出现,说明该菌产蛋白酶。
五、试验报告记载要求
1、姓名、班级、学号、试验开始日期/时间等。
2、实验的设计方案、所用的仪器名称、药品名称及重量;所使用的样品名称、来源。
3、试验操作步骤记载。
4、实验条件记载(温度、浓度、仪器条件等)。
5、实验分析。
6、实验中应注意的问题/收获。
六、思考题
查阅资料,设计一个实验来筛选脂肪酶或其他酶的产生菌。
实验二 枯草芽孢杆菌的紫外线诱变选育
一、实验目的与要求
目的:
通过实验,观察紫外线对枯草芽孢杆菌的诱变效应,并学习物理因素诱变育种的方法。
要求:
1、复习微生物学及实验过程所学到的微生物培养的方法和过程,了解影响微生物生长各种条件因素。
2、独立查阅相关资料,设计实验方案,并对实验所需的各种药品、玻璃仪器及分析设备列出清单,写出详尽的试验过程及需要。
3、三人一组,互相配合,开展实验,动手完成实验,并记录并分实验中的实验现象、数据,必要时及时修改试验计划。
4、总结试验数据,经教师认定后,撰写实验报告。
二、实验原理、内容
物理诱变因子以紫外线辐射的使用最为普遍,尽管几十年来各种新的诱变剂不断出现和被应用于诱变育种,但到目前为止,对于经诱变处理后得到的高单位抗生素产生菌中,有80%左右是通过紫外线诱变后经筛选而获得的。在紫外线的波长在200-380nm之间,但对诱变最有效的波长仅仅是在253-265cm,一般紫外线杀菌灯所发射的紫外线大约有80%是254nm。紫外线诱变得主要生物学效应是由于DNA变化而造成的,DNA对紫外线有强烈的吸收作用,尤其是碱基中嘧啶更为敏感。它比嘌呤更为敏感。紫外线引起DNA结构变化的形式很多,但其最主要的作用是引起DNA的分子结构发生改变(同链DNA的相邻嘧啶间形成共价结合的胸腺嘧啶二聚体),阻碍碱基间的正常配对,从而微生物突变或死亡。经紫外线损伤的DNA,能被可见光复活,因此,经诱变处理后的微生物菌种要避免长波紫外线和可见光的照射,故经紫外线照射后样品需用黑纸或黑布包裹。
三、实验主要仪器设备和材料
菌种:枯草芽孢杆菌;
器皿:紫外线灯(15W);试管、锥形瓶、移液管、玻璃珠、培养皿;
培养基及药品:牛肉膏、蛋白胨、可溶性淀粉、NaCL、水、碘液。
四、实验方法、操作步骤
1、菌悬液的制备: 取培养48小时的活化枯草芽孢杆菌的斜面1—2支,用10ml无菌生理盐水将菌苔洗下,并入盛有灭菌玻璃珠的小三角烧瓶中,振荡10分钟,以打碎菌块。菌悬液以10倍稀释法稀释成10-1-10-8稀释液。
2、平板制作:将淀粉琼脂培养基溶化后,冷至55℃左右时倒平板,凝固后待用。
3、紫外线处理:
(1)将紫外线灯开关打开预热约20分钟。
(2) 取直径6cm无菌平皿9套,涂平板取10-6、10-7、10-8三个稀释度涂平板,每个稀释度涂平板3只,每只平板加稀释菌液0.1ml,用无菌玻璃刮棒涂匀。
(3) 将盛有菌悬液的平皿置于紫外线灯下分别搅拌照射0分钟 、3分钟及5分钟。
4、培养:将上述涂匀的平板,用黑布(或黑纸)包好,置37℃培养48小时。注意每个平皿背面要标明处理时间和稀释度。
5、计数:将培养48小时后的平板取出进行细菌计数,根据对照平板上菌落数,计算出每毫升菌液中的活菌数。同样计算出紫外线处理3分钟、5分钟、7分钟后的存活细胞数及其存活/致死率。

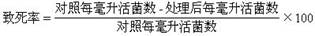
6、观察诱变效应:将细胞计数后的平板,分别向菌落数在5—6个左右的平板内加碘液数滴,在菌落周围将出现透明圈。分别测量透明圈直径与菌落直径并计算其比值(HC值)。与对照平板进行比较,根据结果,说明诱变效应。并选取HC比值大的菌落移接到试管斜面上培养。此斜面可作复筛用。
五、实验结果
将实验结果填入下表
表1 诱变结果(存活率或致死率)

表2 诱变结果(透明圈和菌落直径大小)

六、试验报告记载要求
1、姓名、班级、学号、试验开始日期/时间等。
2、实验的设计方案、所用的仪器名称、药品名称及重量;所使用的样品名称、来源。
3、试验操作步骤记载。
4、实验条件记载(温度、浓度、仪器条件等)。
5、实验分析。
6、实验中应注意的问题/收获。
七、思考题
1、用于诱变的菌悬液(或孢子悬液)为什么要充分振荡?
2、经紫外线处理后的操作和培养为什么要在暗处或红光下进行?
实验三 发酵过程中糖的利用
一、实验目的与要求
目的:
1、了解发酵过程中碳源的利用规律。
2、掌握用DNS法测定还原糖的含量的方法。
要求:
1、复习发酵工程中所学到的糖质原料的种类、发酵过程中糖的转化等过程,了解影响糖利用的各种因素。
2、独立查阅相关资料,设计实验方案,并对实验所需的各种药品、玻璃仪器及分析设备列出清单,写出详尽的试验过程及需要。
3、三人一组,互相配合,开展实验,动手完成实验,并记录并分实验中的实验现象、数据,必要时及时修改试验计划。
4、总结试验数据,经教师认定后,撰写实验报告。
二、实验原理
糖类是微生物生命活动中主要的碳源和能源物质。一方面微生物的生长需要糖类,另一方面,糖也构成了代谢产物中碳架的主题所以在发酵过程中,糖的消耗是一项重要的生理指标,是判断发酵进程的主要依据。
将少量微生物接种到一定体积的、适合的新鲜培养基中,在适宜的条件下进行培养,定时测定培养液中的还原糖含量,以还原糖含量作纵坐标,生长时间作横坐标,绘制出的曲线可以反映微生物在一定环境条件下所表现出的生长规律。因此通过测定微生物的碳源利用规律,对于科研和生产都具有重要的指导意义。
测定还原糖含量有多种不同的方法,如斐林试剂法、蒽酮比色法、3,5二硝基水杨酸法(DNS法)等。它们各有优缺点。本实验采用的是DNS法。DNS法是利用3,5-二硝基水杨酸溶液与还原糖溶液共热后,被还原成棕红色的氨基化合物,在一定范围内还原糖的量和棕红色物质颜色深浅的程度呈一定比例关系这一原理而设计的,可用于比色测定。操作简便、快速、杂质干扰较少。
三、实验主要仪器设备及材料
天平、分光光度计,比色杯,恒温摇床,灭菌锅、移液管,试管,三角瓶、滤纸、比色管
菌种:黑曲霉
培养基:
黑曲霉斜面培养基:去皮马铃薯200g,葡萄糖20g,琼脂15-20g,加水至1000mL。
发酵培养基:葡萄糖15%,硫酸铵0.3%。
试剂:
标准葡萄糖溶液:准确称取100mg分析纯的无水葡萄糖(预先在105℃干燥至恒重),用少量蒸馏水溶解后,定量转移到100mL容量瓶中,再定容到刻度,摇匀,浓度为1mg/mL。
3,5-二硝基水杨酸试剂配制
甲液:溶解6.9g结晶酚于15.2mL 10%氢氧化钠溶液中,并用水稀释至69mL,在此溶液中加入6.9g亚硫酸氢钠。
乙液:称取255g酒石酸钾钠加到300mL10%氢氧化钠溶液中,再加入880mL 1% 3,5-二硝基水杨酸溶液。将甲乙二溶液混合即的黄色试剂,贮于棕色瓶中备用,在室温放置7 -10天以后使用。
四、实验方法、操作步骤
1、活化菌种:
斜面培养基配制与灭菌:去皮马铃薯200g切成小块,加水约500ml,煮沸30min,然后用纱布过滤,滤液加蔗糖20克,琼脂20克,溶化后用自来水定容至1000ml,分装于带棉塞试管内,121℃下灭菌20min,取出摆成斜面,用接种环挑取冰箱保存的黑曲霉菌种接种在斜面培养基上,在恒温培养箱中35℃培养3-4天,待长满大量黑色孢子后即为活化的斜面种子。
2、摇瓶发酵培养:
发酵培养基的配制与灭菌:按照葡萄糖15%、硫酸铵0.3%的比例在三角瓶中配制40ml,待葡萄糖和硫酸铵全部溶解后在121℃下灭菌20min下灭菌。等冷却后进行转种。接种量为每瓶3-4环。于转速200r/min的摇床上培养,35℃下培养3天。
3、测定指标:发酵0、24、48、72h分别各取下摇瓶检测还原糖的含量,以观察发酵过程中黑曲霉的耗糖速率。
测定步骤:
① 葡萄糖的标准曲线制作
葡萄糖标准溶液的配制:准确称取100mg分析纯的无水葡萄糖(预先在105℃干燥至恒重),用少量蒸馏水溶解后,定量转移到100mL容量瓶中,再定容到刻度,摇匀,浓度为1mg/mL。
取六支试管,分别按表一中所示过程方法试剂。将各管溶液混合均匀,在沸水浴中加热5min,取出后立即用冷水冷却到室温,再向各试管中加入21.5mL蒸馏水,摇匀。于520nm波长处测定A值,并将测得的A值列于表一中。以吸光度为纵坐标、糖的毫克数或浓度为横坐标,绘制标准曲线。
表一 试剂组成及A520值

②发酵液中含糖量的测定
取发酵液4ml过滤除去菌体及残渣,准确计量取滤液0.1ml, 定容至50ml,制成500倍稀释试样。
③取干燥试管,编号,按表2所示的量,精确加入待测液和试剂(ml)
表2 样品还原糖的测定

④加完试剂后,其余操作步骤与制作葡萄糖标准曲线时的相同,测定出各管溶液的吸光度值。
4、计算:以各样品的吸光度值的平均值在标准曲线上查出相应的还原糖毫克数,按下式计算样品中还原糖的百分含量:

五、试验报告记载要求
1、姓名、班级、学号、试验开始日期/时间等。
2、实验的设计方案、所用的仪器名称、药品名称及重量;所使用的样品名称、来源。
3、试验操作步骤记载。
4、实验条件记载(温度、浓度、仪器条件等)。
5、实验分析。
6、实验中应注意的问题/收获。
六、思考题
1、用比色法测定物质含量时,为什么要做空白对照管?
2、比色测定的原理是什么?操作步骤有哪些?
实验四 摇床培养确定酵母菌体的培养和营养条件
一、实验目的与要求
目的:
1、通过实验,掌握微生物斜面培养基、种子培养基及发酵培养基制备方法,学会对已确定菌种进行实验室发酵工艺;学会筛选微生物最适生长及产物形成的营养条件和培养条件,确定特定产物发酵的工艺参数。
2、通过本试验使学生复习以前所学的微生物学及实验技能,掌握正交实验设计方法,同时通过本试验使学生熟练掌握使用分光光度计、恒温振荡培养箱等仪器的使用。
要求:
1、复习微生物学及实验过程所学到的微生物培养的方法和过程,了解影响微生物生长各种条件因素。
2、独立查阅相关资料,设计实验方案,并对实验所需的各种药品、玻璃仪器及分析设备列出清单,写出详尽的试验过程及需要。
3、三人一组,互相配合,开展实验,动手完成实验,并记录并分实验中的实验现象、数据,必要时及时修改试验计划。
4、总结试验数据,经教师认定后,撰写实验报告。
二、实验原理、内容
正交试验设计(Orthogonal experimental design)是研究多因素多水平的又一种设计方法,它是根据正交性从全面试验中挑选出部分有代表性的点进行试验,这些有代表性的点具备了“均匀分散,齐整可比”的特点,正交试验设计是分式析因设计的主要方法。是一种高效率、快速、经济的实验设计方法。日本著名的统计学家田口玄一将正交试验选择的水平组合列成表格,称为正交表。正交表具有两条性质:(1)每一列中各数字出现的次数都一样多。(2)任何两列所构成的各有序数对出现的次数都一样多。所以称之谓正交表。例如作一个四因素三水平的实验,按全面实验要求,须进行34=81种组合的实验,且尚未考虑每一组合的重复数。若按L9(34)正交表安排实验,只需作9次,按L18(37)正交表进行18次实验,显然大大减少了工作量。因而正交实验设计在很多领域的研究中已经得到广泛应用。本实验通过测定培养一定时间的微生物生物量来确定适宜的营养条件,通常生物量的测定方法有比浊法和直接称重法。由于本实验使用的酵母在液体深层通气发酵过程中是以均一混浊液的状态存在的,所以可以采用直接比色法进行测定。
三、实验主要仪器设备和材料
仪器设备:全恒温振荡培养箱、分光光度计、电热恒温水浴槽、电炉;
所需菌种:酵母
四、实验方法、操作步骤
1、培养基的配制(见表1、2) ,表1中的各因素水平可由组内同学商议而定。
表1 正交表试验设计

2、将上述培养基配制好以后,每250 ml三角瓶装入培养基100 ml,于121℃下灭菌30 min,冷却。
3、冷却后接种(接种量为5%),置于28℃培养箱进行培养。
4、测OD值:将接种0 h、 12 h、24 h、36 h、48 h、60 h不同时间的菌悬液摇均匀后于560nm波长、1cm比色皿中测定OD值。比色测定时,以未接种的培养基作空白对照,并将OD值填入表中,最终确定最佳培养基的组成及发酵时间。
表2 正交表实验方案

五、试验报告记载要求
1、姓名、班级、学号、试验开始日期/时间等。
2、实验的设计方案、所用的仪器名称、药品名称及重量;所使用的样品名称、来源。
3、试验操作步骤记载。
4、实验条件记载(温度、浓度、仪器条件等)。
5、实验分析。
6、实验中应注意的问题/收获。
六、思考题
1、正交实验设计法的优点?
2、本实验为什么采用560nm波长测定酵母菌悬液的光密度?如果你在实验中需要测定大肠杆菌生长的0D值,你将如何选择波长?
主要参考书
《发酵工程实验技术》,陈坚主编,化学工业出版社,20##年。
《生物工程专业实验》,贾士儒主编,中国轻工业出版社,20##年。
《生物分离与纯化技术》,辛秀兰主编,科学出版社,20##年。
《微生物学实验教程》,周德庆,高等教育出版社,20##年第二版。
《发酵工程实验指导》,吴根福主编,高等教育出版社,20##年。
