实验五 燃烧热的测定
一、实验目的
1. 掌握燃烧热的定义,了解恒压燃烧热与恒容燃烧热的差别及相互关系;
2. 熟悉热量计中主要部件的原理和作用,掌握氧弹热量计的实验技术;
3. 用氧弹热量计测定苯甲酸和萘的燃烧热;
4. 学会用雷诺图解法校正温度改变值。
二、实验原理
1mol物质完全氧化时的反应热称为燃烧热。所谓完全氧化是指C→CO2(气),H2→H2O(液),S→SO2(气),而N、卤素、银等元素变为游离状态。如在25℃苯甲酸的燃烧热为-3226.8kJ/mol:
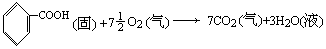
燃烧热可在恒容或恒压情况下测定。由热力学第一定律可知:在不做非膨胀功情况下,恒容燃烧热Qv=△U,恒压燃烧热Qp=△H。在氧弹热量计中测得燃烧热为Qv,而一般热化学计算用Qp,两者的关系为:
Qp=Qv+△nRT (5.1)
式中△n为反应前后生成物和反应物中气体的摩尔数之差;R为摩尔气体常数;T为反应温度(K)。
氧弹热量计的基本原理是能量守恒定律。样品完全燃烧后所释放的能量使得氧弹本身及其周围的介质和热量计附件的温度升高,则测量介质在燃烧前后体系温度的变化值,就可求算该样品的恒容燃烧热。其关系式如下:
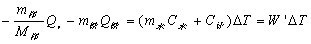 (5.2)
(5.2)
式中m样和M样分别为样品的质量和摩尔质量;Qv为样品的恒容燃烧热;m铁和Q铁是引燃铁丝的质量和单位质量燃烧热;m水和C水是以水作为测量介质时,水的质量和比热容;C计称为热量计的水当量,即除水之外,热量计升高1℃所需的热量;△T为样品燃烧前后水温的变化值。
三、仪器 试剂
氧弹热量计 1套 万用表 1个
数字式精密温差测量仪 1台 台秤 1台
氧气钢瓶 1只 温度计(0~50℃) 1支
氧气减压阀 1只 小台钟 1只
压片机 1台 烧杯(1000mL) 1只
电炉(500W) 1个 电子天平 1台
塑料桶 1个 引燃铁丝
直尺 1把 苯甲酸(分析纯)
剪刀 1把 萘(分析纯)
四、实验步骤
1. 将热量计及其全部附件加以整理并洗净。
2. 压片 取约16cm长的燃烧丝A绕成小线圈。放在干的燃烧杯中称量。另用台称称取约0.7~0.8g的苯甲酸,把燃烧丝放在苯甲酸中,在压片机中压成片状(不能压得太紧,太紧会压断燃烧丝或点火后不能燃烧),压好后样品形状如图3.1所示。将此样品放在燃烧杯中称量,从而可得样品的质量m样。
3. 充氧气 把氧弹的弹头放在弹头架上,将装有样品的燃烧杯放入燃烧杯架上,把燃烧丝的两端分别紧绕在氧弹头中的两根电极上,用万用表测量电极间的电阻值(两电极与燃烧杯不能相碰或短路)。把弹头放入弹杯中,用手将其拧紧。再用万用表检查电极之间的电阻,若变化不大,则充氧。
使用高压钢瓶时必须严格遵守操作规则。开始先用少量氧气(约0.5MPa),然后开启出口。借以赶走弹中空气。然后充入氧气(1.5MPa)。氧弹结构见图3.2。充好氧气后,再用万用表检查两电极间电阻,变化不大,将氧弹放入内筒(热量计结构参看l图3.3)
4. 调节水温 将温差测量仪探头放入外筒水中(环境),调节数字显示在“2”左右,取3000mL以上水,将温差测量仪探头放入水中,调节水温,使其低于外筒水温1K左右,用容量瓶取3000mL已调温的水注入内筒,水面盖过氧弹(两电极应保持干燥),如有气泡逸出,说明氧弹漏气,寻找原因,排除。装好搅拌头(搅拌时不可有金属磨擦声),把电极插头插紧在两电极上,盖上盖子,将温差测量仪探头插入内筒中(拔出探头之前,记下外筒水温读数;探头不可碰到氧弹)。
5. 点火 检查控制箱的开头,注意“振动、点火”开头应在振动档,旋转“点火电源”旋钮到最小。打开总电源开头,打开搅拌开头,待马达运转2min~3min后,每隔0.5min读取水温一次(精确至±0.002℃)直至连续五次水温有规律微小变化,把“振动、点火”
五、实验注意事项
1. 待测样品需干燥,受潮样品不易燃烧且称量有误。
2. 注意压片的紧实程度,太紧不容易燃烧。燃烧丝需压在片内,如浮在片子面上会引起样品熔化而脱落,不发生燃烧。
3. 在燃烧第二个样品时,内筒水须再次调节水温。
六、数据记录及处理
表1. 苯甲酸和萘燃烧热的测定
室温:20.1℃,大气压:97.6 kPa
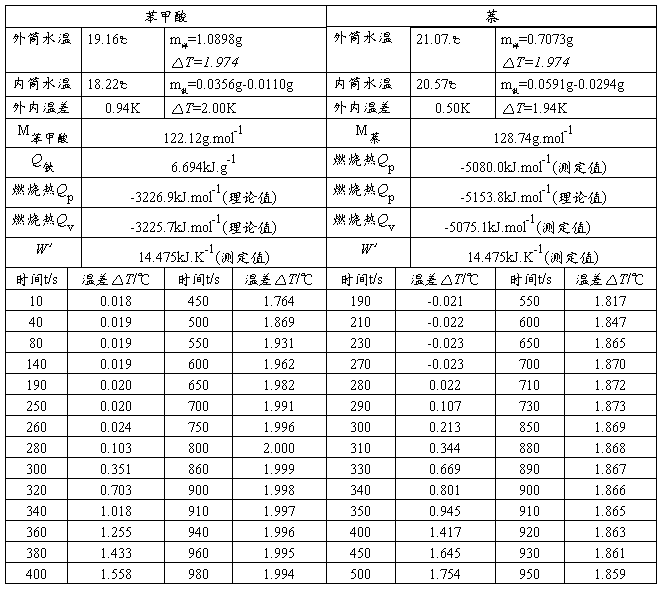
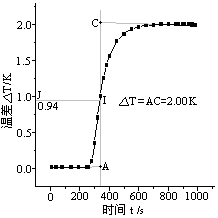
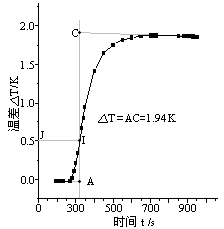
图1. 苯甲酸 图2. 萘
苯甲酸: C6H5COOH(s)+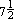 O2(g)→7CO2(g)+3H2O(l) △n= -0.5mol
O2(g)→7CO2(g)+3H2O(l) △n= -0.5mol
已知:Qp= -3226.9kJ.mol-1,Q铁=6.694 kJ.g-1
Qv=Qp-△nRT= -3226.9+0.5×8.314×(273.15+19.16)/1000= -3225.7kJ.mol-1
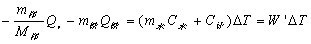
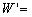 (3225.7×1.0898/122.12+6.694×0.0246)/2.00=14.475kJ.K-1
(3225.7×1.0898/122.12+6.694×0.0246)/2.00=14.475kJ.K-1
萘: C10H8(s)+12 O2(g)→10CO2(g)+4H2O(l) △n= -2.0mol
Qv= -(14.475×1.94-6.694×0.0297)×128.74/0.7073= -5075.1kJ.mol-1
Qp=Qv+△nRT= -5075.1-2.0×8.314×(273.15+21.07)/1000= -5080.0kJ.mol-1
表1. 苯甲酸和萘燃烧热的测定
室温:20.1℃,大气压:97.6 kPa
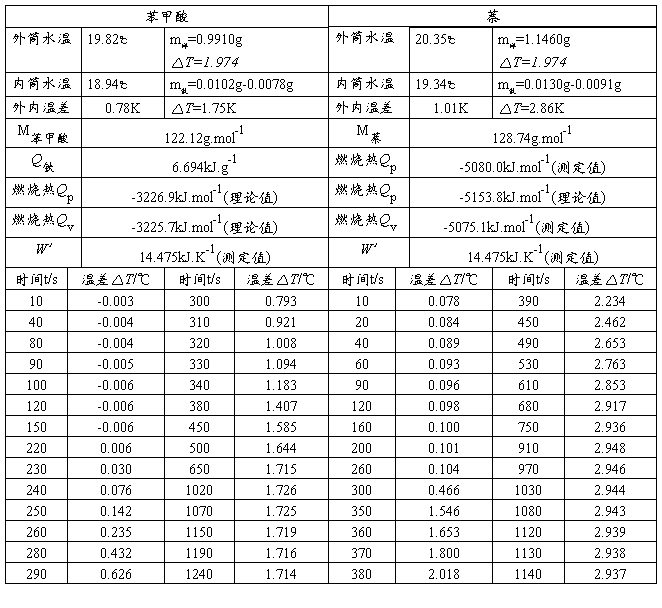
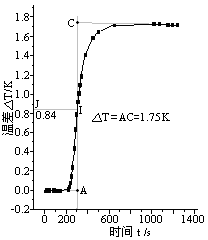
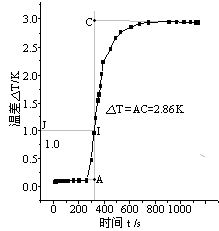
图1. 苯甲酸 图2. 萘
苯甲酸: C6H5COOH(s)+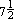 O2(g)→7CO2(g)+3H2O(l) △n= -0.5mol
O2(g)→7CO2(g)+3H2O(l) △n= -0.5mol
已知:Qp= -3226.9kJ.mol-1,Q铁=6.694 kJ.g-1
Qv=Qp-△nRT= -3226.9+0.5×8.314×(273.15+19.82)/1000= -3225.7kJ.mol-1
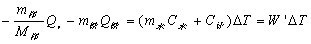
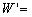 (3225.7×0.9910/122.12+6.694×0.0024)/1.75=14.967kJ.K-1
(3225.7×0.9910/122.12+6.694×0.0024)/1.75=14.967kJ.K-1
萘: C10H8(s)+12 O2(g)→10CO2(g)+4H2O(l) △n= -2.0mol
Qv= -(14.965×2.86-6.694×0.0039)×128.74/1.146= -4805.1kJ.mol-1
Qp=Qv+△nRT= -5265.3-2.0×8.314×(273.15+20.35)/1000= -4810.0 kJ.mol-1
第二篇:实验三 凝固点降低法测定摩尔质量
实验九 凝固点降低法测定摩尔质量
一、目的要求
1、 通过本实验加深对稀溶液依数性质的理解
2、 掌握溶液凝固点的测量技术
3、 用凝固点降低法测定萘的摩尔质量。
二、仪器与试剂
凝固点降低实验装置1套;数字贝克曼温度计、25m1移液管1支;电子天平l台。
分析纯的苯、萘。
三、实验原理
固体溶剂与溶液成平衡的温度称为溶液的凝固点。含非挥发性溶质的双组分稀溶液的凝固点低于纯溶剂的凝固点。凝固点降低是稀溶液依数性质的一种表现。当确定了溶剂的种类和数量后,溶剂凝固点降低值仅取决于所含溶质分子的数目。对于理想溶液,根据相平衡条件,稀溶液的凝固点降低与溶液成分关系由范特霍夫凝固点公式给出
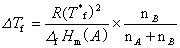
式中: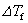 凝固点降低值,Tf* 纯溶剂的凝固点;
凝固点降低值,Tf* 纯溶剂的凝固点;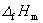 (A)摩尔凝固热,nA和nB分别为溶剂和溶质的物质的量。当溶液浓度很稀时,nB ≤ nA,,则
(A)摩尔凝固热,nA和nB分别为溶剂和溶质的物质的量。当溶液浓度很稀时,nB ≤ nA,,则
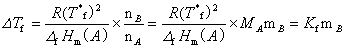
其中MA为溶剂的摩尔质量;mB为溶质的质量摩尔浓度;Kf即称为质量摩尔凝固点降低常数。
若已知某种溶剂的凝固点降低常数 Kf ,并测得溶剂和溶质的质量分别为mA , mB的稀溶液的凝固点降低值DTf,则可通过下式计算溶质的摩尔质量MB。
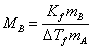
式中Kf的单位为K· kg·mol-1
凝固点降低值的大小,直接反映了溶液中溶质有效质点的数目。如果溶质在溶液中有离解、缔合、溶剂化和配合物生成等情况,这些均影响溶质在溶剂中的表观分子量。因此凝固点降低法也可用来研究溶液的一些性质,例如电解质的电离度、溶质的缔合度、活度和活度系数等。
纯溶剂的凝固点为其液相和固相共存的平衡温度。若将液态的纯溶剂逐步冷却,在未凝固前温度将随时间均匀下降,开始凝固后因放出凝固热而补偿了热损失,体系将保持液一固两相共存的平衡温度而不变,直至全部凝固,温度再继续下降。其冷却曲线如图C6.1中1所示。但实际过程中,当液体温度达到或稍低于其凝固点时,晶体并不析出,这就是所谓的过冷现象。此时若加以搅拌或加入晶种,促使晶核产生,则大量晶体会迅速形成,并放出凝固热,使体系温度迅速回升到稳定的平衡温度;待液体全部凝固后温度再逐渐下降。冷却曲线如图C6.1中。
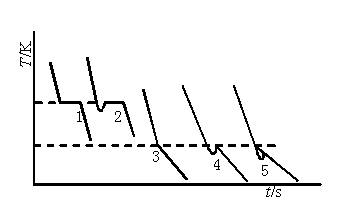
图C6.1 纯溶剂和溶液的冷却曲线
溶液的凝固点是该溶液与溶剂的固相共存的平衡温度,其冷却曲线与纯溶剂不同。当有溶剂凝固析出时,剩余溶液的浓度逐渐增大,因而溶液的凝固点也逐渐下降。因有凝固热放出,冷却曲线的斜率发生变化,即温度的下降速度变慢,如图C6.1中3所示。本实验要测定已知浓度溶液的凝固点。如果溶液过冷程度不大,析出固体溶剂的量很少,对原始溶液浓度影响不大,则以过冷回升的最高温度作为该溶液的凝固点,如图C6.1中4所示。
在测量过程中应该设法控制适当的过冷程度,一般可通过控制寒剂的温度、搅拌速度等方法来达到。
确定凝固点的另一种方法是外推法,如图C6.2所示,首先记录绘制纯溶剂与溶液的冷却曲线,作曲线后面部分(已经有固体析出)的趋势线并延长使其与曲线的前面部分相交,其交点就是凝固点。
四、实验步骤
1、溶剂为苯,测定萘的摩尔质量。
2、先测苯的凝固点,记录在数据记录表格中。
3、苯的凝固点为5.45℃,苯的Kf=5.12 K· kg·mol-1。苯的密度随室温的变化按下式计算:
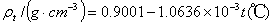
4、称取0.2-0.3克萘。粗称1克,压片,分为四份,每组一份,再用天平精确称量并记录。
5、本实验关键在于搅拌的速度,开始缓慢搅拌,至接近近似凝固点时,改为急速搅拌,温度开始上升时,立即缓慢搅拌,直至温度稳定后读数。
五、数据记录与处理
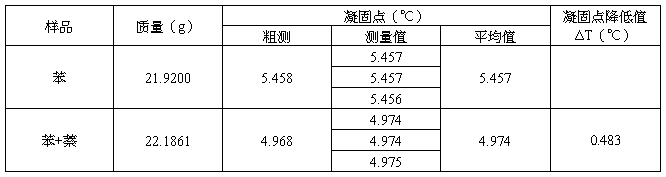
六、实验数据处理:
m苯=21.9200g
m苯+萘=22.1861g
MB=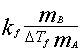 =
=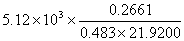 =128.68 g/mol
=128.68 g/mol
七、结论
萘的摩尔质量是128.68g/mol。
