实验三 凝固点降低法测定摩尔质量预习思考题
1、为了提高实验的准确度是否可用增加溶质浓度的方法增加值?
答案:不可以,溶质加的太多,不是稀溶液,就不能符合凝固点降低公式了。
2、冰浴温度过高或过低有什么不好?
答案:过高会导致冷却太慢,过低则测不出正确的凝固点。
3、搅拌速度过快和过慢对实验有何影响?
答案:在温度逐渐降低过程中,搅拌过快,不易过冷,搅拌过慢,体系温度不均匀。温度回升时,搅拌过快,回升最高点因搅拌热而偏听偏高;过慢,溶液凝固点测量值偏低。所以搅拌的作用一是使体系温度均匀,二是供热(尤其是刮擦器壁),促进固体新相的形成。
4、根据什么原则考虑加入溶质的量,太多或太少会有何影响?
答案:根据稀溶液依数性,溶质加入量要少,而对于称量相对精密度来说,溶质又不能太少。
5、凝固点降低法测定摩尔质量使用范围内如何?
答案::稀溶液
6、凝固点下降是根据什么相平衡体系和哪一类相线?
答案:二组分低共熔体系中的凝固点降低曲线,也称对某一物质饱和的析晶线
7、为什么要用空气套管,不用它对实验结果有何影响?
答案:减缓降温速率,防止过准予发生。
8、若溶质在溶液中有离解现象,对摩尔质量的测定值有何影响?
答案:因为凝固点下降多少直接影响,直接反映了溶液中溶质的质点数,所以当有离解时质点数增加,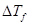 变大,而从公式
变大,而从公式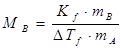 可看出,
可看出,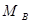 会偏小。
会偏小。
9、为什么要初测物质的凝固点?
答案:防止过冷出现,节省时间
10、为什么会产生过冷现象?如何控制过冷程度?
答案:由于新相难以生成,加入晶种或控制搅拌速度
11、测定溶液的凝固点时必须减少过冷现象吗?
答案:若过冷严重,温度回升的最高温度不是原尝试溶液的凝固点,测得的凝固点偏低。
12、测定凝固点时,纯溶剂温度回升后有一恒定阶段,而溶液没有,为什么?
答案:由于随着固态纯溶剂从溶液中的不断析出,剩余溶液的浓度逐渐增大,因而剩余溶液与溶剂固相的平衡温度也在逐渐下降,在步冷曲线上得不到温度不变的水平段,只出现折点.
13、选做溶剂时,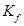 大的灵敏度高还是
大的灵敏度高还是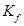 小的灵敏度高?
小的灵敏度高?
答案:大的
14、测定溶液凝固点时,过冷温度不能超过多少度?
答案: 0.5,最好是0.2,
15、溶剂和溶质的纯度与实验结果有关吗?
答案:有
16、如不用外推法求凝固点,一般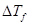 会偏大还是偏小?
会偏大还是偏小?
答案:大
17、一般冰浴温度要求不低于溶液凝固点几度为宜?
答案:2-3℃
18、测定溶液的凝固点时析出固体较少,测得的凝固点准确吗?
答案:准确,因为溶液的凝固点随答:着溶剂的析出而不断下降。析出的固体少测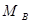 越准确。
越准确。
19、若溶质在溶液中有缔合现象,对摩尔质量的测定值有何影响?
答案:因为凝固点下降多少直接影响,直接反映了溶液中溶质的质点数,所以当有缔合时时质点数减少,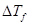 变小,而从公式
变小,而从公式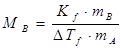 可看出,
可看出,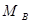 会偏大。
会偏大。
20、测定溶液的凝固点时析出固体较多,测得的凝固点准确吗?
答案:不准确,因为溶液的凝固点答:随着溶剂的析出而不断下降。析出的固体多会使凝固点下降的多,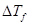 变大,所测
变大,所测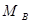 会偏小。
会偏小。
第二篇:实验八 凝固点降低法测定摩尔质量
实验八 凝固点降低法测定摩尔质量
一、实验目的
1. 用凝固点降低法测定萘的摩尔质量。
2. 掌握溶液凝固点的测量技术,加深对稀溶液依数性质的理解。
二、实验原理
当稀溶液凝固析出纯固体溶剂时,则溶液的凝固点低于纯溶剂的凝固点,其降低值与溶液的质量摩尔浓度成正比。即
ΔT=Tf* -Tf = Kf mB (1)
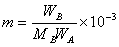
式中,MB为溶质的分子量。将该式代入(1)式,整理得:
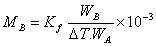 (2)
(2)
若已知某溶剂的凝固点降低常数Kf值,通过实验测定此溶液的凝固点降低值ΔT,即可计算溶质的分子量MB。通常测凝固点的方法是将溶液逐渐冷却,但冷却到凝固点,并不析出晶体,往往成为过冷溶液。然后由于搅拌或加入晶种促使溶剂结晶,由结晶放出的凝固热,使体系温度回升,当放热与散热达到平衡时,温度不再改变。此固液两相共存的平衡温度即为溶液的凝固点。
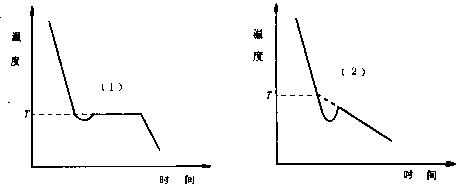
图1. 溶剂(1)与溶液(2)的冷却曲线
三、仪器药品
1. 仪器
凝固点测定仪1套; 烧杯2个;精密温差测量仪1台;放大镜1个;普通温度计(0℃~50℃)1支;压片机1台;移液管(25mL)1支。
 2. 药品
2. 药品
环已烷(或苯),萘,粗盐,冰。
四、实验步骤
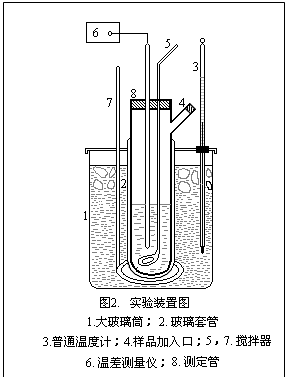
1.按图2所示安装凝固点测定仪,注意测定管、搅拌棒都须清洁、干燥,温差测量仪的探头,温度计都须与搅拌棒有一定空隙。防止搅拌时发生摩擦。
2. 调节寒剂的温度,使其低于溶剂凝固点温度2~3℃,并应经常搅拌,不断加入碎冰,使冰浴温度保持基本不变。
3. 调节温差测量仪,使探头在测量管中时,数字显示为“0”左右。
4. 准确移取25.00mL溶剂,小心加入测定管中,塞紧软木塞,防止溶剂挥发,记下溶剂的温度值。取出测定管,直接放入冰浴中,不断移动搅拌棒,使溶剂逐步冷却。当刚有固体析出时,迅速取出测定管,擦干管外冰水,插入空气套管中,缓慢均匀搅拌,观察精密温差测量仪的数显值,直至温度稳定,即为苯的凝固点参考温度。取出测定管,用手温热,同时搅拌,使管中固体完全熔化,再将测定管直接插入冰浴中,缓慢搅拌,使溶剂迅速冷却,当温度降至高于凝固点参考温度0.5℃时,迅速取出测定管,擦干,放入空气套管中,每秒搅拌一次,使溶剂温度均匀下降,当温度低于凝固点参考温度时,应迅速搅拌(防止过冷超过0.5℃),促使固体析出,温度开始上升,搅拌减慢,注意观察温差测量仪的数字变化,直至稳定,此即为溶剂的凝固点。重复测量三次。要求溶剂凝固点的绝对平均误差小于±0.003℃。
5. 溶液凝固点的测定,取出测定管,使管中的溶剂熔化,从测定管的支管中加入事先压成片状的0.2~0.3g的萘,待溶解后,用上述方法测定溶液的凝固点。先测凝固点的参考温度,再精确测之。溶液凝固点是取过冷后温度回升所达到的最高温度,重复三次,要求凝固点的绝对平均误差小于±0.003℃。
五、注意事项
1. 搅拌速度的控制是做好本实验的关键,每次测定应按要求的速度搅拌,并且测溶剂与溶液凝固点时搅拌条件要完全一致。
2. 寒剂温度对实验结果也有很大影响,过高会导致冷却太慢,过低则易出现过冷现象而测不出正确的凝固点。
3. 测定凝固点温度时,注意防止过冷温度超过0.5℃,为了减少过冷度,可加入少量溶剂的微小晶种,前后加入晶种大小应尽量一致。
六、数据记录及处理
表1. 凝固点降低法测定摩尔质量的实验数据 溶剂温度t=21.06℃

ρ环已烷(g·cm-3)=0.7971-0.8879×10-3t=0.7971-0.8879×10-3×21.06=0.7784g·cm-3
WA=ρAVA=25.00×0.7784=19.46g
萘的摩尔质量MB:128.17 g·mol-1(理论值)
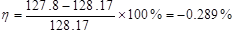 相对误差:
相对误差:
表1. 凝固点降低法测定摩尔质量的实验数据 溶剂温度t=26.96℃
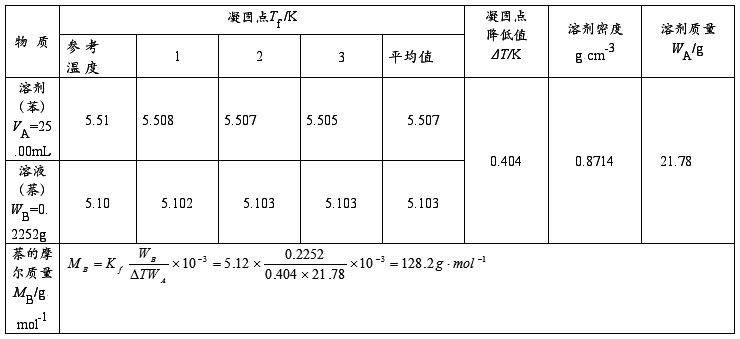
ρ苯(g·cm-3)=0.90005-1.0638×10-3t=0.90005-1.0638×10-3×26.96=0.8714g·cm-3
WA=ρAVA=25.00×0.8714=21.78g
萘的摩尔质量MB:128.17 g·mol-1(理论值)
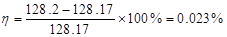 相对误差:
相对误差:
七、思考题
1. 为什么要先测近似凝固点?
答:主要是为了控制过冷程度。当温度冷却至凝固点时要通过急速搅拌,防止过冷超过要求,促使晶体析出。
2. 根据什么原则考虑加入溶质的量?太多或太少影响如何?
答:溶质的加入量应控制在凝固点降低0.3℃左右。过多,溶液的凝固点降低太多,析出溶剂晶体后,溶液的浓度变化大,凝固点也随之降低,不易准确测定其凝固点。过少,溶液的凝固点降低少,相对测定误差也大。
3. 为什么测定溶剂的凝固点时,过冷程度大一些对测定结果影响不大,而测定溶液凝固点时却必须尽量减少过冷现象?
答:对于纯溶剂,过冷现象存在时,析出大量晶体并不改变溶剂浓度,所以其凝固点不变。对于溶液,过冷现象存在时,析出大量晶体会改变溶液浓度,而溶液的凝固点随浓度增大而下降,所以溶液要尽量减少过冷现象,保持溶液浓度基本不变。
