华南师范大学实验报告
学生姓名 吴俊烽 学 号 20112401019
专 业 化学教育 年级班级 11化四
课程名称 物理化学实验 实验项目 凝固点降低法测定摩尔质量
指导老师 肖信 时 间 2013年11月26日
【实验目的】
1.用凝固点降低法测定尿素的摩尔质量;
2.掌握固点降低法测摩尔质量的原理;
3. 理解、绘制冷却曲线,并通过冷却曲线校正凝固点。
【实验原理】
假设溶质在溶液中不发生缔合和分解,也不与固态纯溶剂生成固溶体,则由热力学理论出发,可以导出理想稀薄溶液的凝固点降低值?Tf(即纯溶剂和溶液的凝固点之差)与溶质质量摩尔浓度bB之间的关系:
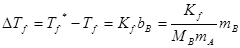 (1)
(1)
由此可导出计算溶质摩尔质量MB的公式: (2)
(2)
以上各式中: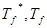 分别为纯溶剂、溶液的凝固点,单位K;mA、mB分别为溶剂、溶质的质量,单位kg;Kf为溶剂的凝固点降低常数,与溶剂性质有关,单位K·kg·mol-1;若已知溶剂的Kf值,通过实验测得?Tf,便可用式(2)求得MB。也可由式(1)通过?Tf-mB的关系,线性回归以斜率求得MB。
分别为纯溶剂、溶液的凝固点,单位K;mA、mB分别为溶剂、溶质的质量,单位kg;Kf为溶剂的凝固点降低常数,与溶剂性质有关,单位K·kg·mol-1;若已知溶剂的Kf值,通过实验测得?Tf,便可用式(2)求得MB。也可由式(1)通过?Tf-mB的关系,线性回归以斜率求得MB。
通常测定凝固点的方法是将溶液逐渐冷却,使其结晶。但是,实际上溶液冷却到凝固点,往往并不析出晶体,这是因为新相形成需要一定的能量,故结晶并不析出,这就是所谓过冷现象。然后由于搅拌或加入晶种促使溶剂结晶,由结晶放出的凝固热,使体系温度回升。从相律看,溶剂与溶液的冷却曲线形状不同。对纯溶剂,固-液两相共存时,自由度f=1-2+1=0,冷却曲线出现水平线段,其形状如图1(1)所示。对溶液,固-液两相共存时,自由度f=2-2+1=1,温度仍可下降,但由于溶剂凝固时放出凝固热,使温度回升,回升到最高点又开始下降,所以冷却曲线不出现水平线段此时应按图1(3)所示方法加以校正。

(1)理想状态下的溶剂 (2)有过冷的溶剂 (3)有过冷的溶液
【仪器和试剂】
凝固点测定仪,精密电子温差测量仪,电子天平,移液管(50mL),环己烷,萘
【操作步骤】
1. 打开测温仪,调节寒剂温度低于溶液凝固点2-3℃(约4.5-3.5℃),然后将空气套管插入槽中。
2. 准确量取25ml环己烷加入凝固点测试试管中,塞紧橡胶塞,插入传感器
3. 将凝固点试管插入寒剂槽中,观察温度和温差,待温度在10℃以下且温差为正值时按下锁定键,温度稳定时,此温度即为环己烷的凝固点
4. 取出凝固点测定试管,使环己烷熔化(最好留有少量晶种),再次插入寒剂中,搅拌。当温度降低到高于初测凝固点的0.5℃,把试管移到空气管中,每10秒记录一次温度
5. 重复第4部2次
6. 称取约0.23g的萘加入凝固点测定试管中,完全溶解后,重复3、4部
【数据的记录和处理】
1.由水的密度,计算所取水的重量WA。
2.将饰演数据填入表中。
3.计算分子量,并计算域理论值的相对误差。
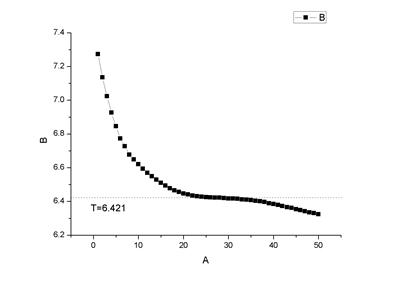
环己烷 1
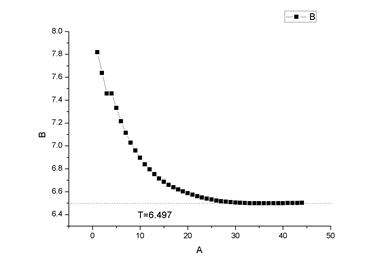
环己烷 2

环己烷 3
================================================================================
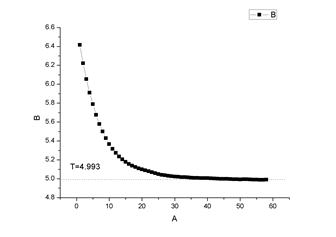
环己烷+萘 1
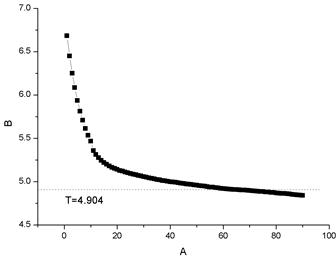
环己烷+萘 2
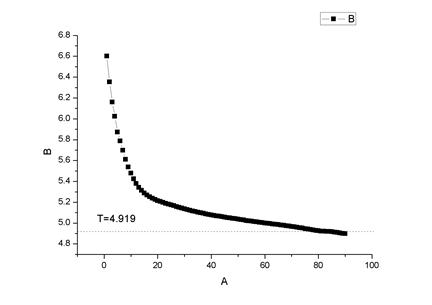
环己烷+萘 3

得萘的相对分子质量为 144.63
文献值为 128.18
相对误差=12.83%
【结果讨论】
1. 从温度变化曲线可以看到,没有出现较明显的“平台”,可能是
A、 寒剂的温度太低,导致溶液的温度下降得太快,溶液到达凝固点时稳定的时间太短,很快就继续降温。
B、 也可能是由于,环己烷和萘都含有较多的杂质。
?上述两点也可能是相对误差较大的原因
2. 从环己烷2和环己烷3的曲线可以看到,温度在到达凝固点后上升了,这是由于溶液凝固是放热过程,而它放热速度大于寒剂吸热的速度,因此导致温度上升。
【思考题】
1.根据什么原则考虑加入溶质的量?太多或太少影响如何?
答:根据稀溶液依数性, 溶质加入量要少;太多不符合稀溶液,太少凝固点下不明显。
2.什么叫凝固点?凝固点降低的公式在什么条件下才适用?它能否用于电解质溶液?
答:固体溶剂与溶液成平衡的温度称为溶液的凝固点。含非挥发性溶质的双组分稀溶液的凝固点低于纯溶剂的凝固点,当确定了溶剂的种类和数量后,溶剂凝固点的降低值仅取决与所含溶质分子的数目。对于理想溶液或浓度很稀的溶液,根据范特霍夫凝固点降低公式知道:在溶液浓度很稀时,如果溶质与溶剂不生成固溶体,溶液的凝固点降低值 与溶质的质量摩尔浓度 (mol·kg-1)成正比。一般只适用于强电解质稀溶液。其次凝固点不应太高或太低,应在常温下易达到。
【参考文献】
[1]何广平,南俊民,孙艳辉等.物理化学实验.化学工业出版社.2007.12
第二篇:物理化学实验报告 - 凝固点降低法测定摩尔质量
C6 凝固点降低法测定摩尔质量
——实验日期:年月日
姓名: 学号: 班级:
一、 实验目的
(一)用凝固点降低法测定萘的摩尔质量。
(二)掌握精密电子温差仪的使用方法。
二、 原理及实验公式
非挥发性溶质二组分溶液,其稀溶液具有依数性,凝固点降低就是依数性的一种表现。根据凝固点降低的数值,可以求出溶质的摩尔质量。
在溶剂中加入溶质时,溶液的凝固点比纯溶剂的凝固点低,其凝固点降低值Δ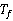 与溶质的质量摩尔浓度
与溶质的质量摩尔浓度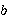 成正比。
成正比。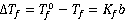
式中,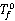 为纯溶剂的凝固点;
为纯溶剂的凝固点;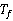 为浓度为
为浓度为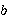 的溶液的凝固点;
的溶液的凝固点;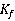 为溶剂的凝固点降低常数。
为溶剂的凝固点降低常数。
若已知某种溶剂的凝固点降低常数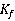 ,并测得溶剂和溶质的质量分别为
,并测得溶剂和溶质的质量分别为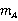 和
和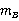 的稀溶液的凝固点降低值Δ
的稀溶液的凝固点降低值Δ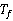 ,则可以通过下式计算溶质的摩尔质量
,则可以通过下式计算溶质的摩尔质量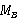 。
。
式中,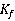 的单位为
的单位为 。
。
三、 凝固点的确定方法
(一)纯溶剂的凝固点确定方法
纯溶剂的凝固点为其液相和固相共存的平衡温度。若将液态的纯溶剂逐步冷却,在未凝固前温度将随时间均匀下降。开始凝固后因放出凝固热而补偿了热损失,体系将保持液-固两相共存的平衡温度而不变,直到全部凝固,温度再继续下降。冷却曲线如图1中1所示。
但在实际过程中,液体温度达到或稍低于其凝固点时,晶体并不析出,此现象即过冷现象。此时若加以搅拌或加入晶种,促使晶核产生,则大量晶体迅速形成,并放出凝固热,使体系温度迅速回升到稳定的平衡温度,待液体全部凝固后,温度再逐渐下降。冷却曲线如图1中2所示。
(二)溶液的凝固点确定方法
溶液的凝固点是该溶液与溶剂的固相共存的平衡温度,冷却曲线与纯溶剂不同。当有溶剂凝固析出时,剩余溶液的浓度逐渐增大,因而溶液的凝固点也逐渐下降。因有凝固热放出,冷却曲线的斜率发生变化,即温度的下降速度变慢,如图1中3所示。本实验要求测定已知浓度溶液的凝固点。如果溶液过冷程度不大,析出固体溶剂的量很少,对原始溶液浓度影响不大,则以过冷回升的最高温度作为该溶液的凝固点,如图1中4所示。
确定凝固点的另一种方法是外推法,如图2所示,首先记录绘制纯溶剂与溶液的冷却曲线,作曲线后面部分(已经有固体析出)的趋势线并延长使其与曲线的前面部分相交,其交点即为凝固点。
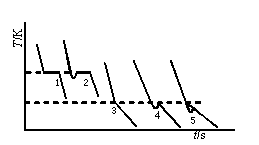
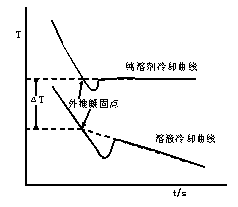
图1 纯溶剂和溶液的冷却曲线 图2 外推法求纯溶剂和溶液的凝固点
四、 仪器和试剂
(一)仪器
1.凝固点管、凝固点管塞、凝固点管套管;
2.小搅拌杆、大搅拌杆;
3.水浴缸、水浴缸盖;
4.精密电子温差仪、温度计;
5.移液管(25mL)、洗耳球;
6.天平(0.001g)。
(二)工具
锤子、毛巾、滤纸、冰块;
(三)试剂
环己烷(A.R)、萘(A.R.)
五、 实验步骤
(一)如图安装实验装置
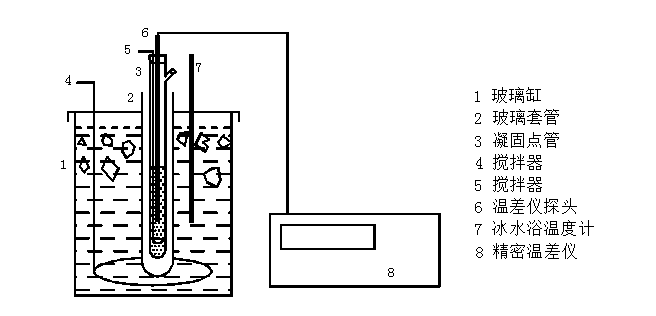
(二)测定纯溶剂环己烷的凝固点
1. 取25.00mL环己烷→移液管→凝固点管;
2. 将精密温差仪探头插入凝固点管,均匀搅拌(慢档),冷却至温度显示基本不变;
3. 按面板上的“置零”钮,此时温差仪显示“0.000”;
4. 拿出冰水浴中的凝固点管(用卫生纸擦干、擦净),用手捂热至结晶完全熔化(精密显示仪约6-7℃);
5. 将凝固点管放入套管,套管放入冰水浴搅拌(慢档),每30秒记录温度(以精密温差仪的报时为准);
6. 当液体开始析出晶体时(不直接观察样品管,观察精密温差仪示数下降开始变慢时)继续读数10分钟;
7. 重复步骤4、5、6 一次;
8. 测量结束后,保留凝固点管内环己烷用作接下来测量实验中萘的溶剂。
(三)测定萘的环己烷溶液的凝固点
1. 用分析天平称取萘0.1000-0.1200g(实测0.1193g)→实验步骤(二)中保留的凝固点管→搅拌至完全溶解;
2. 将凝固点管放入套管,套管放入冰水浴搅拌(慢档),每30秒记录温度(以精密温差仪的报时为准);
3. 当液体开始析出晶体时(不直接观察样品管,观察精密温差仪示数下降开始变慢时)继续读数10分钟;
4. 拿出冰水浴中的凝固点管(用卫生纸擦干、擦净),用手捂热至结晶完全熔化(精密显示仪约6-7℃);
5. 重复步骤2、3 一次;
6. 测量结束,实验完毕。整理仪器,清洗凝固点管、搅拌器、温差仪探头,将环己烷倒入废液瓶。
注意事项:
1. 测温探头擦干后再插入凝固点管。不使用时注意妥善保护测温探头。
2. 加入固体样品时要小心,勿粘在壁上或撒在外面,以保证量的准确。
3. 熔化样品和溶解溶质时切勿升温过高,以防超出温差仪量程。
六、 数据记录及处理
(一)溶剂(环己烷)数据处理与计算
数据记录:
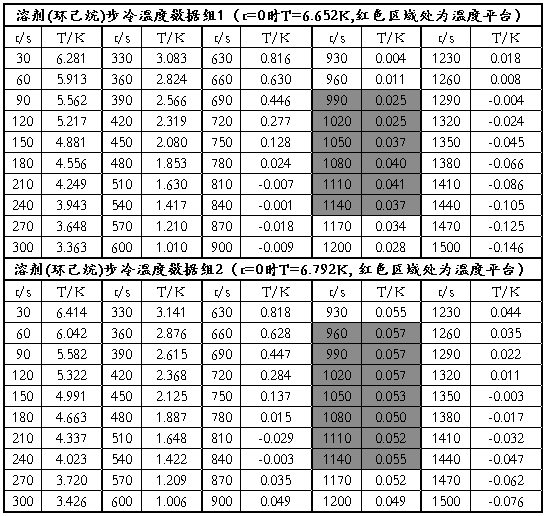
数据处理:
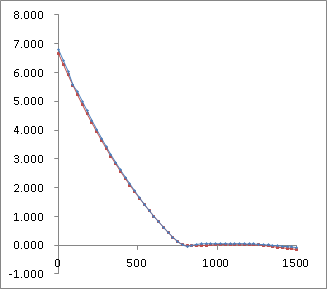
纯溶剂(环己烷)步冷曲线
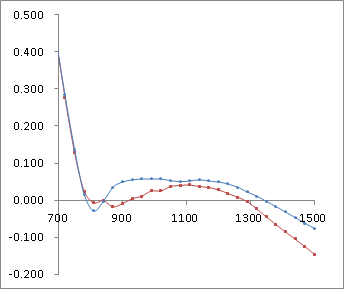
纯溶剂(环己烷)平台范围步冷曲线
注:红色折线为溶剂(环己烷)温度数据组1,蓝色折线为溶剂(环己烷)温度数据组2。
解:观察图像,得t=1050s、1080s、1110s时的数据1、2值最接近,取作平台平均温度的计算。
由数据组1中t=1050s、1080s、1110s时的数据求得平均平台温度为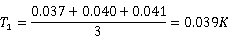
由数据组2中t=1050s、1080s、1110s时的数据求得平均平台温度为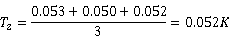
取平均值得
(二)溶液凝固点(萘的环己烷溶液)数据处理与计算
数据记录:
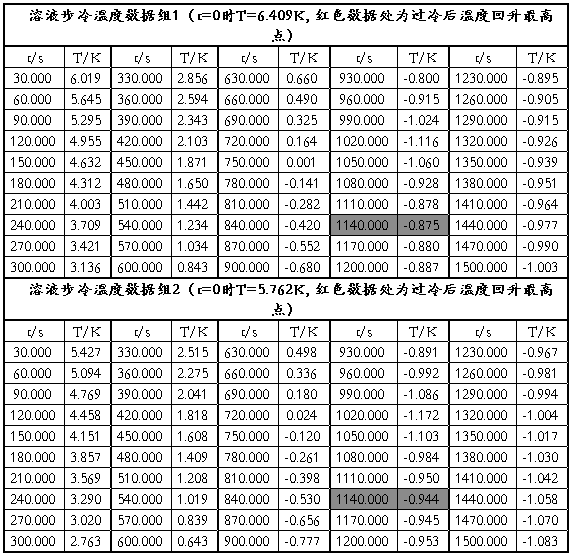
数据处理:
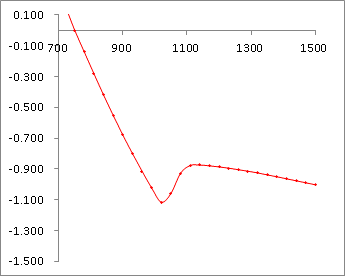

数据组1外推法求凝固点步冷曲线
数据组2外推法求凝固点步冷曲线
数据组1:
溶液至过冷前(t < 1020s)步冷数据点拟合直线方程为:y = -0.0043x + 3.3243
溶液完全凝固后(t > 1140s)步冷数据点拟合直线方程为:y = -0.0004x - 0.4475
交点处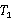 = -0.836K
= -0.836K
数据组2:
溶液至过冷前(t < 1020s)步冷数据点拟合直线方程为:y = -0.0040x + 3.0749
溶液完全凝固后(t > 1170s)步冷数据点拟合直线方程为:y = -0.0004x - 0.4466
交点处 = -0.838K
= -0.838K
取平均值得:
(三)萘的摩尔质量计算与误差分析
摩尔质量计算:
测得实验室室温为15℃
则实验溶剂环己烷质量为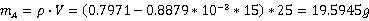
溶质萘的质量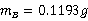
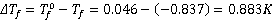
查表得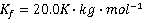
由公式得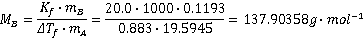
误差计算: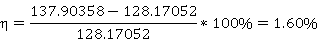
产生误差(测定结果偏大)的原因可能有以下几点:
1. 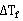 测定值偏小
测定值偏小
2. 溶质在溶液中缔合或生成配合物
七、 思考题
(一) 如果溶质在溶液中离解、缔合和生成配合物,对摩尔质量测量值如何影响?
答:溶质在溶液中离解,就会使有效质点增多,导致溶液凝固点降低大小比理论值更大,由公式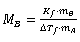 得:
得: 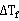 增大,则
增大,则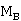 减小,摩尔质量测定值偏小;溶质在溶液中缔合或生成配合物则会使摩尔质量测定值偏大。
减小,摩尔质量测定值偏小;溶质在溶液中缔合或生成配合物则会使摩尔质量测定值偏大。
(二) 加入溶质的量太多或太少有何影响?
答:加入溶质太少,溶液凝固点下降不会呈现公式所呈现的比例关系,实际值会比公式计算所得理论值小,所以使摩尔质量测定值偏大;加入溶质太多,实际值会比公式计算所得理论值大,所以使摩尔质量测定值偏小。
(三)利用反应物、产物的某物理性质间接测量浓度进行动力学研究,应满足什么条件?
答:晶体内分子或原子的排列是有规律的,而液体内则是无规律的。而结晶中心有助于这种无序到有序的转化。液体越纯净,结晶中心越难形成。如果降低至凝固点以下仍未形成,就会产生过冷现象。
