凝固点降低法测定摩尔质量
一、实验目的
1.用凝固点降低法测定萘的摩尔质量;
2.学会用步冷曲线对溶液凝固点进行校正;
3.通过本实验加深对稀溶液依数性的认识。
二、实验原理
稀溶液具有依数性,凝固点降低是依数性的一种表现,它与溶液质量摩尔浓度的关系为:

其中, 为凝固点降低值,
为凝固点降低值, 、
、 分别为纯溶剂、溶液的凝固点,
分别为纯溶剂、溶液的凝固点, 为溶液质量摩尔浓度,
为溶液质量摩尔浓度, 为凝固点降低常数,它只与所用溶剂的特性有关。如果稀溶液是由质量为
为凝固点降低常数,它只与所用溶剂的特性有关。如果稀溶液是由质量为 的溶质溶于质量为
的溶质溶于质量为 的溶剂中而构成,则上式可写为:
的溶剂中而构成,则上式可写为:

即

式中:  ——溶剂的凝固点降低常数(单位为
——溶剂的凝固点降低常数(单位为 );
);
 ——溶质的摩尔质量(单位为
——溶质的摩尔质量(单位为 )。
)。
如果已知溶液的 值,则可通过实验测出溶液的凝固点降低值
值,则可通过实验测出溶液的凝固点降低值 ,利用上式即可求出溶质的摩尔质量。
,利用上式即可求出溶质的摩尔质量。
实验中,要测量溶剂和溶液的凝固点之差。对于纯溶剂如图1(a)所示,将溶剂逐渐降低至过冷(由于新相形成需要一定的能量,故结晶并不析出),温度降低至一定值时出现结晶,当晶体生成时,放出的热量使体系温度回升,而后温度保持相对恒定。对于纯溶剂来说,在一定压力下,凝固点是固定不变的,直到全部液体凝固成固体后才会下降。相对恒定的温度即为凝固点。
对于溶液来说,除温度外还有溶液浓度的影响。当溶液温度回升后,由于不断析出溶剂晶体,所以溶液的浓度逐渐增大,凝固点会逐渐降低。因此,凝固点不是一个恒定的值。如把回升的最高点温度作为凝固点,这时由于已有溶剂晶体析出,所以溶液浓度已不是起始浓度,而大于起始浓度,这时的凝固点不是原浓度溶液的凝固点。要精确测量,应测出步冷曲线,按下一页图1(b)所示方法,外推至 校正。
校正。

图1 溶剂和溶液的步冷曲线
三、实验仪器与试剂
仪器:冰点下降装备一套;贝克曼温度计;普通温度计;烧杯;移液管(25ml)。
试剂:苯;萘;冰。
四、实验步骤
1.将仪器洗净烘干,并使搅拌棒能自由操作,不碰温度计,冰槽中放入适量冷水和冰块,使温度保持在2—3℃。
2.纯苯(溶剂)凝固点测定
用移液管移取25ml苯加入内管中,调整温度计位置使水银全部淹没在苯中,搅动苯液,使温度逐渐降低,当温度回升时停止搅拌,观察温度计读数,待温度恒定时记下温度,此即为苯的凝固点。将内管取出,待苯融化后重复测定两次。各次测定值之差应不大于0.005℃,取平均值为苯的凝固点。
3.溶液凝固点的测定
准确称取0.5g左右纯萘,加入盛有苯的内管中,待溶解后,用上述方法测该溶液的凝固点。溶液温度回升时达不到恒定,所以取温度的最高点作为溶液的凝固点。重复测定两次,各次测定之差不大于0.005℃。取平均值作为溶液的凝固点。
五、数据处理
1.求室温下苯的质量
实验中溶剂苯的密度 ,现知室温19.56℃,则
,现知室温19.56℃,则 ,所以苯的质量m=21.98g。
,所以苯的质量m=21.98g。
2.分别测溶剂凝固点和溶液凝固点
表1 溶剂和溶液凝固点测量数据记录表

其中溶液中含有萘0.4956g。
3.绘制溶剂的步冷曲线并求其凝固点

图2 纯溶剂步冷曲线
根据步冷曲线可以求得苯的凝固点Tf=5.484℃。
4.绘制溶液的步冷曲线并求溶液的凝固点

图3 溶液的步冷曲线

图4 步冷曲线有效数据区线性拟合结果
两条曲线的线性拟合,求解两直线交点的坐标(采用直接取点法),可得溶液凝固点的温度值为:Tf = 4.586℃
综上,用步冷曲线法得到溶液凝固点为4.586℃。
5.计算萘的相对分子质量和测定的相对误差
由3、4可得 ℃
℃
再由公式 ,求得M=128.56。
,求得M=128.56。
而查表得到萘的相对分子质量为128.18,所以得到测定的相对误差为 。
。
六、思考题
1. 若溶质在溶液中产生解离、缔合等现象时,对实验结果有何影响?
发生解离时 会偏小;发生缔合时
会偏小;发生缔合时 会偏大。
会偏大。
2.测凝固点时,纯溶剂温度回升后有一恒定阶段,而溶液则没有,为什么?
由于随着固态纯溶剂从溶液中的不断析出,剩余溶液的浓度逐渐增大,因而剩余溶液与溶剂固相的平衡温度也在逐渐下降,在步冷曲线上得不到温度不变的水平段,只出现折点。
3.溶液浓度太稀或太浓对实验结果有什么影响?为什么?
若溶液太稀,溶液的凝固点降低少,相对测定误差也大;若溶液太浓,溶液不符合凝固点降低公式。
4.冰槽温度调节在2~3℃之间,过高或过低有什么不好?
过高会导致冷却太慢,过低造成过度过冷测不出正确的凝固点。
第二篇:凝固点降低法测定萘摩尔质量
凝固点降低法测定摩尔质量
——实验日期:20xx年12月27日
姓名:王海全学号:1215030210 班级:矿物加工工程1202
一、 实验目的
(一)用凝固点降低法测定萘的摩尔质量。
(二)加深对稀溶液依数性质的理解。
二、 实验原理
非挥发性溶质二组分溶液,其稀溶液具有依数性,凝固点降低就是依数性的一种表现。根据凝固点降低的数值,可以求出溶质的摩尔质量。
在溶剂中加入溶质时,溶液的凝固点比纯溶剂的凝固点低,其凝固点降低值Δ??与溶质的质量摩尔浓度?成正比。
Δ??=??0???=???
式中,??0为纯溶剂的凝固点;??为浓度为?的溶液的凝固点;??为溶剂的凝固点降低常数。 若已知某种溶剂的凝固点降低常数??,并测得溶剂和溶质的质量分别为??和??的稀溶液的凝固点降低值Δ??,则可以通过下式计算溶质的摩尔质量??。
??=
式中,??的单位为?·??·????1。 ??·?? ??
三、 凝固点的确定方法
(一)纯溶剂的凝固点确定方法
纯溶剂的凝固点为其液相和固相共存的平衡温度。若将液态的纯溶剂逐步冷却,在未凝固前温度将随时间均匀下降。开始凝固后因放出凝固热而补偿了热损失,体系将保持液-固两相共存的平衡温度而不变,直到全部凝固,温度再继续下降。冷却曲线如图1中1所示。
但在实际过程中,液体温度达到或稍低于其凝固点时,晶体并不析出,此现象即过冷现象。此时若加以搅拌或加入晶种,促使晶核产生,则大量晶体迅速形成,并放出凝固热,使体系温度迅速回升到稳定的平衡温度,待液体全部凝固后,温度再逐渐下降。冷却曲线如图1中2所示。
(二)溶液的凝固点确定方法
溶液的凝固点是该溶液与溶剂的固相共存的平衡温度,冷却曲线与纯溶剂不同。当有溶剂凝固析出时,剩余溶液的浓度逐渐增大,因而溶液的凝固点也逐渐下降。因有凝固热放出,冷却曲线的斜率发生变化,即温度的下降速度变慢,如图1中3所示。本实验要求测定已知浓度溶液的凝固点。如果溶液过冷程度不大,析出固体溶剂的量很少,对原始溶液浓度影响不大,则以过冷回升的最高温度作为该溶液的凝固点,如图1中4所示。
确定凝固点的另一种方法是外推法,如图2所示,首先记录绘制纯溶剂与溶液的冷却曲线,作曲线后面部分(已经有固体析出)的趋势线并延长使其与曲线的前面部分相交,其交点即为凝固点。
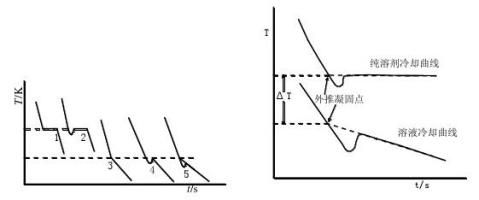
图1 纯溶剂和溶液的冷却曲线 图2 外推法求纯溶剂和溶液的凝固点
四、 仪器和试剂
(一)仪器
1.凝固点管、凝固点管塞、凝固点管套管;
2.小搅拌杆、大搅拌杆;
3.水浴缸、水浴缸盖;
4.精密电子温差仪、温度计;
5.移液管(25mL)、洗耳球;
6.天平(0.001g)。
(二)工具
锤子、保温瓶、试管、环形搅拌棒、移液管、贝克曼温度计一支、分析天平、滤纸、冰块;
(三)试剂
环己烷(A.R)、萘(A.R.)
五、 实验步骤
(一)如图安装实验装置

(二)测定纯溶剂环己烷的凝固点
1.
2.
3.
4.
5.
6.
7.
8. 取25.00mL环己烷→移液管→凝固点管; 将精密温差仪探头插入凝固点管,均匀搅拌(慢档),冷却至温度显示基本不变; 按面板上的“置零”钮,此时温差仪显示“0.000”; 拿出冰水浴中的凝固点管(用卫生纸擦干、擦净),用手捂热至结晶完全熔化(精密显示仪约6-7℃); 将凝固点管放入套管,套管放入冰水浴搅拌(慢档),每30秒记录温度(以精密温差仪的报时为准); 当液体开始析出晶体时(不直接观察样品管,观察精密温差仪示数下降开始变慢时)继续读数10分钟; 重复步骤4、5、6 一次; 测量结束后,保留凝固点管内环己烷用作接下来测量实验中萘的溶剂。
(三)测定萘的环己烷溶液的凝固点
1.
2.
3.
4.
5.
6. 用分析天平称取萘0.1000-0.1200g(实测0.1193g)→实验步骤(二)中保留的凝固点管→搅拌至完全溶解; 将凝固点管放入套管,套管放入冰水浴搅拌(慢档),每30秒记录温度(以精密温差仪的报时为准); 当液体开始析出晶体时(不直接观察样品管,观察精密温差仪示数下降开始变慢时)继续读数10分钟; 拿出冰水浴中的凝固点管(用卫生纸擦干、擦净),用手捂热至结晶完全熔化(精密显示仪约6-7℃); 重复步骤2、3一次; 测量结束,实验完毕。整理仪器,清洗凝固点管、搅拌器、温差仪探头,将环己烷倒入废液瓶。 注意事项:
1. 测温探头擦干后再插入凝固点管。不使用时注意妥善保护测温探头。
2. 加入固体样品时要小心,勿粘在壁上或撒在外面,以保证量的准确。
3. 熔化样品和溶解溶质时切勿升温过高,以防超出温差仪量程。
六、 数据记录及处理
(一)溶剂(环己烷)数据处理与计算
数据记录:

数据处理:

纯溶剂(环己烷)平台范围步冷曲线 纯溶剂(环己烷)步冷曲线
注:红色折线为溶剂(环己烷)温度数据组1,蓝色折线为溶剂(环己烷)温度数据组2。
解:观察图像,得t=1050s、1080s、1110s时的数据1、2值最接近,取作平台平均温度的计算。
由数据组1中t=1050s、1080s、1110s时的数据求得平均平台温度为
?1=0.037+0.040+0.041=0.039? 由数据组2中t=1050s、1080s、1110s时的数据求得平均平台温度为
?2=
取平均值得
??0=
?1+?2=0.046? 0.053+0.050+0.052=0.052?
(二)溶液凝固点(萘的环己烷溶液)数据处理与计算
数据记录:
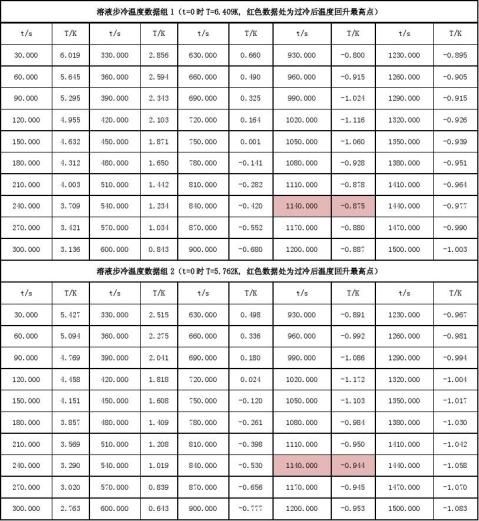
数据处理:
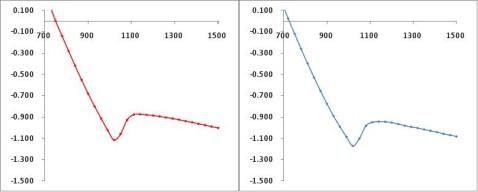
数据组1外推法求凝固点步冷曲线
数据组1:
数据组2外推法求凝固点步冷曲线
溶液至过冷前(t<1020s)步冷数据点拟合直线方程为:y = -0.0043x + 3.3243 溶液完全凝固后(t> 1140s)步冷数据点拟合直线方程为:y = -0.0004x - 0.4475 交点处?1= -0.836K 数据组2:
溶液至过冷前(t<1020s)步冷数据点拟合直线方程为:y = -0.0040x + 3.0749 溶液完全凝固后(t> 1170s)步冷数据点拟合直线方程为:y = -0.0004x - 0.4466 交点处?2= -0.838K 取平均值得:
??=
?1+?2
=?0.837?
(三)萘的摩尔质量计算与误差分析
摩尔质量计算:
测得实验室室温为15℃
则实验溶剂环己烷质量为??=?·?= 0.7971?0.8879?10?3?15 ?25=19.5945?
溶质萘的质量??=0.1193?
???=??0???=0.046? ?0.837 =0.883?
查表得??=20.0?·??·????1
由公式得
??=??·??20.0·1000·0.1193==137.90358?·????1 ??误差计算:
137.90358?128.17052η=?100%=1.60% 产生误差(测定结果偏大)的原因可能有以下几点:
1. ?Tf测定值偏小
2. 溶质在溶液中缔合或生成配合物
七、 思考题
(一)如果溶质在溶液中离解、缔合和生成配合物,对摩尔质量测量值如何影响?
答:溶质在溶液中离解,就会使有效质点增多,导致溶液凝固点降低大小比理论值更大,由公式??=??·??
Δ??·???Tf增
大,则MB减小,摩尔质量测定值偏小;溶质在溶液中缔合或生成配合物则会使摩尔质量测定值偏大。
(二)加入溶质的量太多或太少有何影响?
答:加入溶质太少,溶液凝固点下降不会呈现公式所呈现的比例关系,实际值会比公式计算所得理论值小,所以使摩尔质量测定值偏大;加入溶质太多,实际值会比公式计算所得理论值大,所以使摩尔质量测定值偏小。
(三)利用反应物、产物的某物理性质间接测量浓度进行动力学研究,应满足什么条件?
答:晶体内分子或原子的排列是有规律的,而液体内则是无规律的。而结晶中心有助于这种无序到有序的转化。液体越纯净,结晶中心越难形成。如果降低至凝固点以下仍未形成,就会产生过冷现象。
