实验七、乙酰苯胺制备
一、实验目的
1.掌握芳胺的乙酰化反应及操作方法。
2.掌握重结晶原理及操作要点。
二、实验原理
芳香族伯和仲胺都易与酰化剂作用发生酰基化反应,生成酰胺。
苯胺很容易进行酰基化反应,常用的酰基化试剂有冰醋酸、乙酸酐、乙酰氯等。除了乙酰苯胺本身具有很重要的用途以外,胺的乙酰化反应在有机合成中常用来保护芳环上的氨基,使其不被反应试剂所破坏。
反应式: NH2O+CH3OHHOCH3+H2O
三、实验仪器及试剂
仪器:
50 mL圆底烧瓶 刺型分馏柱 温度计 接受管 锥形瓶 200 mL烧杯 玻璃棒 布氏漏斗 抽滤瓶 表面皿
试剂:
苯胺 冰醋酸 30 g碎冰(反应接近完成时再称取)
四、实验操作
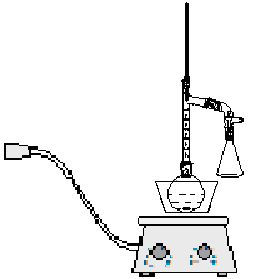
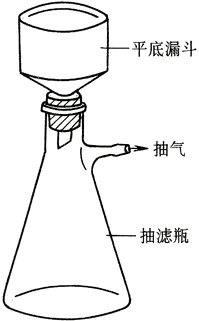
装置如下图。
在50 mL圆底烧瓶中放入5 mL(5.11 g,0.055 mol)新蒸馏的苯胺和8 mL(8.5 g,0.14 mol)的冰醋酸,1~3粒沸石,按照上图安装好仪器(注意在安装刺形分馏柱时,中间不用铁夹应夹在圆底烧瓶的颈部,接收用的锥形瓶也应用铁夹或升降台固定)。在可控温电热套中加热,调节电压在50 V下反应10 min,然后升压至100 V反应5 min后调低至90 V反应25 min,最后再调高到150 V反应10 min后停止反应,关闭电热套的电源(注意记录整个反应过程中的现象)。将反应液趁热倒入盛有30 g碎冰的烧杯中搅拌,待冰融化后,减压过
滤,尽量除去滤饼中的水,得淡黄色固体(粗产品),产品放在表面皿上干燥,称重。
五、实验记录
所加试剂的量
所得产物的量
六、思考与讨论
1.本实验应注意什么才能使反应完全?
2.乙酰基做为芳环氨基的保护基团,除去本实验对苯胺的保护外,讨论还可用于哪些与之类似的化合物的保护?
七、注意事项
1.久置的苯胺易氧化成深色,实验前应该先蒸馏一次。
2
第二篇:对溴乙酰苯胺的制备


化学与环境学院
有机化学实验报告
实验名称 对溴乙酰苯胺的制备
【实验目的】
1、学习芳烃卤化反应理论,掌握芳烃溴化方法;
2、熟悉溴的物理化学性质及其使用操作方法;
3、巩固重结晶及熔点技术。
【实验原理】(包括反应机理)
素对苯环上的取代属于亲电取代反应,常用的催化剂有铁、铝、磷及其卤化物等。苯环上有乙酰氨基,乙酰氨基是邻对位取代基团,由于空间位阻大,主要产物是对溴乙酰苯胺。
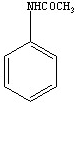
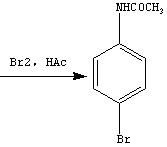
【主要试剂及物理性质】

【仪器装置】
1、主要仪器:
磁力搅拌器、水浴锅、250mL三口烧瓶、恒压滴液漏斗、温
度计、量杯、抽滤瓶、布氏漏斗、真空泵、冷凝管
2、实验装置:


【实验步骤及现象】



【实验结果】
理论产量:m(对溴乙酰苯胺)=n(对溴乙酰苯胺)*M(对溴乙酰苯胺)=n(乙酰苯胺)*M(对溴乙酰苯胺)=m(乙酰苯胺)/M(乙酰苯胺)*M(对溴乙酰苯胺)=3.5/135*214g=5.55g
实际产量:4.52g
产率:4.52/5.55*100%=81.4%
【实验讨论】
1、为什么对溴乙酰苯胺只有81.4%,是什么原因使得其产物损失?
答:①在转移过程中有少量产品粘在容器内壁上未转移完全;
②反应温度没有控制好,温度有时偏高,使得产物对溴乙酰苯胺容易被氧化,使产率降低;
③控制溴的滴加速度是影响产率重要原因。乙酰苯胺的醇溶液与溴-冰醋酸在搅拌下反应,生成邻对位的一溴代物和溴化氢气体。由于邻位位阻大,因此产物以对溴乙酰苯胺为主。在将溴滴加到乙酰苯胺里面时,滴加速度不能过快,否则反应太过剧烈,会导致一部分溴来不及参与反应就与溴化氢一起逸出,用时也可能会产生二溴代产物。
④反应温度和时间控制的影响:乙酰苯胺是活性居中的芳香族化合物,为了加快反应的进行,本实验将反应温度提高到45℃,搅拌1h,后又升到60℃使反应进行完全。温度过低
反应缓慢,时间消耗长;温度过高容易生成二溴代物,产生更多的副产物。
2、溴具有强腐蚀性和刺激性,必须在通风橱中量取,操作时应戴上乳胶手套。
3、滴溴时滴速不宜过快,否则反应太剧烈,会导致一部分溴来不及参与就与溴花氢一起逸出,用时也可能会产生二溴代产物。
【思考题】
1、乙酰苯胺的一溴代物为什么以对位异构体为主?
答:乙酰氨基能让苯环上邻对位的氢变得活泼,而邻位因空间阻碍的关系不易反应,所以就对位为主。
2、在溴化反应中,反应温度的高低对反应结果有何影响? 答:温度过低反应缓慢,时间消耗长;温度过高容易生成二溴代物,产生更多的副产物。且该反应是采用溴的亲电取代反应,使得乙酰苯胺的对位连有溴原子。经资料得到,支链越多,结构越不紧凑熔点越低。反应过程中,温度不能过高,否则会使的溴和乙酸被蒸发出来,使得产率降低。
3、在反应混合物的后处理过程中,加入亚硫酸氢钠的目的是什么?
答:亚硫酸氢钠可以除去未反应的溴单质:
-+?H2O+Br2+SO32?→SO2+2Br+2H,所以可以是溶液黄色褪去。 4
4、产物可能存在哪些杂质,如何除去?
答:产物中可能残留有溴单质,溴化氢,醋酸,乙醇等杂质。将反应物倒入水中,产生了偏黄色的的固体,这是由于固体里含有溴单质,溴单质可用亚硫酸氢钠溶液除去,溴化氢、醋酸和乙醇易挥发,重结晶也可除去杂质。
【实验成绩】
指导老师签名:
