聚苯胺导电聚合膜的制备及表征
一、实验目的
1、了解聚合物的合成方法、性能和主要反应;
2、通过电化学聚合实验,掌握电化学聚合的实验技术以及相应的电化学测试方法;
3、通过电解法氧化还原聚苯胺,了解其颜色的变化和聚苯胺氧化或者还原反应的关系;
4、了解酸碱度对其氧化还原反应的影响。
二、背景知识及实验原理
20世纪70年代后期,由于聚乙炔的发现而产生了以共轭高分子为基础的导电高分子学科,并得到了迅猛的发展,而导电聚合物自20世纪80年代中期被Mac Diarmid等重新开发以来,以其原料易得、合成简单、较高的导电率和潜在溶液和熔融加工性能,以及良好的环境稳定性的等优点,成为目前最受关注的三大导电高分子品种(聚苯胺、聚噻吩和聚吡咯)之一。正是以上这些优点,使聚苯胺有广阔的应用前景。导电聚苯胺具有良好的电磁屏蔽和微波吸收性能,如聚苯胺/聚氯乙烯导电共混材料的电磁屏蔽常数大于50dB。在二次电池(塑料电池)中使用聚苯胺具有良好的充放电效果,循环充电2000次,库伦效率仍接近100%。导电聚苯胺是一种良好的金属防腐蚀材料,同时还是较好的防污材料,可在舰船上广泛应用。另外,聚苯胺还有电致变色、电子发光等可被将来利用的性能。
聚苯胺的合成方法很多,如化学氧化聚合物、电化学聚合法、现场聚合法、缩合聚合法等,其中化学氧化聚合法较为简单,易于大批量生产,因而吸引了许多注意力。本实验用电化学聚合法合成聚苯胺,并且对其电化学和光学性能进行表征。
聚苯胺的形成是通过阳极偶合机理完成的。
聚苯胺链的形成是活性链端(-NH2)反复进行上述反应,不断增长的结果。由于在酸性条件下,聚苯胺链具有导电性质,保证了电子能通过聚苯胺链传导至阳极,是增长继续。只有当头头偶合反应发生,形成偶氮结构,才使得聚合停止。
PAN有4种不同的存在形式,它们分别具有不同的颜色。苯胺能经电化学聚合形成绿色的叫作翡翠绿的PAN导电形式。当膜形成后,PAN的4种形式都能得到,并可以非常快地进行可逆的电化学相互转化。完全还原形式的五色盐可在低于-0.2V时得到,翡翠绿在0.3~0.4V时得到,翡翠基蓝在0.7V时得到,而紫色的完全氧化形式在0.8V时得到。因此,可通过改变外加电压实现翡翠绿和翡翠基蓝之间的转化,也可以通过改变pH值来实现。区分不同光学性质是由苯环和喹二亚胺单元的比例决定的,它能通过还原或质子化程度来控制。
三、仪器及试剂
仪器:容量瓶、烧杯、导电玻璃、饱和甘汞电极、铂电极;电脑工作仪器一套
试剂:苯胺、不同PH值的标准溶液、浓硫酸。
四、实验步骤及现象
1、苯胺、硫酸水溶液的配置:
取一200ml容量瓶,往其中加入约150ml蒸馏水,再分别取0.02mol(1.86ml)的苯胺和0.2mol(10.65ml)浓硫酸加入其中,冷却加水至刻线,配置苯胺的酸性水溶液。
现象:加入苯胺和浓硫酸后,有油状液体在瓶底部,加水逐渐溶解,最后溶液澄清,微黄。
2、电解槽的装配:
以饱和甘汞电极为参比电极,pt丝电极为辅助电极,导电玻璃(经过超声波清洗仪清洗过的玻璃片)为研究电极组成三电极体系。将各导线与各电极接好(绿色接工作电极,白色接参比电极,红色接辅助电极),插入装有已配置好的苯胺溶液的小烧杯中(注意溶液不能淹没导电夹,三个电极不能接触)。
3、聚苯胺膜的制备:
选择i-t法,设定点位0.8~0.9V(0.9V),扫描400s,做出聚苯胺导电膜在配制的0.2mol的硫酸和苯胺介质中的循环伏安曲线图,得到苯胺膜。
现象:随着电镀的进行导电玻璃上逐渐形成一层绿色的膜。
4、CHI660B仪器的预调节:
打开CHI660B的电脑操作界面,选择循环伏安法,扫描范围调节在-0.4~1.0V,扫描速率调在50mV/s;点击开始键,并进行扫描,扫描完成后将数据及图像储存。
6、PH值的测定:
制备一份浓度为0.5mol/L的硫酸溶液,及pH值不同的标准溶液三份(pH=4.003,6.864,9.128);以饱和甘汞电极为参比电极,测定聚苯胺膜电极在各种不同pH溶液中的循环伏安曲线图,绘制pH-E响应曲线。再测定浓度为0.5mol/L的硫酸溶液的电位值,从标准溶液的pH-E曲线中找出该溶液的pH值。
现象:电解时,玻璃膜的颜色由绿色变为蓝色,最后变为微紫色,接着又变回绿色,并且电解时的铂丝上有细小气泡生成。
五、实验结果及处理
根据实验数据可以用Origin作图,以下五副图为聚苯胺在不同PH(0,4.003,6.864,9.128)下的循环伏安曲线图及其四个不同PH下的循环伏安曲线图的叠加。
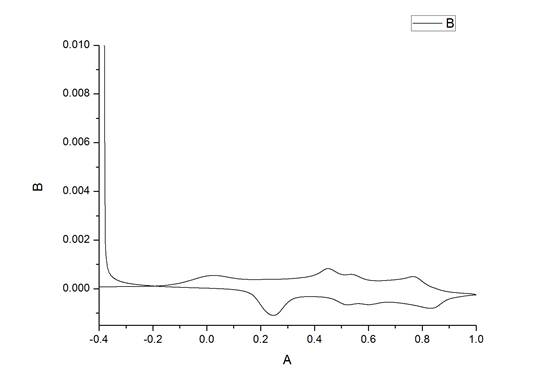 图1 聚苯胺在0.5mol/L硫酸(PH=0)溶液中循环伏安曲线
图1 聚苯胺在0.5mol/L硫酸(PH=0)溶液中循环伏安曲线
从上图1可以看出聚苯胺在0.5mol\L硫酸(PH=0)溶液中有多个峰,其中每个峰都是一个氧化还原反应过程的电压值,上面的曲线代表的是还原反应,聚苯胺由微紫色还原成蓝色再到绿色;下面的曲线代表的是氧化反应,聚苯胺由绿色到蓝色再到微紫色。其中峰的高度代表的是电流的大小,峰越高,代表电流越大,氧化或者还原的速率越大。
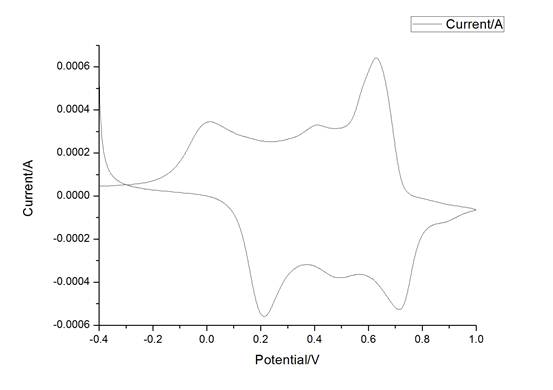 图2 聚苯胺在PH=4.003的标准溶液中循环伏安曲线
图2 聚苯胺在PH=4.003的标准溶液中循环伏安曲线
由上图2可以看出,聚苯胺在酸性条件下的循环伏安曲线有四个峰,其中两个是还原峰,两个是氧化峰。并且在氧化还原的过程中,有一个氧化峰对应着一个还原峰,其电势在氧化或者还原的过程中,都有着一定的对称性(从还原线开始到氧化线)。在电压变化0.3V时,其氧化速率达到了一个最大值,再经过0.5V的电压变化后,又达到了一个峰值;在还原的过程中,电压经过0.3V的变化后达到了第一个峰值,再经过0.6V的变化又达到了另一个峰值(在还原的过程中,还原应该从0.3V开始,即还原线和氧化线的交点)。
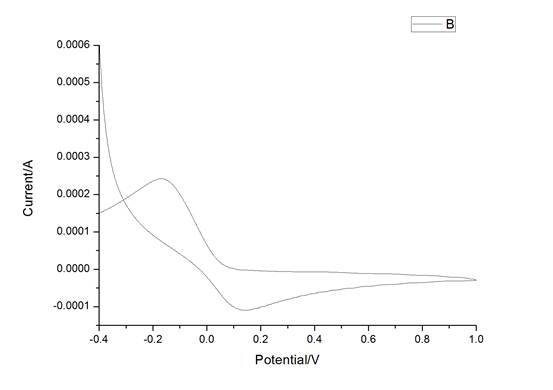
图3 聚苯胺在PH=6.864的标准溶液中循环伏安曲线
由上图3可以看出在中性条件下的聚苯胺氧化膜的氧化还原反应的峰值很小,不太明显,并且只有一个。可能是PH增大,其氧化还原反应减弱。

图4 聚苯胺在PH=9.128的标准溶液中循环伏安曲线
由上图4可以看出在碱性条件下的聚苯胺的氧化还原反应中,只有氧化反应有明显的峰值,而还原反应没有明显的峰值。可能是发生单向氧化,即发生氧化反应,但是还原反应不明显。也可能是氧化还原的聚苯胺的量较少,得出来的曲线变化不太明显导致。
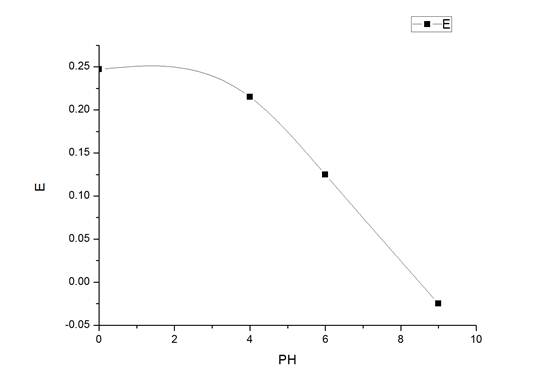
图5 聚苯胺氧化过程中的PH-E曲线
由图5可以知道,其氧化电势随着PH的增大而减小,并且在酸性较强的情况下,其下降的趋势较缓慢,在PH较大的情况下,其氧化电势E和PH呈简单的线性关系。
六、实验小结与讨论
由图1至图4,可以得到一些结论:每一次的循环伏安曲线都会有峰值,并且从理论上来说,一个还原峰就对应着一个氧化峰。并且其氧化还原的过程有电流的峰值,峰值的绝对值越大,表示电流越大,反应速率越大。通过四幅图还可以看出,PH的值越小,即酸性越大,其氧化还原峰越多,并且越明显;PH值越大,即碱性越大,其氧化还原峰越少,并且没有酸性条件下明显。这表明聚苯胺的氧化还原反应和溶液的PH值(酸碱度)有关,酸度越大,聚苯胺就越容易发生氧化还原反应;碱度越大,聚苯胺就越难发生氧化还原反应。
本实验中应该要注意在进行电镀和电解的时候,聚苯胺膜电极应该与另外两个电极的表面正对,以减少其误差(主要是溶液的电阻率)。另外,在电解的时候,不要碰到烧杯,以防其循环伏安曲线突然变化,而导致误差的产生。
七、实验思考题
1、为什么导电玻璃要在聚合前认真仔细的处理?
答:因为如果不把导电玻璃清洗干净,玻片上含有杂质就会影响聚苯胺膜的生成,影响循环伏安曲线的绘制,最终导致误差的产生。
2、什么是修饰电极?
答:修饰电极是把特殊化学性质的分子,离子或聚合物修饰在电极表面,以实现对电极的功能进行设计的目的。
3、聚苯胺光学吸收的原理是什么?
答:光能激发聚苯胺中的苯环和亚胺单元之间的转化,从而改变其光学性质。
第二篇:聚苯胺导电聚合膜的制备及表征
聚苯胺导电聚合膜的制备及表征
摘要:聚苯胺,高分子化合物的一种,具有特殊的电学、光学性质,经掺杂后可具有导电性。合成聚苯胺的常用方法之一是电化学法。电化学法包括循环伏安法、恒电流法、恒电势法、脉冲电流法等。其中,循环伏安法制得的聚苯胺膜质地均匀、导电性良好、氧化还原可逆性优良、膜厚易控制以及膜与基体结合牢固、可获得自支撑膜,应用最为广泛。本实验采用循环伏安法合成聚苯胺,并且对其电化学和光学性能进行表征。
关键词:导电聚苯胺,合成方法,电化学性能,循环福安曲线图,表征
1前言
聚苯胺,高分子化合物的一种,具有特殊的电学、光学性质,经掺杂后可具有导电性。在电子工业、信息工程、国防工程等的开发和发展方面都具有多种用途。
聚苯胺的电活性源于分子链中的P电子共轭结构:随分子链中P电子体系的扩大,P成键态和P*反键态分别形成价带和导带,这种非定域的P电子共轭结构经掺杂可形成P型和N型导电态。不同于其他导电高分子在氧化剂作用下产生阳离子空位的掺杂机制,聚苯胺的掺杂过程中电子数目不发生改变,而是由掺杂的质子酸分解产生H+和对阴离子(如Cl-、硫酸根、磷酸根等)进入主链,与胺和亚胺基团中N原子结合形成极子和双极子离域到整个分子链的P键中,从而使聚苯胺呈现较高的导电性。这种独特的掺杂机制使得聚苯胺的掺杂和脱掺杂完全可逆,掺杂度受pH值和电位等因素的影响,并表现为外观颜色的相应变化,聚苯胺也因此具有电化学活性和电致变色特性。
聚苯胺经一定处理后,可制得各种具有特殊功能的设备和材料,如可作为生物或化学传感器的尿素酶传感器、电子场发射源、较传统锂电极材料在充放电过程中具有更优异的可逆性的电极材料、选择性膜材料、防静电和电磁屏蔽材料、导电纤维、防腐材料等等。[
聚苯胺的合成方法很多,如化学氧化聚合物、电化学聚合法、现场聚合法、缩合聚合法等,其中化学氧化聚合法较为简单,易于大批量生产,因而吸引了许多注意力。本实验用电化学聚合法合成聚苯胺,并且对其电化学和光学性能进行表征。
聚苯胺的形成是通过阳极偶合机理完成的。
聚苯胺链的形成是活性链端(-NH2)反复进行上述反应,不断增长的结果。由于在酸性条件下,聚苯胺链具有导电性质,保证了电子能通过聚苯胺链传导至阳极,是增长继续。只有当头头偶合反应发生,形成偶氮结构,才使得聚合停止。
PAN有4种不同的存在形式,它们分别具有不同的颜色。苯胺能经电化学聚合形成绿色的叫作翡翠绿的PAN导电形式。当膜形成后,PAN的4种形式都能得到,并可以非常快地进行可逆的电化学相互转化。完全还原形式的五色盐可在低于-0.2V时得到,翡翠绿在0.3~0.4V时得到,翡翠基蓝在0.7V时得到,而紫色的完全氧化形式在0.8V时得到。因此,可通过改变外加电压实现翡翠绿和翡翠基蓝之间的转化,也可以通过改变pH值来实现。区分不同光学性质是由苯环和喹二亚胺单元的比例决定的,它能通过还原或质子化程度来控制。
2实验部分
2.1试剂和仪器
仪器:容量瓶、烧杯、导电玻璃、饱和甘汞电极、铂电极;RST5200电化学工作站(郑州世瑞思仪器科技有限公司)
试剂:苯胺(AR)、不同PH值的标准溶液、浓硫酸(AR)。
2.2 实验方法
2.2.1苯胺、硫酸水溶液的配置
取一200ml容量瓶,往其中加入约150ml蒸馏水,再分别取0.02mol(1.86ml)的苯胺 和0.2mol(10.65ml)浓硫酸加入其中,冷却加水至刻线,配置苯胺的酸性水溶液。
2.2.2 电解槽的装配
以饱和甘汞电极为参比电极,pt丝电极为辅助电极,导电玻璃(经过超声波清洗仪清洗过的玻璃片)为研究电极组成三电极体系。将各导线与各电极接好(绿色接工作电极,白色接参比电极,红色接辅助电极),插入装有已配置好的苯胺溶液的小烧杯中(注意溶液不能淹没导电夹,三个电极不能接触)。
2.2.3 聚苯胺膜的制备
选择i-t法,设定点位0.8~0.9V(0.9V),扫描400s,做出聚苯胺导电膜在配制的0.2mol的硫酸和苯胺介质中的循环伏安曲线图,得到苯胺膜。
2.2.4 CHI660B仪器的预调节
打开CHI660B的电脑操作界面,选择循环伏安法,扫描范围调节在-0.4~1.0V,扫描速率调在50mV/s;点击开始键,并进行扫描,扫描完成后将数据及图像储存。
2.2.5 PH值的测定
制备一份浓度为0.02mol/L的苯胺溶液,及浓度不同的硫酸溶液三份(C=0.5,0.05,0.005);以饱和甘汞电极为参比电极,测定聚苯胺膜电极在各种不同浓度硫酸溶液中的循环伏安曲线图,绘制I-E响应曲线。再测定PH=3的硫酸溶液的电位值,从标准溶液的I-E曲线中找出该溶液的I值。
3实验结果与讨论
3.1实验数据处理
根据实验数据将所得图形导入Origin中,以下4副图为聚苯胺在不同浓度的硫酸溶液(0.5,0.05,0.005,)和PH=4的溶液下的循环伏安曲线图及其四个不同浓度下的循环伏安曲线图的叠加。
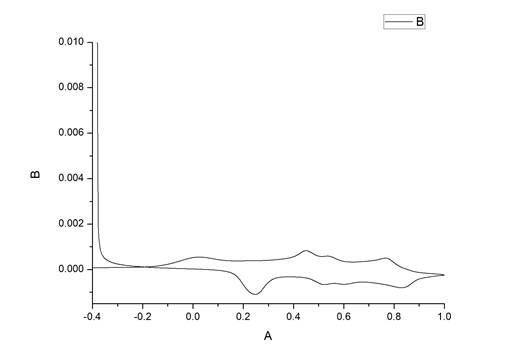 图1 聚苯胺在0.5mol/L硫酸溶液中循环伏安曲线
图1 聚苯胺在0.5mol/L硫酸溶液中循环伏安曲线
从上图1可以看出聚苯胺在0.5mol\L硫酸(PH=0)溶液中有多个峰,其中每个峰都是一个氧化还原反应过程的电压值,上面的曲线代表的是还原反应,聚苯胺由微紫色还原成蓝色再到绿色;下面的曲线代表的是氧化反应,聚苯胺由绿色到蓝色再到微紫色。其中峰的高度代表的是电流的大小,峰越高,代表电流越大,氧化或者还原的速率越大。
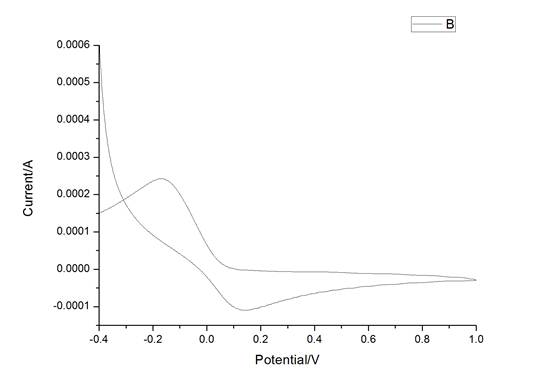
图2 聚苯胺在C=0.05mol/L的硫酸溶液中循环伏安曲线
由上图2可以看出在中性条件下的聚苯胺氧化膜的氧化还原反应的峰值很小,不太明显,并且只有一个。可能是PH增大,其氧化还原反应减弱.
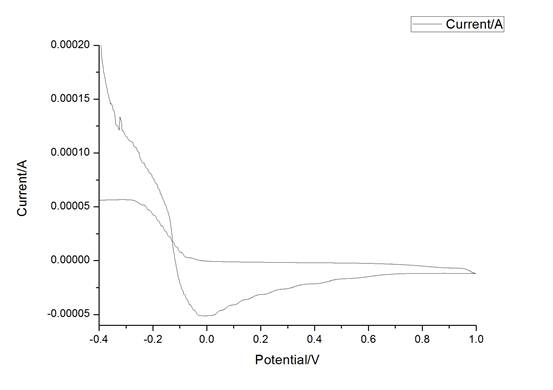
图3聚苯胺在C=0.005mol/L的标准溶液中循环伏安曲线
由上图3可以看出,由上图2可以看出在弱酸性条件下的聚苯胺的氧化还原反应中,只有氧化反应有明显的峰值,而还原反应没有明显的峰值。可能是发生单向氧化,即发生氧化反应,但是还原反应不明显。也可能是氧化还原的聚苯胺的量较少,得出来的曲线变化不太明显导致。
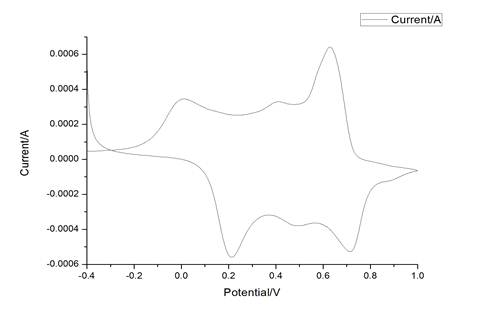
图4 聚苯胺在PH=4的溶液中循环伏安曲线
由上图4可以看出,聚苯胺在酸性条件下的循环伏安曲线有四个峰,其中两个是还原峰,两个是氧化峰。并且在氧化还原的过程中,有一个氧化峰对应着一个还原峰,其电势在氧化或者还原的过程中,都有着一定的对称性(从还原线开始到氧化线)。在电压变化0.3V时,其氧化速率达到了一个最大值,再经过0.5V的电压变化后,又达到了一个峰值;在还原的过程中,电压经过0.3V的变化后达到了第一个峰值,再经过0.6V的变化又达到了另一个峰值(在还原的过程中,还原应该从0.3V开始,即还原线和氧化线的交点)。
4结论
由图1至图4,可以得到一些结论:每一次的循环伏安曲线都会有峰值,并且从理论上来说,一个还原峰就对应着一个氧化峰。并且其氧化还原的过程有电流的峰值,峰值的绝对值越大,表示电流越大,反应速率越大。通过四幅图还可以看出,硫酸浓度越大,即酸性越强,其氧化还原峰越多,并且越明显;浓度越小,即酸性越弱,其氧化还原峰越少,并且没有酸性条件下明显。这表明聚苯胺的氧化还原反应和溶液的酸碱度值(PH值)有关,酸度越大,聚苯胺就越容易发生氧化还原反应;碱度越大,聚苯胺就越难发生氧化还原反应。
查文献知在酸性溶液采用循环伏安法电化学合成聚苯胺循环伏安曲线上出现三对明显的氧化还原峰。表征聚苯胺生长速度的阴极沉积电量Q随着苯胺浓度的增加、质子酸浓度的增加而增加。在无机质子酸HSO4、HCl、HNO3和HClO4掺杂下,苯胺循环伏安电聚合峰形状相似,说明聚苯胺在的形核和生长机理相同.但聚合电量和聚合速率却明显依赖于质子酸的类型,变化顺序有H2SO4>HCl>HNO3>HClO4.
参考文献
[1]钱卫军,尹斌,张祖训,分析化学报告,24(9),1996,993~997
[2]金绪刚,黄承亚,龚克成,半导体光电,18(3),1997,203~207
[3]夏都灵,电子科技大学学报,29(6),2000,669~672
Preparation and characterization of polyaniline conductive polymer film
Abstract: Polyaniline, a polymer compound has special electrical, optical properties after doping conductive. One common method for the synthesis of polyaniline is electrochemical method. Electrochemical method include cyclic voltammetry, constant current method, the constant potential method, pulse current method. Among them, the polyaniline produced from cyclic voltammetry method have good conductivity, redox excellent reversibility, and is easy to control the thickness of the film and the substrate with a solid, self-supporting film available.It’s used the most widely. In this study,we used the cyclic voltammetry method and Characterize the electrochemical and optical properties.
Keywords: Conducting polyaniline, synthesis, electrochemical, cyclic voltammetry , characterization.
