有 机 化 学 实 验 报 告

实 验 名 称: 甲基橙的制备
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级: 化工xx班
姓 名: xxx 学 号 xxx
指 导 教 师:
日 期: 2013年xx月18日
一、 实验目的
1. 通过甲基橙的制备学习重氮化反应和偶合反应的实验操作;
2. 巩固盐析和重结晶的原理和操作。
二、 实验原理
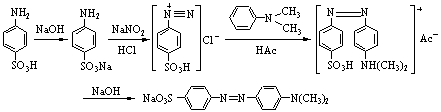
三、 主要试剂及用量

四、 仪器装置
烧杯,量筒,玻璃棒,滴管,电磁炉,抽虑装置,表面皿





五、 实验步骤及现象
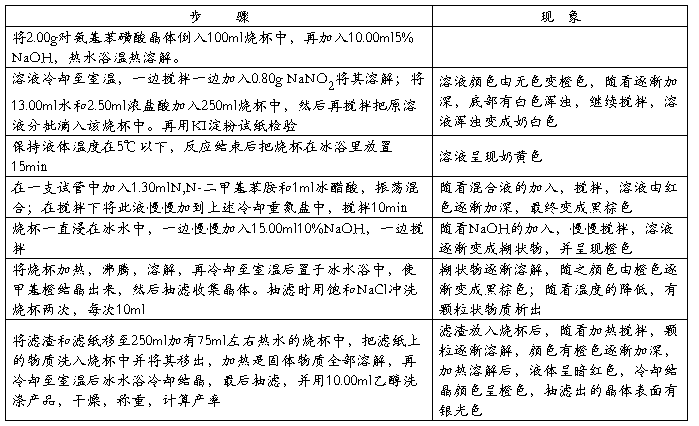
六、 实验结果

理论上2.00g的对氨基苯磺酸可得到甲基橙的质量:
m1=(2.00g×327.33g/mol)÷173.83g/mol=3.77g;
实验的产率:ω=(2.7g÷3.77g)×100%=71.6%。
七、 实验讨论
1、本次的实验产率可能有一点偏低。
2、没有控制好实验温度,会降低产率。
3、冷却时间不够长,导致晶体未完全析出。
第二篇:甲基橙
甲基橙的制备
一、实验目的
熟悉重氮化反应和偶合反应的原理,掌握甲基橙的制备方法。
练习重结晶的实验操作。
二、实验原理
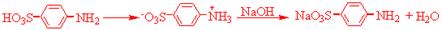
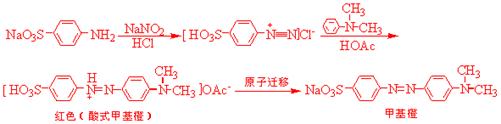
三、药品和仪器
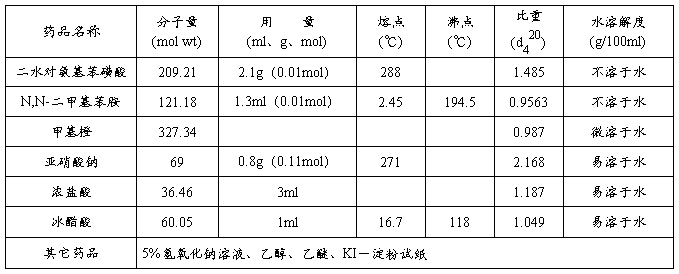
仪器:烧杯 温度计 表面皿
四、实验操作
1、重氮盐的制备
在50ml烧杯中、加入10ml 5%氢氧化钠溶液和2.1g对氨基苯磺酸晶体,温热使结晶溶解,用冰盐浴冷却至0℃以下。另在一试管中配制0.8g亚硝酸钠和6ml水的溶液。将此配制液也加入烧杯中。维持温度0-5℃,在搅拌下,慢慢用滴管滴入3ml浓盐酸与10ml水配成的溶液,直至用淀粉-碘化钾试纸检测呈现蓝色为止,继续在冰盐浴中放置15分钟,使反应完全,这时往往有白色细小晶体析出。
2、偶合反应
在试管中加入1.3ml N,N-二甲基苯胺和1ml 冰醋酸,并混匀。在搅拌下将此混合液缓慢加到上述冷却的重氮盐溶液中,加完后继续搅拌10min。然后缓缓加入约25ml 5%氢氧化钠溶液,直至反应物变为橙色(此时反应液为碱性)。甲基橙粗品呈细粒状沉淀析出。
将反应物置沸水浴中加热5分钟,冷至室温后,再放入冰浴中冷却,使甲基橙晶体析出完全。抽滤,依次用少量水、乙醇和乙醚洗涤,压紧抽干。干燥后得粗品约3.0g。
粗产品用1%氢氧化钠进行重结晶。待结晶析出完全,抽滤,依次用少量水、乙醇和乙醚洗涤,压紧抽干,得片状结晶。产量约2.5g。
将少许甲基橙溶于水中,加几滴稀盐酸,然后再用稀碱中和,观察颜色变化。
本实验约需4-6小时。
五、实验注意事项
1、对氨基苯磺酸为两性化合物,酸性强于碱性,它能与碱作用成盐而不能与酸作用成盐。
2、重氮化过程中,应严格控制温度,反应温度若高于5℃,生成的重氨盐易水解为酚,降低产率。
3、若试纸不显色,需补充亚硝酸钠溶液。
4、重结晶操作要迅速,否则由于产物呈碱性,在温度高时易变质,颜色变深。用乙醇和乙醚洗涤的目的是使其迅速干燥。
六、思考题
1、在重氮盐制备前为什么还要加入氢氧化钠?如果直接将对氨基苯磺酸与盐酸混合后,再加入亚硝酸钠溶液进行重氮化操作行吗?为什么?
2、制备重氮盐为什么要维持0-5℃的低温,温度高有何不良影响?
3、重氮化为什么要在强酸条件下进行?偶合反应为什么要在弱酸条件下进行。
1、本实验中重氮盐的制备为什么要控制在0~5℃中进行?偶合反应为什么要在弱酸介质中进行?
答:重氮反应过程中,若反应温度较高,一方面亚硝酸分解的速度加剧,使重氮化反应不完全。另一方面,温度过高,生成的重氮盐易水解成苯酚:重氮盐与芳胺进行的偶合反应在中性或弱酸性介质中进行更有利。因为,在强酸性介质中,芳胺将转变为铵盐(ArN+RR’H),导致芳环的电子云密度太低,而不能进行偶合反应。
2、粗甲基橙进行重结晶时,依次用少量水、乙醇和乙醚洗涤,目的何在?
答:用水洗涤是为了减少甲基橙吸附的碱。碱性大时,温度稍高甲基橙就易变质,颜色变深呈褐色。用少量乙醇、乙醚洗涤是为了除去剩余的被甲基橙吸附的碱和其它有机物。同时,也是为了使产品甲基橙能迅速变干。因为,湿的甲基橙受光作用后颜色会变深。
3、把冷的重氮盐溶液慢慢倒入低温新制备的氯化亚铜的盐酸溶液中,将会发生什么反应?写出产物的名称。
答:将会发生Sandmeyer反应,即重氮基被氯取代,同时放出氮气。
4、.N,N–二甲基苯胺与重氮盐偶合时为什么总是在取代氨基的对位发生?
答:因为芳环上的取代氨基是个很强的给电子基,通过其与苯环的p-π共轭作用使苯环的电子云密度增加,尤其是邻对位。由于重氮盐进攻邻位时位阻较大,因此,偶合反应优先发生在取代氨基的对位。当对位被占,则发生在邻位。偶合反应绝对不会在取代氨基的间位上发生。
