�߶���ѧ˫����
һ ֪ʶ��Ҫ��
1. ˫���ߵ�һ���壺
ƽ��������������F1��F2�ľ����ľ���ֵ�dz�����С��|F1F2|���ĵ�Ĺ켣��˫���ߡ������������˫���ߵĽ��㣬�������ľ���|F1F2|�н��ࡣ
2. ˫���ߵĵڶ����壺
ƽ������һ������ľ���͵�һ����ֱ�ߵľ���ı��dz���e��e>1���ĵ�Ĺ켣��˫���ߡ������˫���ߵĽ��㣬��ֱ�߽�˫���ߵ��ߣ�����e��˫���ߵ������ʡ�
3. ˫���ߵı����̣�
��1��������x���ϵģ�
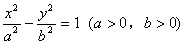
��2��������y���ϵģ�
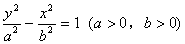
��3����a��bʱ��x2��y2��a2��y2��x2��a2�е���˫���ߡ�
ע��c2��a2��b2
4. ˫���ߵļ������ʣ�
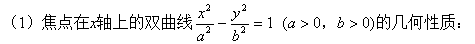
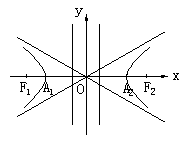
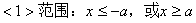
<2>�Գ��ԣ�ͼ�ι���x�ᡢy�ᣬԭ�㶼�Գơ�
<3>���㣺A1��-a��0����A2��a��0��
�߶�A1A2��˫���ߵ�ʵ�ᣬ��|A1A2|��2a��
�߶�B1B2��˫���ߵ����ᣬ��|B1B2|��2b��
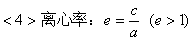
eԽ��˫���ߵĿ��ھ�Խ������
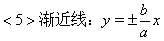

5����˫���ߵĽ����߷���Ϊ��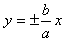
����������ֱ��Ϊ���������ߵ�˫����ϵ���̿���д�ɣ�
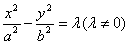
���������⡿
��1. ѡ���⡣


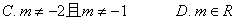
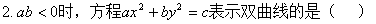
A. ��Ҫ����������� B. ��ֵ�����Ҫ����
C. ��ֱ�Ҫ���� D. �Ȳ����Ҳ����Ҫ����
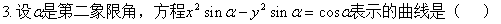
A. ������x���ϵ���Բ B. ������y���ϵ���Բ
C. ������y���ϵ�˫���� D. ������x���ϵ�˫����
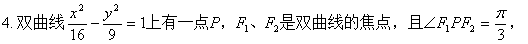
���F1PF2������� ��

��2. 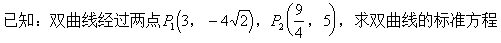
��3. ��֪B��-5��0����C��5��0���ǡ�ABC���������㣬��
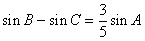 ����A�Ĺ켣���̡�
����A�Ĺ켣���̡�
��4. ��1��������Բ ��˫���ߵı����̡�
��˫���ߵı����̡�
��2������˫����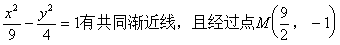 ��˫���ߵı����̡�
��˫���ߵı����̡�
��5. 
��1������M��1��1����ֱ�߽�˫������A��B���㣬��MΪAB���е㣬��ֱ��AB�ķ��̣�
��2���Ƿ����ֱ��l��ʹ��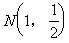 Ϊֱ��l��˫���߽صõ��ҵ��е㣬���������ֱ��l�ķ��̣���������˵�����ɡ�
Ϊֱ��l��˫���߽صõ��ҵ��е㣬���������ֱ��l�ķ��̣���������˵�����ɡ�
������
1. ��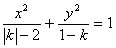 ��ʾ������y���ϵ�˫���ߣ���ô���İ뽹��c��ȡֵ��Χ�ǣ� ��
��ʾ������y���ϵ�˫���ߣ���ô���İ뽹��c��ȡֵ��Χ�ǣ� ��
A. 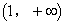 B. ��0��2�� C.
B. ��0��2�� C. 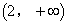 D. ��1��2��
D. ��1��2��
2. ˫���ߵ����������ߵļн�Ϊ60°����˫���ߵ�������Ϊ�� ��
A. 2��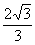 B. 2 C.
B. 2 C. 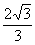 D.
D. 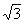
3. ԲC1��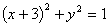 ��ԲC2��
��ԲC2��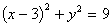 ����ԲMͬʱ��ԲC1��ԲC2�����У���ԲԲ��M�Ĺ켣���̡�
����ԲMͬʱ��ԲC1��ԲC2�����У���ԲԲ��M�Ĺ켣���̡�
[�����]
��һ��
�⣺1. ������������˫���ߵı����̶���
��֪��2+m��m+1Ӧͬ�ż��ɡ�
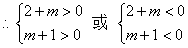
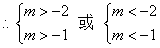
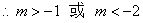
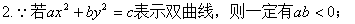
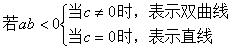
��ѡA
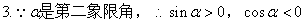
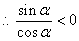
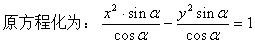
��֪��x2��ϵ��Ϊ����y2��ϵ��Ϊ��
��̱�ʾ������y���ϵ�˫����
4. ��˫���߷���֪��a��4��b��3��c��5
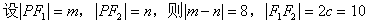
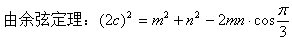
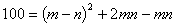
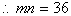
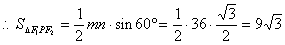 ��
��
������
�⣺������˫���߷���ΪAx2��By2��1����AB>0��
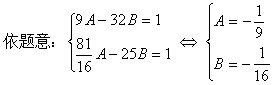

������
�������ڡ�ABC�������Ҷ����ɰ�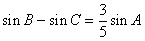 ת��Ϊ
ת��Ϊ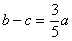 �����ͼ�ο�֪����A�Ĺ켣����B��CΪ�����㣬ʵ�᳤Ϊ6��˫���ߵ���֧��
�����ͼ�ο�֪����A�Ĺ켣����B��CΪ�����㣬ʵ�᳤Ϊ6��˫���ߵ���֧��
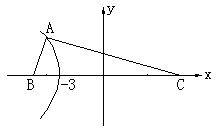
�⣺�ڡ�ABC�У�|BC|��10
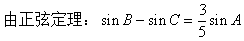
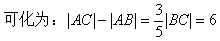
�ඥ��A�Ĺ켣����B��CΪ�������㣬ʵ�᳤Ϊ6��˫���ߵ���֧
�֡�c��5��a��3����b��4
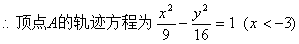
ע����1���������Ҷ�������ʵ�ֱ���ǵ�ת����������켣���̵Ĺؼ���
��2�������������߶���ģ�����ֱ��д���켣���̣�
��3����켣Ҫ�������ز�©��Ӧɾ�������������ĵ㡣
���ģ�
�⣺��1������Բ����֪��
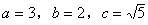
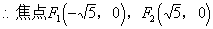

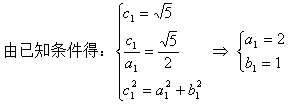

��2���ⷨһ��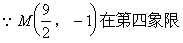
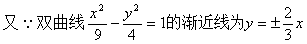
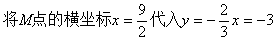
��˫���ߵĽ������x����

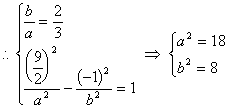

�ⷨ����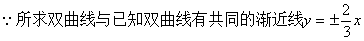

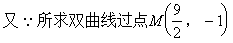
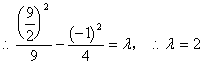

���壺
�⣺��1����AB�ķ���Ϊ��y��1��k��x��1��
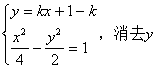
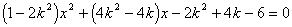
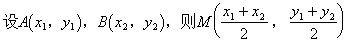
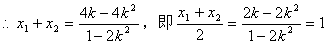
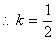
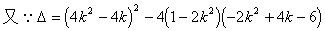
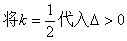
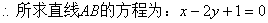
��1�����ⷨ��
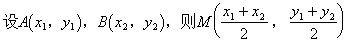
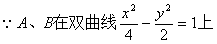
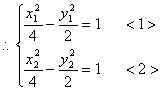
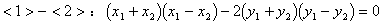
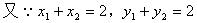
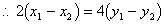
��x1��x2ʱ��ֱ��AB��˫����û�н��㡣
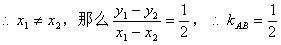
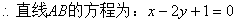
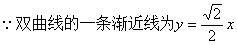

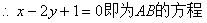
��2�������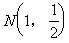 ��ֱ��l��˫������C��x3��y3����D��x4��y4������
��ֱ��l��˫������C��x3��y3����D��x4��y4������
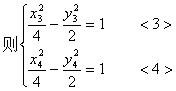
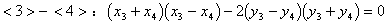
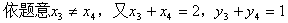
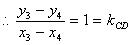
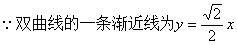
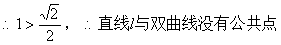
������
1. �𰸣�A
2. �𰸣�A
3. �������������Ĺؼ���Ѱ�Ҷ���M�����������������Բ���У���Ȼ��Բ�ľ���뾶�Ĺ�ϵ��
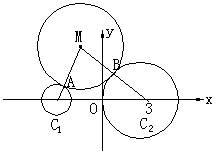
�⣺�趯ԲM��ԲC1��ԲC2�ֱ������ڵ�A��B��������Բ���еij�Ҫ����֪��
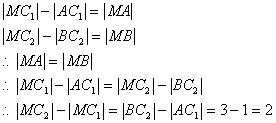
������M��������C1��C2�ľ���IJ���2
����˫���߶��壬����M�Ĺ켣��˫������֧����M��C2�ľ��������C1�ľ��룩
����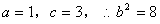
��M��x��y��
��켣����Ϊ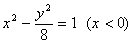
��ϰ�⡻
1��ax2+by2=b(ab<0),���������ǣ� ��
A��˫���߽�����x����
B��˫���߽�����y����
C����Բ������x����
D����Բ������y����
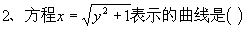
A��˫���� B��˫���ߵ�һ֧ C����Բ D��Բ
3��һ��Բ������Բ��M��x2+y2=1�͡�N:x2+y2-8x+12=0�����У���ԲԲ�ĵĹ켣Ϊ�� ��
A�������� B��Բ C��˫���ߵ�һ֧ D����Բ
4����ab<0���ǡ�����ax2+by2=c����ʾ˫���ߵģ� ��
A����Ҫ���������
B����ֲ���Ҫ����
C����Ҫ����
D���Ȳ����Ҳ����Ҫ����
5����֪������F1��-5��0����F2��5��0��������P����|PF1|-|PF2|=2a,��a=3��5ʱ��P��Ĺ켣Ϊ�� ��
A��˫���ߺ�һֱ��
B��˫���ߺ�һ������
C��˫���ߺ�һ֧��һ������
D��˫���ߵ�һ֧��һ��ֱ��
6����֪����ax2-ay2=b,��a��b��ţ��̱�ʾ�� ��
A��������x���ϵ���Բ
B��������y���ϵ���Բ
C��������x���ϵ�˫����
D��������y���ϵ�˫����
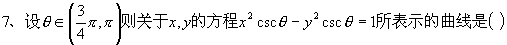
A��������y���ϵ�˫����
B��������x���ϵ�˫����
C��������y���ϵ���Բ
D��������x���ϵ���Բ

��|AB|=m�����ABF2���ܳ��ǣ� ��
A.4a B.4a-m C.4a+2m D.4a-2m

A������ B������ C�����л����� D����������ཻ
10������x2sin��+y2cos��=1��ʾ������y���ϵ�˫���ߣ���Ǧ��ڵ�_______���ޡ�
11��˫����4x2-y2+64=0��һ��P������һ������ľ������1�����P����һ������ľ������_______.
�𰸣�
1��5 B B A C C
6��9 D C C C
10����
11��17
�ڶ�ƪ����һ֪ʶ�ܽ�
��һ��ѧ��ĩ����
���������У���ɫ��ζ���ǣ� ����
A��SO2 B��NO2 C��Cl2 D��N2
A����������ѧʽ��SO2������������������ɫ���壬��ǿ�Ҵ̼�����ζ��
B����������(NO2)
�ֳ�Ϊ�����������Ǵ�м��ṹ�ĵ��ͷ��ӡ���м������������ӣ�������������ɼ��й����һ�����뷴���й������������������Ϊ����ɫ���壬������ˮ�Ҿ��д̼�����ζ��
C��Cl2,������ͨ���ʻ���ɫ���ж����д̼�����ζ���ܶȱȿ������������ſ������ռ���Һ̬ʱΪ���ɫ
D��������N2����������һ����ɫ��ζ��������壬��ͨ������
���Դ��ǣ� D ����
�����õ������ԭ��������H��1��O��16��C��12��N��14��S��32��Cl��35.5��Ca��40��Mg��24��Al��27��Ba��137, I��127
( �ڢ�� )
ѡ���� ( ÿС��ֻ��1 ��ѡ��������� 25��2=50��)
1.���й������������У�����ȷ����( B )
A.���ǵؿ��ﺬ�����Ľ���Ԫ�� B.�ڳ����£������ܺ�������Ӧ
C.����һ�ֱȽϻ��õĽ��� D.�ڻ�ѧ��Ӧ�У�������ʧȥ���ӣ��ǻ�ԭ��
2.����������һ���ǽ���Ԫ�ص���( D )
A.��ʧȥ���ӵ����� B.�����ᷴӦ������
C.ԭ�ӵ������ֻ��1�����ӵ�Ԫ�� D.ԭ�Ӻ�����11�����ӵ�Ԫ��
3.Ϊ�˼���ijFeCl2��Һ�Ƿ���ʣ�������Һ�м���( )
A.NaOH��Һ B.��Ƭ C.ʯ����Һ D.KSCN��Һ
4.��ʵ�����Ҫ��ʹAlCl3��Һ�е�Al3+ȫ���������� ��Ӧѡ�������Լ��е�( C )
A.Ba(OH)2��Һ B.NaOH��Һ C.��ˮ D.����
5.������Ŀ�ĵ����������������е�һ�ֶԲ������п�ʴ���Ƴɵġ�����������( B )
A. ���� B.����� C.�ռ� D.����
6.��84������Һ���ճ������й㷺ʹ�ã�������Һ��ɫ ����Ư�����á�������Ч�ɷ������������е�һ�֣�����������( )
A.NaOH B.NaClO C.KMnO4 D.Na2O2
7.�������岻����ɿ�����Ⱦ����( )
A.N2 B.NO C.NO2 D.SO2
8.��NO2 ��ˮ�ķ�Ӧ��( D )
A.��Ԫ�صĻ��ϼ۲������仯 B.NO2ֻ��������
C.NO2ֻ�ǻ�ԭ�� D.NO2�������������ǻ�ԭ��
9.���������������Ӧʱ������SԪ�ػ�NԪ�صĻ��ϼ۲������仯����( )
A. ϡ���� B.Ũ���� C. Ũ���� D.ϡ����
10.�����������������������ﵫ������ˮ����( )
A.CO2 B.SiO2 C.SO3 D.Fe2O3
11.���������мȿ���Ũ�������ֿ����ù���NaOH�������( )
A. Cl2 B.O2 C.SO2 D.NH3
12. һ������Ũ������������ͭ��ַ�Ӧ�ռ����������ǣ� ��
A ֻ��NO2 B ֻ��NO
C NO2��NO D NO2��H2
13. ��ҵ���÷�ͭм��ԭ���Ʊ�����ͭ��Ϊ�˽�Լԭ�Ϻͷ�ֹ��Ⱦ�������˲��õķ�����( )
A.Cu + HNO3(Ũ) �� Cu(NO3)2
B.Cu +HNO3(ϡ) �� Cu(NO3)2
14.SO2��Cl2������Ư���ԣ�������ͬ״���µ����������������ͬʱ�����ڳ�ʪ����ɫ���ʣ��ɹ۲쵽��������( D )
A��������ɫ B��������ɫ C������ɫ����ԭ D����ɫ����
15.��������CO2ͨ��������Һ�У��ܲ�����������( A )
A����������Һ B��ʯ��ˮ C���Ȼ�����Һ D���Ȼ�����Һ
16.��һ���Լ�֤����ʯ���к���ʯ��ʯ��ʯӢ�������Լ��������˵���( )
A������ B������ C��NaOH��Һ D���Ȼ�����Һ
17. ��֤���������������̼�����Ե�ʵ����ʵ��( )
A��CO2����ˮ�γ�̼�ᣬSiO2������ˮ
B��CO2ͨ������Թ������������������
C��������SiO2��̼���η�Ӧ����CO2
D���Ȼ���ͨ�������̼������Һ�зų����壬ͨ������Թ�������Һ�����ɳ���
18. ��aL������狀�����淋Ļ��Һ�ֳ����ȷݣ�һ������b mol�ռ�պðѰ�ȫ���ϳ�����һ�����Ȼ�����Һ��Ӧʱ������c mol�Ȼ������ɴ˿�֪ԭ��Һ��NO3- �������ʵ���Ũ���ǣ���λ��mol?L��1�� ( )
A�� B�� C�� D��
19.�����з�Ӧ�У�����ֻ���ֳ�ǿ�����Եķ�Ӧ�� �� ��
A��C��ŨH2SO4��Ӧ B��Cu��ŨH2SO4��Ӧ
C��CuO��H2SO4��Ӧ D��Mg(OH)2��H2SO4��Ӧ
20.���������Լ��ɽ�NaCl��Na2CO3����NH4��2SO4��NH4Cl������Һ���ֿ�( )��
A��AgNO3��Һ B��BaCl2��Һ��
C��Ba��OH��2��Һ D��KOH��Һ
21.���������м��ܸ�ϡH2SO4��Ӧ�����ܸ�����������Һ��Ӧ����( )
��NaHCO3 ��Al2O3 ��Al(OH)3 ��Al
A��ȫ�� B���ڢۢ� C���٢ۢ� D���ۢ�
22. ����ɫ��ǿ������Һ�У��ܴ����������( )
A��Na+��Al3+��NO3����Cl�� B��K+��Na+��Cl����AlO2��
C��Fe2+��K+��SO42����Cl�� D��Na+��HCO3����K+��NO3��
23.ͬ��ͬѹ�£�����������ĸ�����ƿ�зֱ������NH3 ����NO2 ��������Ȫʵ�飬��ͼ��ʾ������ַ�Ӧ��ƿ����Һ�����ʵ���Ũ��( )
A. ��>�� B.��<�� C.��=�� D.����ȷ��
24.��һ֧2 0 ml ʢ��NO2 ��O2 ���������Թܵ���ʢˮ��ˮ���У�����ַ�Ӧ����ˮ���Թ��в�������ʱ���Թ���������2 ml ���塣��ԭ���������NO2 �������Ϊ( B )
A.12.8 ml B.17.2 ml C.13.6 ml D.16.8 ml
25.���ܱ�������ʢ��H2��O2��Cl2�Ļ�����壬ͨ�����ȼ����������������ȫ��Ӧ������
��Һ�����ʵ���������Ϊ25.26%����������ԭ�е�H2��O2��Cl2������֮��Ϊ�� ��
A��6:3:1 B��9:6:1 C��13:6:1 D��10:6:1
( �ڢ�� )
26.(8��)ij����Һ�п��ܺ���Ag+��Fe3+��K+��Ba2+��NH4+ �����ӣ���������ʵ�飺
��1�����������ϡ���ᣬ�а�ɫ�������ɡ�
��2�����ˣ�����Һ�м��������ϡ���ᣬ���а�ɫ�������ɡ�
��3�����ˣ�ȡ������Һ������2��KSCN��Һ��û�����Ե�������֡�
��4����ȡ�������裨3���е���Һ������NaOH��Һ��ʹ��Һ�ʼ��ԣ����ȣ��ɲ���ʹʪ��ĺ�ɫʯ����ֽ����ɫ�����塣
����ʵ������ش𣺴���Һ��һ������ ���ӣ�
һ�������� ���ӣ�����_________________���Ӳ���ȷ���Ƿ���ڣ�Ҫ������Щ���ӵ�ʵ�鷽���� ��������______________________________________________��
27.(12��)����Ҫ��ش�������⣺
(1) ��ȥ���������������е���������(������Ϊ����)��д���йصķ�Ӧ����ʽ��
��ͭ�� (����) ��
��FeCl3 ��Һ(FeCl2 ) ��
��N2 (O2) ____________________________________________________��
(2)��ͼ��ʾ����仯��δ֪���о�������Ԫ�أ�EΪ����ɫ��ĩ���ݴ˻ش��������⣺
��д��A��B�Ļ�ѧ����ʽ���������ת�Ƶķ������Ŀ��
____________________________________________________________
����B��C�ı仯������C����Һ�������������е����ʣ�������ˮ�������� ����Ҫԭ���� ���������� ����Ҫԭ���� ��
28.(8��) �������£�����A��B��C�ֱ�Ϊ���塢����ɫ���塢��ɫ���壬�ں��ʷ�Ӧ�����£����ǿ������п�ͼ���з�Ӧ����֪E��Һ����ɫ��Һ����ش�
(1) (�û�ѧʽ���)
A��______________B��________________
(2)��Ӧ�ٵĻ�ѧ����ʽΪ____________________________________________________
��Ӧ�۵����ӷ���ʽΪ___________________________________________________
��Ӧ�ݵĻ�ѧ����ʽΪ___________________________________________________
29.(10��)��ͼΪʵ������ȡ�����������Cl2�������м���Cl2����ʵ���װ�á�����Dƿ�з��и����ɫ������E��Ϊͭ����E�Ҷ˳����ܿڸ���Ϊʯ����
�Իش�
��1��A�з�����Ӧ�ķ���ʽΪ_____________ _________________________________��
��2��Ϊ�õ����﴿����������һ����Bƿ�м��뱥��ʳ��ˮ����������______________��
��3��C��ʢ�ŵ��Լ�Ϊ_____________��
��4��E����������Ӧ�ķ���ʽΪ____________________________________________��
(5) F��Ӧ������Լ�Ϊ ���������� ��
(6) ��A����14.6g HCl ��������������������ͨ��������KI��Һ���ܲ������ʵ������ Ϊ_____________g��
30.(6��)ʵ�����ﳣ���Ȼ�狀�������ʯ�һ�ϼ�����ȡ������
(1)����Ҫ500 ml (��״��)�������������ȡ�Ȼ�淋������Ƕ��� ��(��������ƽ����)
(2)����5000 ml (��״��)��������ˮ���100 ml ��Һ����ˮ��NH3 �����ʵ���Ũ���Ƕ��� ��( ������NH3 ��ˮ�ķ�Ӧ)
31.(6��)��һС��þ���Ͻ�����100mL�����У�Ȼ�������е��� ��Һ�����ɳ����������ͼ���NaOH��Һ���������ͼ��ʾ��
��1���Ͻ���þ�������Ե�������
��2����������ʵ���Ũ�ȡ�
������һ��20xx����ѧ����ĩ���� ��ѧ�Ծ�
( �� �� )
( ʱ����90���� �� ���֣�100��)
�����ˣ���һ��ѧ������
�����õ������ԭ��������H��1��O��16��C��12��N��14��S��32��Cl��35.5��Ca��40��
Mg��24��Al��27��Ba��137,I��127
ѡ���� ( ÿС�����һ��ѡ��������⣬2��25=50�� )
��� 1 2 3 4 5 6 7 8 9 10 11 12 13
��
��� 14 15 16 17 18 19 20 21 22 23 24 25
��
26.(8��) ����ʵ������ش𣺴���Һ��һ������ ���ӣ�
һ�������� ���ӣ�����_____________���Ӳ���ȷ���Ƿ���ڣ�Ҫ������Щ���ӵ�ʵ�鷽���� ��������______________________________________________��
27.(12��)
(1) ��ͭ�� (����) ��
��FeCl3 ��Һ(FeCl2 ) ��
��N2 (O2) ____________________________________________________��
(2) ��д��A��B�Ļ�ѧ����ʽ���������ת�Ƶķ������Ŀ�� ____________________________________________________________
����B��C�ı仯������C����Һ�������������е����ʣ�������ˮ�������� ___��
��Ҫԭ���� _______________________________________________________
�������� ����Ҫԭ���� _____________________________��
28.(8��) (1) (�û�ѧʽ���)
A��______________B��________________
(2)��Ӧ�ٵĻ�ѧ����ʽΪ____________________________________________________
��Ӧ�۵����ӷ���ʽΪ___________________________________________________
��Ӧ�ݵĻ�ѧ����ʽΪ___________________________________________________
29.(10��) �Իش�
��1��A�з�����Ӧ�ķ���ʽΪ_____________ _________________________________��
��2��Ϊ�õ����﴿����������һ����Bƿ�м��뱥��ʳ��ˮ����������______________��
��3��C��ʢ�ŵ��Լ�Ϊ_____________��
��4��E����������Ӧ�ķ���ʽΪ____________________________________________��
(5) F��Ӧ������Լ�Ϊ ���������� ��
(6) ��A����14.6g HCl ��������������������ͨ��������KI��Һ���ܲ������ʵ������ Ϊ_____________g��
30.(6��)ʵ�����ﳣ���Ȼ�狀�������ʯ�һ�ϼ�����ȡ������
(1)����Ҫ500 ml (��״��)�������������ȡ�Ȼ�淋������Ƕ��� ��(��������ƽ����)
(2)����5000 ml (��״��)��������ˮ���100 ml ��Һ����ˮ��NH3 �����ʵ���Ũ���Ƕ��� ��( ������NH3 ��ˮ�ķ�Ӧ)
31.(6��)��һС��þ���Ͻ�����100mL�����У�Ȼ�������е��� ��Һ�����ɳ����������ͼ���NaOH��Һ���������ͼ��ʾ��
��1���Ͻ���þ�������Ե�������
��2����������ʵ���Ũ�ȡ�
������һ��20xx����ѧ����ĩ����
���
1. B 2. D 3.D 4. C 5.B
6.B 7. A 8. D 9. A 10. B
11. B 12. C 13. C 14. D 15. A
16. A 17. B 18. B 19. A 20. C
21. A 22. B 23. C 24. B 25. C
26. Ag+��Ba2+��NH4+ ��Fe3+ ��K+ ����ɫ��Ӧ���ò�˿մȡ��Һ�ھƾ��������ղ�����ɫ�ܲ����۲������ɫ
27.(1) ��2Al + 2H2O + 2OH- = AlO2- + 3H2 ���� 2Al + 6H+ == 2Al3+ + 3H2��
�� 2FeCl2 + Cl2 ==3 FeCl3
�� 2Cu + O2 == 2CuO
(2) 2Na +2H2O == 2NaOH + H2�� ��������NaOH ����CO2 ���٣�NaOH����
������NaHCO3 ����CO2 ������Na2CO3ת��ΪNaHCO3
28. A��Fe B��Cl2
�� 2Fe + 3Cl2 == 2FeCl3
�� Fe +2H+ == Fe2+ + H2��
�� 4Fe(OH)2 + O2 + 4H2O == 4Fe(OH)3
29. MnO2 +4HCl === MnCl2 + Cl2�� + 2H2O ������HCl���壻ŨH2SO4 ��
Cu + Cl2 === CuCl2 ����Һ�����ն����������50.4 g
30. NH4Cl ��1.2 g C (NH3) = 2.2 mol?L-1
31. m (Al) = 0.27g m (Mg) = 0.12 g
C(HCl) == 0.5 mol?L-1
