定制式义齿产品技术审评规范
根据《医疗器械注册管理办法》(国家食品药品监督管理局令第16号)的要求并结合定制式义齿产品的特点,为规范该类产品的技术审查工作和指导该类产品的注册申报工作,特制定本规范。
一、术语
下列术语定义适用于本规范
(一)义齿
人工制作的能够恢复缺失牙齿的形态、功能、外观的修复体。
(二)固定义齿
患者不可自行摘戴的义齿,由固位体、桥体和连接体组成,也包括牙体缺损的固定修复体,如冠、嵌体、桩核、贴面及种植义齿的上部结构。
(三)固位体
为了义齿的固位,而制作在基牙或种植体上的固位部分。
(四)桥体
是固定义齿位于缺牙区的人工牙,用以恢复缺失牙的形态和功能。
(五)连接体
在固定义齿中连接固位体和桥体的部分,在活动义齿中指大、小连接体。
(六) 活动义齿(可摘义齿)
牙列缺损的活动修复为可摘局部义齿,由固位体、连接体、人工牙和基托组成;牙列缺失的活动修复为总义齿,由人工牙和基托组成。
二、适用范围
本规范所称定制式义齿是指人工制作的能够恢复牙体缺损、牙列缺损、牙列缺失的形态、功能及外观的修复体。定制式义齿产品可以分为固定义齿及活动义齿两类。
本规范适用于《医疗器械分类目录》中Ⅱ-6863-16定制式义齿产品。
三、技术审查要点
(一)产品名称
定制式义齿产品的产品名称,以产品的结构或功能予以命名。如“金属烤瓷冠”、“桩核”等。
1、固定义齿
(1)按功能命名
冠、桥、嵌体、桩核、贴面等。
(2)按材料结构命名
金属冠与桥、全瓷(渗透瓷、CAD/CAM瓷块、铸瓷)冠与桥、金属烤瓷(铸造、金沉积)冠、桥等。
2、活动义齿
(1)按功能命名
可摘局部义齿、总义齿等。
(2)按材料结构命名
弯制支架可摘局部义齿、铸造支架可摘局部义齿、树脂基托总义齿、铸造基托总义齿等。
(二)产品工作原理
义齿产品是义齿加工企业,依据医生提供的义齿加工单和患者的牙模,选择合适的材料和工艺,生产出符合医生设计要求的产品,并能够使牙体缺损或牙列缺失、牙列缺损患者的咀嚼功能和形态得以恢复。
(三)产品适用的相关标准
义齿根据产品特点可参照以下相关标准(但不局限以下标准)
1、GB/T 191-2000包装储运图示标志;
2、GB/T 6387-1986 齿科材料名词术语
3、GB/T 17168-1997 齿科铸造贵金属合金
4、YY 0301-1998 牙科学 陶瓷牙
5、YY 0305-1998 羟基磷灰石生物陶瓷
6、YY 0270-2003 义齿基托聚合物
7、YY 0300-1998 牙科学 合成树脂牙
8、ISO 9693-1999 齿科金属——烤瓷修复体系
9、ISO 6872:1995/Amd.1 :1997 齿科陶瓷(Dental ceramic)
10、ISO 22112:2005牙科学 修复用人工牙(Dentistry –Artificial teech for dental prostheses)
11、ISO 6871-1:1994 铸造金属合金 第1部分:钴合金
12、ISO 6871-2:1994 铸造金属合金 第2部分:镍合金
13、ISO 1562:2004 牙科 铸造金合金(Dentistry -Casting gold alloys)
14、ISO 8891:1998 贵金属含量在25%~75%(不含75%)的齿科铸造合金(Dental casting alloys with nobel metal content of at least 25% but less than 75%)
注:以上标准适用于最新版本。
(四)产品的预期用途
定制式固定义齿:用于牙列缺损或牙体缺损的修复。
定制式活动义齿:用于牙列缺损、牙列缺失的修复。
(五)产品的主要风险
义齿产品在进行风险分析时至少应包括以下的主要危害,企业还应根据自身产品特点确定其他危害。(见表1)
表1义齿产品的主要危害

(六)产品的主要技术要求
1、固定义齿的主要技术要求
(1)定制式固定义齿应按医疗机构提供的工作模型及设计文件制造。
(2)定制式固定义齿的制作,应使用具有医疗器械注册证书的齿科烤瓷合金、齿科铸造合金、瓷粉、瓷块、复合树脂、铸造蜡、铸造包埋材料及其它按医疗器械管理的产品。
(3)定制式固定义齿中牙冠的颜色,应符合设计文件的要求。
(4)定制式固定义齿固位体、连接体的表面应光滑、有光泽、无裂纹、无孔隙。
(5)金瓷结合性能
金属烤瓷定制式固定义齿的金瓷结合强度应不小于25MPa。
(6)耐急冷热性能
按照YY 0301-1998 6.5规定的方法试验, 定制式固定义齿的任何瓷质部分不得出现裂纹。
(7)义齿与相邻牙之间的接触部位应与同名天然牙的接触部位相同。
(8)定制式固定义齿边缘与工作模型的密合性
定制式固定义齿边缘与工作模型之间不应有明显的缝隙,且用牙科探针划过时,应无障碍感。
(9)义齿的咬合面应有接触点,但不应产生咬合障碍。
(10)人工牙的形态及唇面微细结构,应与同名天然牙基本一致。
2、活动义齿的主要技术要求
(1)定制式活动义齿应按医疗机构提供的工作模型及设计文件制造。
(2)定制式活动义齿的制作,应使用具有医疗器械注册证书的齿科铸造合金、陶瓷牙、合成树脂牙、义齿基托树脂、基托蜡、铸造蜡、铸造包埋材料及其它按医疗器械管理的产品。
(3)定制式活动义齿中除组织面外,人工牙、基托、卡环及连接体均应光滑。
(4)定制式活动义齿的组织面不得存在残余石膏。
(5)义齿基托、连接体和卡环不应有气孔、裂纹和夹杂。
(6)定制式活动义齿中合成树脂牙的颜色,符合设计文件的要求。
(7)定制式活动义齿中义齿基托树脂部分的色稳定性良好。
a)光源和试验箱
见YY0270-2003 中8.4.2.7的规定。
b)步骤
适当选取(或截取)定制式活动义齿中义齿基托树脂较宽区域,其中部分被锡箔或铝箔覆盖,置入试验箱(2.7.1)中的照射光源下,并浸入(37±5)℃水中,照射24h。在阴天漫反射日光下或其光线不低于1000lx,三个观察者目力观察照射部分与被锡箔或铝箔覆盖部分颜色的差别,观察时间不大于2s。
c)试验结果
记录三个观察者对颜色差别的评定,取其两个或两个以上相同的评定作为试验结果。定制式活动义齿中义齿基托树脂的颜色,被照射部分与未被照射部分比较只能有轻微(很难察觉)的变化。
(8) 可摘局部义齿应具有稳固的固位性能。可摘局部义齿与其工作模型固位稳定无翘动且便于摘戴。
(9) 全口总义齿的上、下颌定制式活动义齿对合后,4-7牙位均应有接触,且上下颌定制式活动义齿之间应无翘动现象。人工牙的工作尖基本位于牙槽嵴顶。
(八)产品的检验规则、抽样原则
产品检验分为出厂检验和周期检验。
1、定制式固定义齿应由检验部门进行逐件出厂检验,合格后方可出厂。出厂检验项目至少应包括固定义齿的主要技术要求中的(1)、(2)、(3)、(4)、(7)、(8)、(9)、(10)。
定制式活动义齿应由检验部门进行逐件出厂检验,合格后方可方可出厂。出厂检验项目至少应包括活动义齿的主要技术要求中的
(1)、(2)、(3)、(4)、(5)、(6)、(9)。
2、周期检验项目为全项目。
(九)产品的临床举证要求
应从产品的工艺、材料和临床应用史三个方面进行临床举证。
(十)标志、包装、运输和贮存
产品说明书、标签和包装标识的编写要求,应符合《医疗器械说明书、标签和包装标识管理规定》(10号令)
1、包装的标志:
制造厂名称、地址和电话;
产品名称;
产品编号;
出厂日期;
产品注册证号。
2 、每一包装内应附有检验合格证
合格证上应有下列内容:
制造厂名称;
检验员代号;
产品名称。
3、包装要求
(1)包装具有防挤压的功能,在正常搬运和贮存期间产品不应损坏;
(2)包装中应有设计单、合格证等。
(十一)产品的不良事件历史记录
应建立不良事件的监测报告制度。
(十二)注册单元划分的原则和实例
产品的注册单元原则上以修复方式为划分依据,预期用途不作为划分注册单元的依据。如固定义齿,活动义齿。
(十三)同一注册单元中典型产品的确定原则、抽样原则和实例
1、同一注册单元内,典型产品作为被检测的产品。典型产品是指能够含盖本注册单元内全部产品工艺的一个或多个产品。
2、抽样原则
按照“同一注册单元内,所检测的产品应当是能够代表本注册单元内其他产品安全性和有效性的典型产品”的原则,抽取样品应能涵盖该注册单元全部产品的生产工艺。
如:活动义齿应抽取带弯制卡环的铸造支架局部义齿和全口总义齿各一套。
如:固定义齿应抽取义齿样品数量不低于3单位的金属烤瓷桥(铸造和沉积)和全瓷桥(渗透瓷、CAD/CAM瓷块和铸瓷)进行检测。
如企业只生产单冠产品,可抽取1颗单冠进行检测。
(十四)注意事项、禁忌症的说明
注意事项至少应包括:
(1)定制式义齿需要由具有专业资质的医师进行戴用调试,,戴用前需要将定制式义齿进行清洁、消毒等。
(2)定制式固定义齿戴用后的咀嚼提示。
(3)定制式活动义齿不能用酸性和碱性清洗剂、饭后和睡前应摘下清洗,不可以用热水浸泡等。
禁忌症至少应有以下内容:
(1)精神病患者有吞服活动义齿危险者;
(2)对齿科材料过敏者;
(3)基牙形态不适合戴用义齿者。
第二篇:定制式义齿产品
定制式义齿产品 技术指导原则
辽宁省食品药品监督管理局技术审评中心 发布
目 次
一、适用范围 ........................................................................................................................................................................ 1
二、内容与要求 .................................................................................................................................................................... 1
(一)产品名称 ................................................................................................................ 1
(二)产品的结构、组成及分类 ....................................................................................... 1
(三)产品应适用的相关标准........................................................................................... 2
(四)产品的预期用途 ..................................................................................................... 2
(五)产品的主要风险 ..................................................................................................... 2
(六)产品的主要技术性能指标 ....................................................................................... 5
(七)产品的检测要求 ..................................................................................................... 7
(八)产品的临床要求 ..................................................................................................... 7
(九)该类产品的不良事件历史记录 ................................................................................ 8
(十)产品说明书、标签和包装标识 ................................................................................ 8
(十一)审查关注点 ............................................................................................................ 9
前 言
根据《医疗器械注册管理办法》(国家食品药品监督管理局令第16号)的要求并结合定制式义齿的特点,制定本技术审查指导原则。
本指导原则旨在指导和规范定制式义齿的技术审评工作,帮助审查人员增进对该类产品的结构、主要性能、预期用途等方面的理解,方便审查人员在产品注册技术审评时把握基本的要求和尺度。
本指导原则由辽宁省食品药品监督管理局技术审评中心提出。 本指导原则起草单位:辽宁省食品药品监督管理局技术审评中心。 本指导原则主要起草人:李非、迟戈、吕大雷。
本指导原则首次发布时间为20xx年8月。
本指导原则第一次修订时间为20xx年2月。
定制式义齿产品技术指导原则
一、适用范围
本指导原则适用于使用已注册的义齿材料生产的定制式义齿产品(以下简称“义齿”)。
本指导原则不适用于使用未注册的材料生产的定制式义齿。
二、内容与要求
(一)产品名称
根据是否能够自由摘戴分为定制式固定义齿和定制式活动义齿。不能使用不规范的名称,如“假牙”,不建议使用的名称有“烤瓷牙”、“可摘义齿”。
(二)产品的结构、组成及分类
1. 定制式固定义齿一般按材料不同分为金属修复体(又称金属牙)和烤瓷熔附金属修复体(又称金属烤瓷牙),按结构分为冠、桥、嵌体和贴面。
金属修复体由合金(如镍铬合金等)铸造而成。
烤瓷熔附金属修复体是由金属(如钴铬合金、镍铬合金、钛合金等)和瓷粉经过加工而成。
1
2.定制式活动义齿由人工牙、基托、连接体、固位体经加工而成,如将树脂人工牙固定在有固位体的金属基托上;定制式活动义齿一般按人工牙的基托材质分为树脂托义齿和金属钢托义齿,按结构分为全口义齿和局部义齿。
(三)产品应适用的相关标准
GB/T191-2000 包装储运图示标志
GB/T2829-2002 周期检验计数抽样程序及表(适用于对过程稳定性的检验)
GB/T6387-1986 齿科材料名词术语
GB/T9938-1988 牙位和口腔区域的标示法
《医疗器械说明书、标签和包装标识管理规定》(国家食品药品监督管理局令第10号)。
《关于印发定制式义齿注册暂行规定的通知》(国食药监械
[2003]365号)。
(四)产品的预期用途
定制式固定义齿:用于人体牙齿缺损、缺失的替代和修补。 定制式活动义齿:用于人体牙齿缺失的替代。
(五)产品的主要风险
2
能量危害没有涉及,生物学危害、环境危害、与医疗器械使用相关的危害、功能性失效、维护和老化引起的危害和形成因素都应逐条全面分析。
表1 定制式义齿危害分析
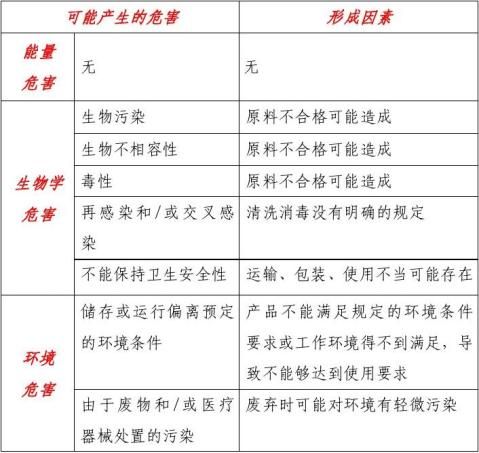
3
4
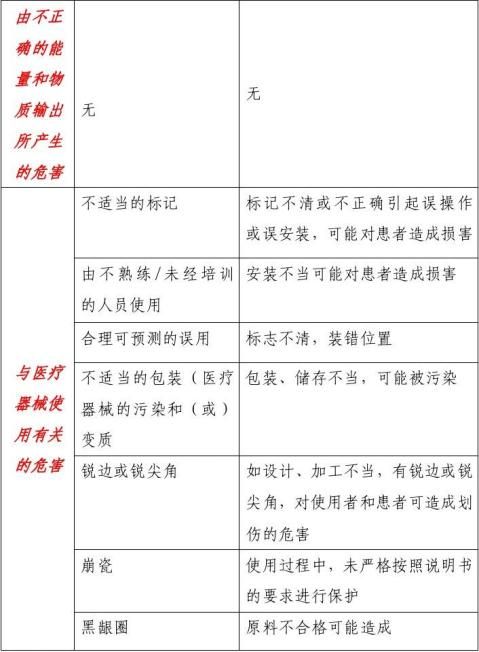
(六)产品的主要技术性能指标
定制式义齿性能可从生物性能、化学性能和机械性能等方面进行描述。
定制式固定义齿的基本要求:
1.修复体的制作应符合口腔临床医生的设计要求。
2.修复体在模型上应有良好的密合度。在修复体边缘处,肉眼应观察不到明显的缝隙,用牙科探针划过时应无障碍感。 5

3.修复体的邻面与相邻牙之间的接触部位应与同名正常牙的接触部位相一致。
4.修复体的咬合面应有接触点,但不应存在咬合障碍。
5.修复体的外形及大小应与同名牙相匹配,应符合牙齿的正常解剖特点。
6.修复体瓷质部分的颜色应与医生设计单中要求的色号相符。用肉眼观察应无裂纹、无气泡。
7.修复体的金属部分应高度抛光,表面粗糙度应达到Ra≤0.025。用肉眼观察应无裂纹、无气泡,内部应无气孔、夹杂。
8.冠修复体唇、颊面的微细结构应与正常牙一致。
9. 修复体应具有耐急冷热性能,按规定的方法进行试验后,不得出现裂纹。
10. 修复体应具有一定的耐腐蚀性能,将其放在模拟的口腔唾液中浸泡,表面不应有明显变色。
定制式活动义齿的基本要求:
1.活动修复体应符合口腔临床医生的设计要求。
2.修复体中除组织面外,假牙、基托、卡环及连接体均应高度抛光。表面粗糙度应达到Ra≤0.025。
3.修复体的组织面不得存在残余石膏。
4.树脂基托不能有肉眼可见气孔和裂纹,铸造的基托、连接体和卡环内部应无气孔、夹杂。
6
5.全口总义齿的上、下颌修复体对咬后,4-7牙位均应有接触,且上下颌修复体之间应无翘动现象。
6. 活动修复体应具有耐急冷热性能,按规定的方法进行试验后,不得出现裂纹。
7. 活动修复体应具有一定的耐腐蚀性能,经耐腐蚀试验后,表面不应有明显锈迹、斑痕等缺陷。
(七)产品的检测要求
出厂检验要求有出厂检验报告、过程检验记录和检测仪器清单。各种规格的义齿都应逐个检测,不应漏检。
出厂检验报告至少应包括以下内容:
(1)产品名称、规格型号、产品编号或批号、生产日期;
(2)检测依据、检测项目、标准要求、检测结果、结果判定、两名检验人员、审核人及批准人签字或盖章、检验日期等;
(3)检验仪器清单,过程检验记录。
出厂检验项目应包括功能、外观、色泽、形态与配合。 注册检验报告应覆盖义齿产品的所有规格。
(八)产品的临床要求
制作应符合口腔临床医生的设计要求。
定制式义齿产品依据国家食品药品监督管理局第16号令附件12有关第二类产品B条“境内产品中国政府已批准同类产品在中国上市,提交同类产品的临床试验资料和对比说明”的规定,以及辽宁省食品药品监督管理局下发的《定制式义齿生产 7
注册实施意见》的相关要求,产品的安全性及有效性得到确认后,可以提出临床豁免。
临床情况说明应从产品的工艺、材料和临床应用史三个方面阐述。并应提供主要材料(烤瓷合金、烤瓷粉、支架合金、聚合物等)有效期内的材料外购证明即外购合同和供方的注册证和登记表。
(九)该类产品的不良事件历史记录
暂无。
(十)产品说明书、标签和包装标识
1. 产品说明书、标签和包装标识的编写应符合《医疗器械说明书、标签和包装标识管理办法》的规定。
2.说明书:
标题要求应写明“XX产品的说明书”,例如“定制式活动义齿说明书”。
内容要求各项标题分别为产品的主要性能、结构、材料组成、适用范围、使用方法、注意事项、禁忌症、维护和保养及使用寿命(一定要注明),还必须有生产企业许可证号、注册证号、注册地址、生产地址、标准编号等。
注意事项:定制式义齿需要有专业资质医师进行安装调试,安装前需要将定制式义齿消毒等。
维护和保养:定制式义齿不能用酸性和碱性清洗剂冲洗,
8
不可咀嚼过硬的食物。定制式固定义齿与自身牙齿清洁方法相同;定制式活动义齿饭后和睡前应摘下清洗,不可以用热水浸泡,摘戴时用力要轻,正确判断方位。
禁忌症主要包括以下方面:
精神病患者有吞服义齿危险者;
生活不能自理者;
对齿科材料过敏者;
口腔粘膜溃疡患者;
基牙形态不适合配戴或安装义齿者;
未成年人慎用。
(十一)审查关注点
注册申请表所填写内容应与标准、说明书等其他材料内容相对应。
注册材料中涉及的产品名称、型号规格、主要结构及性能应审查是否与标准相一致。
义齿加工所用齿科材料必须具备医疗器械生产企业的注册证和认购表。
金属修复体与烤瓷熔附金属修复体所使用的合金材料不可混淆。
9
