定制式义齿生产企业许可证现场检查内容
一、检查内容
定制式义齿生产现场检查按照《定制式义齿生产企业许可证现场检查评分表》(以下简称现场检查评分表)规定进行,检查内容分为 5部分,其中否决项6项,总分为 300 分,各部分内容和分值分别为:
1.人员资质 70分
2.场地设施 80分
3.法规及管理文件 40分
4.生产能力 40分
5.检验能力 70分
二、评定方法
1.按《现场检查评分表》中检查方法进行评分时,最多将该条目规定的分数全部扣除。
2.对于《现场检查评分表》中未明确评分方法时,应按评分通则评分,即该条目实得分等于该条目标准分乘以得分系数。得分系数及含义分别为:
1.0 全面达到规定要求;
0.8 执行较好,但仍需改进;
0.7 基本达到要求,部分执行较好;
0.6 基本达到要求;
0.5 已执行,但尚有一定差距;
0 未开展工作。
3.现场检查记录中的“合计”应包括总实得分及总得分率。总实得分为各部分实得分之和,总得分率=总实得分/总分×100%。
三、判定标准
1.“否决项”均合格且各部分得分率均达到80%以上的,则检查结果判定为合格。
2.“否决项”均合格且各部分的得分率均达到60%以上,但其中一部分的得分率不足80%的,应要求企业进行整改并复查;复查仍不合格的,则检查结果判定为不合格。
3.有1项“否决项”不合格的,则检查结果判定为不合格。
4.“否决项”均合格,但其中一部分得分率不足60%的, 则检查结果判定为不合格。
四、检查结论
1.现场检查后,应及时填写《定制式义齿生产企业许可证现场检查记录》(以下简称现场检查记录)。
2.按照检查判定标准,检查结果为合格或不合格的,检查人员应在《现场检查记录》的“检查结论”栏中填写相应的检查意见,并对否决项和主要存在的问题进行描述。
3.检查人员、企业负责人(或法定代表人)及相关人员均应在《定制式义齿生产企业许可证现场检查记录》上签字并加盖企业公章(如有)。
五、现场检查人员不得少于2人。检查人员必须遵守现场检查工作纪律。
六、定制式义齿生产企业许可证现场检查记录
检查事项类型:核发□ 变更□ 换发□ 日常监督□
被检查企业:
检查场地:
拟生产产品名称:

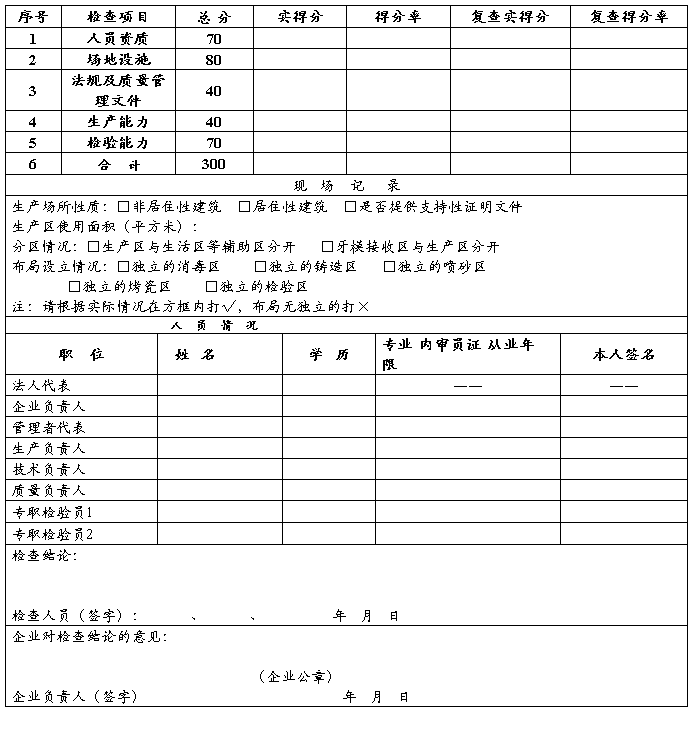
检查情况:
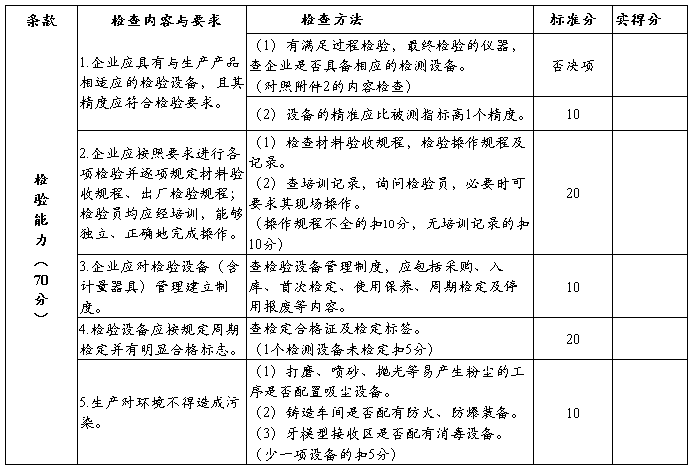
七、定制式义齿生产企业许可证现场检查评分表
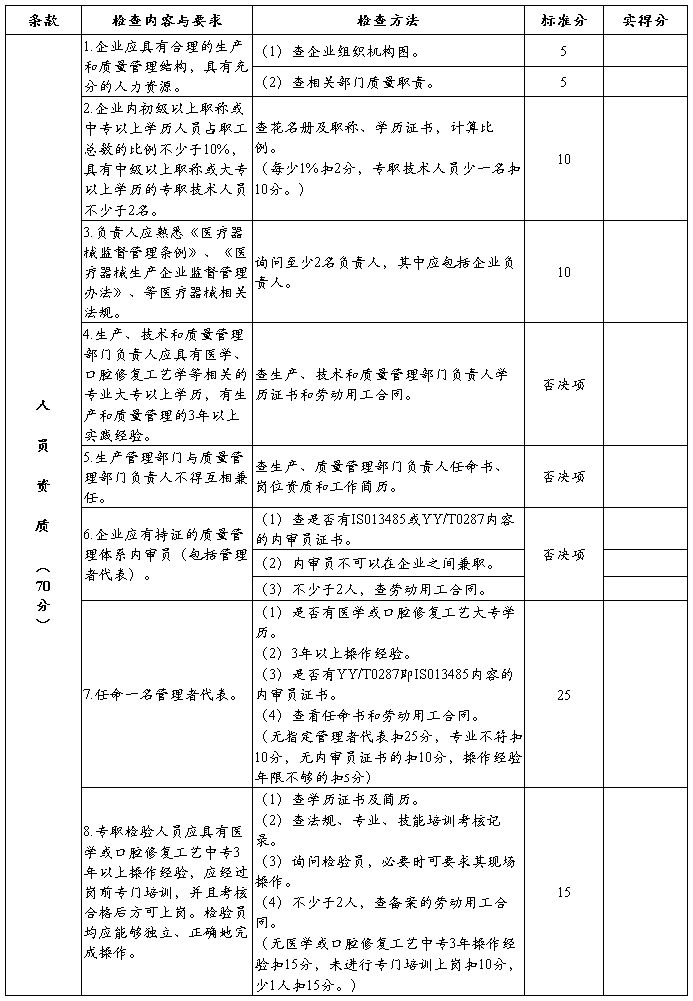
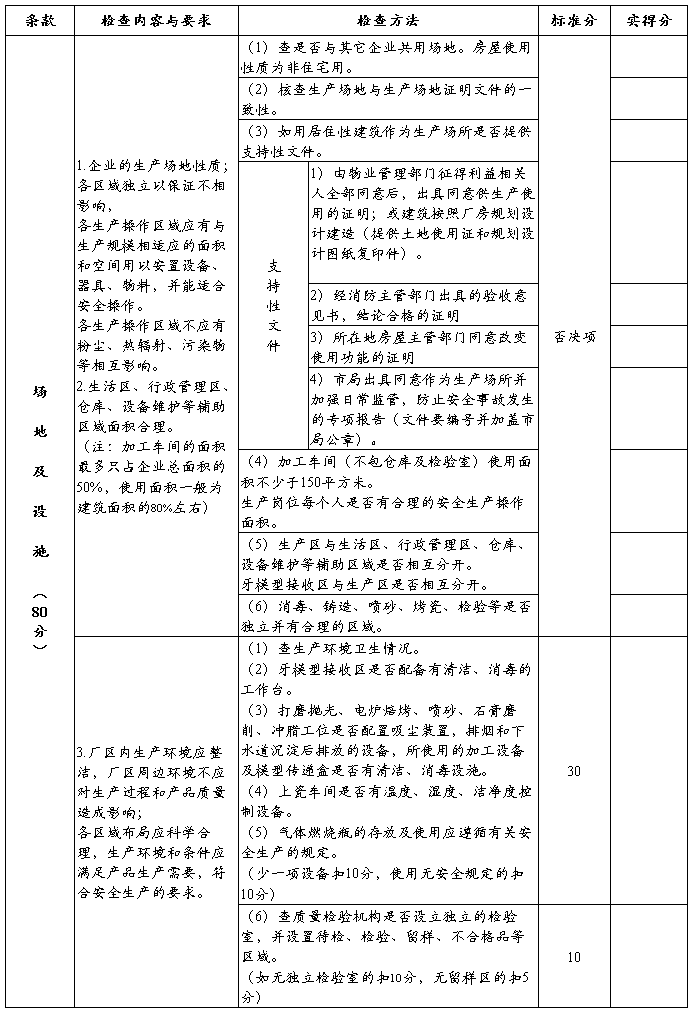

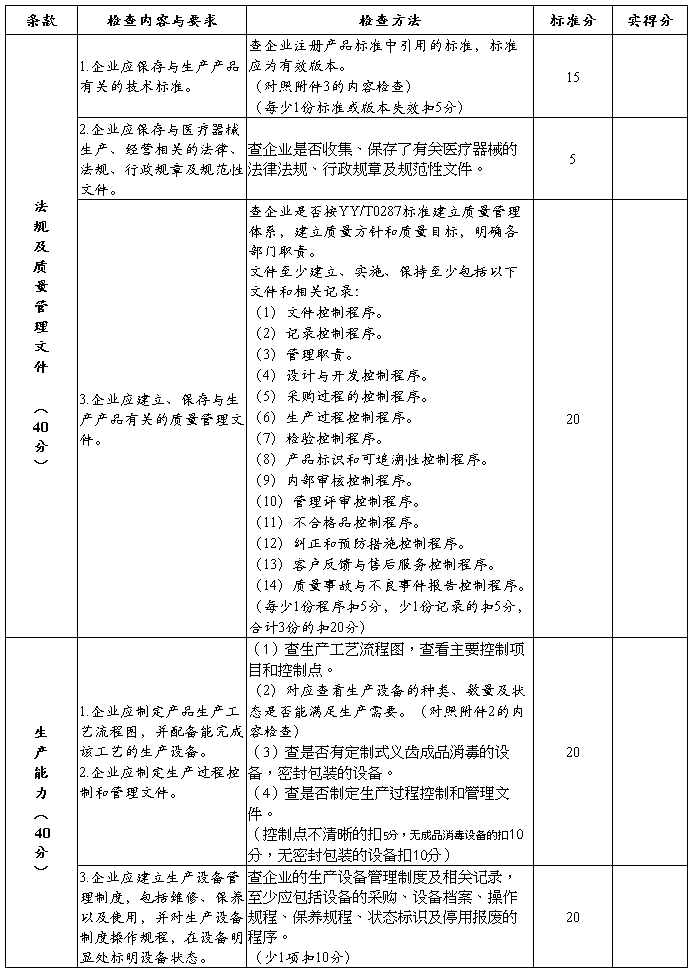
附件2:
义齿加工应具备的加工设备、常用
器械和检验仪器名称
一、固定修复体加工生产设备
1.高(中)频离心铸造机 2.烤瓷炉
3.超声波或蒸汽清洗机 4.喷砂抛光机
5.石膏模型修整机(石膏打磨机) 6.电解抛光机
7.技工打磨机 8.金属切割磨光机
9.牙科种钉机(石膏代型盒) 10.箱形电阻炉
11.技工振荡器 12.消毒设备
13.真空搅拌机 14.空压机
15.密封包装设备 16.吸尘设备
二、活动修复体加工生产设备
1.高(中)频离心铸造机 2.喷砂抛光机
3.石膏模型修整机(石膏打磨机) 4.电解抛光机
5.技工打磨机 6.金属切割磨光机
7.塑料聚合器 8.箱形电阻炉
9.复模机(琼脂溶化器) 10.技工振荡器
11.真空搅拌机 12.空压机
13.冲蜡及树脂成型器(蒸锅) 14.消毒设备
15.塑料抛光机 16.密封包装设备
17.吸尘设备
三、常用器械
1.托盘 2.橡皮碗和调拌刀 3.蜡刀与雕刀
4.烤瓷工具 5.各种技工钳、剪 6.喷灯
7.颌架 8.模型传递盒
四、检验设备设施
1.模型观测仪 2.蜡型精密卡尺 3.金属精密卡尺
4.标准比色板 5.专用放大镜 6.天平
7.粗糙度标准检测模块
五、消毒设备设施
可以采取物理、化学方法进行消毒,应具备达到消毒效果的设备设施及手段。(采用化学方法时,化学物质残留量应符合相关规定)
附件3:
有关定制式义齿产品的相关国家、行业标准
一、已发布实施的标准
1.GB/T 6387-1986 齿科材料名词术语 适用于齿科材料名词术
语,供教学、科研、医疗及生产等领域使用。
2.GB/T 9937-1988 齿科材料、器械、设备、测试和操作中的名词术语 适用于口腔医学教学、科研、临床、生产等领域及有关部门在制订标准及编写教材、技术书籍、论文报告时使用。
3.GB/T 9938-1988 牙位和口腔区域的标示法 适用于口腔临床、教学、科研和生产等领域。
4.GB/T 16886.3-2008医疗器械生物学评价 第3部分:遗传毒性、致癌性和生殖毒性试验 规定了遗传毒性、致癌性和生殖及发育毒性试验。
5.GB/T 16886.5-2003医疗器械生物学评价 第5部分:细胞毒性试验:体外法 描述了评价医疗器械体外细胞毒性的试验方法。
6.GB/T 16886.10-2005医疗器械生物学评价 第10部分:刺激与迟发型超敏反应试验 规定了评价器械及其材料潜在刺激和致敏作用的试验方法。
7.GB/T 16886.11-1997医疗器械生物学评价 第11部分:全身毒性试验 规定医疗器械释放其成分进入人体的潜在全身毒性评价方法,包括热原试验方法。
8.YY/T 0112-1993模拟口腔环境冷热疲劳试验方法 适用于口腔材料在模拟口腔环境条件下的冷热疲劳试验。
9.YY/T 0127.9-2001口腔材料生物学评价 第二单元:口腔材料生物试验方法 细胞毒性试验(琼脂覆盖法及分子滤过法) 用于检测牙科材料在通过琼脂或琼脂糖扩散后或通过乙酸纤维素滤膜扩散后的非特异性细胞毒性。
10.YY/T 0127.10-2001口腔材料生物学评价 第二单元:口腔材料生物试验方法 鼠伤寒沙门氏杆菌回复突变试验(Ames试验) 检测口腔材料的诱变性试验之一。
11.YY/T 0244-1996口腔材料生物试验方法 短期全身毒性试验:经口途径 适用于评价口腔材料短期经口服用后对机体的毒性。
12.YY/T 0268-2001牙科学 用于口腔的医疗器械生物相容性临床前评价 第1单元:评价与试验项目选择。
13.YY/T 0279-1995 口腔材料生物试验方法 口腔粘膜刺激试验 适用于评价暂时或长期与口腔黏膜组织接触的口腔材料对口腔黏膜组织产生的刺激作用。
14.YY 0301-1998 牙科学 陶瓷牙 适用于活动修复的陶瓷牙。分为带孔陶瓷牙和带钉陶瓷牙。
15.YY 0305-1998 羟基磷灰石生物陶瓷 适用于承受力或仅承受压力的牙科和外科植入用羟基磷灰石生物陶瓷及制品。
二、已发布待实施的标准
1.YY/T 0268-2008代替YY/T0268-2001 牙科学 口腔医疗器械生物学评价 第1单元:评价与试验(20##年6月1日实施)。
2.YY0620-2008牙科学 铸造金合金(20##年12月1日实施)。
3.YY0621-2008牙科金属 烤瓷修复体系(20##年12月1日实施)。
4.YY0626-2008 贵金属含量25%~75%的牙科铸造合金(20##年12月1日实施)。
5.YY1070-2008代替YY91070-1999 牙科基托/模型蜡(20##年12月1日实施)。
6.YY0315-2008 代替YY0315-1999 钛及钛合金人工牙种植体(20##年12月1日实施)。
第二篇:江苏省《定制式义齿生产企业现场检查表》(20xx版)
江苏省定制式义齿生产企业现场检查表
(2011版)
申请事项:企业开办□ 生产地址变更□ 许可证换发□ 体系考核□
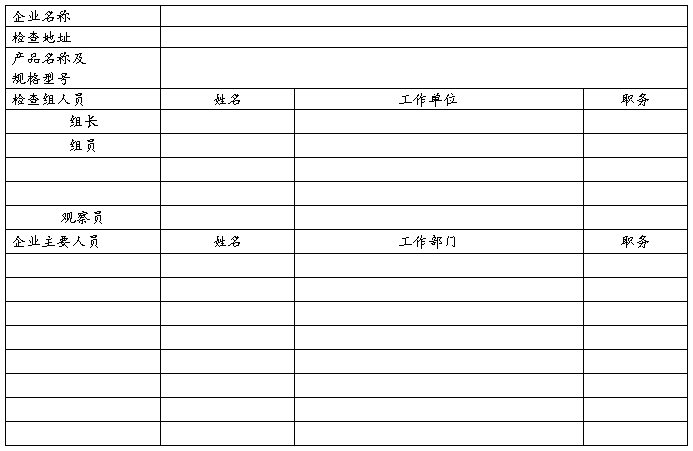
检查情况
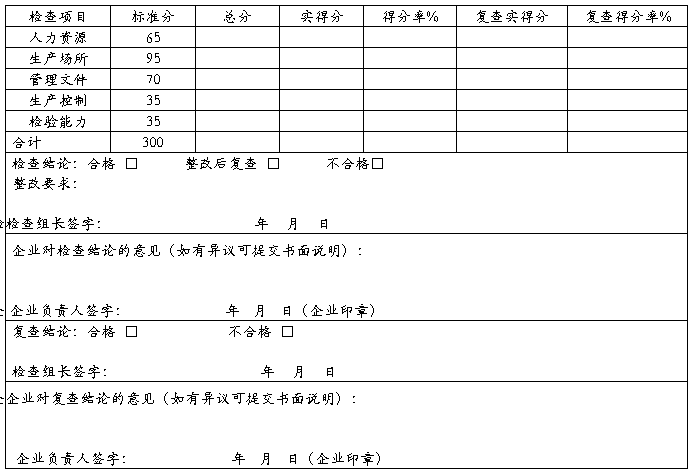
检查记录
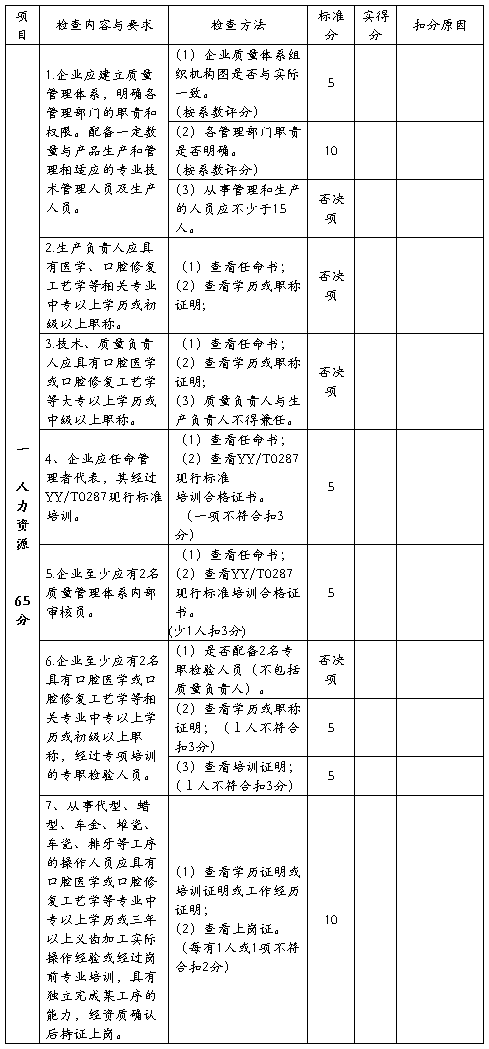

检查表说明
一、本表适用于定制式义齿医疗器械生产企业申请办理《医疗器械生产企业许可证》现场检查及质量体系考核时使用。
二、本表检查结束后用A4纸打印一式四份,分别留存于省、市、县(区)食品药品监督管理局以及申请企业。
三、核实检查地址是否与《许可证》申请材料中生产地址一致。
四、产品名称及规格型号应与《许可证》申请材料一致。
五、企业主要人员指企业陪同检查的管理层人员、专职检验人员、内审员。
六、检查评判标准
1、合格:否决项全部合格,其余检查项的得分率均达到80%以上;
2、整改后复查:否决项全部合格,其余检查项的得分率均达到60%以上而不足80%的,要求企业限期整改后申请复查。
3、不合格:①否决项有一项不合格;②否决项全部合格但其余检查项有一项得分率不足60%。③复查后仍不满足合格标准的。
六、评分方法
1、按扣分规定评分;扣分以本条款分数扣完为止。
2、按评分系数评分:实得分等于每条款的满分值乘以得分系数(得分系数:达到规定要求的系数为1.0;工作已开展仍需改进的系数为0.8;工作已开展但差距较大的系数为0.5;达不到规定要求的系数为0)。
七、缺项(条)处理
1、缺项(条)指:检查内容中与本企业产品生产无关的条款以及本次检查时尚未发生事项的条款。如企业开办现场检查时,带*号的条款可作为合理缺项。
2、缺项条款不计算分值。缺项状况分数评定方法:该项目的标准分扣除缺项分的分值为应得总分。得分率=实得分/应得总分×100%。
八、检查结论确认
检查组与企业负责人应对检查结论进行确认,签字后加盖企业公章(如有)。
定制式义齿生产用基本材料
一、主体材料(在义齿中保留其成份的材料)
1、金属材料
铸造、锻造、烤瓷、焊接用金合金、银合金、钛合金、钯合金、钴-铬(Co-Cr)合金(分烤瓷和支架用两种)、镍铬(Ni-Cr)合金、纯钛等原材料及齿科用不锈钢丝、基托内衬网
2、陶瓷材料
金属烤瓷用瓷粉(遮色瓷、体瓷、透明瓷、修饰瓷、釉粉、釉液等)、全瓷用瓷粉、瓷块、瓷牙
3、高分子树脂材料
合成树脂牙、义齿基托树脂(粉、液)、牙冠树脂(粉、液)、光敏固化树脂、弹性树脂、膜片
二、辅助材料(义齿加工中使用的基本材料)
1、铸造包埋料(磷酸盐类、硅酸乙脂类、铝基类、锆基类等)
2、模型材料(石膏、蜡、琼脂)
3、其它(电解液、酸、精密附件、蜡型清洗剂、分离剂、粘合剂、单钉、套钉、合金助焊剂、复模材料等)
三、说明
1、以上材料仅为举例。
2、使用已注册的主体材料加工的义齿按二类医疗器械管理,使用未注册的主体材料加工的义齿按三类医疗器械管理。
3、凡已列入医疗器械管理的辅助材料应取得医疗器械产品注册证。
定制式义齿生产、检验用设备
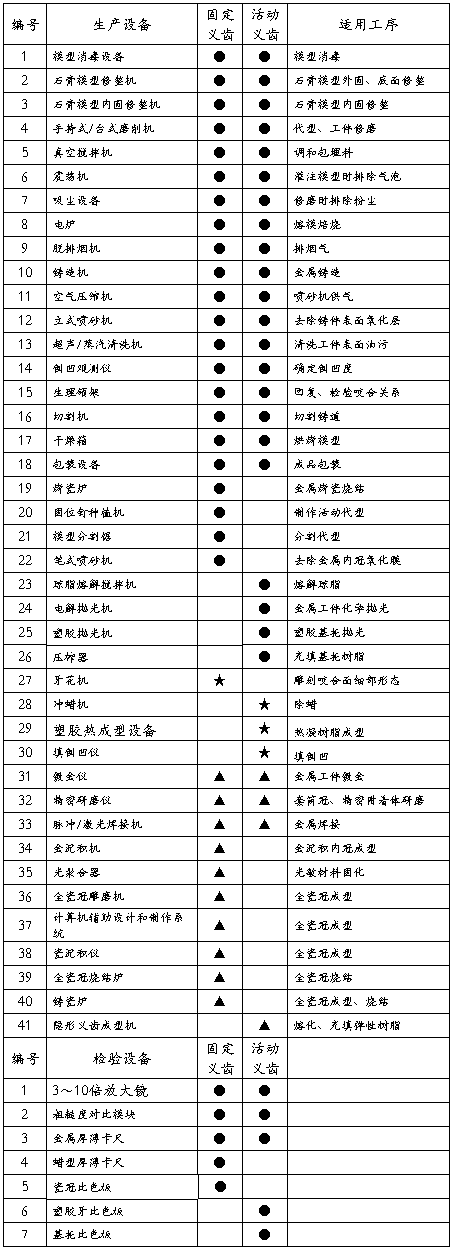
注:企业应根据生产的义齿品种和生产工艺,配置相适应的生产和检验设备。●表示必须配置的基本设备,★表示可选配的设备,▲表示生产特殊品种所需的专用设备。
