第一部分:AES,AAS,AFS
AES原子发射光谱法是根据待测元素的激发态原子所辐射的特征谱线的波长和强度,对元素进行定性和定量测定的分析方法。
特点:
1.灵敏度和准确度较高
2.选择性好,分析速度快
3.试样用量少,测定元素范围广
4.局限性
(1)样品的组成对分析结果的影响比较显著。因此,进行定量分析时,常常需要配制一套与试样组成相仿的标准样品,这就限制了该分析方法的灵敏度、准确度和分析速度等的提高。
(2)发射光谱法,一般只用于元素分析,而不能用来确定元素在样品中存在的化合物状态,更不能用来测定有机化合物的基团;对一些非金属,如惰性气体、卤素等元素几乎无法分析。
(3)仪器设备比较复杂、昂贵。
术语:
自吸
自蚀
? 击穿电压:使电极间击穿而发生自持放 电的最小电压。
? 自持放电:电极间的气体被击穿后,即使没有外界的电离作用,仍能继续保持电离,使放电持续。
? 燃烧电压:自持放电发生后,为了维持放电所必需的电压。
由激发态直接跃迁至基态所辐射的谱线称为共振线。由较低级的激发态(第一激发态)直接跃迁至基态的谱线称为第一共振线,一般也是元素的最灵敏线。当该元素在被测物质里降低到一定含量时,出现的最后一条谱线,这是最后线,也是最灵敏线。用来测量该元素的谱线称分析线。
 仪器:
仪器:
光源的作用: 蒸发、解离、原子化、激发、 跃迁。
光源的影响:检出限、精密度和准确度。
光源的类型:
直流电弧
交流电弧
电火花
电感耦合等离子体(ICP)

ICP原理
当高频发生器接通电源后,高频电流I通过感应线圈产生交变磁场(绿色)。
开始时,管内为Ar气,不导电,需要用高压电火花触发,使气体电离后,在高频交流电场的作用下,带电粒子高速运动,碰撞,形成“雪崩”式放电,产生等离子体气流。在垂直于磁场方向将产生感应电流(涡电流,粉色),其电阻很小,电流很大(数百安),产生高温。又将气体加热、电离,在管口形成稳定的等离子体焰炬。
ICP-AES法特点
1.具有好的检出限。溶液光谱分析一般列素检出限都有很低。
2.ICP稳定性好,精密度高,相对标准偏差约1%。
3.基体效应小。
4.光谱背景小。
5.准确度高,相对误差为1%,干扰少。
6.自吸效应小
进样:
溶液试样
气动雾化器
超声雾化器
超声雾化器:不连续的信号
气体试样可直接引入激发源进行分析。有些元素可以转变成其相应的挥发性化合物而采用气体发生进样(如氢化物发生法)。
例如砷、锑、铋、锗、锡、铅、硒和碲等元素。
固体试样
(1). 试样直接插入进样
(2). 电弧和火花熔融法
(3). 电热蒸发进样
(4). 激光熔融法
分光仪棱镜和光栅
检测器:目视法,摄谱法,光电法
干扰:
光谱干扰:
在发射光谱中最重要的光谱干扰是背景干扰。带状光谱、连续光谱以及光学系统的杂散光等,都会造成光谱的背景。
非光谱干扰:
非光谱干扰主要来源于试样组成对谱线强度的影响,这种影响与试样在光源中的蒸发和激发过程有关,亦被称为基体效应。
光源中未离解的分子所产生的带状光谱是传统光源背景的主要来源。
光源温度越低,未离解的分子就越多,背景就越强。
校准背景的基本原则是,谱线的表观强度I1+b减去背景强度Ib。常用的校准背景的方法有校准法和等效浓度法。
基体效应,
在实际工作中,常常向试样和标准样品中加入一些添加剂以减小基体效应,提高分析的准确度,这种添加剂有时也被用来提高分析的灵敏度。
添加剂主要有光谱缓冲剂和光谱载体。
? 光谱缓冲剂:为了减少试样成分对弧焰温度的影响,使弧焰温度稳定,试样中加入一种或几种辅助物质,用来抵偿试样组成变化的影响。
分析方法:
定性:铁光谱比较法,标准试样光谱比较法
半定量:常采用摄谱法中比较黑度法
定量:内标法
校准曲线法
标准加入法
AAS:原子吸收光谱法(AAS)是基于气态的基态原子外层电子对紫外光和可见光范围的相对应原子共振辐射线的吸收强度来定量被测元素含量为基础的分析方法。
特点:
Ø 选择性好:谱线比原子发射少,谱线重叠概率小 。
Ø 灵敏度高:适用于微量和痕量的金属与类金属元素定量分析。
Ø 精密度(RSD%)高:一般都能控制在5%左右。
Ø 操作方便和快速: 无需显色反应。
Ø 应用范围广。
Ø 局限性:不适用于多元素混合物的定性分析;对于高熔点、形成氧化物、形成复合物或形成碳化物后难以原子化元素的分析灵敏度低。
①. 自然宽度ΔυN
它与原子发生能级间路迂时激发态原子的有限寿命有关。
一般情况下约相当于10-4 Å
②. 多普勤(Doppler)宽度ΔυD
这是由原子在空间作无规热运动所引致的。故又称热变宽。
碰撞变宽:原子核蒸气压力愈大,谱线愈宽。
同种粒子碰撞——赫尔兹马克(Holtzmank)变宽, 异种粒子碰撞——称罗论兹(Lorentz)变宽。
场致变宽:在外界电场或磁场的作用下,引起原子核外层电子能级分裂而使谱线变宽现象称为场致变宽。由于磁场作用引起谱线变宽,称为Zeeman (塞曼)变宽。
自吸变宽:光源空心阴极灯发射的共振线被灯内同种基态原子所吸收产生自吸现象。
Ø 锐线光源:所发射谱线与原子化器中待测元素所吸收谱线中心频率(v0)一致,而发射谱线半宽度(?vE)远小于吸收谱线的半宽度(?vA)。
仪器:
Ø 空心阴极灯(Hollow Cathode Lamp,HCL)
Ø 由待测元素的金属或合金制成空心阴极圈和钨或其他高熔点金属制成;阳极由金属钨或金属钛制成。
在高压电场下, 阴极向正极高速飞溅放电, 与载气原子碰撞, 使之电离放出二次电子, 而使场内正离子和电子增加以维持电流。 载气离子在电场中大大加速, 获得足够的能量, 轰击阴极表面时, 可将被测元素原子从晶格中轰击出来, 即谓溅射, 溅射出的原子大量聚集在空心阴极内, 与其它粒子碰撞而被激发, 发射出相应元素的特征谱线-----共振谱线。
Ø 单色器
Ø 由入射狭缝、反射镜、准直镜、平面衍射光栅、聚焦镜和出射狭缝组成。
Ø 检测系统
光电倍增管(PMT)是原子吸收分光光度计的主要检测器,
Ø 数据处理与控制系统
计算机光谱工作站
原子化系统
Ø 火焰原子化系统
Ø 中性火焰:燃烧充分、温度高、干扰小、背景低,适合于大多数元素分析。
Ø 贫燃火焰:燃烧充分,温度比中性火焰低,氧化性较强,适用于易电离的碱金属和碱土金属元素分析,分析的重现性较差。
Ø 富燃火焰:火焰燃烧不完全,具有强还原性,即火焰中含有大量CH、C、CO、CN、NH等组分,干扰较大,背景吸收高,适用于形成氧化物后难以原子化的元素分析。
Ø 特点:简单,火焰稳定,重现性好,精密度高,应用范围广。
Ø 缺点:原子化效率低、只能液体进样
Ø 石墨炉原子化法(GFAAS)
Ø 特点:
Ø 采用直接进样和程序升温方式,原子化温度曲线是一条具有峰值的曲线。
Ø 可达3500℃高温,且升温速度快。
Ø 绝对灵敏度高,一般元素的可达10-9~10-12 g。
Ø 可分析70多种金属和类金属元素。
Ø 所用样品量少(1~100 mL)。
Ø 但是石墨炉原子化法的分析速度较慢,分析成本高,背景吸收、光辐射和基体干扰比较大。
Ø 低温原子化法:低温原子化法也称为化学原子化法,包括冷原子化法和氢化物发生法。
干扰:
Ø 物理干扰:指样品溶液物理性质变化而引起吸收信号强度变化,物理干扰属非选择性干扰。
Ø 物理干扰一般都是负干扰。
Ø 消除方法:
Ø 配制与待测样品溶液基体相一致的标准溶液。
Ø 采用标准加入法。
Ø 被测样品溶液中元素的浓度较高时,采用稀释方法来减少或消除物理干扰。
Ø 化学干扰:待测元素在原子化过程中,与基体组分原子或分子之间产生化学作用而引起的干扰。
Ø 消除方法:
Ø 改变火焰类型、改变火焰特性、加入释放剂、加入保护剂、加入缓冲剂、采用标准加入法 。
Ø 背景干扰也是光谱干扰,主要指分子吸与光散射造成光谱背景。分子吸收是指在原子化过程中生成的分子对辐射吸收,分子吸收是带光谱。光散射是指原子化过程中产生的微小的固体颗粒使光产生散射,造成透过光减小,吸收值增加。
背景干扰,一般使吸收值增加,产生正误差
条件选择:
Ø HCL电流选择:
Ø HCL电流小,HCL所发射谱线半宽度窄,自吸效应小,灵敏度增高;
Ø 但HCL电流太小,HCL放电不稳定,影响分析灵敏度和精密度。
Ø 吸收谱线选择:
Ø 首选最灵敏的共振吸收线。
Ø 共振吸收线存在光谱干扰或分析较高含量的元素时,可选用其他分析线。
分析:
定量:标准曲线法,标准加入曲线法
AFS: 原子荧光光谱法是以原子在辐射能激发下发射的荧光强度进行定量分析的发射光谱分析法。
特点:
Ø 原子荧光光谱法具有较低的检出限、较高的灵敏度、较少的干扰、吸收谱线与发射谱线比较单一、标准曲线的线性范围宽(3~5个数量级)等特点。
Ø 仪器结构简单且价格便宜,由于原子荧光是向空间各个方向发射,比较容易设计多元素同时分析的多通道原子荧光分光光度计。
Ø 原子荧光光谱法的定量分析主要采用标准曲线法,也可以采用标准加入法。
仪器与原子吸收光谱法相近
Ø 原子荧光光谱的产生
Ø 气态自由原子吸收特征辐射后跃迁到较高能级,然后又跃迁回到基态或较低能级。同时发射出与原激发辐射波长相同或不同的辐射即原子荧光。
Ø 原子荧光为光致发光,二次发光,激发光源停止时,再发射过程立即停止。
Ø 共振荧光
Ø 气态原子吸收共振线被激发后,再发射与原吸收线波长相同的荧光即是共振荧光。它的特点是激发线与荧光线的高低能级相同。
Ø 非共振荧光
Ø 当荧光与激发光的波长不相同时,产生非共振荧光。
Ø 非共振荧光又分为直跃线荧光、阶跃线荧光、anti Stokes(反斯托克斯)荧光。
Ø 直跃线荧光
Ø 激发态原子跃迁回至高于基态的亚稳态时所发射的荧光称为直跃线荧光。
Ø 由于荧光的能级间隔小于激发线的能线间隔,所以荧光的波长大于激发线的波长。
Ø 如果荧光线激发能大于荧光能,即荧光线的波长大于激发线的波长称为Stokes荧光;反之,称为anti-Stokes荧光。直跃线荧光为Stokes荧光。
Ø 阶跃线荧光
Ø 正常阶跃荧光为被光照激发的原子,以非辐射形式去激发返回到较低能级,再以辐射形式返回基态而发射的荧光。
Ø 很显然,荧光波长大于激发线波长。非辐射形式为在原子化器中原子与其他粒子碰撞的去激发过程。
Ø 热助阶跃线荧光为被光照激发的原子,跃迁至中间能级,又发生热激发至高能级,然后返回至低能级发射的荧光。
Ø 敏化荧光
Ø 受光激发的原子与另一种原子碰撞时,把激发能传递给另一个原子使其激发,后者再以辐射形式去激发而发射荧光即为敏化荧光。
Ø 火焰原子化器中观察不到敏化荧光,在非火焰原子化器中才能观察到。
Ø 在以上各种类型的原子荧光中,共振荧光强度最大,最为常用。
Ø 处于激发态的原子核外层电子除了以光辐射形式释放激发能量外,还可能产生非辐射形式释放激发能量,所发生的非辐射释放能量过程使光辐射的强度减弱或消失,称为荧光猝灭。
Ø A* + B = A + B + ΔH
Ø 可用氩气来稀释火焰,减小猝灭现象
Ø 荧光猝灭的程度可以采用荧光量子效率(φ)表示:
Ø φ = φf/φA
Ø φf单位时间时内发射的荧光光子数
Ø φA单位时间内吸收激发光的光子数
仪器:
Ø 原子荧光分光光度计的组成
Ø 原子荧光分光光度计与原子吸收分光光度计的结构相似。
Ø 为了避免锐线光源所发射的强光辐射对弱原子荧光信号检测的影响,单色器和检测器的位置与激发光源位置呈90o角。
Ø 原子荧光分光光度计都配置了氢化物(冷原子)发生器。
Ø 氢化物发生法:氢化物发生法是依据8种元素As、Bi、Ge、Pb、Sb、Se、Sn和Te的氢化物在常温下为气态,利用某些能产生初生态还原剂(H·)或某些化学反应,与样品中的这些元素形成挥发性共价氢化物。
氢化物的发生器:氢化物发生器一般包括进样系统、混合反应器、气液分离器和载气系统。
Ø 氢化物发生法的特点:
Ø 分析元素在混合反应器中产生氢化物与基体元素分离,消除基体效应所产生的各种干扰。
Ø 与火焰原子化法的雾化器进样相比,氢化物发生法具有预富集和浓缩的效能,进样效率高。
Ø 连续流动式氢化物发生器易于实现自动化。
Ø 不同价态的元素的氢化物发生的条件不同,可以进行该元素的价态分析。
Ø 无法分析不能形成氢化物或挥发性化合物的元素,氢化物发生法存在液相和气相等干扰。
第二部分:UV ,IR
 UV: 基于物质对200-800nm光谱区辐射的吸收特性建立起来的分析测定方法称为紫外-可见吸收光谱法或紫外-可见分光光度法。
UV: 基于物质对200-800nm光谱区辐射的吸收特性建立起来的分析测定方法称为紫外-可见吸收光谱法或紫外-可见分光光度法。
特点:1. 灵敏度高。可以测定10-7-10-4g·mL-1的微量组分。
2. 准确度较高。其相对误差一般在1%-5%之内。
3. 仪器价格较低,操作简便、快速。
4. 应用范围广。
紫外吸收光谱:200 ~ 400 nm
可见吸收光谱:400 ~ 800 nm
两者都属电子光谱。
紫外-可见吸收光谱的定量依据仍然是Lamber-Beer(朗伯-比耳)定律。
有机化合物的紫外-可见吸收光谱:
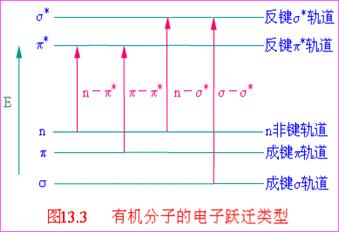
A.σ→σ*跃迁主要发生在真空紫外区。
B.π→π*跃迁吸收的波长较长,孤立的 跃迁一般在200nm左右
C. n→π*跃迁一般在近紫外区(200 - 400 nm),吸光强度较小。
D. n→σ*跃迁吸收波长仍然在(150 -250nm)范围,因此在紫外区不易观察到这类跃迁。
无机化合物的紫外-可见吸收光谱
? 电荷转移吸收光谱出现的波长位置,取决于电子给予体和电子接受体相应电子轨道的能量差。
? 中心离子的氧化能力越强,或配体的还原能力越强(相反,若中心离子的还原能力越强,或配体的氧化能力越强),则发生电荷转移跃迁时所需能量越小,吸收光谱波长红移。
? 配位场跃迁。
? 配位场跃迁吸收谱带的摩尔吸光系数小,一般emax<100,电荷转移跃迁则一般emax>104。
术语:
? 生色团:指分子中能吸收紫外或可见光的基团,它实际上是一些具有不饱和键和含有孤对电子的基团。
? 助色团:本身不产生吸收峰,但与生色团相连时,能使生色团的吸收峰向长波方向移动,且使其吸收强度增强的基团。例如-OH、-OR、-NH2、-SH、-Cl、-Br、-I等。
? 红移和蓝移:因取代基的变更或溶剂的改变,使吸收带的最大吸收波长lmax向长波方向移动称为红移,向短波方向移动称为蓝移。
? 增色效应和减色效应:最大吸收带的摩尔吸光系数emax增加时称为增色效应;反之称为减色效应。
? 强带和弱带:emax³104的吸收带称为强带;emax<103的吸收带称为弱带。
? R带:由含杂原子的生色团的n®p*跃迁所产生的吸收带。它的特点是强度较弱,一般e<100,吸收峰通常位于200 ~ 400 nm之间。
? K带:由共轭体系的p®p*跃迁所产生的吸收带。其特点是吸收强度大,一般e>104,吸收峰位置一般处于217 ~ 280 nm范围内。
? B带:由芳香族化合物的p®p*跃迁而产生的精细结构吸收带。 B带是芳香族化合物的特征吸收,但在极性溶剂中时精细结构消失或变得不明显。
? E带:由芳香族化合物的p®p*跃迁所产生的吸收带,也是芳香族化合物的特征吸收,可分为E1和E2带。
影响因素:
? 共轭效应
共轭不饱和键越多,红移越明显,同时吸收强度也随之加强。
? 溶剂效应
溶剂的极性越大,溶剂与溶质分子间产生的相互作用就越强,溶质分子的振动也越受到限制,因而由振动而引起的精细结构也损失越多。
?  溶剂效应:溶剂极性对p®p*和n®p*跃迁谱带的影响
溶剂效应:溶剂极性对p®p*和n®p*跃迁谱带的影响
? 当溶剂极性增大时,由p®p*跃迁产生的吸收带发生红移, n®p*跃迁产生的吸收带发生蓝移
? 溶剂的选择:
? 尽量选用非极性溶剂或低极性溶剂;
? 溶剂能很好地溶解被测物,且形成的溶液具有良好的化学和光化学稳定性;
? 溶剂在样品的吸收光谱区无明显吸收。
? pH值的影响:
?  如果化合物在不同的pH值下存在的型体不同,则其吸收峰的位置会随pH值的改变而改变。
如果化合物在不同的pH值下存在的型体不同,则其吸收峰的位置会随pH值的改变而改变。
仪器:
光源、单色器、吸收池、检测器和信号指示系统五个部分构成。
定性分析
比较法,最大吸收波长计算法
结构分析
1顺式异构体的lmax比反式异构体的小。
2
3构象,直立>平伏
 定量分析
定量分析
单组份定量
多组分定量
导数分光光度法
氢键强度测定
只要测定同一化合物在不同极性溶剂中n®p*跃迁吸收带,就能计算其在极性溶剂中氢键的强度。
IR:红外吸收光谱法是利用物质分子对红外辐射的特征吸收,来鉴别分子结构或定量的方法。
? 特点:红外吸收只有振-转跃迁,能量低;
? 应用范围广:除单原子分子及单核分子外,几乎所有有机物均有红外吸收;
? 分子结构更为精细的表征:通过IR谱的波数位置、波峰数目及强度确定分子基团、分子结构;
? 定量分析;
? 固、液、气态样均可用,且用量少、不破坏样品;
? 分析速度快。
? 与色谱等联用(GC-FTIR)具有强大的定性功能。

原理:
样品受到频率连续变化的红外光照射时,样品分子选择性地吸收某些波数范围的辐射,引起偶极矩的变化,产生分子振动和转动能级从基态到激发态的跃迁,并使相应的透射光强度减弱。
红外光谱中,吸收峰出现的频率位置由振动能级差决定,吸收峰的个数与分子振动自由度的数目有关,而吸收峰的强度则主要取决于振动过程中偶极矩的变化以及能级的跃迁概率。
分子吸收辐射产生振转跃迁必须满足两个条件:
条件一:辐射光子的能量应与振动跃迁所需能量相等。
条件二:辐射与物质之间必须有耦合作用
双原子分子的振动
影响基本振动跃迁的波数或频率的直接因素为化学键力常数k和原子质量。
多原子分子
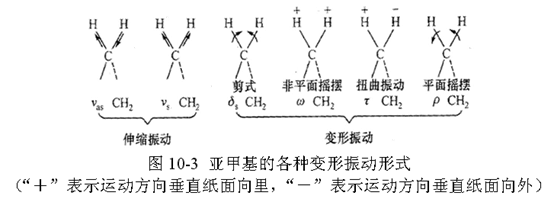
理论振动数(峰数)
设分子的原子数为n,
? 对非线型分子,理论振动数=3n-6
如H2O分子,其振动数为3×3-6=3
? 对线型分子,理论振动数=3n-5
如CO2分子,其理论振动数为3×3-5=4

实际振动数:
峰数常常少于理论计算出的振动数,这是因为:
a)偶极矩的变化Dm=0的振动,不产生红外吸收;
b)谱线简并(振动形式不同,但其频率相同);
c)仪器分辨率或灵敏度不够,有些谱峰观察不到。
在红外光谱中还可观察到其它跃迁谱峰:
泛频峰
倍频峰:由基态向第二、三….振动激发态的跃迁(DV=±2、± 3.);
合频峰:分子吸收光子后,同时发生频率为n1,n2的跃迁,此时
产生的跃迁为n 1+n2的谱峰。
差频峰:当吸收峰与发射峰相重叠时产生的峰n 1-n2。
泛频峰可以观察到,但很弱,可提供分子的“指纹”。
读谱:
频率:影响基本振动跃迁的波数或频率的直接因素为化学键力常数k和原子质量。
把能代表基团存在、并有较高强度的吸收谱带称为基团频率,通常是由基态(v=0)跃迁到第一振动激发态产生的,其所在的位置一般又称为特征吸收峰。
强度:振动能级的跃迁概率和振动过程中偶极距的变化是影响红外吸收峰强度的两个主要因素,基频吸收带一般较强,而倍频吸收带较弱。
基频振动过程中偶极矩的变化越大,其对应的峰强度也越大;振动的对称性越高(即化学键两端连接的原子的电负性相差越小),振动中分子偶极矩变化越小,谱带强度也就越弱。
另外,反对称伸缩振动的强度大于对称伸缩振动的强度,伸缩振动的强度大于变形振动的强度。
影响因素:
? (1). 诱导效应(Induction effect):取代基电负性—静电诱导—电子分布改变—k 增加—特征频率增加(移向高波数)。
? 共轭效应(Conjugated effect):电子云密度均化—键长变长—k 降低—特征频率减小(移向低波数)。
中介效应:孤对电子与多重键相连产生的p-p 共轭,结果类似于共轭效应。
当诱导与共轭两种效应同时存在时,振动频率的位移和程度取决于它们的净效应。
? . 空间效应:
? 包括空间位阻效应、环状化合物的环张力效应等。
取代基的空间位阻效应使分子平面与双键不在同一平面,此时共轭效应下降,红外峰移向高波数。

? 3. 氢键:
? 氢键的形成使电子云密度平均化(缔合态),使体系能量下降,X—H伸缩振动频率降低,吸收谱带强度增大、变宽;
? 形成分子内氢键时,X—H伸缩振动谱带的位置、强度和形状的改变均较分子间氢键小。
? 同时,分子内氢键的影响不随浓度变化而改变,分子间氢键的影响则随浓度变化而变化。
? 4. 互变异构
? 5. 振动耦合
? 6. Fermi共振
当弱的泛频峰与强的基频峰位置接近时,其吸收峰强度增加或发生谱峰分裂,这种泛频与基频之间的振动耦合现象称为Fermi共振。
1)试样状态
通常,物质由固态向气态变化,其波数将增加。
2)溶剂效应
极性基团的伸缩振动频率通常随溶剂极性增加而降低。因此红外光谱通常需在非极性溶剂中测量。
仪器:

2. 吸收池
红外吸收池使用可透过红外的材料制成窗片;
3. 单色器
通常采取程序增减狭缝宽度的办法,即随辐射能量降低,狭缝宽度自动增加,保持到达检测器的辐射能量的恒定。
4. 检测器及记录仪

进样:
10.4.1 对试样的要求
1)试样应为“纯物质”(>98%),通常在分析前,样品需要纯化;
对于GC-FTIR则无此要求。
2)试样不含有水(水可产生红外吸收且可侵蚀盐窗);
3)试样浓度或厚度应适当,以使T在合适范围。
10.4.2 制样方法
液体或溶液试样
1)沸点低易挥发的样品:液体池法。
2)高沸点的样品:液膜法(夹于两盐片之间)。
3)固体样品可溶于CS2或CCl4等无强吸收的溶液中。
固体试样
1)压片法:
2)石蜡糊法:
3)薄膜法:
气体试样:
可在玻璃气槽内进行测定,
应用:
定性:定量:
读红外谱
伸缩
氢键:3400~3200 宽而强的峰
N-H:3500~3300 中等强峰
饱和C-H:<3000
不饱和 C-H:>3000
三键,累积双键:2500~2000
C=O:1820~1600 最强吸收
C=C,C=N,N=O:1680~1500
单核芳烃,C=C,1600~1500 两个对称峰,用来确定有无芳核
C-H弯曲振动:1500~1300
第三部分:核磁NMR 质谱 MS
NMR:将磁性原子核放入强磁场后,用适宜频率的电磁波照射,它们会吸收能量,发生原子核能级跃迁,同时产生核磁共振信号,得到核磁共振

原理
1自旋磁矩
n g—磁旋比,不同的核具有不同的磁旋比,对某元素是定值。是磁性核的一个特征常数
n 把自旋核放在场强为B0的磁场中,由于磁矩 m与磁场相互作用,核磁矩相对外加磁场有不同的取向,共有2I+1个,各取向可用磁量子数m表示
n m=I, I-1, I-2, ……-I
n △E与核磁矩及外磁场强度成正比, B0越大,能级分裂越大, △E越大
n 处于低能态的核将吸收射频能量而跃迁至高能态,这种现象叫做核磁共振现象。
n 对自旋量子数I=1/2的同一核来说,,因磁矩为一定值,g—为常数,所以发生共振时,照射频率的大小取决于外磁场强度的大小。外磁场强度增加时,为使核发生共振,照射频率也相应增加;反之,则减小。
2屏蔽
n 任何原子核都被电子云所包围,当1H核自旋时,核周围的电子云也随之转动,在外磁场作用下,会感应产生一个与外加磁场方向相反的次级磁场,实际上会使外磁场减弱,这种对抗外磁场的作用称为屏蔽效应.
n 影响屏蔽常数的因素:
n 原子屏蔽原子屏蔽可指孤立原子的屏蔽,也可指分子中原子的电子壳层的局部屏蔽,称为近程屏蔽效应。
n 分子内屏蔽:指分子中其他原子或原子团对所要研究原子核的磁屏蔽作用。
n 分子间屏蔽:指样品中其他分子对所要研究的分子中核的屏蔽作用。影响这一部分的主要因素有溶剂效应、介质磁化率效应、氢键效应等。

3化学位移
由于氢核具有不同的屏蔽常数σ,引起外磁场或共振频率的移动,这种现象称为化学位移。固定照射频率, σ大的原子出现在高磁场处, σ小的原子出现在低磁场处

4,自旋耦合
n 氢核吸收峰的裂分是因为分子中相邻氢核之间发生了自旋相互作用,自旋核之间的相互作用称为自旋—自旋偶合。
n 自旋偶合不影响化学位移,但会使吸收峰发生裂分,使谱线增多,简称自旋裂分。
n 自旋偶合产生峰裂分后,裂分峰之间的间距称为偶合常数,用J表示,单位为Hz。
J 值大小表示氢核间相互偶合作用的强弱。与化学位移不同,不因外磁场的变化而变化,
n J 值的大小与B0无关。影响J值大小的主要因素是原子核的磁性和分子结构及构象。因此,偶合常数是化合物分子结构的属性。
n (2)简单自旋偶合体系J值等于多重峰的间距,复杂自旋偶合体系需要通过复杂计算求得。
n 超过三个化学键的J耦合一般较弱。
当I = 1/2时,N = n+1,称为“n+1规律”。
化学环境完全相同的原子,虽然它们有很强的偶合作用,但无裂分现象。
例:-CH3不发生裂分
(2)分子中化学位移相同的氢核称为化学等价核;把化学位移相同,核磁性也相同的称为磁等价核。磁等价核之间虽有偶合作用,但无裂分现象,在NMR谱图中为单峰。
例如:Cl-CH2-CH2-Cl 分子中, -CH2上的氢核皆是磁等价核,出现的信号强度相当于4个 H 核的单峰
化学位移相同,偶合常数也相同,磁等价核一定是化学等价核
n 磁不等价核之间才能发生自旋偶合裂分。如下情况是磁不等价 氢核
A:化学环境不相同的氢核;
B:与不对称碳原子相连的-CH2上的氢核
C:固定在环上的-CH2中的氢核;
D:单键带有双键性质时,会产生磁不等价氢核
E:单键不能自由旋转时,也会产生磁不等价氢核。
3)一组相同氢核自旋裂分峰数目由相邻氢核数目n 决定
n 裂分峰数目遵守n+1规律——相邻n个H,裂分成n+1峰
n 裂分峰之间的峰面积或峰强度之比符合二项展开式各项系数比的规律。(a+b)n n为相邻氢核数
n (5)氢核邻近有两组偶合程度不等的H 核时,其中一组有n个,另一组有n′+1个,则这组H 核受两组 H 核自旋偶合作用,谱线裂分成(n+1)(n′+1)重峰。
n . 电子结构对耦合常数的影响
n (1). 核周围电子密度对耦合常数的影响
n 电子密度增加,传递耦合的能力增强,耦合常数增大。原子序数增加,核周围电子密度也增加,耦合常数也增大。
n (2). 化学键对耦合常数的影响
n 相隔化学键数目多,耦合常数小;多重键耦合常数值大;相隔超过三个化学键的远程耦合可以忽略不计。
2. 几何结构对耦合常数的影响
n 一般地,键长越长耦合越弱。
仪器:
n 12.4.1 谱仪的基本组件
n 磁体:产生强的静磁场。
n 射频源:用来激发核磁能级之间的跃迁。
n 探头:位于磁体中心的圆柱形探头作为NMR信号检测器,是NMR谱仪的核心部件。样品管放置于探头内的检测线圈中。
n 接收机:用于接收微弱的NMR信号,并放大变成直流的电信号。
n 匀场线圈:用来调整所加静磁场的均匀性,提高谱仪的分辨率。
n 计算机系统:用来控制谱仪,并进行数据显示和处理。
氢谱:
特点
n 质子的磁旋比γ较大,天然丰度为99.98%,其NMR信号的绝对灵敏度是所有磁性核中最大的。
n 质子是有机化合物中最常见的原子核,1H NMR谱在有机化合物结构解析中最常用。
n 化学位移d数值反映质子的化学环境。
n 谱峰面积与其代表的质子数目呈正比。
影响因素:
n 诱导效应
n 1H核受一个或几个电负性较强原子或基团的拉电子作用,则周围的电子云密度降低,屏蔽效应降低,化学位移值增大,吸收峰左移。
n 若1H核与一个或几个给电子基团连接,则其周围的电子云密度增加,屏蔽效应增加,化学位移值减小,吸收峰右移。
n 共轭效应
n 电负性较强的原子存在并以单键形式连接到双键上,由于发生p-p共轭,电子云自电负性原子向p键方向移动,使p键上相连的1H电子云密度增加,因此δ降低,共振吸收移向高场。
n 电负性较强的原子以不饱和键的形式连接,且产生p-p共轭,则电子云将移向电负性原子,使p键上连接的1H电子云密度降低,因此δ变大,共振吸收移向高场。

n 磁各向异性效应:如果分子具有多重键或共轭多重键,在外磁场作用下,p电子会沿着分子的某一方向流动,它对邻近的质子附加一个各向异性的磁场,使某些位置的质子处于该基团的屏蔽区,δ值移向高场,而另一些位置的质子处于该基团的去屏蔽区,δ值移向低场。
n 诱导效应通过化学键传递,而磁各向异性效应则通过空间相互作用。
n 范德华效应:当两个原子相互靠近时,由于受到范德华力作用,电子云相互排斥,导致原子核周围电子云密度降低,屏蔽减小,谱线向低场移动,这种效应称为范德华效应。
n 氢键:氢的化学位移对氢键很敏感。当分子形成氢键后,由于静电场的作用,使氢外围电子云密度降低而去屏蔽,δ值增加,也就是说,无论是分子内还是分子间氢键的形成都使氢受到去屏蔽作用。
n 溶剂效应:同一化合物在不同溶剂中的化学位移会有所差别,这种由于溶质分子受到不同溶剂影响而引起的化学位移变化。
解谱:
n 一级1H NMR谱具有以下特征信息:
n 吸收峰的组数,代表分子中处于不同化学环境的质子种类。
n 从谱图中可直接得到J和d值。各组峰中心为该组质子的化学位移d,其数值说明分子中基团的情况;各峰之间的裂距(相等)为耦合常数J,其数值与化学结构密切相关。
n 各组峰的分裂符合n+1规律,分裂数目说明各基团的连接关系,分裂后各组峰强度比符合(a+b)n展开式系数比。
n 吸收峰的面积与产生该吸收峰的质子数呈正比。
n 分析图谱的一般步骤为:
n 1. 检查谱图是否符合规则:
n 2. 标识杂质峰、溶剂峰、旋转边带等非待测样品的信号。
n 3. 计算不饱和度。
n 4. 确定各组峰代表的质子数。
n 5. 推出可能的结构单元。
n 6. 识别谱中的一级裂分谱,验证J值。
n 7. 解析高级谱,
n 8. 结合其他分析方法数据推导化合物的结构。
n 9. 仔细核对各组信号的化学位移和耦合常数。
碳谱:
特点:
(1)化学位移范围宽
(2)可检测不与氢相连的碳的共振
吸收峰
(3)灵敏度低,耦合复杂
(4)13C核的自旋-晶格弛豫时间T1较长。
(5)谱峰强度不与碳原子数呈正比
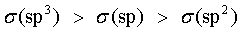 碳的轨道杂化
碳的轨道杂化
诱导 空间 共轭 电场 重原子 同位素 分子内氢键 介质
MS
质谱法(Mass spectrometry)是通过对被测样品离子的质荷比进行测定的一种分析方法。被分析的样品首先要离子化,然后利用不同离子在电场或磁场中运动行为的不同,把离子按质荷比(m/z)分离而得到质谱,
原子质谱分析包括以下几个步骤:
1.样品原子化;
2.转化为离子流或离子束,一般为单电荷正离子;
3.按质量-电荷比(质荷比,m/z)分离;
4.计算各种离子的数目或测定由试样形成的离子轰击传感器时产生的离子电流。
因为在2步中形成的离子多为单电荷,故m/z值通常就是该离子的质量数。
 仪器:基本构成
仪器:基本构成
分析系统:
1,离子源
高频火花离子源
电感耦合等离子体
辉光放电
其他
激光
离子轰击
2,质量分析器
质量分析器(Mass Analyzer)是质谱仪器的重要组成部分,它位于离子源和检测器之间,其作用是依据不同方式将样品离子按质荷比(m/z)分离。
1磁质量分析器
2四级滤质器
3离子回旋共振分析器
3,检测器
Faraday杯
电子倍增器
4,真空系统
ICPMS
特点
试样在常温下引入;
气体的温度很高使试样完全蒸发和解离;
试样原子离子化的百分比很高;
产生的主要是一价离子;
离子能量分散小;
外部离子源,即离子并不处在真空中;
离子源处于低电位,可配用简单的质量分析器。
当等离子体中离子种类与分析物离子具有相同的m/z,即产生光谱干扰。
1.同质量类型离子
同质量类型离子干扰是指两种不同元素有几乎相同质量的同位素。
2.多原子离子干扰
一般认为,多原子离子并不存在于等离子体本身中,而是在离子的引出过程中,由等离子体中的组分与基体或大气中的组分相互作用而形成。
3.氧化物和氢氧化物干扰
4.仪器和试样制备所引起的干扰
基体效应
共存物中含有低电离能元素如碱金属、碱土金属和镧系元素且超过限度,由于它们提供的等离子体的电子数目很多,进而抑制包括分析物元素在内的其他元素的电离,影响分析结果。
可采用稀释、基体匹配、标准加入法或者同位素稀释法降低至最小。
分子质谱
按照样品的离子化过程,离子源(Ion Sources)主要可分为气相离子源和解析离子源。
按照离子源能量的强弱,离子源可分为硬离子源和软离子源。
电子轰击源(Electron-Impact Soures ,EI)应用最为广泛,主要用于挥发性样品的电离。
电子轰击源电离效率高,能量分散小,结构简单,操作方便,工作稳定可靠,产生高的离子流,因此灵敏度高。
化学电离源(Chemical Ionization Sources, CI )和电子轰击电离源主要差别在于CI源工作过程中要引进一种反应气体。
场电离源(Field ionization Sources, FI)是应用强电场诱导样品电离的一种离子化方式。
样品无需气化再电离,特别适于非挥发性、热不稳定的生物样品或相对分子质量高达100,000的高分子物质。
快原子轰击源(Fast Atomic bombardment Sources, FAB)主要用于极性强、高分子量的样品分析。
激光解吸电离源(Laser Desorption Ionization Sources,LD)是一种结构简单、灵敏度高的新电离源。
应用:
定性:标准谱图检索定性
将在一定质谱分析条件下获得的质谱图与相同条件下标准谱图对照是对已知纯化合最简便定性方法。
相对分子质量测定
分子离子峰的m/z可提供准确分子相对质量,是分子鉴定的重要依据。获得分子离子、准确地确认分子离子峰是质谱定性分析的主要方法之一。
在质谱图中,可根据如下特点确认分子离子峰: 1. 原则上除同位素峰外,分子离子或准分子离子是谱图中最高质量峰,两者均可推导出分子量。 2. 它要符合氮律。 3.判断最高质量峰与失去中性碎片形成碎片离子峰是否合理。 4.当化合物含有氯和溴元素,有时可帮助识别分子离子峰。
分子式确定
定量:
. 质谱直接定量分析
质谱直接定量分析有几个基本假设或条件:
1.组分特征峰及强度不受样品中其他组分或本底干扰。
2.样品中任何组分的离子流强度与其在进样装置中的分压呈正比。
3.样品中存在具有相同特征谱峰的组分,发生质谱峰叠加时,叠加峰的强度是各被叠加峰强度的线性累加。
单一组分定量:
可在质谱上确定合适的m/z值,其峰高与组分浓度呈正比,这个技术称为选择离子检测。
混合的样品多组分定量:
各组分特征峰无叠加,可以代表各个组分具有特定m/z值的质谱特征峰强度作为定量依据。若组分特征峰发生叠加,则需通过叠加特征峰强度的线性累加方程计算各组分含量
X射线光谱法
原理
X射线是由高能电子的减速运动或原子内层轨道电子跃迁产生的短波电磁辐射。X射线的波长在10-6~10 nm,在X射线光谱法中,常用波长在0.01~2.5 nm范围内。
X射线的发射
1.用高能电子束轰击金属靶;
2.将物质用初级X射线照射以产生二级射线——X射线荧光;
3.利用放射性同位素源衰变过程产生的X射线发射;
4.从同步加速器辐射源获得。在分析测试中,常用的光源为前3种,第4种光源虽然质量非常优越,但设备庞大,国内外仅有少数实验室拥有这种设施。
特征X射线是基于电子在原子最内层轨道之间的跃迁所产生的。
特征X射线的产生,也要符合一定的选择定则。这些定则是:
1.主量子数△n≠0
2.角量子数△L=±1
3.内量子数△J=±1或0。
不符合上述选律的谱线称为禁阻谱线。
X射线的吸收
X射线照射固体物质时,一部分透过晶体,产生热能;一部分用于产生散射、衍射和次级X射线(X荧光)等;还有一部分将其能量转移给晶体中的电子。因此,用X射线照射固体后其强度会发生衰减。
X射线的散射分为非相干散射和相干散射:
非相干散射:X射线与原子中束缚较松的电子作随机的非弹性碰撞,把部分能量给予电子,并改变电子的运动方向。
相干散射:X射线与原子中束缚较紧的电子作弹性碰撞。一般说来,这类电子散射的X射线只改变方向而无能量损失,波长不变,其相位与原来的相位有确定的关系。
X射线衍射所需条件有两个:1.原子层之间间距必须与辐射的波长大致相当;2.散射中心的空间分布必须非常规则。
当能量高于原子内层电子结合能的高能X射线与原子发生碰撞时,驱逐一个内层电子而出现一个空穴,使整个原子体系处于不稳定的激发态,激发态原子寿命约为10-12~10-14s,然后自发地由能量高的状态跃迁到能量低的状态,这个过程称为驰豫过程。
当较外层的电子跃入内层空穴所释放的能量不在原子内被吸收,而是以辐射形式放出,便产生X射线荧光,其能量等于两能级之间的能量差。
当较外层的电子跃迁到空穴时,所释放的能量随即在原子内部被吸收而逐出较外层的另一个次级光电子,称为Auger效应,亦称次级光电效应或无辐射效应,所逐出的 次级光电子称为Auger电子。
次级光电子称为Auger电子。
辐射源
X射线管
放射性同位素
次级X射线
X射线滤光片
入射波长限定装置
X射线单色器
检测器 正比计数器
闪烁计数器
半导体检测器
信号处理器
脉冲高度选择器
脉冲高度分析器
XRF
采用从X射线管或同位素源出来的X射线来激发试样。在此种情况下,试样中的元素将初级X射线束吸收而激发并发射出它们自己的特征X射线荧光。这一分析方法称为X射线荧光法。
X射线荧光法(XRF)是所有元素分析方法中最常用的一种。它可以对原子序数大于氧(>8)的所有元素进行定性分析。
优点:对试样无损伤。
X射线荧光分析法可能是元素分析中最为有效方法之一。优点:
1. 特征X射线谱线简单,且谱线仅与元素的原子序数有关,方法的特征性强;
2. 各种形状和大小试样均可分析,不破坏试样;
3. 分析含量范围广、自微量至常量均可进行分析、精密度和准确度也较高。
局限:
1.不能分析原子序数小于5的元素;
2. 灵敏度不够高,一般只能分析含量在0.0x%以上的元素;
3. 对标准试样要求很严格。
定性分析
X荧光的本质就是特征X射线,Moseley定律就是定性分析的基础。
常用定量和半定量方法
X射线荧光分析中常用的定量和半定量方法有标准曲线法、加入法、内标法等。
选择内标元素时应注意:
1.试样中不含该内标元素;
2.内标元素与分析元素的激发和吸收性质要尽量相似;
3.一般要求内标元素的原子序数在分析元素的原子序数附近(相差l~2);
4.两种元素间没有相互作用。
X射线吸收法应用于基体效应极小的试样
X射线衍射
应用
1.晶体结构分析
2. 粒子大小的测定
测定单晶晶体结构的主要设备是四圆衍射仪。单晶结构分析是结构分析中最有效的方法之一。它能为一个晶体给出精确的晶胞参数,同时还能给出晶体中成键原子间的键长、键角等重要的结构化学数据
表面分析
表面分析是指对表面及微区的特性和表面现象进行分析、测量的方法和技术,电子束激发、光子激发、离子轰击、近场显微镜法。
光电子能谱法
光电子能谱法是指采用单色光或电子束照射试样,使电子受到激发而发射,通过测量这些电子的(相对)强度与能量分布的关系,从中获得有关信息。
用X射线作激发源的称X射线光电子能谱(XPS)、用紫外光作激发源的称紫外光电子能谱(UPS)、测量俄歇电子能量分布的称俄歇电子能谱(AES)。有的教材将前两者称为光子探针技术,而将AES称为电子探针技术。
电子能谱法所能研究的信息深度d取决于逸出电子的非弹性碰撞平均自由程λ。
所谓平均自由程(电子逸出深度)是指电子在经受非弹性碰撞前所经历的平均距离。
XPS 理论依据是Einstein的光电子发射公式(光电效应),
电子结合能是指一个原子在光电离前后的能量差,即原子终态(2)与始态(1)之间的能量差:
Eb = E(2) - E(1)
气体试样可以视为自由原子或分子。
固体试样:
X射线光电子能谱图是以检测器单位时间内接收到的光电子数(光电子强度)对电子结合能或光电子动能作图。
XPS主要是研究原子的内层电子结合能。
由固体的热效应及表面荷电作用等物理因素引起的谱峰位移称为物理位移。由电子所处的化学环境不同而引起的谱峰位移称为化学位移。
由于紫外线的能量比X射线能量低,只能激发原子或分子的价电子,所测定的是价电子的结合能,习惯上称为电离能。
紫外光电子能谱图的形状取决于入射光子的能量和电离后离子的状态以及具体的实验条件。
紫外光电子能谱的特点是研究原子或分子的价电子:
1.定性分析:具有分子“指纹”性质
2.表面分析:可用于研究固体表面吸附、催化及表面电子结构等。
3. 测量电离能。
4. 研究化学键:观察紫外光电子能谱各种谱带的形状,可以得到有关分子轨道成键性质的某些信息
Auger电子能谱法(AES)是用具有一定能量的电子束(或X射线)激发试样,以测量二次电子中的那些与入射电子能量无关,而本身具有确定能量的Auger电子峰为基础的分析方法。
Auger电子能谱能反映3类化学效应—即原子化学环境的改变引起Auger电子能谱结构的变化:
电荷转移、价电子谱、等离子激发。
Auger电子能谱原则上适用于任何固体,灵敏度高,可以探测的最小面浓度达0.1%单原子层;其采样深度为1 ~ 2 nm,比XPS 还要浅;它的分析速度比XPS更快,因此有可能跟踪某些快的变化。
1. 定性分析
2. 定量分析
3. 表面元素的化学状态分析
4. 微区分析
电子能谱仪通常采用的激发源有三种:X射线源、真空紫外灯和电子枪。由于各能谱仪之间除激发源不同外,其他部分基本相同,因此,配备不同激发源,可使一台能谱仪具有多种功能。
单色器—电子能量分析器
1. 半球形电子能量分析器
2. 筒镜电子能量分析器
检测器 必须采用电子倍增器,如单通道电子倍增器或多通道电子倍增器。
电子能谱法的特点
1.可分析除H和He之外的所有元素;可以直接测定来自试样单个能级光电发射电子的能量分布,且直接得到电子能级结构的信息。
2. 能提供有关化学键方面的信息,直接测量价层电子及内层电子轨道能级。而相邻元素的同种谱线相隔较远,相互干扰少,元素定性标识性强。
3. 是一种无损分析。
4. 是一种高灵敏超微量表面分析技术。分析所需试样约10-8g即可,绝对灵敏度达10-18g,试样分析深度约2 nm。
二次离子质谱法 SIMS
扫描隧道显微镜 STM
原子力显微镜 AFM
近场光学显微镜 SNOM
激光共焦扫描显微镜 LCSM
分子发光分析
本章所介绍的包括荧光分析法、磷光分析法和化学发光分析法。
Ø 灵敏度高。较吸收光度法一般要高2 ~ 3个数量级。
Ø 选择性比较高。物质对光的吸收具有普遍性,但吸光后并非都有发光现象。即便都有发光现象,但在吸收波长和发射波长方面不尽相同,这样就有可能通过调节激发波长和发射波长来达到选择性测定的目的。
Ø 样品量小,操作简便,工作曲线的动态线性范围宽。
发光检测的高灵敏度,
. 分子能级与跃迁
分子能级比原子能级复杂;
在每个电子能级上,都存在振动、转动能级;
基态(S0)→激发态(S1、S2、激发态振动能级):吸收特定频率的辐射;量子化;跃迁一次到位;
激发态→基态:多种途径和方式(见能级图);速度最快、激发态寿命最短的途径占优势;
非辐射能量传递过程
振动弛豫:同一电子能级内以热能量交换形式由高振动能级至低相邻振动能级间的跃迁。发生振动弛豫的时间10 -12 s。
内转换:同多重度电子能级中,等能级间的无辐射能级交换。
通过内转换和振动弛豫,高激发单重态的电子跃回第一激发单重态的最低振动能级。
外转换:激发分子与溶剂或其他分子之间产生相互作用而转移能量的非辐射跃迁;
外转换使荧光或磷光减弱或“猝灭”。
系间跨越:不同多重态,有重叠的转动能级间的非辐射跃迁。
改变电子自旋,禁阻跃迁,通过自旋—轨道耦合进行。
辐射能量传递过程
荧光发射:电子由第一激发单重态的最低振动能级→基态( 多为 S1→ S0跃迁),发射波长为 l ‘2的荧光; 10-7~10 -9 s 。
由图可见,发射荧光的能量比分子吸收的能量小,波长长; l ‘2 > l 2 > l 1 ;
磷光发射:电子由第一激发三重态的最低振动能级→基态( T1 → S0跃迁);
荧光量子产率:荧光物质吸光后所发射的荧光的光子数与所吸收的激发光的光子数之比值。
由于激发态分子的衰变过程包含辐射跃迁和非辐射跃迁,故荧光量子产率可表示为
?f = kf / (kf + ΣK)
分子产生荧光必须具备的条件
 (1)具有合适的结构;
(1)具有合适的结构;
(2)具有一定的荧光量子产率。
荧光量子产率(j):
1)跃迁类型:p* → p的荧光效率高,系间跨越过程的速率常数小,有利于荧光的产生;
(2)共轭效应:提高共轭度有利于增加荧光效率并产生红移
(3)刚性平面结构:可降低分子振动,减少与溶剂的相互作用,故具有很强的荧光。如荧光素和酚酞有相似结构,荧光素有很强的荧光,酚酞却没有。
4)取代基效应:芳环上有供电基,使荧光增强
1.猝灭
发光分子与溶剂或溶质分子之间所发生的导致发光强度下降的物理或化学作用过程。
与发光分子相互作用而引起发光强度下降的物质,称为猝灭剂。
2.动态猝灭与静态猝灭
猝灭剂与发光物质的激发态分子之间的相互作用引起动态猝灭;猝灭剂与发光物质的基态分子之间的相互作用引起静态猝灭。
激发光谱与发射光谱的关系
a.Stokes位移
激发光谱与发射光谱之间的波长差值。发射光谱的波长比激发光谱的长,振动弛豫消耗了能量。
b.发射光谱的形状与激发波长无关
c. 镜像规则
通常荧光发射光谱与它的吸收光谱(与激发光谱形状一样)成镜像对称关系。
随着溶液浓度的进一步增大,将会出现发光强度不仅不随溶液浓度线性增大、甚至出现随浓度的增大而下降的浓度效应。
荧光分析仪器
测量荧光的仪器主要由四个部分组成:激发光源、样品池、双单色器系统、检测器。
特殊点:有两个单色器,光源与检测器通常成直角
基本流程如图:
单色器:选择激发光波长的第一单色器和选择发射光(测量)波长的第二单色器;
光源:灯和高压汞灯,染料激光器(可见与紫外区)
检测器:光电倍增管。
荧光计上配上磷光测量附件即可对磷光进行测量。
1. 直接测定法
要求被分析物本身具有荧光。
通常采用相对测量方法,如工作曲线法。
每次测绘工作曲线最好用同一种稳定的荧光物质校准仪器的读数。
2. 间接测定法
被分析物本身不发荧光,或者因荧光量子产率太低而无法进行直接测定,便只能采用间接测定的办法。
如:光衍生法、荧光猝灭法、敏化荧光法等
化学发光分析
化学发光是由化学反应提供的能量激发物质所产生的光辐射。生物发光是指产生于生物体系中的化学发光
优点:(1). 灵敏度很高。(2). 仪器设备简单,无须光源和单色器,因而也消除了散射光和杂散光的干扰;(3). 线性范围宽;(4). 分析速度快。
局限:目前可供应用的发光体系尚有限,发光机理有待进一步研究,方法的选择性有待进一步提高。
(1)能够发光的化合物大多为有机化合物,芳香族化合物;
(2)化学发光反应多为氧化还原反应,激发能与反应能相当
DE=170~300 kJ/mol;位于可见光区;
(3)发光持续时间较长,反应持续进行;
定性依据:
(1)在一定条件下,峰值光强度与被测物浓度成线性;
2)在一定条件下,曲线下面积为发光总强度(S),其与被测物浓度成线性:

反应可采用静态或流动注射的方式进行:
静态方式:用注射器分别将试剂加入到反应器中混合, 测最大光强度或总发光量;试样量小,重复性差;
流动注射方式:用蠕动泵分别将试剂连续送入混合器,定时通过测量室,连续发光,测定光强度;试样量大;
? 光是电磁辐射,其作用于物质,光子与物质分子发生碰撞时,产生散射光。
? 当物质颗粒尺寸等于或大于入射光波长,产生丁达尔散射。
? 当物质颗粒尺寸小于入射光波长,产生拉曼散射和瑞利散射。
? 弹性碰撞时 无能量交换,且不改变频率,,仅改变运动方向,称瑞利散射;
? 非弹性碰撞不但改变方向,还有能量交换和频率改变,称拉曼散射。
? 1. 适合水体系的研究,尤其对生物样品和无机物的研究远较红外吸收光谱方便。
? 2. 一次可同时覆盖50~4000 cm-1波数的区间。
? 3. Raman光谱谱峰清晰尖锐,更适合定量研究。尤其是共振Raman光谱,灵敏度高,检出限可到10-6~10-8 mol·L-1。
? 4. Raman光谱所需样品量少,mg级即可。
? 5. 由于共振Raman光谱中谱线的增强是选择性的,因此可用于研究发色基团的局部结构特征。
? 11.2.1 Raman散射与Raman位移
? 当频率为ν0的位于可见或近红外光区的强激光照射样品时,有0.1%的入射光子与样品分子发生弹性碰撞,此时,光子以相同的频率向四面八方散射。这种散射光频率与入射光频率相同,而方向发生改变的散射,称为Rayleigh(瑞利)散射。
? 入射光与样品分子之间还存在着概率更小的非弹性碰撞(仅为总碰撞数的十万分之一),光子与分子间发生能量交换,使光子的方向和频率均发生变化。这种散射光频率与入射光频率不同,且方向改变的散射为Raman散射,对应的谱线称为Raman散射线(Raman线)。
? 与入射光频率ν0相比,频率降低的为Stokes(Stokes)线,频率升高的则为反Stokes线。Stokes线或反Stokes线与入射光的频率差为Raman位移。
? Stokes线远强于反Stokes线,
? 忽略反Stokes线,
即可得到物质的Raman光谱图。
? 若偏振器平行、垂直于激光方向时,散射光的强度分别为I║、I^,则两者之比称为退偏比,即rP=I^/ I║。
? 退偏比与分子的极化率有关,
rP越小,分子的对称性越高。通过测定Raman线的退偏比,可以确定分子的对称性。
? Raman光谱仪主要由光源、样品池、单色器及检测器组成,如图所示:

? 现代Raman光谱仪的光源多采用高强度的激光光源。
? 激光光源包括连续波激光器和脉冲激光器。
? 由于高强度激光光源易使试样分解,尤其是对生物大分子、聚合物等,因此一般采用旋转技术加以克服。
11.3.1.2 样品池
? Raman光谱法用玻璃作窗口。
? 单色器
? 色散型Raman光谱仪采用多单色器系统,如双单色器、三单色器。最好的是带有全息光栅的双单色器,能有效消除杂散光,使与激光波长非常接近的弱Raman线得到检测。
? 在傅里叶变换Raman光谱仪中,以Michelson(迈克耳孙)干涉仪代替色散元件,光源利用率高,可采用红外激光光源,以避免分析物或杂质的荧光干扰。
? 检测器
? 一般采用光电倍增管。
? 11.4.1 定性分析
? Raman位移△ 表征了分子中不同基团振动的特性,因此,可以通过测定△ 对分子进行定性和结构分析。另外,还可通过退偏比ρ的测定确定分子的对称性。
测定有机分子的骨架,并能够方便地区分各种异构体,如位置异构、几何异构、顺反异构
? 由于Raman信号弱,仪器价格较贵,激光Raman光谱法在定量分析中不占太大优势,直到共振Raman光谱法和表面增强Raman光谱法出现。
共振Raman光谱
当入射激光波长与待测分子的某个电子吸收峰接近或重合时,Raman跃迁的概率大大增加,使这一分子的某个或几个特征Raman谱带强度可达到正常Raman谱带的104~106倍,这种现象称为共振Raman(Resonance Raman)效应。
表面增强Raman光谱
一、电位分析之直接电位法
利用电极电位与浓度的关系测定物质含量的电化学分析法称为电位分析法。
膜电极
膜电极组成的半电池,没有电极反应;相界间没有发生电子交换过程。表现为离子在相界上的扩散,造成双电层存在,产生界面电位差。该类主指离子选择性电极。
参比电极:可逆性 重现性 稳定性
盐桥
作用
接通电路,消除或减小液接电位。
(2)使用条件
a.盐桥中电解质不含有被测离子。
b.电解质的正负离子的迁移率应该基本相等。
c.要保持盐桥内离子浓度的离子强度5~10倍于被测溶液。常用作盐桥的电解质有:KCl,NH4Cl,KNO3等。
u 膜电位及其产生
u 离子选择电极膜电位是膜内扩散电位和膜与电解质溶液形成的内外界面的界面电位的代数和。
u 扩散电位
在两种不同离子或离子相同而活度不同的液/液界面上,由于离子扩散速度的不同,能形成液接电位,它也可称为扩散电位。
u 如果膜与溶液接触时,膜相中可活动的离子与溶液中的某些离子有选择的发生互相作用,这种强制性和选择性的作用,从而造成两相界面的电荷分布不均匀,产生双电层形成电位差,这种电位称为界面电位。
u 膜电位是膜内扩散电位和膜与电解质溶液形成的内外界面的界面电位的代数和。
玻璃电极的结构同样由电极腔体(玻璃管)、内参比溶液、内参比电极、及敏感玻璃膜组成,而关键部分为敏感玻璃膜。


pH值的实用定义
当使用玻璃pH电极测量pH时,与饱和甘汞参比电极组成电池。电池图解式为:
Ag,AgCl︱内参比液︱玻璃膜︱试液‖KCl(饱和)︱Hg2Cl2,Hg
u 当测量pH较高,尤其Na+浓度较大的溶液时,测得的pH值偏低,称为钠差或碱差。
u 当测量pH小于1的强酸或盐度大水溶液,测得的pH值偏高时,称为酸差。
电位滴定法
u 以指示电极、参比电极及试液组成测量电池。
u 要加滴定剂于测量电池溶液里。
u 电位滴定法不依赖Nernst方程,而依赖于物质相互反应量的关系。
u 电位变化代替了经典滴定法指示剂的颜色变化确定终点,使其测量的准确度和精度都有了相当的改善,大大拓宽了应用范围。
伏安和极谱法
u 液相传质方式:
u 对流:所谓的对流,即粒子随着流动的液体而移动。
u 电迁移:在电场作用下,荷正电粒子向负极移动,荷负电粒子向正极移动。
u 扩散:当溶液中粒子存在浓度梯度时,这种粒子从高浓度向低浓度的移动过程。
极限电流减去残余电流, ,称为极限扩散电流,它与物质的浓度呈正比,这是极谱定量分析的基础。
滴汞电极作为工作电极
干扰电流及其消除方法
残余电流:来源于微量杂质的氧化还原,以及电极/溶液界面双层充电电流ie。一般采用作图法加以扣除。新的极谱分析技术如脉冲极谱应运而生。
迁移电流:加入大量支持电解质可以消除迁移电流。
极谱极大:在电流-电位曲线上出现的比扩散电流要大得多的突发的电流峰,称为极谱极大。其原因是汞滴在生长过程中产生了对流效应。通常采用加入表面活性剂来抑制。
氧电流:空气饱和的溶液中,氧的浓度约为0.25mM。一般采用通入惰性气体,或在中性或碱性溶液中加入Na2SO3,强酸中加入Na2CO3或Fe粉,从而消除氧的电流干扰。
可逆波与不可逆

还原波和氧化波
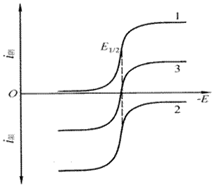
伏安法
线性扫描伏安法
单扫描极谱法
单扫描极谱(Single Sweep Polarography)也称示波极谱法,可以认为它是线性扫描伏安法的一种特殊类型,其特点为:
1.在汞滴的生长后期施加线性扫描电压;
2.用阴极射线示波器记录电流-电位曲线;
3.在一滴汞生长周期内完成一个极谱波的测定。
循环伏安法
循环伏安法(Cyclic Voltammetry)的电位扫描曲线是从起始电位开始,线性扫描到终止电位后,再回过头来扫描到起始电位。其电位-时间曲线如同一个三角形,故又称三角波电位扫描。
溶出伏安法
溶出伏安法(Stripping Voltammetry)是先将被测物质以某种方式富集在电极表面,而后借助线性电位扫描或脉冲技术将电极表面富集物质溶出(解脱),根据溶出过程得到的电流-电位曲线来进行分析的方法。
富集过程往往通过电解来实现,电解富集时工作电极作为阴极,溶出时作为阳极,称之为阳极溶出法;相反,工作电极作为阳极来电解富集,而作为阴极进行溶出,则称为阴极溶出法。如果富集过程是通过吸附作用完成的,则称为吸附溶出伏安法。
电解分析
电解分析(electrolytic analysis)包括两种方法:一是利用外电源将被测溶液进行电解,使欲测物质能在电极上析出,然后称析出物的重量,算出该物质在样品中的含量,这种方法称为电重量分析法(electrolytic gavimetry);二是使电解的物质由此得以分离,而称为电分离分析法(electrolytic separation)。
过电位的大小与许多因素有关,但主要有以下几方面:
(1) 电极材料和电极表面状态: 过电位的大小与电极材料有极大关系。例如,铅电极上氢的过电位为1.09V,汞电极上为1.14V,锌和镍电极上为O.747V,而铜电极上为0.584V。过电位的大小也与电极表面状态有关。例如,在上述条件,氢的超电位在光亮铂片上为0.068V,而镀铂黑电极上为0.030V。正是利用了氢在汞电极上有较大的过电位,使一些比氢还原性更强的金属先于氢在电极上析出,因而消除氢离子的干扰。这也是汞作极谱电极的优势之一。
(2)析出物质的形态: 一般说来,电极表面析出金属的过电位很小的,大约几十毫伏。在电流密度不太大时,大部分金属析出的过电位基本上与理论电位一致,例如,银、镉、锌等。但铁、钴、镍较特殊,当其以显著的速度析出时,过电位往往达到几百毫伏。如析出物是气体,特别是氢气和氧气,过电位是相当大的。例如,在酸性介质中,在光亮铂阳极上,电流密度为20mA/cm2时,氧的过电位比较小,而在碱性介质中则高达1.4V。可见介质也有大的影响。
(3)电流密度: 一般说,电流密度越大,过电位也越大。见表16-1。
(4)温度: 通常过电位随温度升高而降低。例如,每升高温度10℃,氢的过电位降低20~30mV。
通常,对于分离两种共存的一价离子,它们的析出电位相差在0.30V以上时,可认为能完全分离;两种共存的二价离子,它们的析出电位相差在0.15V以上时,即达到分离的目的在电解分析中,有时利用所谓“电位缓冲”的方法来分离各种金属离子。这种方法就是在溶液中加入各种去极化剂。由于它们的存在,限制阴极(或阳极)的电位变化,使电极电位稳定于某值不变。这种去极化剂在电极上的氧化或还原反应并不影响沉积物的性质,但可以防止电极上发生其它的反应。
控制电流电解法
控制电流电解法一般是指恒电流电解法,它是在恒定的电流条件下进行电解,然后直接称量电极上析出物质的质量来进行分析。
控制电位电解法
控制电位电解法是在控制阴极或阳极电位为一恒定值的条件下进行电解的方法。
库伦分析法
库仑分析法(coulometry)是在电解分析法的基础上发展起来的一种分析方法。它不是通过称量电解析出物的重量,而是通过测量被测物质在100%电流效率下电解所消耗的电量来进行定量分析的方法,定量依据是法拉第定律。
电重量分析法比较适合高含量物质测定,而库仑分析法即是用于痕量物质的分析,仍然具有很高的准确度。库仑分析法,与大多数其它仪器分析方法不同,在定量分析时不需要基准物质和标准溶液,是电量对化学量的绝对分析方法。
气相色谱法GC

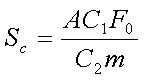
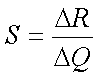 填充柱气相色谱仪
填充柱气相色谱仪
1. 气路系统
2.进样系统
3. 分离系统
4. 温控系统
检测器
1.灵敏度
气相色谱检测器灵敏度(S)定义为:通过检测器物质量变化(△Q)与响应信号变化(△R)之比:

热导检测器(TCD)是根据不同的物质具有不同的热导系数原理制成的。
故选择热导系数大的氢气或氦气作载气有利于灵敏度提高。
利用含碳有机物在火焰中燃烧产生离子,在外加的电场作用下,使离子形成离子流,根据离子流产生的电信号强度,检测被色谱柱分离出的组分。
氢火焰离子化检测器(FID
电子捕获检测器(ECD)
对具有电负性物质(如含卤素、硫、磷、氰等的物质)的检测有很高灵敏度(检出限约10-14g·cm-3)。
火焰光度检测器(FPD)
这种检测器可用于大气中痕量硫化物以及农副产品,水中的毫微克级有机磷和有机硫农药残留量的测定。
氮磷检测器(NPD)
马拉松农药。它对N、P化合物有较高的响应
固体固定相
1. 固体吸附剂
活性炭,硅胶,石墨化炭黑,氧化铝,分子筛
2. 高分子多孔微球
3. 化学键合固定相
载体
气相色谱载体又称担体,为多孔性颗粒材料。其作用是提供一个大的惰性表面,使固定液能在表面上形成一层薄而均匀的液膜。
对载体的要求 具有足够大的表面积和良好的孔穴结构,使固定液与试样的接触面较大,能均匀地分布成一薄膜,但载体表面积不宜太大,否则犹如吸附剂,易造成峰拖尾;表面呈化学惰性,没有吸附性或吸附性很弱,更不能与被测物起反应;热稳定性好;形状规则,粒度均匀,具有一定机械强度。
红色载体是将硅藻土与粘合剂在900℃煅烧后,破碎过筛而得,因铁生成氧化铁呈红色,故称红色载体,其特点是表面孔穴密集、孔径较小、比表面积较大。对强极性化合物吸附性和催化性较强,如烃类、醇、胺、酸等极性化合物会因吸附而产生严重拖尾。因此它适宜于分析非极性或弱极性物质。
白色载体是将硅藻土与20%的碳酸钠(助熔剂)混合煅烧而成,它呈白色、比表面积较小、吸附性和催化性弱,适宜于分析各种极性化合物。
酸洗碱洗硅烷化:用硅烷化试剂与载体表面硅醇基反应,使生成硅烷醚,以除去表面氢键作用力。
固定液的基本要求
(l)对固定液要求首先是选择性好固定液的基本要求
(2)组分分子与固定液间的作用 液相里主要存在的作用力是组分与固定液分子间的作用力,这种作用力反映了组分在固定液中的热力学性质。
固定液的分类
按固定液相对极性分类
此法规定非极性固定液角鲨烷的极性为0,强极性固定液β,β′-氧二丙睛的极性为100.
填充柱制备
1. 固定液涂渍
2. 柱填充、老化
一般将色谱柱与真空泵连接,在泵抽吸、振动或轻轻敲击条件下将涂渍固定液载体紧密填入色谱柱,然后将柱接入色谱柱箱内,在一定载气流下加热进行色谱柱老化,以除去残余溶剂、挥发性杂质,促进固定液膜更趋均匀。
毛细管柱的特点
1. 柱的渗透性好。
2. 柱效高,可采用长色谱柱。
3. 相比高、传质加快、柱容量小。
液相色谱HPLC
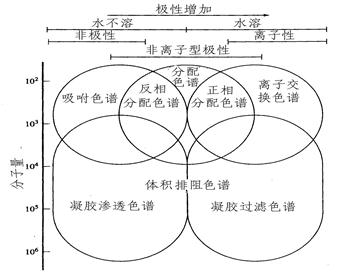
对流动相溶剂的要求是:
1. 化学惰性,
2.适用的物理性质,
3.溶剂清洗和更换方便,毒性小、纯度高、价廉等,便于操作和安全。
