九年级化学-化学方程式 整理小结
一、酸+ 碱== 盐+水
1、氢氧化钠与稀盐酸:NaOH + HCl == NaCl + H2O;
2、氢氧化钠与稀硫酸: 2 NaOH + H2SO4 == Na2SO4+ 2H2O
3、氢氧化钙溶液与稀硫酸:Ca(OH)2 + H2SO4 == CaSO4 + 2H2O
4、石灰水与稀盐酸:Ca(OH)2 + 2HCl == CaCl2 +2H2O
5、氢氧化镁中和胃酸过多:Mg(OH)2 + 2HCl == MgCl2 +2H2O
6、用氢氧化铝中和胃酸过多:Al(OH)3 + 3HCl == AlCl3 +3H2O
7、氢氧化铜与稀硫酸:Cu(OH)2 + H2SO4 == CuSO4↓ + 2H2O
二、酸+(某些)金属氧化物== 盐+水
8、.盐酸除铁锈:Fe2O3 + 6HCl == 2FeCl3 + 3H2O;
红色 黄色
9、硫酸除铁锈:Fe2O3 + 3H2SO4 == Fe 2(SO4)3 + 3H2O
10、氧化铜与稀硫酸:CuO + H2SO4 == CuSO4 + H2O
黑色 蓝色
11、氧化铜与稀盐酸:CuO + 2HCl == CuCl2 + H2O;
12、氧化钙与稀盐酸:CaO + 2HCl == CaCl2 + H2O;
三、碱+(某些)非金属氧化物== 盐+水
13、二氧化碳通入澄清石灰水:CO2 + Ca(OH)2 == CaCO3↓+ H2O;
14、二氧化碳与氢氧化钠:CO2 +2NaOH == Na2CO3 + H2O
15、二氧化硫与氢氧化钠溶液:SO2 +2NaOH == Na2SO3 + H2O
16、三氧化硫与氢氧化钠溶液:SO3 +2NaOH == Na2SO4 + H2O
四、酸+金属==盐+氢气
17、铝与盐酸反应制氢气:2Al + 6HCl == 2AlCl3 + 3H2↑;
18、铝与盐酸、硫酸反应制氢气:2Al + 3H2SO4 == Al2(SO4)3 + 3H2↑
19、镁与盐酸、硫酸反应制氢气:Mg + 2HCl == MgCl2 + H2↑;Mg + H2SO4 == MgSO4 + H2↑
20、铁与盐酸、硫酸反应制氢气:Fe + 2HCl == FeCl2 + H2↑;Fe + H2SO4 == FeSO4 + H2↑ 浅绿色 浅绿色
21、锌与盐酸、硫酸反应制氢气:Zn + 2HCl == ZnCl2 + H2↑;Zn + H2SO4 == ZnSO4 + H2↑
五、其他
22.生石灰与水反应:CaO + H2O == Ca(OH)2
23、实验室制二氧化碳:CaCO3 + 2HCl == CaCl2 + CO2↑+ H2O;
24、泡沫灭火器原理:Na2CO3 + 2HCl == 2NaCl+ CO2↑+ H2O
六、俗名与化学式
1、生石灰:CaO 5、盐酸:HCl
2、熟石灰、消石灰:Ca(OH)2 6、纯碱:Na2CO3
3、火碱、烧碱、苛性钠:NaOH 7、醋酸:CH3COOH
4、石灰石、大理石、鸡蛋壳:CaCO3
一、酸+ 碱== +
1、氢氧化钠与稀盐酸:
2、氢氧化钠与稀硫酸:
3、氢氧化钙溶液与稀硫酸:
4、石灰水与稀盐酸:
5、氢氧化镁中和胃酸过多:
6、用氢氧化铝中和胃酸过多:
7、氢氧化铜与稀硫酸:
二、 酸+(某些)金属氧化物== +
8、.盐酸除铁锈:
9、硫酸除铁锈:
10、氧化铜与稀硫酸:
11、氧化铜与稀盐酸:
12、氧化钙与稀盐酸:
三、碱+(某些)非金属氧化物== +
13、二氧化碳通入澄清石灰水:
14、二氧化碳与氢氧化钠:
15、二氧化硫与氢氧化钠溶液:
16、三氧化硫与氢氧化钠溶液:
四、酸+金属== +
17、铝与盐酸反应制氢气:
18、铝与硫酸反应制氢气:
19、镁与盐酸反应制氢气:
20、铁与硫酸反应制氢气:
21、锌与硫酸反应制氢气:
五、其他
22.生石灰与水反应:
23、实验室制二氧化碳:
24、泡沫灭火器原理:
六、俗名与化学式
1、生石灰: 5、盐酸: 2、熟石灰、消石灰: 6、纯碱:
3、火碱、烧碱、苛性钠: 7、醋酸:4、石灰石、大理石、鸡蛋壳:
第二篇:九年级化学化学方程式小结
九年级化学-化学方程式整理小结
 一.化合反应
一.化合反应

 1.镁带燃烧: 2Mg + O
2 ==== 2MgO
1.镁带燃烧: 2Mg + O
2 ==== 2MgO
 2.铁丝燃烧及生锈:3Fe + 2O
2 ==== Fe
3O
4 ;4Fe + 3O
2 ===== 2Fe
2O
3(缓慢氧化)
2.铁丝燃烧及生锈:3Fe + 2O
2 ==== Fe
3O
4 ;4Fe + 3O
2 ===== 2Fe
2O
3(缓慢氧化)
 3.铜丝加热及生锈: 2Cu + O
2 === 2CuO ; 2Cu + O
2 + H
2O + CO
2 == Cu
2(OH)
2CO
3
3.铜丝加热及生锈: 2Cu + O
2 === 2CuO ; 2Cu + O
2 + H
2O + CO
2 == Cu
2(OH)
2CO
3
 4.铝丝加热或形成氧化膜:4Al + 3O
2 === 2Al
2O
3
4.铝丝加热或形成氧化膜:4Al + 3O
2 === 2Al
2O
3

 5.氢气燃烧或爆炸: 2H
2 + O
2 === 2H
2O
5.氢气燃烧或爆炸: 2H
2 + O
2 === 2H
2O
 6.碳的燃烧:2C + O
2 ==== 2CO(不完全燃烧);C + O
2 === CO
2(完全燃烧)
6.碳的燃烧:2C + O
2 ==== 2CO(不完全燃烧);C + O
2 === CO
2(完全燃烧)
 7.硫的燃烧:S + O
2 === SO
2
7.硫的燃烧:S + O
2 === SO
2
 8.磷的燃烧:4P + 5O
2 === 2P
2O
5
8.磷的燃烧:4P + 5O
2 === 2P
2O
5
 9.二氧化碳被碳还原:C + CO
2 === 2CO
9.二氧化碳被碳还原:C + CO
2 === 2CO
 10.人工固氮(合成氨):N
2 + 3H
2 ======= 2NH
3
10.人工固氮(合成氨):N
2 + 3H
2 ======= 2NH
3
11.生石灰溶于水:CaO + H2O == Ca(OH)2
12.二氧化碳溶于水:CO2 + H2O == H2CO3
 13.二氧化硫溶于水:SO
2 + H
2O == H
2SO
3
13.二氧化硫溶于水:SO
2 + H
2O == H
2SO
3
14.二氧化硫在空气中转化为三氧化硫:2SO2 + O2 ==== 2SO3
 15.三氧化硫溶于水:SO
3 + H
2O == H
2SO
4
15.三氧化硫溶于水:SO
3 + H
2O == H
2SO
4
 16.工业上制盐酸(氢气在氯气中燃烧):H2 + Cl2 === 2HCl
16.工业上制盐酸(氢气在氯气中燃烧):H2 + Cl2 === 2HCl
17.金属钠在氯气中燃烧:2Na + Cl2 2NaCl
18.浓盐酸与浓氨水相靠近:NH3 + HCl == NH4Cl
 二.分解反应
二.分解反应
 1.碳酸氢铵(碳铵)受热分解:NH4HCO3 NH3↑+ CO2↑+ H2O
1.碳酸氢铵(碳铵)受热分解:NH4HCO3 NH3↑+ CO2↑+ H2O
 2.碱式碳酸铜(铜绿受热分解):Cu2(OH)2CO3 2CuO + H2O + CO2↑
2.碱式碳酸铜(铜绿受热分解):Cu2(OH)2CO3 2CuO + H2O + CO2↑
 3.加热高锰酸钾制氧气:2KMnO4 K2MnO4 + MnO2 + O2↑
3.加热高锰酸钾制氧气:2KMnO4 K2MnO4 + MnO2 + O2↑
 4.二氧化锰催化双氧水制氧气:2H2O2 2H2O + O2↑
4.二氧化锰催化双氧水制氧气:2H2O2 2H2O + O2↑
5.电解水:2H2O 2H2↑+ O2↑
 6.碳酸分解:H2CO3 == CO2↑+ H2O
6.碳酸分解:H2CO3 == CO2↑+ H2O
 7.碳酸钙高温煅烧分解:CaCO3 CaO + CO2↑
7.碳酸钙高温煅烧分解:CaCO3 CaO + CO2↑
8.电解熔融状态的氧化铝制取金属铝:2Al2O3 4Al + 3O2↑

 三.置换反应
三.置换反应
 1 氢气还原金属氧化物:Fe2O3 + 3H2 2Fe + 3H2O;Fe3O4 + 4H2 3Fe + 4H2O;
1 氢气还原金属氧化物:Fe2O3 + 3H2 2Fe + 3H2O;Fe3O4 + 4H2 3Fe + 4H2O;

 CuO + H2 Cu + H2O
CuO + H2 Cu + H2O
 2.碳粉还原金属氧化物:2Fe2O3 + 3C 4Fe + 3CO2↑;Fe3O4 + 2C 3Fe + 2CO2↑;
2.碳粉还原金属氧化物:2Fe2O3 + 3C 4Fe + 3CO2↑;Fe3O4 + 2C 3Fe + 2CO2↑;
2CuO + C 2Cu + CO2↑
 3.制取水煤气:C + H2O CO + H2
3.制取水煤气:C + H2O CO + H2
4.铝与盐酸、硫酸反应制氢气:2Al + 6HCl == 2AlCl3 + 3H2↑;2Al + 3H2SO4 == Al2(SO4)3 + 3H2↑
5.镁与盐酸、硫酸反应制氢气:Mg + 2HCl == MgCl2 + H2↑;Mg + H2SO4 == MgSO4 + H2↑
6.铁与盐酸、硫酸反应制氢气:Fe + 2HCl == FeCl2 + H2↑;Fe + H2SO4 == FeSO4 + H2↑
7.锌与盐酸、硫酸反应制氢气:Zn + 2HCl == ZnCl2 + H2↑;Zn + H2SO4 == ZnSO4 + H2↑
8.湿法炼铜法,铁与硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu

 9.铜与硝酸银溶液反应:Cu + 2AgNO3 == Cu(NO3)2 + 2Ag
9.铜与硝酸银溶液反应:Cu + 2AgNO3 == Cu(NO3)2 + 2Ag
 10.铝热剂反应:2Al + Fe2O3 Al2O3 + 2Fe;8Al + 3Fe3O4 4Al2O3 + 9Fe
10.铝热剂反应:2Al + Fe2O3 Al2O3 + 2Fe;8Al + 3Fe3O4 4Al2O3 + 9Fe
11.金属镁与二氧化碳反应:2Mg + CO2 2MgO + C
四.复分解反应:
1.酸碱中和反应:HCl + NaOH == NaCl + H2O;
Cu(OH)2 + H2SO4 == CuSO4 + 2H2O
H2SO4 + Ba(OH)2 == BaSO4↓+ 2H2O;
Ca(OH)2 + 2HCl == CaCl2 +2H2O
2.金属氧化物与酸溶液反应:Fe2O3 + 6HCl == 2FeCl3 + 3H2O;
CuO + H2SO4 == CuSO4 + H2O
MgO + 2HCl == MgCl2 + H2O;
Al2O3 + 3H2SO4 == Al2(SO4)3 + 3H2O
3.碳酸盐与酸溶液反应:CaCO3 + 2HCl == CaCl2 + CO2↑+ H2O;Na2CO3 + 2HCl == 2NaCl+ CO2↑+ H2O
K2CO3 + H2SO4 == K2SO4 + CO2↑+ H2O
4.盐溶液与碱溶液反应:Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH;CuSO4 + 2NaOH== Cu(OH)2↓+Na2SO4
CuSO4 + Ba(OH)2 == BaSO4↓+ Cu(OH)2↓
5.Ag+与Cl-反应:HCl + AgNO3 == AgCl↓+ HNO3;NaCl + AgNO3 == AgCl↓+ NaNO3
6.Ba2+与SO42-反应:BaCl2 + CuSO4 == BaSO4↓+ CuCl2;H2SO4 + BaCl2 == BaSO4↓+ 2HCl
7.纯碱与氯化钙溶液反应:Na2CO3 + CaCl2 == CaCO3↓+ 2NaCl
8.铵盐与碱反应产生氨气:NH4NO3 + NaOH == NaNO3 + NH3↑+ H2O
(NH4)2SO4 + Ca(OH)2 == CaSO4 + 2NH3↑+ 2H2O

 五.其他反应类型:
五.其他反应类型:
 1.一氧化碳还原金属氧化物:Fe2O3 + 3CO 2Fe + 3CO2;Fe3O4 + 4CO 3Fe + 4CO2;
1.一氧化碳还原金属氧化物:Fe2O3 + 3CO 2Fe + 3CO2;Fe3O4 + 4CO 3Fe + 4CO2;
CuO + CO Cu + CO2
2.非金属氧化物与碱溶液反应:CO2 + Ca(OH)2 == CaCO3↓+ H2O;CO2 +2NaOH == Na2CO3 + H2O
 SO2 +2NaOH == Na2SO3 + H2O
SO2 +2NaOH == Na2SO3 + H2O
 3.有机物燃烧:CH4 + 2O2 CO2 + 2H2O; C2H6O + 3O2 2CO2 + 3H2O
3.有机物燃烧:CH4 + 2O2 CO2 + 2H2O; C2H6O + 3O2 2CO2 + 3H2O
 C6H12O6 + 6O2 6CO2 + 6H2O
C6H12O6 + 6O2 6CO2 + 6H2O
 CxHyOz + (
CxHyOz + (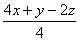 )O2 xCO2 +
)O2 xCO2 + 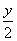 H2O
H2O
 4.绿色植物光合作用:6CO
2 + 6H
2O C
6H
12O
6 + 6O
2
4.绿色植物光合作用:6CO
2 + 6H
2O C
6H
12O
6 + 6O
2
化学方程式的练习:
一.化合反应
1.镁带燃烧:
2.铁丝燃烧及生锈:
3.铜丝加热及生锈:
4.铝丝加热或形成氧化膜:
5.氢气燃烧或爆炸:
6.碳的燃烧:
7.硫的燃烧:
8.磷的燃烧:
9.二氧化碳被碳还原:
10.人工固氮(合成氨):
11.生石灰溶于水:
12.12.二氧化碳溶于水:
13.二氧化硫溶于水:
14.二氧化硫在空气中转化为三氧化硫:
15.三氧化硫溶于水:
16.工业上制盐酸(氢气在氯气中燃烧):
17.金属钠在氯气中燃烧:
18.18.浓盐酸与浓氨水相靠近:
二.分解反应
1.碳酸氢铵(碳铵)受热分解:
2.碱式碳酸铜(铜绿受热分解):
3.加热高锰酸钾制氧气:
4.二氧化锰催化双氧水制氧气:
5.电解水:
6.碳酸分解:
7.碳酸钙高温煅烧分解:
8.电解熔融状态的氧化铝制取金属铝:
9.三.置换反应
1 氢气还原金属氧化物:
2.碳粉还原金属氧化物:
3.制取水煤气:
4.铝与盐酸、硫酸反应制氢气:
5.镁与盐酸、硫酸反应制氢气:
6.铁与盐酸、硫酸反应制氢气:
7.锌与盐酸、硫酸反应制氢气:
8.湿法炼铜法,铁与硫酸铜溶液反应:
9.铜与硝酸银溶液反应:
10.铝热剂反应:
11.金属镁与二氧化碳反应:
四.复分解反应:
1.酸碱中和反应:
2.金属氧化物与酸溶液反应:
3.碳酸盐与酸溶液反应:
4.盐溶液与碱溶液反应:
5.Ag+与Cl-反应:
6.Ba2+与SO42-反应:
7.7.纯碱与氯化钙溶液反应:
8.铵盐与碱反应产生氨气:
五.其他反应类型:
1.一氧化碳还原金属氧化物:
2.非金属氧化物与碱溶液反应:
3.有机物燃烧:
 4.绿色植物光合作用:
4.绿色植物光合作用:
