三液系(三氯甲烷-醋酸-水)相图的绘制
一、实验目的
1. 熟悉相律和用三角形坐标表示三组分相图的方法;
2. 用溶解度法绘制具有一对共轭溶液的三组分相图。
二、实验原理
在室温定压下,三组分体系的状态和组分之间的关系通常可用等边三角形坐标表示,如图1
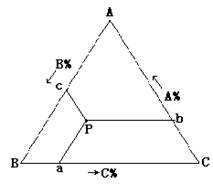
等边三角形三顶点表示纯物A、B、C。AB、BC、CA三边分别表示A和B、B和C、C和A所组成的二组分体系的组成。三角形内任一点则表示三组分体系的组分。如P点的组成为A%=Cb、B%=Ac、C%=Ba.
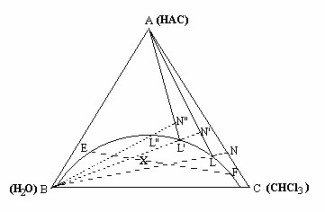
具有一对共轭溶液的三组分体系的相图如图二所示。该三液系中,A和B及A和C完全互溶,而B和C部分互溶。曲线为溶解度曲线。曲线外是单相区,曲线内是两相区。物系点落在两相区内,即分成两相。
绘制溶解度曲线方法较多。本实验是先在完全互溶的两组分以一定的比例混合所成的均相溶液中滴加入组分B,物系点则沿NB线上移动,直至溶液变浑,即位L点。然后加入A,物系点沿LA上升至N,点而变清。如再加入B,则物系点又沿N,B移至L,使再次变浑。再滴加A使变清……,最后连接L,L,,L,,……各点,即可绘制其溶解度曲线。
三、仪器与药品
1、仪器
滴定管(50ml,酸式)1支;移液管(5ml,刻度)2支;
移液管(10ml,刻度)1支;锥形瓶(100ml)2支;漏斗架 1支
2、药品
氯仿(分析纯),冰醋酸(分析纯)
四、实验步骤
在洁净的酸式滴定管内装水;
移取6ml氯仿及2ml醋酸于干燥洁净的100ml磨口锥形瓶中,然后慢慢滴入水,且不停地振摇,至溶液由清变浑,即为终点,记下水的体积。再向此瓶中加入2ml醋酸,体系又成均相,继续用水滴定至终点。同法再依次加入3.5ml、6.5ml醋酸,并分别再水滴定,记录各次各组分的用量。
另取一干燥洁净的100ml磨口锥形瓶,用移液管移入1ml氯仿和3ml醋酸。用水滴至终点,以后依次在添加2ml、5ml、6ml醋酸。分别用水滴至终点,记录各次各组分的用量。
五、实验数据
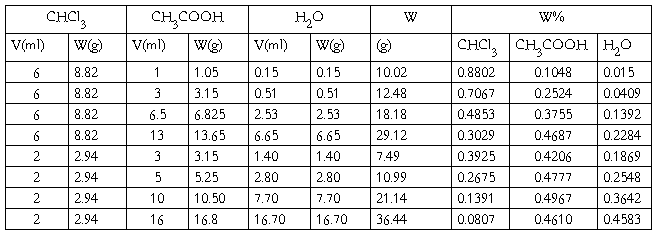
六、数据处理
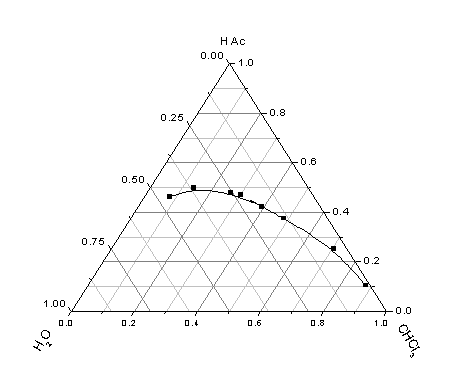
七、问题讨论:
1.为什么试验中用到的玻璃器皿需要干燥?
答:因为所测定的体系含有水的组成。
2.在滴加水的过程中须一滴滴加入,且不断振摇锥形瓶,待出现浑浊并在2~3分钟内不消失,即为终点。为什么在接近终点时要多加振摇?
答:接近终点时,这时溶液已近饱和,溶解平衡需要较长的时间。
3.如果结线不通过物系点,其原因可能是什么?
答:实验所得的连接线未通过物系点,原因主要是溶液振荡分层平衡不够,多振荡,让醋酸水溶液与醋酸氯仿溶液充分分层。
4.在用水滴定溶液Ⅱ的最后,溶液由清到浑的终点不明显,这是为什么?
答:因为这时溶液已经接近饱和,溶解的平衡需要较长的时间。
第二篇:物化实验报告(电动势)
华 南 师 范 大 学 实 验 报 告
专业:材料化学 年级班级:12级材料化学
课程名称:物理化学实验 指导老师:林晓明
实验项目:电导法测定乙酸乙酯皂化反应的速率常数
原电池电动势的测定与应用实验报告
一、实验目的
1.掌握电位差计的测定原理和原电池电动势的测定方法;
2.加深对可逆电极、可逆电池、盐桥等概念的理解;
3.测定以下电池(I)及电池(II)的电动势;
4.了解可逆电池电动势测定的应用。
二、实验原理
1.对消法测定原电池电动势
原电池电动势不能直接用伏特计来测量,因为电池与伏特计接通后有电流通过,在电池两极上会发生极化现象,使电极偏离平衡状态。另外,电池本身有内阻,伏特计所量得的仅是不可逆电池的端电压。准确测定电池的电动势只能在无电流(或极小电流)通过电池的情况下进行,需用对消法:
原理:是在待测电池上并联一个大小相等,方向相反的外加电势差,这样待测电池中没有电流通过,外加电势差的大小即等于待测电池的电动势。
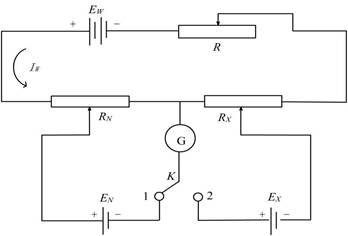
Ew-工作电源;EN-标准电池;
EX-待测电池;R-调节电阻;
RX-待测电池电动势补偿电阻;
RN-标准电池电动势补偿电阻;
K-转换电键; G-检流计
2.原电池电动势的测定
电池的书写习惯是左方为负极,右方为正极。负极进行氧化反应,正极进行还原反应。如果电池反应是自发的,则电池电动势为正。符号“∣”表示两相界面,“‖”表示盐桥。在电池中,电极都具有一定的电极电势。当电池处于平衡态时,两个电极的电极电势之差就等于该可逆电池的电动势。规定电池的电动势等于正、负电极的电极电势之差,即: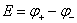
电池(I):

负极反应: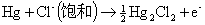
正极反应: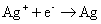
总反应: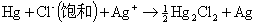
银电极的电极电势: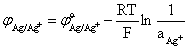
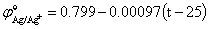
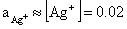
饱和甘汞电极的电极电势:

从上述电池的两个电极电位可算出电池的理论电动势,将测定值与之比较.
3.电动势测定的应用——求溶液的pH值
电池(II):
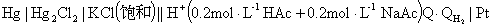
正极反应:
醌氢醌电极电极电势:
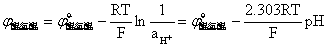
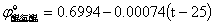
三、仪器和试剂
1.实验仪器:
SDC数字电位差计1台、饱和甘汞电极1支、光亮铂电极1支、银电极1支、
250 mL烧杯1个、20 mL小烧杯2个、U形管2个
2.实验试剂:
0.02 mol·L-1的硝酸银溶液、0.2 mol·L-1的醋酸钠溶液、0.2 mol·L-1的醋酸溶液、饱和氯化钾溶液、醌氢醌晶体、硝酸钾、琼脂
四、实验步骤
1.制备盐桥
在250 mL烧杯中,加入100 mL蒸馏水和3 g 琼脂,盖上表面皿,放在石棉网上用小火加热至近沸,继续加热至琼脂完全溶解。然后加入40 g硝酸钾,充分搅拌使硝酸钾完全溶解后,趁热用滴管将它灌入干净的U形管中,两端要装满,中间不能有气泡,静置待琼脂凝固后便可使用。制备好的盐桥不使用时应浸入饱和硝酸钾溶液中,防止盐桥干涸。
2.组合电池
(1)取一20 mL小烧杯洗净后,用数毫升0.02 mol?L-1的硝酸银溶液连同银电极一起淌洗,然后装此溶液至烧杯的2/3处,插入银电极,用硝酸钾盐桥与饱和甘汞电极连接构成电池。
(2)另取一20 mL小烧杯,洗净后用数毫升0.2 mol?L-1的HAc与0.2 mol?L-1的NaAc的混合溶液连接同铂电极一起淌洗,然后装此混合液至烧杯的2/3处,加入少量醌氢醌粉末,用干净的小玻棒搅匀使之溶解,但仍保持溶液中含少量固体,然后插入光亮铂电极,架上盐桥与饱和甘汞电极组成电池。
3.测定电池的电动势
(1)根据Nernst公式计算实验温度下电池(I)、(II)的电动势理论值。
(2)正确接好测量电池(I)的线路。用SDC数字电位差计测量电池(I)的电动势。每隔2分钟测一次,共测三次。
(3)同法,用SDC数字电位差计测量电池(II)的电动势,要测至平衡时为止。
(4)测量完毕后,倒去两个小烧杯的溶液,洗净烧杯的溶液。盐桥两端淋洗后,浸入硝酸钾溶液中保存.
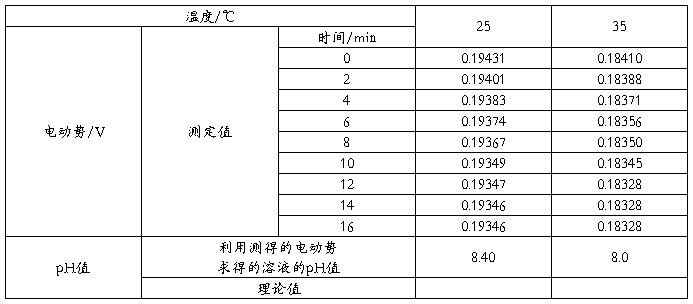
五、实验记录及数据处理
室温:17.8℃ 气压:1025.5 hPa
表一:实验数据记录表
电池(I)测定记录
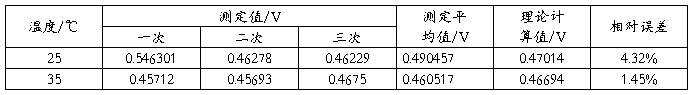
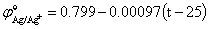
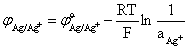

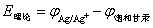
绝对误差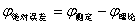 相对误差
相对误差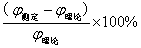
根据上式便可算出25℃及35℃的实验数据
电池(II)测定记录
由醌氢醌电极电极电势:
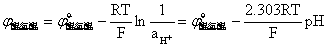
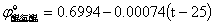
电动势法测定化学反应的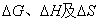 :
:
在恒温恒压可逆的条件下,电池所作的电功是最大有用功。利用对消法测定电池的电动势,即可获得相应的电池反应的自由能改变值: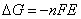
根据吉布斯-亥姆霍兹公式,有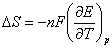
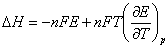

式中n为电极反应中电子的计量系数,F为法拉第常数,E为电池的电动势。
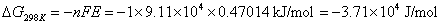
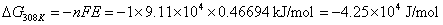
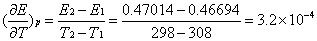
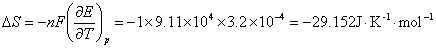

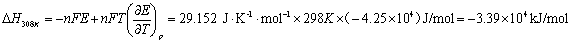 六、实验注意事项
六、实验注意事项
1.为使极化影响降到最小,测量前可初步估算被测电池的电动势大小,以便在测量时能迅速找到平衡点;
2.制备电极时,防止将正负接错;
3.甘汞电极使用时请将电极帽取消,用完后用氯化钾溶液浸泡;
4.制备盐桥时,灌注速度要掌控好,不能留下气泡;
5.实验中的液体废物不能直接倒入下水道,要倒入废液缸,以便集中处理。
6.在测量电池电动势时,尽管采用的是对消法,但是在对消点前,测量回路将有电流通过,所以在在测量过程中不能使测量回路一直联通,否则回路中将一直有电流通过,电极就会产生极化,溶液的浓度也会发生变化,测得的就不是可逆电池电动势,所以应接通一下调一下,直至平衡。
七、提问与思考
1.为何测电动势要用对消法?对消法的原理是什么?
答:原电池电动势不能直接用伏特计来测量,因为电池与伏特计接通后有电流通过,在电池两极上会发生极化现象,使电极偏离平衡状态。另外,电池本身有内阻,伏特计所量得的仅是不可逆电池的端电压。准确测定电池的电动势只能在无电流(或极小电流)通过电池的情况下进行,需用对消法:
原理:是在待测电池上并联一个大小相等,方向相反的外加电势差,这样待测电池中没有电流通过,外加电势差的大小即等于待测电池的电动势。
2.测电动势为何要用盐桥?如何选用盐桥以适合不同体系?
答:对于双液电池电动势的测定需用盐桥消除液体接通电势。
(2)选择盐桥中电解质的要求是:①高浓度(通常是饱和溶液);②
电解质正、负离子的迁移速率接近相等;③不与电池中的溶液发生反应。具体选择时应防止盐桥中离子与原电池溶液中的物质发生反应,如原电池溶液中含有能
与Cl-作用而产生沉淀的Ag+、Hg离子或含有能不K+离子作用的ClO-
离子,则不可使用KCl盐桥,应选用KNO3或NH4NO3盐桥
3.使用醌氢醌电极的限制条件得什么?
答:醌氢醌电极在pH>8.5以上的介质中电极电势不稳定,在有其他氧化剂或还原剂存在时会引起误差,故仅能用于弱酸或弱碱性溶液,不能用于强碱性溶液的测定。
4.如果测量过程中,检零指示呈溢出符号,试从接线上分析可能是什么原因?
答: 可能的原因是正负极接反了或电路中的某处有断路。
八、参考文献
[1] 何广平,南俊明,孙艳辉.物理化学实验.北京:化学工业出版社,2007
[2] 傅献彩, 沈文霞,姚天扬. 物理化学. 北京:高等教育出版社,1990
[3] 江琳才,何广平,孙艳辉,左晓希,马国正.物理化学第四版.北京:高等教育出版社,2013
