华 南 师 范 大 学 实 验 报 告
学生姓名 学 号
专 业 年级、班级
课程名称 实验项目 纯液体饱和蒸气压的测定—静态法
实验类型 □验证 □设计 ■综合 实验时间 年 月 日
实验指导老师 实验评分
一、实验目的
1. 明确纯液体饱和蒸汽压和蒸汽压的概念及其与温度的关系,加深对劳修斯-克拉贝龙(Clausius-Clapeyron)方程式的理解。
2. 掌握静态法测定纯液体饱和蒸汽压的原理及方法,并学会用图解法求纯液体的平均并学会由图解法求其平均摩尔气化热和正常沸点。
3. 了解数字式低真空侧压仪=,熟悉常用的气压计的使用及校正的方法,初步掌握真空实验技术。
二、实验原理
在一定温度下(距离临界温度较远时),纯液体与其蒸气达平衡时的蒸气压称为该温度下液体的饱和蒸气压,简称为蒸气压。蒸发一摩尔液体所吸收的热量称为该温度下液体的摩尔气化热。 液体的饱和蒸气压与温度的关系用克劳修斯-克拉贝龙方程式表示:
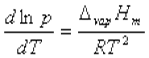
式中,R为摩尔气体常数;T为热力学温度;ΔvapHm为在温度T时纯液体的摩尔气化热。
在温度变化范围不大时,ΔvapHm可以近似作为常数,积分上得:
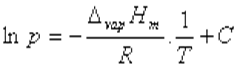
由此式可以看出,以lnp对 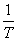 作图,应为一直线,直线的斜率为m=
作图,应为一直线,直线的斜率为m=  ,由斜率可求算液体的ΔvapHm=-Rm
,由斜率可求算液体的ΔvapHm=-Rm
当液体的饱和蒸汽压登月外界压力时,液体沸腾,此时的温度即为该液体的沸点,当外压为1atm(1.01325kPa)时,液体的沸点成为正常沸点。
测定液体饱和蒸气压的方法很多。本实验采用静态法,是指在某一温度下,直接测量饱和蒸 气压,此法一般适用于蒸气压比较大的液体。实验所用仪器是纯液体饱和蒸气压测定装置,如图Ⅲ-3-1所示。
平衡管由A球和U型管B、C组成。平衡管上接一冷凝管5,以橡皮管与压力计相连。A内装待测液体,当A球的液面上纯粹是待测液体的蒸气,而B管与C管的液面处于同一水平时,则表示B管液面上的(即A球液面上的蒸气压)与加在C管液面上的外压相等。此时,体系气液两相平衡的温度称为液体在此外压下的沸点。用当时的大气压减去压力计两水银面的高度差,即为该温度下液体的饱和蒸气压。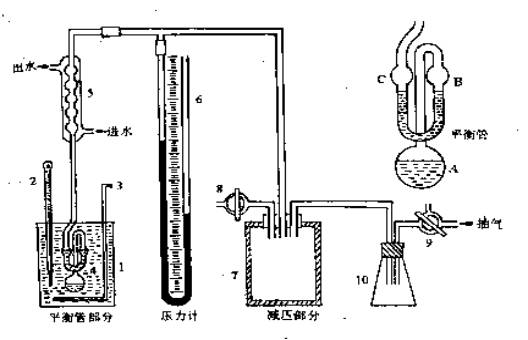
纯液体饱和蒸气压测定装置图
1.恒温水浴;2.温度计;3.搅拌;4.平衡管;5.冷凝管;6.水银压力计;7.缓冲瓶;8.进气活塞;9.三通活塞;10.安全瓶。
三、仪器试剂
液体蒸汽压测定装置1套 真空泵(公用) 1台 纯水 100oC水银玻璃温度计1支
四、实验步骤
1.将纯水倒入等压计中
(这部分已由老师装置完毕)
检查U形管两边处于同一水平,水面接近B球底部位置。
2.系统气密性检查
关闭直通活塞,旋转三通活塞使系统与真空泵连通,开动真空泵,抽气减压至汞压力计两臂汞面压差为-53.3kPa(400mmHg)时,关闭三通活塞,使系统与真空泵、大气皆不通。观察压力计示数,如果在3分钟内示数维持不变,则表明系统不漏气。否则应逐段检查装置每个部分,消除漏气原因。
3.排除管内的空气
先将恒温槽温度调至40oC接通冷凝水,抽气降压至液体轻微沸腾,此时弯管内的空气不断随蒸气管逸出(速度不宜过快,若过快可适当打开漏入空气,但不应使空气倒灌),如此沸腾3分钟,可认为空气被排除干净。
4.饱和蒸气压的测定
当空气被排除干净,且体系温度恒定后,打开直通活塞缓缓放入空气(切不可太快,以免空气倒灌入弯管中,如果发生空气倒灌,则须重新排除空气),直至B管、C管中液面平齐,关闭直通活塞,立即记录此时的温度与压力差(如果放入空气过多,C管中液面低于B管的液面,须再缓慢抽气,再调平齐)。
然后,将恒温槽温度升高5℃,因温度升高后,液体的饱和蒸气压增大,液体会不断沸腾。为了避免B、C管中液体大量蒸发,应随时打开直通活塞缓缓放入少量空气,保持 C管中液面相对平静。当体系温度恒定后,再次放入空气使B、C管液面平齐,记录温度和压差。然后依次每升高5℃,测定一次压差,总共测7个值。
五、实验记录和数据处理
1、记录:将测得数据计计算结果列表:
室温:24.4oC 气压计读数:102.600kPa 校正后压强102.217kPa
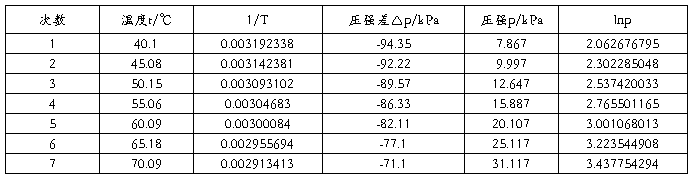
2、根据实验数据作出lgP—1/T图,根据斜率求出摩尔汽化热△vapH与正常沸点。

纯水的正常沸点为在一个大气压下,(101.3kPa)下的沸点。由上面的回归方程可知,
T正常=374.10K=100.95oC
△vapHm=-Rm=41.04KJ
3、计算T正常、△vapHm的相对误差,并对数据结果进行讨论。
T正常相对误差Et=(374.10-373.15)/373.15×100%=0.25%
△vapHm相对误差Et=(41.04-40.63)/40.63×100%=1.01%
六、讨论与思考
1、根据测量数据,将校正压力p取对数值lnp作为纵坐标,以开氏温度倒数1/T作为横坐标,绘制散点图。由出lnp-1/T关系图可以看出,直线相关性较高,线性较好,因而斜率m较为准确,可以用于进行平均摩尔汽化热△vapHm与正常沸点T正常的代入计算。通过计算结果,并与参考文献数值比较,相对误差比较小,因此实验数据较为完好。
2、实验过程中,进行了两次。第一次实验相对失败,由于在空气漏入时没有控制得当,导致U形管中过多的水倒灌入A球,以至于U形管液面过低难以读数,且空气进入馆内,气密性受到影响,实验不能进行下去。
3、在更换了仪器之后,重新开始进行实验。后续进行较为顺利。但在U形管调节过程中,难以控制恰好两边平衡,且平衡后因A球内水继续沸腾液面依然会出现差值。故实验中在调节时适当预留液面差,待A球内沸腾后渐渐平衡液面差,则左右液面恰好接近持平。通过多次实验总结经验,掌握了该方法后实验速度较快提高。
4、参见数据。纯水的平均摩尔汽化热比文献值要略高,主要原因为该参数是温度的函数,随着温度变化而变化。实验平均温度约55.1℃,比原定平均温度55℃,因此比文献值略高。而正常沸点是在101.325kPa下,而本次实验的大气压校正后较标准大气压偏大,因此测得沸点较文献值高。
六、提问与思考
1、什么是液体的饱和蒸汽压?什么叫正常沸点?液体的沸点与外压有何关系?
在密闭条件中,在一定温度下,与固体或液体处于相平衡的蒸气所具有的压力称为饱和蒸气压;在外压为一个大气压的时候液体的沸点称为正常沸点;液体沸点随着外压增大而增大。
2、本实验方法能否用于测定其它溶液的蒸汽压?为什么?
视具体情况而定,一般不可以。因为溶液浓度随着溶剂的蒸发而增大,蒸汽压也因此变化,故难以测量准确。
3、等压计U形管液体有什么作用?冷凝器有什么作用?
U形管中液体可以用于指示管内蒸汽压与外压平衡的指标,用于等效测量管内气压;用于冷凝蒸汽,防止蒸汽被抽入真空泵中。
4、怎样从数字式低真空测压仪示数得出纯液体饱和蒸汽压?
通过U形管两边持平,等效地读出外压即等于液体饱和蒸汽压。
5、能否在加热情况下检查是否漏气?
不能。加热过程中温度不能恒定,气-液两相不能达到平衡,压力也不恒定
6、实验中为什么要防止空气倒灌?
若发生倒灌则管内不再是纯液体的蒸汽,测量的将不是纯液体蒸汽压。
7、实验时抽气和漏入空气的速度应如何控制?为什么?
不论抽气还是漏入空气都应该尽可能地慢,防止气压变化过大在管中变化过于明显,导致出现倒灌或者爆沸的现象
8、实验时大烧杯中的水为什么一定要淹没等压计的U形管?
保证整个体系处于同一恒温状态,使得U形管左右两边温度相等,才能用外压等效处理为U形管内饱和蒸汽压强。
七、参考文献
[1]何广平 南俊民等 物理化学实验.北京:化学工业出版社,2008
[2] 付献彩、沈文霞、姚天扬编,《物理化学》,第四版,上册,第144页,高等教育出版社(1990)。
第二篇:物化实验报告_液体饱和蒸气压的测定
实验4 液体饱和蒸气压的测定
丛乐 2005011007 生51
实验日期:20##年11月24日星期六 提交报告日期:20##年12月8日星期六
助教老师:叶逢春
1 引言
1.1实验目的
1. 运用克劳修斯-克拉贝龙方程,求出所测温度范围内平均摩尔气化焓及正常沸点。
2. 掌握测定饱和蒸汽压的方法。
1.2 实验原理
在通常温度下(距离临界温度较远时),纯液体与其蒸气达平衡时的蒸气压称为该温度下液体的饱和蒸气压,简称为蒸气压。蒸发1摩尔液体所吸收的热量称为该温度下液体的摩尔气化热。
液体的蒸气压与液体的本性及温度等因素有关。随温度不同而变化,温度升高时,蒸气压增大;温度降低时,蒸气压降低,这主要与分子的动能有关。当蒸气压等于外界压力时,液体便沸腾,此时的温度称为沸点,外压不同时,液体沸点将相应改变,当外压为pø(101.325kPa)时,液体的沸点称为该液体的正常沸点。
液体的饱和蒸气压与温度的关系用克劳修斯(Clausius)-克拉贝龙(Clapeyron)方程式表示:
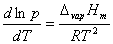
式中,R为摩尔气体常数;T为热力学温度;ΔvapHm为在温度T时纯液体的摩尔气化热。
假定ΔvapHm与温度无关,或因温度变化范围较小,ΔvapHm可以近似作为常数,积分上式,得:

或 
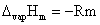
式中:B——积分常数。
从上式可知:若将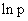 对1/T作图应得一直线,斜率m=
对1/T作图应得一直线,斜率m=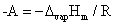
由此可得 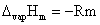 ,同时从图上可求出标准压力时的正常沸点。
,同时从图上可求出标准压力时的正常沸点。
2 实验操作
2.1 实验药品、仪器型号及测试装置示意图
1.仪器
等压管1支、稳压瓶1个、负压瓶1个、恒温槽1套、冷凝管1个、真空泵1台、自耦调压变压器1台(TDG1/250型)、搅拌器1个、压力计1台(LZ-PI型)、温度测量控制仪1台(CK-1B型)。
2.药品
无水乙醇(分析纯;20℃时密度:0.789-0.791g/ml;Mr=46.07)
2.2 实验条件
表1 实验条件记录

2.3 实验操作步骤及方法要点
1. 装置与装样
按图1安装好整套装置,并把乙醇装入等压管中,使液面在等压管的三分之二处。
2. 检漏

图1 纯液体饱和蒸气压测定装置:1、等压管,2、冷凝管,3、搅拌器,4、加热器,5、1/10゜C温度计,6、辅助温度计,7、稳压瓶,8、负压瓶,9、干燥管。
将H活塞关上,打开活塞I、F和G,用真空泵抽气到压力计显示的气压为25~30kPa时,关上I、F和G。等片刻后,利用压力计分段检查系统是否漏气。
3. 升温
开动搅拌器,调节加热器电压在160V左右。
4. 排气
当水浴温度超过50℃时,等压管内液体开始沸腾,即大量气泡通过液栅由C管排出。沸腾3-5分钟(每秒钟约排出3-4个气泡)就可以除去AB间的空气及溶在液体中的空气。注意调节加热器电压,控制恒温槽温度在52℃附近。
5. 蒸汽压的测定
排气完后,打开活塞H,使体系通过毛细管缓慢吸入空气逐渐升高压力,直到稳压瓶中的压力快接近蒸气压时为止。然后调节调压器,改变加热电压,直到BC液面相对位置不变,此时表示温度己恒定。最后将BC液面基本调平,稳定一分钟左右,迅速记下温度t,压力计P的读数。
继续用加热器加热水浴,加热过程中适当调节活塞H,使液体不激烈沸腾,当温度升高3—4℃时再重复上述步骤。—直升温到75℃附近。总共测6—7个点即可。
6. 结束
实验完后,将系统与大气相通,关闭调压器,整理实验台。最后,将实验数据输入计算机进行计算。
7. 实验注意事项
1)等压管中AB液面间的空气必须排净。
2)在操作过程中要防止液体倒吸,即c处气体通过液栅吸入AB的空间。一旦倒吸,重新排气。
3)在升温时,需随时调节活塞H,避免液体激烈沸腾。
3 结果与讨论
3.1 原始实验数据
1) 原始实验测量数据
下表中数据为实验中测定的温度及与之对应的饱和蒸气压:(见表2)
表2 实验测定温度与对应饱和蒸气压
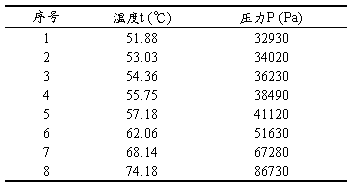
2) 原始计算机数据处理结果:
方程In(P/Pa)= -B/T + A;A = 14.31695;B = 5026.281;
相关度R = 1.000015
乙醇沸点:Tb=78.24526℃,相对误差U1 = -0.00606%;
摩尔蒸发焓:△vapHm= 41788.5 J/mol, 相对误差U2 = 3.33458%
3) 实验相关文献值(无水乙醇)
△vapHm= 42.6 kJ·mol-1;Tb=351.54K(78.34℃)
摘自本实验文献[3]
3.2计算的数据、结果
1) 对原始数据的计算和处理
实验中测定的温度及与之对应的饱和蒸气压如下表2所示:
表2 实验测定温度与对应饱和蒸气压
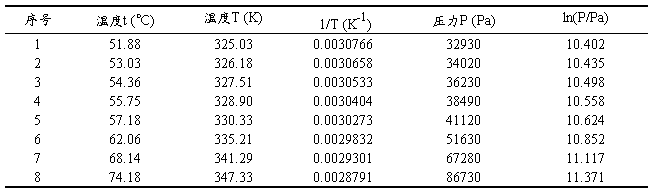
2) 进行ln(P/Pa)— 1/T作图和正常沸点的计算
利用表2中数据(由于表2中数据点1在拟合中明显偏离其他数据点,因此舍去此点,即舍去温度51.88℃时测定的数据),在Origin Pro中作ln(P/Pa)— 1/T图,并进行线性拟合。
结果如下图2所示:
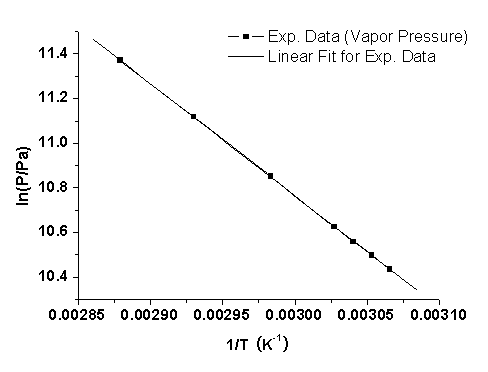
图3无水乙醇ln(P/Pa)—1/T图
通过回归分析,可得标准曲线的方程为:
Y = A + B * X;
其中A = 25.84191; B = -5025.907;
R = -0.9999778782
根据此式可以从直线斜率求得平均摩尔蒸发焓:
斜率m = B = △vapHm/R = -5025.907;
△vapHm= -m · R = 5025.907×8.314472 = 41785.39 J/mol
其中R为摩尔气体常数,数值取R = 8.314472 J·mol-1K-1
将直线延长到p=101.325kPa处,可求得无水乙醇的正常沸点:
Tb = 351.0736K = 77.9236℃
3) 无水乙醇的蒸气压和温度的关系式。
根据前述计算所得的直线斜率和截距可知,无水乙醇的蒸气压和温度的关系式为:
In(P/Pa)= B/T + A;A = 25.84191;B = -5025.907
(上式中P为无水乙醇的蒸气压,单位为Pa;T为温度,单位为K)
3.3讨论分析
1) 测定结果与文献值的比较
由文献值(见3.1)可知:△vapHm= 42.6 kJ·mol-1; Tb=351.54K (78.34℃)
本实验中测得结果为: △vapHm= 41785.39 J/mol; Tb = 351.0736K (77.9236℃)
测定结果与文献值的相对误差为
ε(△vapHm)= (41785.397- 42600/41785.397)×100% = -1.949492%
ε(Tb)= (77.9236-78.34/77.9236)×100% = -0.534370%
利用实验室计算软件对数据进行处理,得到的结果如下:
乙醇沸点:Tb = 78.24526℃,相对误差U1 = -0.00606%;
摩尔蒸发焓:△vapHm= 41788.5 J/mol, 相对误差U2 = 3.33458%
测定值与文献值之间的偏差处在合理的范围之内,相对较小,说明本次实验结果是较为可靠和准确的。
而考虑到本次实验与测定文献值时所使用的仪器、方法以及条件(表1)可能存在不同,这一偏差的存在属于正常现象。
2) 测量过程中产生误差的可能原因及分析
对各个实验过程进行分析,产生误差的可能原因有以下几点:
(a) 温度测定过程中产生的误差:在进行温度测定的过程中,由于搅拌器的搅拌不可能使得体系中各部分的温度达到绝对均匀。所以,通过温度测量仪测得的是测温探头附近液体的温度,此温度与饱和蒸气的温度不一定完全一致,从而使所测数据和最终计算结果与实际值间存在误差。
(b) 实验中环境条件改变产生的误差:在测量过程中,虽然采用恒温槽使得体系的温度处于恒定状态,但仍然不能完全保证测定条件没有发生变化。同时,由于实验中测定仪器直接与外界环境接触,所以当外界环境温度、大气压力和湿度改变时,测量仪器所处状态的不同可能影响其测得数据的准确性。
特别是考虑到实验中使用了较多的数字式电子测定仪器,当温度和湿度改变时,电子元件的物理化学特性(如电阻、电容、化学势等)很可能发生改变,从而导致所测得数据的误差。
(c) 测量体系的改变:在实验中认为测量体系的组成没有变化,始终为无水乙醇。但是在实际情况下,体系组成改变的可能也是存在的。具体而言,如果排气或升温过程中液体沸腾过于剧烈,可能使蒸发出的液体将仪器磨口密封用的甘油溶解,之后混有甘油的蒸汽返回体系时就可能改变体系组成,从而使体系饱和蒸气压发生变化,引入误差。为避免这一现象,升温时需随时调节活塞H,防止液体剧烈沸腾。
(d) 测量仪器的系统误差:由于测温仪器本身不可能绝对精确,实验测量过程中也可能存在由此导致的系统误差,影响结果的准确性。
3) 对实验中异常现象的分析和讨论
液面不稳定现象:
测量中当体系升至较高温度时(约65℃以上),两侧液面会长时间出现小范围波动。这一现象产生的原因可能是:当体系温度较高时,液体(包括体系和恒温槽介质)蒸发速度较快,恒温槽内的温度也远高于室温。这使得整个体系很难继续保持各部分的温度和组成基本均一稳定,而且恒温槽调节温度恒定的能力也有所下降。
因此,在测定中我们根据助教老师的建议,在温度低于60℃的情况下多测定几组数据。同时,实验中我们待温度和液面稳定一段时间后再读数和记录,从而基本避免了此异常现象对结果的影响。
实验室软件与Origin Pro拟合结果存在微小差异:
在撰写实验报告时,我发现利用Origin Pro对所得数据进行拟合后所得到的结果与实验室软件的结果之间存在微小的差异。
实验室软件:△vapHm= 41788.5 J/mol; Tb =351.39526K (78.24526℃)
Origin Pro:△vapHm= 41785.39 J/mol; Tb = 351.0736K (77.9236℃)
两组数据△vapHm和Tb数值的相对偏差分别为0.0074%和0.41%,产生这一偏差的主要原因可能是在拟合计算过程中,两种软件所采用数据的有效位数不同,从而使得拟合出的结果有微小差异。
4) 对仪器装置、操作步骤、实验方法的改进意见及体会
完成此次实验后,我深切地感受到蒸气压实验利用我们所掌握的物化知识,从实验的角度对我们进行了一次充分的训练。实验结果是次要的,而我们所掌握的实验方法和总结分析才是关键。结合实验过程,我对本项试验有如下几点建议和体会:
(a) 判断液面相平且稳定的辅助线:在测定过程中的关键一步是调节两侧液面相平且稳定,从而保证压力记读数等于测定体系内饱和蒸汽的压力。如果在试管中标记出几条辅助线(可使用记号笔完成),则可以为判断提供一个固定不动的参照物,从而有利于通过肉眼判断液面是否相平且稳定。
(b) 实验装置和过程的设计:实验中的难点之一是每次升温后需重新调节电压使得体系温度再次处于恒定状态。本小组实验中所得的经验是:调节电压时可以根据前面两次测定时的电压差,直接确定第三次电压的基本范围,将电压直接调至此范围内,从而迅速找到最佳电压,提高实验效率。
(c) 恒温槽的液体介质:在本次试验中恒温槽的介质是水,由于测定过程中体系温度最高可达75℃左右,而水的沸点约为100℃,因此在测定最后几个数据时,由于水的蒸发作用较强,体系的稳定程度开始下降。在今后的实验中如果能够利用沸点更高的介质组成恒温槽,则可能有助于缓解这一问题。
5) 实验的总结与体会
本次物化实验中,物化实验室的叶逢春助教老师对我们进行了耐心的指导,给予了我们热情的帮助。特别是在实验前老师为我们详细讲解了所有实验装置的使用和实验中容易出现的问题及解决办法。因此,在随后的实验中我们遇到类似问题时就能够从容应对和处理。如果没有各位老师和助教的辛勤准备和付出,我们绝对无法顺利的完成本次的实验。非常非常感谢您,您辛苦乐!
4 结论
本次实验运用克劳修斯-克拉贝龙方程为理论依据,测定了无水乙醇的饱和蒸汽压,并求得所测温度范围内平均摩尔气化焓及正常沸点,具体结果如下:
无水乙醇正常沸点为: Tb = 351.0736K = 77.9236℃,相对误差ε1 = -1.949492%
无水乙醇平均摩尔蒸发焓:△vapHm= 41785.39 J/mol,相对误差ε2 = -0.534370%
无水乙醇饱和蒸气压与温度的关系:In(P/Pa)= B/T + A;A = 25.84191;B = -5025.907
(上式中P为无水乙醇的蒸气压,单位为Pa;T为温度,单位为K;下同)
而利用实验室计算软件对数据进行处理,得到的结果如下:
乙醇沸点:Tb=78.24526℃,相对误差U1 = -0.00606%;
摩尔蒸发焓:△vapHm= 41788.5 J/mol, 相对误差U2 = 3.33458%
方程In(P/Pa)= -B/T + A;A = 14.31695;B = 5026.281。
5 参考文献
[1]傅献彩,沈文霞,姚天扬。物理化学上册。第四版。北京:高等教育出版社,1990:144
[2]清华大学化学系物理化学实验编写组. 物理化学实验。北京:清华大学出版社.1991
[3]Ed. by Robert C. Weast. Handbook of Chemistry and Physics, 58th Ed. Ohio CRC Press, 1977
[4]朱文涛 编著 物理化学 清华大学出版社
6 附录
思考题:
1、说明饱和蒸气压、正常沸点、沸腾温度的含义。
答:(1)在通常温度下(距离临界温度较远),某物质在密闭空间内气液两相共存时,纯液体与其蒸气达平衡时的蒸气压(气相的压力)称为该温度下液体的饱和蒸气压,简称为蒸气压。
(2)正常沸点是指某种物质在外压为标准大气压pø(101.325kPa)时的沸点。
(3)沸腾温度是指某种物质在某一特定大气压力下的沸点。
2、克-克方程在什么条件下才能使用?为什么本实验测定的只是平均蒸发焓?
答:(1)克-克方程在:蒸气可视为理想气体,液体体积相较气体体积可以忽略,且体系内气、液两相平衡时可以使用。
(2)由于蒸发焓与测定温度有关(即不同温度下摩尔蒸发焓不同),而本实验测定中认为蒸发焓为常数,以方便积分运算,所以本实验是利用克-克方程和一定温度范围内的实验数据进行蒸发焓计算,所得结果只是这一温度区间的平均蒸发焓。
3、稳压瓶、负压瓶的作用是什么?什么时候需用活塞H与G?
答:(1)稳压瓶的作用:在实验中调节G和H活塞可控制稳压瓶内的气压。通过此调节可使等压管两侧BC中的液面相平,这样在液面稳定后,压力记所测得稳压瓶中的压力与乙醇饱和蒸气的压力基本相等,从而测得不同温度下乙醇的饱和蒸气压。
(2)负压瓶的作用是当稳压瓶压强过高(即B液面高于C)时,可以通过打开G活塞来向稳压瓶提供负压,降低稳压瓶气压使得B液面下落,调节BC液面相平。
(3)C液面比B高的时候,调节H活塞,B液面比C高的时候,调节G活塞。
4、计算证明赶气3—5分钟后AB空间的空气确已除净。
答:证明过程如下,不妨设AB管可容纳气体的体积为20ml,且在每秒3~4个气泡的情况下,蒸气进入AB空间的速度为0.5ml/s,同时每秒钟有0.5ml气体排至C管。由于气泡体积相对AB管体积较小,所以气体排至C管后,可以认为在AB内气体的组成没有收到影响。
在除去空气的过程中,若初始空气体积分数为X0 = 1,则0.5ml乙醇蒸气进入AB后空气体积分数变为X1 = 20·X0/(20+0.5),同时排出0.5ml混合气体,但如前所述此步不影响AB内气体组成。
因此,在排气3分钟(即180秒)后,AB内空气体积分数X180 = (20×1/20.5)180 = 0.012;
而在排气5分钟(即300秒)后,X300 = (20×1/20.5)300 = 6.1×10-4 = 0.061%。
综上,排气3~5分钟后,AB管内空气的确已经除净。
异常情况附注:
如果利用实验室软件所得到的方程:ln(P/Pa)= -B/T + A;A = 14.31695;B = 5026.281进行计算,则得到的正常沸点(101.325kPa)为Tb = 1800.978K(1527.828℃),此数值与文献值偏差过大,似乎不合理。比较此公式和自行处理数据时得到的公式,最大的不同在于参数A的数值。我们所得的A值为25.84191,因此得到的结果为Tb = 351.0736K (77.9236℃)。此现象产生的原因可能是软件与我们自行进行数据处理时所使用的计算和显示方式不同。
