黏度法测定水溶性高聚物相对分子质量
一、实验目的
1.掌握用乌氏粘度计测定液体粘度的原理和方法
2.测定聚乙二醇的平均相对分子质量
二、实验原理
粘度是指液体对流动所表现的阻力,这种阻力反抗液体中相邻部分的相对移动,可看作由液体内部分子间的内摩擦而产生。当相距为 ds 的两液层以不同速率 (v 和dv)移动时,产生的流速梯度为dv/ds。建立平稳流动时,维持一定流速所需要的力f’与液层接触面积A 以及流速梯度dv/ds成正比:
f’= η ? A? dv/ds ①
单位面积液体的粘滞阻力用 f 表示,f= f’/A,则:
f = η ? (dv/ds ) ②
此式称为牛顿粘度定律表示式,比例常数η称为粘度系数,简称粘度,单位为 Pa?s。
如果液体是高聚物的稀溶液,则溶液的粘度反映了溶剂分子之间的内摩擦力、高聚物分子之间的内摩擦力、以及高聚物分子和溶剂分子之间的内摩擦力三部分。三者之和表现为溶液总的粘度 η。其中溶剂分子之间的内摩擦力所表现的粘度如用 η0表示的话,则由于溶液的粘度一般说来要比纯溶剂的粘度高,我们把两者之差的相对值称为增比粘度,记作ηsp:
ηsp= ( η- η0 )/η0 ③
溶液粘度与纯溶剂粘度之比称为相对粘度ηr :
ηr = η /η0 ④
增比粘度表示了扣除溶剂内摩擦效应后的粘度,而相对粘度则表示整个溶液的行为。它们之间的关系为:ηsp= η/η0 - 1 = ηr - 1 ⑤
高分子溶液的增比粘度一般随浓度的增加而增加。为了便于比较,将单位浓度下所显示出的增比粘度称为比浓粘度η sp/c 。而将 lnη r/c 称为比浓对数粘度。为进一步消除高聚物分子之间的内摩擦效应,将溶液无限稀释,这时溶液所呈现的粘度行为基本上反映了高聚物分子与溶剂分子之间的内摩擦,这时的粘度称为特性粘度 [η]:
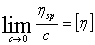 ⑥
⑥
特性粘度与浓度无关,实验证明,在聚合物、溶剂、温度三者确定后,特性粘度的数值只与高聚物平均相对分子质量有关,它们之间的半经验关系式为:
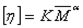 ⑦
⑦
式中的 K 为比例系数,α是与分子形状有关的经验常数。这两个参数都与温度、聚合物和溶剂性质有关。
粘度测定的方法有用毛细管粘度计测量液体在毛细管中的流出时间、落球粘度计测定圆球在液体中的下落速率、旋转粘度计测定液体与同心轴圆柱体相对转动阻力等三种。本实验采用第一种方法。
高分子溶液在毛细管粘度计中因重力作用而流出时,遵守泊肃叶定律:
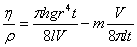 ⑧
⑧
式中,ρ:液体密度;l:毛细管长度;r:毛细管半径;t:流出时间;h:流经毛细管液体的平均液柱高度;g:重力加速度;V:流经毛细管液体的体积;m:与仪器几何形状有关的参数,当 r / l << 1 时,取 m = 1。 此式可改写为:
η / ρ = αt - β /t ⑨
当 β 小于1,t 大于 100s 时,第二项可忽略。对稀溶液,密度与溶剂密度近似相等,可以分别测定溶液和溶剂的流出时间,求算相对粘度 ηr :
ηr= η / η 0 = t / t0 ⑩
根据测定值可以进一步计算增比粘度(ηr - 1),比浓粘度(η sp /c),比浓对数粘度(ln η r /c)。对一系列不同浓度的溶液进行测定,在坐标系里绘出比浓粘度和比浓对数粘度与浓度之间的关系,外推到 c = 0 的点,此处的截距即为特性粘度[η]。在 K、α 已知时,可求得平均相对分子质量。
对于聚乙二醇,在 25℃ 时,K = 1.56×10-2(Kg-1?dm3),α = 0.5。
三、仪器与试剂
乌氏粘度计 1支; 恒温水浴 1套;
移液管(10mL) 2只; 秒表 1块;
洗耳球 1个; 蒸馏水;
已配好浓度的聚乙二醇
四、实验步骤
1、粘度计的洗涤
先将洗液灌入粘度计内,并使其反复流过毛细管部分。然后将洗液倒入专用瓶中,再顺次用自来水、过滤过的蒸馏水洗涤干净。容量瓶、移液管也都应清洗干净。
2、溶剂流出时间t0的测定
开启恒温水浴,设置恒温25℃。并将黏度计垂直安装在恒温水浴中(G球及以下部位均浸在水中),用移液管吸10mL过滤过的蒸馏水,从A管注入粘度计F球内,恒温10min,在C管和B管的上端套上干燥清洁橡皮管,并用夹子夹住C管上的橡皮管下端,使其不通大气。用洗尔球在B管的上端吸气,将水从F球经D球、毛细管、E球抽至G球中部,取下洗尔球,同时松开C管上夹子,使其通大气。此时溶液顺毛细管而流下,当凹液面最低处流经刻度a线时,立刻按下秒表开始记时,至b处则停止记时。记下液体流经a、b之间所需的时间。
3、溶液流出时间的测定
取出粘度计,倾去其中的水,加入少量的无水酒精润洗黏度计,甩干。用移液管吸取10mL聚乙醇溶液,注入粘度计内,同上法,安装粘度计,测定溶液的流出时间t,然后依次加入2.0,3.0,5.0,10.0 ml蒸馏水。每次稀释后,先在C管处用洗耳球打气,使溶液混合均匀。然后将稀释液多次抽洗黏度的E球和G球及毛细管部分,使粘度计内各处溶液的浓度相等,按同样方法进行测定。
4、粘度计的最后清洗处理
测完后,倾尽粘度计内的溶液,依次用自来水、蒸馏水洗净。再加上少量的无水酒精,用电吹风吹干。将黏度计放入盛放黏度计的盒中。
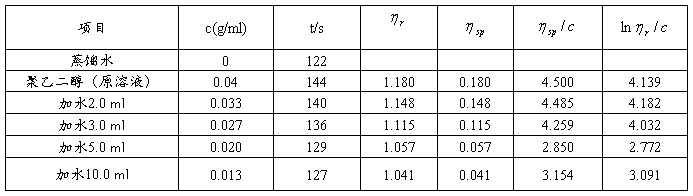
五、数据记录与处理
1、根据实验对不同浓度溶液测出的相应留出时间,并计算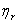 ,
,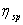 ,
,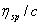 和
和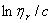 并填入下表。
并填入下表。
2、做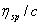 与c及
与c及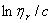 与c的关系图:
与c的关系图:
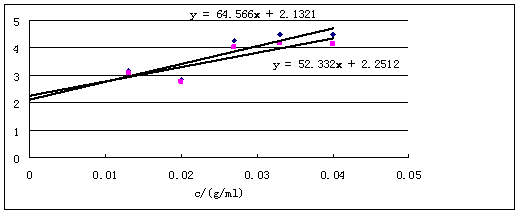
从图中读得特性粘度[η]=2.13=1.56×10-3(Kg-1?dm3)×M 1/2,求得M=1.86×104g/mol
六、问题与讨论
1、乌氏粘度计中的C管的作用是什么?能否去除C管改为双管粘度计使用?
答:C管的作用是形成气承悬液柱。不能去除C管改为双管粘度计,因为没有了C管,就成了连通器,不断稀释之后会导致粘度计内液体量不一样,这样在测定液体流出时间时就不能处在相同的条件之下,因而没有可比性。只有形成了气承悬液柱,使流出液体上下方均处在大气环境下,测定的数据才具有可比性。
2、粘度计毛细管的粗细对实验结果有何影响?
答:粘度计毛细管的过粗,液体流出时间就会过短,那么使用Poisuille公式时就无法近似,也就无法用时间的比值来代替粘度;如果毛细管过细,容易造成堵塞,导致实验失败。
3、为什么用[η]来求算高聚物的分子量?它和纯溶剂粘度有无区别?
答:特征黏度反映了在无限稀溶液中,溶剂分子与高分子间的内摩擦效应,它决定于溶剂的性质和聚合物分子的形态及大小;而纯溶剂黏度反映了溶剂分子间的内摩擦力效应,所以二者值不同
4、乌贝路德黏度计为什么一定要竖直放置?
答:使溶液在重力的作用下流出,减少溶液在流动时与器壁之间的内摩擦,从而提高实验的准确度。
第二篇:物化实验报告(2)
实验一、 溶液电导的测定和应用
同实验者
室温Cº 大气压Pa 年 月 日
一、实验目的
二、实验原理(简述基本原理并写出计算Λm、а、Kcº所依据的公式)
1、简述基本原理
2、计算Λm、а、Kcº所依据的公式
三、实验仪器和试剂
四、实验步骤(简述主要步骤)
五、数据处理
1、不同浓度醋酸溶液电导率测定值及Λm、а、Kcº 计算值
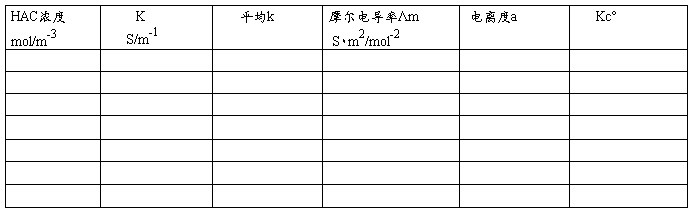
2、 计算Kcº的平均值
六、思考题
1、测量溶液电导率时,测量顺序为什么一般从低浓度开始依次进行?
2、醋酸的极限摩尔电导能否用作图法求出?为什么?
实验二、旋光法测定蔗糖转化反应的速率常数
同实验者
室温Cº 大气压Pa 年 月
一、实验目的
二、实验原理
1、 基本原理
2、计算半衰期t½, 速率常数k的公式
三、实验仪器和试剂
四、实验步骤(简述主要步骤)
五、数据处理
1、 实验数据
T= , a∞平均=
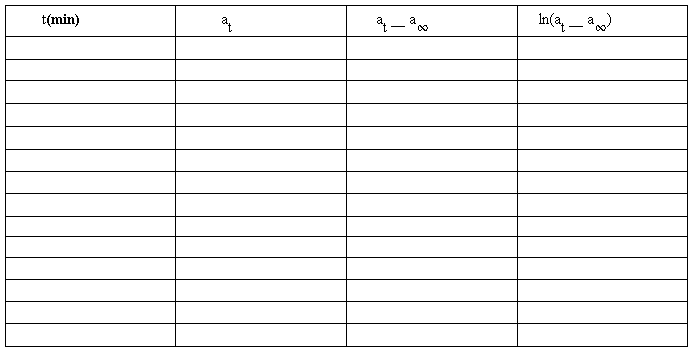
2、以ln(at a∞)对t 作图

3、 由图求出速率常数k和半衰期t½
六、思考题
1、 混合蔗糖和HCL溶液时,是将HCL溶液加到蔗糖中,能否将蔗糖加到HCL溶液中?
2、 一级反应有那些特点?配制蔗糖溶液时,其浓度是否需要准确?
