����ѧһ�����Ծ�
һ��ѡ���� ( ��15�� 30�� )
1. 2 �� (0910)
��һ����(���������ȵ������ֹ���)��,����1 mol��������,��1 mol�����������ȫ������һ������ѧ���ʵ��ڣ� ( )
(A) (1/2)L/[L] (B) 2L/[L]
(C) (1/2)L/[L] (D) 2L/[L]
2. 2 �� (0155)
������������о�����������ʱ,����������һ������? ( )
(A) Q=0 (B) W=0
(C) ��U=0 (D) ��H=0
3. 2 �� (0983)
��һ��(�����,����,����ͬ��)�����ϵ��,��ѹֻ��������������,����˹������ֵ���¶�������α仯? ( )
(A) (¶G/¶T)p> 0
(B) (¶G/¶T)p< 0
(C) (¶G/¶T)p= 0
(D) �Ӿ�����ϵ����
4. 2 �� (0074)
��һ��������װ��ˮ��ˮ��ͨһ����˿�������ع��磬ͨ���ˮ������˿���¶Ⱦ��������ߣ�����ˮ�͵���˿Ϊ��ϵ������Ϊ���������У� ( )
(A) Q < 0 , W = 0 , ��U < 0
(B) Q = 0 , W < 0 , ��U > 0
(C) Q > 0 , W = 0 , ��U > 0
(D) Q < 0 , W = 0 , ��U > 0
5. 2 �� (9031)
��101.325 kPa��,385 K��ˮ��Ϊͬ���µ�ˮ����,�Ըñ仯����,���и�ʽ���ĸ���ȷ? ( )
(A) ��S��+��S��>0 (B) ��S��+��S��<0 (C) ��S��+��S��=0 (D) ��S��+��S����ֵ����ȷ��
6. 2 �� (0065)
��һ��ѹ��Ͳ���������������Ͳ�⣬��Ͳ��ѹ����Ͳ��ѹ�����ʱ�رջ�������ʱͲ���¶Ƚ��� ( )
(A) ���� (B) ����
(C) ���� (D) ���ж�
7. 2 �� (0890)
���������ھ���������,������ѹѹ�����ȶ�,�˱仯�е���ϵ�ر�DS���������ر�DS��ӦΪ��������������������������
(A) DS��> 0 , DS��< 0
(B) DS��< 0 , DS��> 0
(C) DS��> 0 , DS��= 0
(D) DS��< 0 , DS��= 0
8. 2 �� (0424)
б�����ȼ���ȵ��� ( )
(A) SO2(g)��������
(B) SO3(g)��������
(C) ��б���ȼ����
(D) ��
9. 2 �� (1003)
�ڱ�ѹ��p$��,383.15 K��ˮ��Ϊͬ���µ�����,����Qp������������,�ĸ���ϵʽ���ܳ���? ( )
(A) ��G < 0 (B) ��H = Qp
(C) ��SISO < 0 (D) ��SISO > 0
*. 2 �� (0090)
����˵����,��һ������? ( )
(A) ��ϵ�ų�������һ�����ڻ������յ�����
(B) ��ϵ�¶ȵĽ���ֵһ�����ڻ����¶ȵ�����ֵ
(C) ����ѧƽ��ʱ��ϵ���¶��뻷�����¶����
(D) ����ϵ1����ϵ2�ֱ��뻷�������ƽ��,�������ϵ���¶���ͬ
11. 2 �� (0805)
2 mol H2�� 2 mol Cl2�ھ��ȸ�Ͳ�ڷ�Ӧ���� HCl ���壬��ʼʱΪ���³�ѹ����( )
(A) ��rU = 0����rH = 0����rS > 0����rG < 0
(B) ��rU < 0����rH < 0����rS > 0����rG < 0
(C) ��rU = 0����rH > 0����rS > 0����rG < 0
(D) ��rU > 0����rH > 0����rS = 0����rG > 0
12. 2 �� (0278)
�������徭�����Ȳ�������̴�״̬ 1 (p1,V1,T1)�仯��״̬ 2 (p2,V2,T2)�������Ĺ�Ϊ�� ( )
(A) p2V2-p1V1
(B) p2(V2-V1)
(C) [p2V /(1-g)](1/V2g-1-1/V1g-1)
/(1-g)](1/V2g-1-1/V1g-1)
(D) (p2V2-p1V1)/(1-g)
13. 2 �� (0182)
���еĹ��̿�Ӧ�ù�ʽ��H=Q���м�����ǣ� ( )
(A) ���������������̬ѹ����ͬ���м�ѹ���б仯�Ĺ���
(B) �������������һֱ�����������Ĺ���
(C) 273.15 K��p$��Һ̬ˮ��ɱ��Ĺ���
(D) �����¼���ʵ������
14. 2 �� (0238)
����һ�������������壬���й��̿��ܷ������ǣ� ( )
(1) ����������ͬʱ����
(2) ������䣬���¶������������Ǿ��ȹ��̣��������
(3) ��ѹ�¾�������
(4) �����¾�������
(A) (1),(4) (B) (2),(3)
(C) (3),(4) (D) (1),(2)
15. 2 �� (0085)
����ϵ�¶Ⱥ㶨�ı仯��,��ϵ�뻷��֮��: ( )
(A) һ�������Ƚ���
(B) һ���������Ƚ���
C����һ�������Ƚ���
(D) �¶Ⱥ㶨���Ƚ�����
��������� ( ��10�� 20�� )
16. 2 �� (9039)
�Էǵ�Һ�����ʣ��������е�ʱ��������ԼΪ J·K-1·mol-1��
17. 2 �� (0258)
1 mol��ԭ�ӷ����������壬��p1=202 650 Pa��T1= 273 K��p/T=�����������¼��ȣ�ʹѹ�����ӵ�p2= 405 300 Pa������ϵ���������W = J��
18. 2 �� (1282)
������ϵ�ͻ���֮����������������ʽ����ij�����ϵ��˵,���صı仯,һ��������__________________________������ö������,�ⲿ���س�Ϊ��������һ��������___________________________�IJ�������̲�����,�ⲿ���ر��Ϊ�ز�����
19. 2 �� (0257)
10 mol��ԭ�ӷ������������ (¶H/¶T)V = J·K-1 ��
20. 2 �� (1034)
��ԭ�����������CV,m = (3/2)R, [(¶T/¶S)p] / [(¶T/¶S)V] ���� _________ ��
21. 2 �� (0381)
��һ���ȸ��������н���ijһ��ѧ��Ӧ������ϵ�����ܱ仯Ϊ ______ ���ʱ仯Ϊ _______ ��
22. 2 �� (9026)
��ʽ��S=nRln(V2/V1)+CVln(T2/T1)�����÷�Χ��__________________________________
________________________��
23. 2 �� (0387)
300 Kʱ����2 mol ZnƬ���ڹ�����ϡ�����У�����Ӧ�ڳ��������н���ʱ����Qp���ڷ�ո��������н���ʱ����QV����QV -Qp= _______ J��
24. 2 �� (9029)
��ʽ��mixS=-R��BnBlnxB��Ӧ��������_________________________________
_______________________________________________________________________��
25. 2 �� (0839)
ѡ���������������������е�һ���������пո�
����Ӧ C(s) + O2(g) = CO2(g) �ں��¡���ѹ�����·������� ��rHm< 0�����ں��ݾ��������·�������rUm _____ 0����rSm _____ 0��
���������� ( �� 4�� 40�� )
26. 10 �� (9009)
��֪Hg(s)���۵�Ϊ234.15 K,�ۻ���Ϊ470 kJ·mol-1,Hg(l)��Cp, m/J·K-1·mol-1 =29.7-0.0067(T/K),
Hg(s)��Cp, m /J·K-1·mol-1 =26.78 �������ѹ��p$��,323.15 K��Hg(l)��223.15 K��Hg(s)��Ħ����֮��ֵ��
27. 10 �� (0249)
ij�����������ʼ̬(p1��V1��T1)���� (1) 1A2��(2)1B2��(3)1DC2 ������̬���� (quasi-static process) �䵽��̬(p2��V2��T2)������ͼ��ʾ���������������ϵ�����Ĺ�����ϵ�����ȼ���ϵ���ܵ�������U�ı���ʽ���ٶ�������Ϊһ������
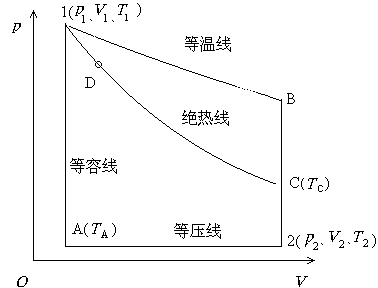
28. 10 �� (0984)
����300 K��1 mol������������������,��ʼѹ��Ϊ15p$,��̬���Ϊ10 dm3���Լ���������DU, DH, DF, DS��DG��
29. 10 �� (1256)
��ͨ�����о�����������ƫĦ�����IJⶨ����,ͬʱ��Ҫ�����ؾ෨Ҫ�㡣
��298 K,p$��,�����ʵ���Ϊn2��NaCl����1000 cm3ˮ��,���γ���Һ�����ΪV,
V��n2�Ĺ�ϵ��ʵ��ȷ��Ϊ��
�ġ��ʴ��� ( �� 1�� 10�� )
30. 10 �� (0766)
ij����״̬�ķ���Ϊ (p+a/V2)V=RT, ���� a �dz�������ѹ�����ܴ�������, ����� 1mol �������p1��V1�����¿�������� p2��V2 ʱ�� Q��W����U����H����S�ͦ�G��
��ѧһ��
һ��ѡ���� ( ��15�� 30�� )
1. 2 �� (0910) [��] (C)
2. 2 �� (0155) [��] (D)
3. 2 �� (0983) [��] (B)
(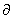 G/
G/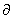 T)p= - S < 0
T)p= - S < 0
4. 2 �� (0074) [��] (B)
5. 2 �� (9031) [��] (A)
6. 2 �� (0065) [��] (C)
7. 2 �� (0890) [��] (C)
��ϵ�����ı仯Ϊ���Ȳ�����仯,���Ԧ�S��> 0����������ϵ��û���Ƚ���,
ѹ�����ޱ仯,����ı仯�ɺ���,���Ի�����״̬δ��, ����S��= 0 (�����������
���ɺ����ǻ���������ʶ,��һ�������,�ܿ�����Ϊ�����������ϵ��������)��
8. 2 �� (0424) [��] (A)
9. 2 �� (1003) [��] (C)
10. 2 �� (0090) [��] (B)
11. 2 �� (0805) [��] (C)
12. 2 �� (0278) [��] (D) 13. 2 �� (0182) [��] (C)
14. 2 �� (0238) [��] (A)
15. 2 �� (0085) [��] (C)
��������� ( ��10�� 20�� )
16. 2 �� (9039) [��] 88
17. 2 �� (0258)
[��] W=0 J
��Ϊp/T=��������p2=2p1ʱ��T2=2T1����V2=V1
����W=0
18. 2 �� (1282)
[��] ��ϵ�ͻ��� ��ϵ�ڲ�
19. 2 �� (0257)
[��] 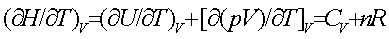 =208 J·K-1
=208 J·K-1
20. 2 �� (1034)
[��] ���� 0.6
��Ϊ [(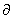 T/
T/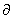 S)p]/[(
S)p]/[(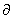 T/
T/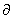 S)V] = CV/Cp= CV,m /Cp,m = 0.6
S)V] = CV/Cp= CV,m /Cp,m = 0.6
21. 2 �� (0381)
[��] 0��p2V2-p1V1
22. 2 �� (9026)
[��] ���������ʼ̬p1,V1,T1�����κι��̵�̬��̬p2,V2,T2�� (2��)
23. 2 �� (0387)
[��] QV -Qp=-��nRT= -4988 J
24. 2 �� (9029)
[��] �����ϵƽ��̬���������塢���»��,���ǰÿ�����嵥������ʱ��ѹ�������,�ҵ��ڻ�Ϻ����ѹ����
25. 2 �� (0839)
[��] = >
���������� ( �� 4�� 40�� )
26. 10 �� (9009)
9009
[��]
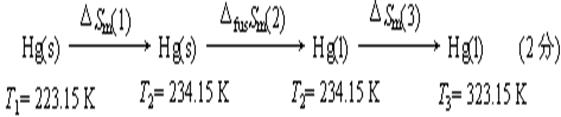
��Ħ����֮��Ϊ��
��Sm=��Sm(1) +��fusSm+ ��Sm(3 )
= p,m(S)dT/T+ ��fusHm/T2+
p,m(S)dT/T+ ��fusHm/T2+  p,m(l)dT/T (3��)
p,m(l)dT/T (3��)
=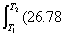 J·K-1·mol-1)dT/T +��fusHm/T2
J·K-1·mol-1)dT/T +��fusHm/T2
+ 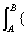 [29.7-0.0067(T/K)] J·K-1·mol-1}dT/T (2��)
[29.7-0.0067(T/K)] J·K-1·mol-1}dT/T (2��)
= (26.78 J·K-1·mol-1)ln(234.15 K/223.15 K)+470×103 J·mol-1 /234.15 K
+ (29.7 J·K-1·mol-1)��ln(323.15 K/234.15 K)
- (0.0067 J·K2·mol-1)×(323.15 K-234.15 K)
= 2.02×103 J·K-1·mol-1 (3��)
27. 10 �� (0249)
[��] (1) Q1=CV (TA-T1)+Cp(T2-TA)
W1=p2(V2-V1)
��U1=Q1-W1=CV (T2-T1) (3��)
(2) Q2=��U2+W2=CV (T2-T1)+RTln(V2/V1)
W2=RTln(V2/V1)
��U2=CV (T2-T1) (3��)
(3) W3=(p2V2-p1V1)/(1-��)= -CV(TC-T1)
��U3=CV (T2-T1)
Q3=��U3+W3=CV (T2-TC) (4��)
28. 10 �� (0984)
[��] �ù���������������¹���,��
��U =��H = 0
ʼ̬��� V1Ϊ��
V1= nRT/p1
= (1mol)(8.314 J·K-1·mol-1)(300 K)/(15×101.325 kPa)
= 1.64 dm3 (2��)
��S = nRln(V2/V1)
= (1mol)(8.314 J·K-1·mol-1)ln(10 dm3/1.64 dm3)
= 15.0 J·K-1 (2��)
��F = nRTln(V1/V2)
= (1 mol)(8.314 J·K-1·mol-1)(300 K)ln(1.64 dm3/10 dm3)
= - 4.51 kJ (2��)
��G =��F = - 4.51 kJ (2��)
29. 10 �� (1256)
1256
[��] (1) ��V2��n2�Ĺ�ϵʽ��V1��n1�Ĺ�ϵʽ��
V2=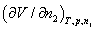
= { 16.6258 + 2.6607(n2/mol)1/2
+ 0.2388(n2/mol)} cm3·mol-1 (1��)
V1= (V-n2V2)/n1
���� n1= (1000/18.02 ) mol = 55.50 mol (1��)
�����κ�Ũ���µ�ƫĦ�������������
(2) �ؾ෨Ҫ�㣺
��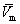 Ϊ��ϵ��ƽ��Ħ�����,��
Ϊ��ϵ��ƽ��Ħ�����,��
��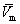 = V/(n1+n2) = (n1V1+n2V2)/(n1+n2)
= V/(n1+n2) = (n1V1+n2V2)/(n1+n2)
= x1V1+x2V2
= V1+ (V2-V1)x2 (1��)
�� (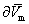 /
/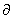 x2)T,p = V2- V1+ x1(
x2)T,p = V2- V1+ x1(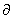 V1/
V1/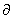 x1)T,p
x1)T,p
+ x2(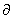 V2/
V2/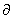 x2)T,p (1��)
x2)T,p (1��)
���������,�� (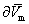 /
/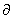 x2)T,p = V2- V1 (1��)
x2)T,p = V2- V1 (1��)
V1= V2- (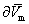 /
/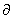 x2)T,p
x2)T,p
=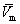 /x2- x1V1/x2- (
/x2- x1V1/x2- (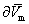 /
/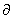 x2)T,p (1��)
x2)T,p (1��)
�� V1=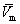 - x2(
- x2(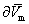 /
/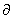 x2)T,p (1��)
x2)T,p (1��)
V2=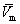 - x1(
- x1(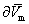 /
/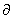 x2)T,p (1��)
x2)T,p (1��)
����ʵ��������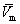 ��x1ͼ��һ����,��������һ�������� x2= 0, x1= 1
��x1ͼ��һ����,��������һ�������� x2= 0, x1= 1
����Ľؾ༴ΪV1,V2ֵ�� (2��)
�ġ��ʴ��� ( �� 1�� 10�� )
30. 10 �� (0766)
0766
[��] p = (RT/V) -a/V2
W=��pdV =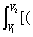 RT/V)-a/V2]dV
RT/V)-a/V2]dV
= RTln(V2/V1)+ a(1/V2-1/V1) (2��)
(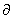 U/
U/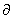 V)T = T(
V)T = T(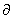 p/
p/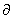 T)V- p = a/V2
T)V- p = a/V2
 =
=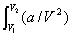 dV ��U = a(1/V1- 1/V2) (3��)
dV ��U = a(1/V1- 1/V2) (3��)
QR= ��U + W = RTln(V2/V1) (1��)
��H =��U +��(pV) =��U + (p2V2- p1V1)
= ��U + [(RT - a/V2) - (RT - a/V1)]
= a[(1/V1)-(1/V2)] + a[(1/V1)-(1/V2)]
= 2a[(1/V1)-(1/V2)] (2��)
��S = QR/T = Rln(V2/V1) (1��)
��G =��H - T��S
= 2a[(1/V1- 1/V2)] - RTln(V2/V1) (1��)
